


2. 南昌大学药学院药理学教研室, 江西 南昌 330006
 , CHUN Chun-xiang1, 2, CHEN Fang-hui1, 2, GAO Yan1, 2, CHU Jia-jia1, 2, LI Teng1, 2, HUANG Qi-ren1, 2
, CHUN Chun-xiang1, 2, CHEN Fang-hui1, 2, GAO Yan1, 2, CHU Jia-jia1, 2, LI Teng1, 2, HUANG Qi-ren1, 2

2. Dept of Pharmacology, College of Pharmacy, Nanchang University, Nanchang 330006, China
现代医学研究表明,血管内皮胰岛素抵抗是糖尿病发生血管并发症的始动环节,是滋生多种代谢相关疾病的共同“土壤” [1, 2]。但目前,国内外对其发病机制尚不完全清楚。因此,阐明血管内皮IR发生的分子机制,发现糖尿病防治药物新的分子作用靶点及开发新的防治药物,对于降低糖尿病患者心脑血管事件发生,改善患者生存质量具有重要意义。PPARγ 是过氧化物增殖酶体激活受体超家族(PPARs) 的成员之一,是体内糖代谢和脂肪细胞分化的重要调节因子,是胰岛素增敏剂噻唑烷二酮类的靶标[3],能改善血管内皮细胞对胰岛素的敏感性,机制可能与其激活了PPARγ依赖的胰岛素信号转导途径有关。另外,PPARγ也能在配体依赖方式下通过抑制其他转录因子,如NF-κB及活化剂蛋白-1家族,从而直接地抑制促炎症基因的表达[4, 5]。研究证实前列腺素衍生物如15-脱氧前列腺素J2(15-d-PGJ2)是PPARγ的天然激动剂[6, 7] 。
卡托普利(captopril,Cap)是第一代的血管紧张素转化酶抑制剂,临床广泛用于合并了糖尿病的高血压或心衰患者的治疗。有研究证实,Cap可通过增加前列腺素衍生物、缓激肽(bradykinin,BK)水平来改善IR[8, 9],那么,它能不能通过直接改变PPARγ的表达或活性来改善IR,目前相关报道甚少,因此,本实验探讨卡托普利改善内皮细胞胰岛素抵抗的机制,为寻找糖尿病血管病变防治的分子靶点拓展新的思路。
1 材料与方法 1.1 细胞株及血清培养基实验用HUVECs株购自美国ATCC(Catalog No: CRL-1730);胎牛血清购自杭州四季青生物工程材料有限公司;DMEM培养基购自Gibco BRL公司。
1.2 药品及试剂NO检测试剂盒购自Beyotime Institute of Biotechnology;ET-1试剂盒购自上海RD生物公司;卡托普利购自上海普康公司;PPARγ抑制剂(GW9662)购自美国Sigma;PPARγ多克隆抗体购自美国Cell Signaling;PPARγ磷酸化抗体购自美国Santa Cruz Biotechnology;β-actin多克隆抗体购自美国Santa Cruz;TRIzol 试剂购自Invitrogen公司;MMLV逆转录酶、RNA酶抑制剂、dNTP、Oligo(dT)15、Taq酶均购自Promega Corporation;引物购自上海捷瑞生物公司;其它各种化学试剂为进口或国产分析纯试剂。
1.3 实验分组及处理方法 1.3.1 Cap对HG诱导的HUVECs IR的改善作用将HUVECs均匀接种在六孔培养板上,随机分为5组,即Control组、IR组、IR+CapⅠ(1×10-6 mol·L-1 )组、IR+CapⅡ(1×10-5 mol·L-1 )组、IR+ CapⅢ(1×10-4 mol·L-1)组。除Control组(5.5 mmol·L-1 葡萄糖的DMEM培养48 h)外,所有各组先用含33 mmol·L-1葡萄糖的DMEM培养48 h,Cap各组再加不同浓度的Cap处理4 h,最后胰岛素(100 nmol·L-1 )处理30 min,收集细胞上清液和细胞,分别进行指标检测。
1.3.2 Cap改善HG诱导HUVECsIR的作用是由PPARγ介导 将HUVECs均匀接种在六孔培养板上,随机分为6组,即Control组、IR组、IR+CapⅡ(1.0×10-5mol·L-1 )组、PPARγ抑制剂GW9662(PI,1.0 μmol·L-1 )组、IR+PPARγ抑制剂(IR+PI,1.0 μmol·L-1 )组、IR+Cap(1.0×10-5 mol·L-1 )+ PPARγ抑制剂(IR+Cap+PI,1.0 μmol·L-1 )组,除Control组和PI组(5.5 mmol·L-1 葡萄糖的DMEM培养48 h)外,所有各组先用含33 mmol·L-1葡萄糖的DMEM培养48 h,Cap各组再加不同浓度的Cap处理4 h,最后胰岛素(100 nmol·L-1 )处理30 min,抑制剂组再加抑制剂GW9662(1.0 μmol·L-1 )处理1 h,收集细胞上清液和细胞,分别进行以下指标检测。
1.4 HUVECs中NO、ET-1水平的检测(a) 参照碧云天生物技术研究所一氧化氮检测试剂盒的使用说明,先做出标准曲线,然后根据各组吸光度,计算出各组NO的含量。(b) 参照人内皮素(ET)酶联免疫试剂盒的使用说明,先做出标准曲线,然后根据各组吸光度,计算出各组ET-1的含量。
1.5 Western blot检测HUVECs内PPARγ、P-PPARγ蛋白的表达细胞经实验因素处理后,经PBS清洗后,用RIPA裂解液进行裂解,蛋白浓度用BCA试剂盒进行测定,细胞裂解物溶于上样缓冲溶液煮沸后经10%的SDS-PAGE电泳分离,并电转到PVDF膜上,取出后将膜放入质量浓度均为50 g·L-1的脱脂牛奶或者BSA中封闭2 h,再用TBST洗膜3次,每次15 min。将膜放入一抗中(1 ∶ 750),4℃孵育过夜。TBST冲洗膜后,将膜放入相应的二抗(1 ∶ 2 000)中,室温平摇2 h后,漂洗3次,每次20 min,用ECL化学发光法进行检测。将曝光条带进行X光胶片扫描后,在医学图形分析系统ImageTool软件上进行分析,将所得PPARγ蛋白带的综合密度分别除以对应组β-actin的综合密度后,Excel表中进行分析。
1.6 HUVECs PPARγ mRNA表达检测PCR扩增所用引物由上海生物工程有限公司合成,PPARγ上游引物:5′-TCTGGCCACCAACTTTGGG-3′;下游引物:5′-CTTCACAAGCATGAACTCCA-3′,PCR扩增片段长度为360 bp。内参β-actin上游引物:5′-CGGGAAATCGTGCGTGAC-3′;下游引物:5′-TGGAAGGTGG ACAGCGAGG-3′ ,PCR扩增片段长度为268 bp。PCR扩增体系为25 μL,其中cDNA为5 μL,上、下游引物各1.0 μL,2X Tag酶为12.5 μL,再用无菌三蒸水补至25.0 μL。PCR循环参数为30,94℃预变性5 min,94℃变性45 s,扩增PPARγ为61℃退火30 s,扩增β-actin 为55℃退火45 s,72℃延伸45 s,最后72℃延伸5 min。取扩增产物6 μL上样,1.5%琼脂糖凝胶电泳后,在透射紫外光分析仪下摄影,并在电脑上用Image Tool图像处理软件进行处理。
1.7 统计学处理各实验组数据以x±s表示,采用统计软件SPSS12进行方差齐性检验、单因素方差分析,组间比较用LSD法。
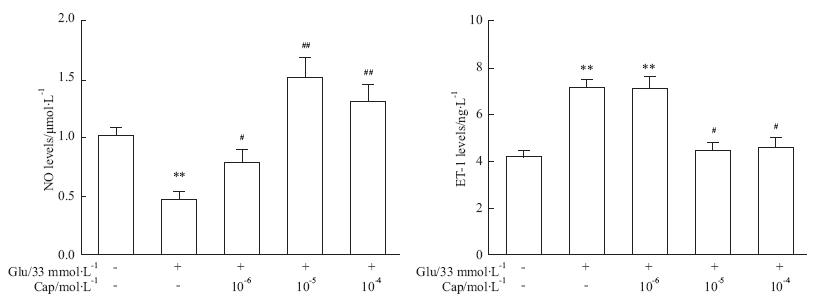
2 结果 2.1 Cap呈浓度依赖性改善HG诱导HUVECs胰岛素抵抗血管内皮IR评价指标常用血清或培养上清液中NO 和ET-1水平来表示。IR组与Control组比较,NO水平明显降低、ET-1水平明显升高(P<0.01 vs Control);用低剂量的卡托普利处理4 h后,与IR相比NO水平明显升高且差异有显著性(P<0.05 vs IR),而ET-1水平与IR组比较组间差异没有统计学意义(P>0.05);中、高剂量的卡托普利处理后,NO升高更明显(P<0.01 vs IR),ET-1水平明显降低(P<0.05),见Fig 1。
|
| Fig 1 NO,ET-1 levels of various treatments in cultured HUVECs (x±s,n=6) **P<0.01 vs control group; #P<0.05,##P<0.01 vs IR group |
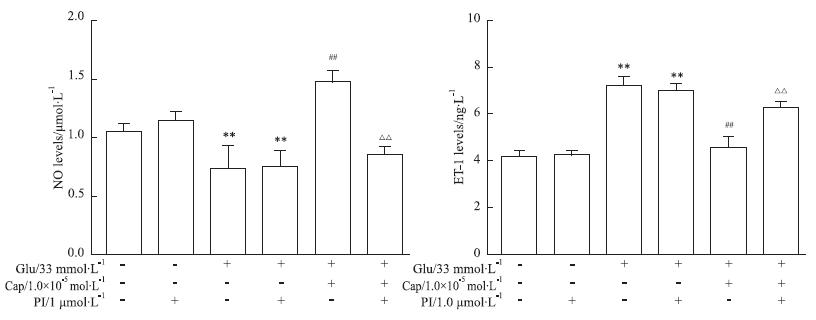
见Fig 2。PI组与Control组比较,NO、ET-1水平无明显差异(P>0.05);IR+PI组与IR组比较,NO、ET-1水平差异也无统计学意义(P>0.05);IR+Cap组与IR组相比NO水平明显升 高、ET-1水平明显下降(P<0.01);而IR+Cap+PI组与IR+Cap组相比NO水平明显下降、ET-1水平明显升高(P<0.01)。
|
| Fig 2 NO,ET-1 levels of various treatments in cultured HUVECs (x±s,n=6) **P<0.01 vs control group; ##P<0.01 vs IR group; △△P<0.01 vs IR+Cap group |
PPARγ mRNA各组样本均由对应的β-actin条带的扫描值标化再与Control组比较。PPARγ mRNA在正常HUVECs中呈基础性表达;HUVECs暴露在高糖培养液中48 h后,PPARγ mRNA的表达与Control组比较,差异无统计学意义(P>0.05)。Cap组中内皮细胞的PPARγ mRNA的表达量与IR组相比组间无明显差异(P>0.05),见Fig 3。

|
| Fig 3 Effect of various treatments on expression levels of PPARγ mRNA of HUVECs (x±s,n=6) The left panel shows a representative electrophoretic diagram for PPARγ,β-actin mRNA by agrose gels; the right panel shows a statistical diagram of grey density |
PPARγ各组样本均由对应的β-actin条带的扫描值标化。PPARγ蛋白、P-PPARγ蛋白在正常HUVECs中呈基础性表达。IR组中PPARγ蛋白、P-PPARγ蛋白表达量无明显变化,与 Control组相比,差异无统计学意义(P>0.05);Cap组中内皮细胞的PPARγ 蛋白的表达量与IR组相比亦无明显差异(P>0.05);而低、中剂量Cap组中内皮细胞的P-PPARγ 蛋白的表达量较IR明显升高,差异具有统计学意义(P<0.05);而高剂量Cap组与IR组相比P-PPARγ蛋白的表达无明显差异(P>0.05),见Fig 4。

|
| Fig 4 Effect of various treatments on expression levels of PPARγ and P-PPARγ in cultured HUVECs (x±s,n=6) The upper panel shows representative Western blot for PPARγ,P-PPARγ and β-actin; the lower panel shows a statistical diagram of grey density. #P<0.05 vs IR group. |
卡托普利可以改善胰岛素抵抗,已有大量的资料证实。可能的作用机制目前有以下几个方面:通过扩血管效应,增加骨骼肌的血流,可促使葡萄糖和胰岛素向胰岛素敏感组织释放, 增加葡萄糖的利用;通过改善胰腺的血液循环从而提高胰岛β细胞的代谢,促进胰岛素分泌,加强靶细胞功能,提高胰岛素的生物效应,改善胰岛素抵抗[10, 11];Captopril还能通过抑制血管紧张素转换酶活性,使组织内BK降解减少,局部血管BK浓度增高,BK具有扩张血管和降压作用,BK是血管内皮L-精氨酸-NO途径的重要激活剂,它作用于内皮的β2受体能引起血管内皮超极化因子及NO的释放,BK降解减少还能进一步促进15-d-PGJ2合成,而15-d-PGJ2是PPARγ的天然激动剂。
在我们的前期工作中,从整体动物、细胞和分子水平观察了PPARγ经典配体如罗格列酮(RG)或匹格列酮(PG)对高糖诱导血管内皮胰岛素抵抗的作用,探讨了其可能的作用机制。结果表明,无论RG或PG预处理和后处理,PG和RG均能明显改善HG诱导HUVEC胰岛素抵抗,其机制是通过非经典PPARγ依赖的NF-κB转录抑制途径(under revision)。PPARγ表达很广泛,包括脂肪细胞、内皮细胞、血管平滑肌细胞、巨噬细胞和心肌细胞等[12] 。
本实验中,卡托普利改善胰岛素抵抗是否通过PPARγ来介导的目前机制还并不清楚。实验中用高糖(33 mmol·L-1)处理内皮细胞48 h后再用胰岛素处理0.5 h,取其细胞上清测NO和ET-1水平,发现其NO水平比正常组明显下降,且差异具有统计学意义;ET-1水平明显升高,且差异具有统计学意义。证明胰岛素抵抗的模型建立成功。胰岛素抵抗模型建立后,在预实验中,我们设计了卡托普利浓度梯度(10-8~10-2 mol·L-1),结果发现,浓度≤10-7 mol·L-1时,Cap对细胞活力和胰岛素抵抗程度均没有影响;而浓度≥10-3 mol·L-1时,细胞活 力明显下降,表现出明显地细胞毒性。因此,我们就选择了1.0×10-5mol·L-1的浓度。用Cap处理4 h后,其NO水平比IR组明显升高,ET-1水平比IR组明显降低,PPARγ蛋白表达水平与IR组相比无明显改变,但P-PPARγ蛋白表达水平比IR组升高。结合文献资料可能存在机制:在高糖和胰岛素的刺激下,内皮细胞受损,导致NO的分泌减少,ET-1的分泌增多,而这两类物质动态平衡维持着血管的正常状态和功能。用Cap处理4 h后,Cap可以使内皮细胞内BK的减少,进而促进15-d-PGJ2的生成,15-d-PGJ2是PPARγ的天然激动剂,可以使PPARγ磷酸化途径被激活,进而改善胰岛素抵抗。
综上所述,卡托普利可以促使P-PPARγ蛋白的表达上调,PPARγ与胰岛素信号之间亦存在着正反馈机制;PPARγ可通过转录激活作用增加靶基因的表达或激活来发挥作用。活化的PPARγ能抑制脂肪细胞表达肿瘤坏死因子-α(TNF-α),减轻TNF-α诱发的胰岛素抵抗,且通过增加c-CBL相关蛋白及胰岛素受体底物2的表达,增强胰岛素的信号转导,从而改善胰岛素抵抗。
| [1] | Ford E S. Risks for all-cause mortality, cardiovascular disease and diabetes associated with the metabolic syndrome:a summary of the evidence [J]. Diabetes Care, 2005, 28(7):1769-78. |
| [2] | Marina C, Maria A M, Simona F,et al. Carotid artery intima-media thickness is associated with Insulin-mediated glucose disposal in nondiabetic normotensive offspring of type 2 diabetic patients [J]. Am J Physiol Endocrinol Metab, 2007, 292(1):E347-52. |
| [3] | 张 宁,孟爱民,王莉莉.选择性PPARγ调节剂治疗二型糖尿病的分子机制研究进展[J].中国药理学通报,2013, 29(2):157-60. Zhang N, Meng A M, Wang L L. Molecular mechanism of selective PPARγ modulators for type 2 diabetes treatment[J]. Chin Pharmacol Bull, 2013, 29(2):157-60. |
| [4] | Veliceasa D, Schulze-Hoepfne Ft, Volpertl O V. PPARγ and agonists against cancer:rational design of complementation treatments [J]. PPAR Res,2008, 2008:945275. |
| [5] | Patel N G, Holder J C, Smith S A. Differential regulation of lipogenesis and leptin production by independent signaling pathways and rosiglitazone during human adipocyte differentiation [J]. Diabetes, 2003, 52(1):43-50. |
| [6] | Scheen A J. Renin-angiotensin system inhibition prevents type 2 diabetes mellitus part1, a meta-analysis of randomized clinical trials [J]. Diabetes Metab, 2004, 30(6):487-96. |
| [7] | Haseqawa H, Takano H, Komurol. Therapeutic implications of PPARgamma in cardiovascular diseases [J]. PPAR Res, 2010, 2010:876049. |
| [8] | Sharma J N, Kesavarao U. The effects of captopril on cardiac regression, blood pressure and bradykinin components in diabetic Wistar Kyoto rats[J]. Immunopathol Pharmacol, 2011, 24(2):337-43. |
| [9] | Adam A, Leclair P, Montpas N, Koumbadinga G A. Altered cardiac bradykinin metabolism in experimental diabetes caused by the variations of angiotensin-converting enzyme and other peptidase [J]. Neurpeptides, 2010, 44(2):69-75. |
| [10] | Hermann T S, Li W, Dominguez H, et al. Quinapril treatment increases insulin-stimulated endothelial function and adiponectin gene expression in patients with type 2 diabetes [J]. Clin Endocrinol Metab, 2006, 91(3):1001-8. |
| [11] | Leung P S, Carlsson P O. Tissue renin-angiotensin system:its expression,localization, regulation and potential role in the pancreas [J]. Mol Endocrinol, 2001, 26(3):155-64. |
| [12] | Videla L A, Pettinelli P. Misregulation of PPAR functioning and its pathogenic consequences associated with nonalcoholic fatty liver disease in human obesity [J]. PPAR Res, 2012, 2012:107434. |