


2. 上海中医药大学中药学院, 上海 201203
2. School of Pharmacy, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China
肥大细胞广泛分布于皮肤及内脏粘膜下的微血管周围。其脱颗粒现象与过敏反应密切相关。其中SFKs参与肥大细胞脱颗粒的起始信号。近年来研究表明,Lyn、Fyn、Syk等均与肥大细胞脱颗粒有关。同时,在研究中发现了越来越多的靶向于SFKs的药物,对其研究也日益深入。SFKs抑制剂可以作为过敏性疾病的潜在药物,为抗过敏药的开发提供了新的研究方向。本文就SFKs在肥大细胞脱颗粒中的作用及其可能机制进行探讨,并对其相关药物针对过敏性疾病的研究进展进行综述。
1 肥大细胞在过敏过程中的机制 1.1 肥大细胞的脱颗粒肥大细胞被认为是免疫系统的一部分,在过敏反应和炎症中起着重要的作用[1]。肥大细胞表面的IgE的Fc受体(FcεRI),可与IgE高亲和力结合,使机体处于致敏状态。当相同的过敏原再次进入致敏机体时,过敏原结合两个以上IgE分子,与FcεR I交联,从而激活肥大细胞,使其发生脱颗粒,释放多种活性介质,从而引起超敏反应[2]。
肥大细胞活化后释放的活性介质主要分为3种:①预存于颗粒内的介质,包括:组胺、肝素、丝氨酸蛋白酶、血清素等;②新合成的介质,包括:前列腺素D2(PGD2)、白三烯(LT)、血小板活化因子等;③细胞因子及趋化因子,其中细胞因子包括:白细胞介素-2(IL-2)、IL-3、IL-4、IL-5、IL-6、IL-10、IL-13,趋化因子包括:血浆炎性趋化因子-2(CCL-2)、CCL-3、CCL-5等[3]。
1.2 FcεR I受体与脱颗粒FcεRI为Fc受体家族成员,属于免疫球蛋白超家族。其最初被定义为一个四聚体复合物(αβγ2),主要分布于表皮朗氏细胞、嗜酸性粒细胞、嗜碱性粒细胞和肥大细胞等。FcεRI的α链是由胞外区、一个跨膜结构域和一个短的胞质尾巴构成,主要结合IgE的Fc区域;β链是胞膜上的一个四次跨膜结构,具有一个免疫受体酪氨酸激活基序(immunoreceptor tyrosine-based activatory motif,ITAM);γ链则是位于胞膜上的以二硫键连接的二聚体,每条γ链上都含有ITAM序列[4]。
FcεRI做为高亲和力的IgE受体,是活化肥大细胞的主要受体。当过敏原与IgE介导的FcεRI交联时,其β链、γ链的ITAM基于Src家族激酶发生磷酸化,形成肥大细胞脱颗粒的起始信号。在脱颗粒的起始信号中,需要受体操纵的膜外钙流进入(receptor-operated calcium entry)和Src家族激酶磷酸化等信号的参与。
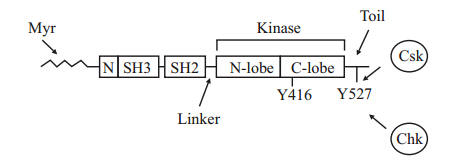
1.3 主要Src家族激酶在脱颗粒中的作用Src家族激酶是一类非受体型酪氨酸激酶,主要家族成员有Fyn、Lyn、Hck、c-Yes、Blk、Fgr、Src以及Lck等。这些物质都是具有酪氨酸蛋白激酶(protein tyrosine kinase)活性的蛋白质。他们构型相似,从N-到C-末端具有相类似的结构域(如Fig 1)[5]。SFKs对调节细胞信号传导有着重要意义,如参与调节细胞的生长、分化、凋亡及免疫等。在肥大细胞中,它们调控脱颗粒过程,是这些酪氨酸激酶重要的功能,然而,它们参与FcεRI介导的肥大细胞活化是非常复杂的。大量文献报道SFKs对肥大细胞脱颗粒具有正负两方面的调节效果。由此提示,SFKs抑制剂可作为一个潜在的,疗效明显的抗过敏药物,其开发及应用将具有远大的前景。
|
| Fig 1 Structure of SFKs |
Lyn激酶是Src家族成员之一,参与多种信号途径,与肥大细胞脱颗粒的过程有关,具有启动活化和抑制脱颗粒两方面的信号传递。据Okayama等[6]研究发现,沉默FcεRIβ可抑制Lyn的再分配,而沉默Lyn可干扰FcεRIβ中ITAM的磷酸化,从而抑制组胺的释放,说明Lyn与FcεRIβ相互作用,且这种作用在FcεRI介导的人肥大细胞脱颗粒中是必不可少的。另外,Lyn激酶对肥大细胞脱颗粒的负面调节作用是通过SH2肌醇磷酸酶-1(SHIP-1)和SHIP-2结构域实现的。Alvarez-Errico等[7]最新研究认为,FcεRI与IgE高亲和力结合导致Lyn激酶的磷酸化。其中Lyn激酶具有LynA和LynB两个亚型。LynB很少与三磷酸肌醇的产生和钙流反应相联系。LynB单独表达导致磷脂酶Cγ-1和Cγ-2磷酸化减少,以及降低磷脂酶Cγ-1与接头蛋白LAT间的相互作用,并增加与负性调控脂质磷酸酶SHIP-1的结合。相反,LynA和LynB均能够引起相似的细胞内酪氨酸磷酸化,LynA或LynB均不能单独使肥大细胞脱颗粒,也不能单独阻断由于缺乏Lyn所形成的细胞因子IL-6的过量产生。由此可见,Lyn对肥大细胞脱颗粒存在促进和抑制的双重作用。
1.3.2 FynFyn激酶在FcεRI介导的人肥大细胞脱颗粒中主要起正向调节作用。Gomez等[8]研究发现,Fyn缺失的肥大细胞不分泌LTB4、LTB5、IL-6、TNF、CCL2和CCL4,并抑制了JNK和p38 MAPK的活化。也有研究结果[9]显示,Fyn激酶调控瞬时受体电位钙通道(TRPC)的钙流进入和所控制的脱颗粒过程。免疫沉淀实验表明,IgE抗原刺激后,Fyn激酶与3型、6型和7型TRPC通道形成复合物,但未发生磷酸化。Lu等[10]研究发现,从三白草根茎分离获得的倍半木脂素saucerneol F,可通过抑制Fyn介导的途径减少MAPK磷酸化及JNK来降低小鼠骨髓来源肥大细胞(BMMCs)的脱颗粒。因此大量实验数据表明,Fyn激酶与FcεRI介导的人肥大细胞脱颗粒现象密切相关,且处于激活肥大细胞脱颗粒的上游阶段。
1.3.3 . Syk脾酪氨酸激酶(Syk)是FcεRI介导的人肥大细胞脱颗粒过程中一种非常关键的调节因子。Sanderson等[11]研究发现,药理学上抑制Syk激酶活性可以完全阻断RBL-2H3肥大细胞或骨髓由来的嗜碱粒细胞的脱颗粒现象。并且Lyn沉默进一步提高肥大细胞脱颗粒的致敏效应,对Lyn的表达干扰破坏了Syk介导的FcεRI近端信号。Lee等[12]研究发现一种小分子化合物,Streptochlorin具有抗过敏作用。其在RBL-2H3细胞中,可抑制Akt、p38、ERK、JNK磷酸化,并抑制Syk、Lyn、Fyn的磷酸化,从而减少TNF-α、IL-6等活性介质的释放。由此可推断,Syk与肥大细胞脱颗粒密切相关,并且参与Lyn及Fyn信号通路。关于Syk的作用可以进一步参考我们以往发表的综述,在此不再赘述[13]。
1.3.4 其他激酶对于其他Src家族激酶亦有相关报道。如Lee等[14]研究认为,Fgr在FcεRI介导的人肥大细胞脱颗粒中作用与Fyn相似,同样具有正向调节作用。其研究发现IgE刺激后,Fgr介导Syk以及下游信号的磷酸化增加。Fgr与Fyn似乎采取一致行动,当过表达Fgr时,引起的Syk磷酸化和脱颗粒现象可被Fyn的过表达进一步增强,却被Lyn的过表达所抑制,说明Fgr通过增加Syk磷酸化来促进肥大细胞脱颗粒过程。而Hong等[15]则进行了Hck与肥大细胞脱颗粒关系的研究。Hek激酶缺乏的肥大细胞脱颗粒和细胞因子明显减少,Lyn的负调节作用增加。并且其认为Lyn、Fyn、Hck在肥大细胞脱颗粒过程中存在层次关系,HCK激酶通过抑制Lyn激酶调节肥大细胞活化。由此可见,SFKs在肥大细胞脱颗粒中作用明显,且存在微妙的内部联系,对微调肥大细胞活化似乎有着至关重要的作用。
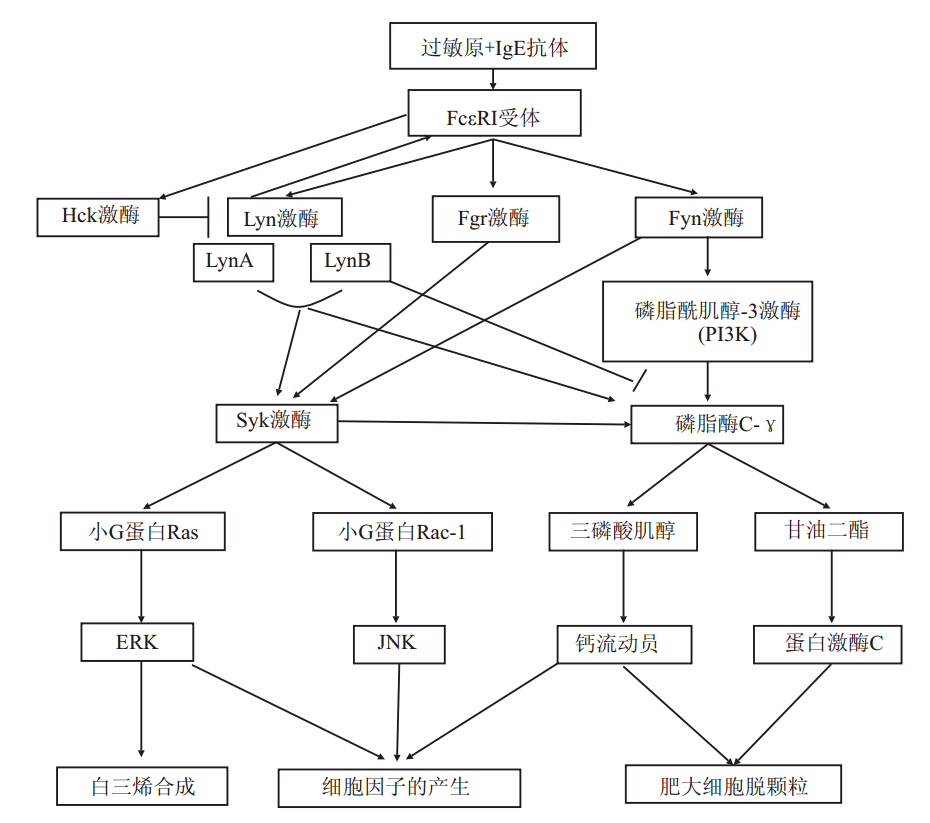
高亲和力IgE受体(FcεRI)与多价抗原结合的相互作用启动一系列信号事件引起肥大细胞脱颗粒和炎症介质的释放。早期的研究表明,Src家族激酶信号级联反应起步于FcεRI受体β亚基的酪氨酸磷酸化。为此学者们分别提出了受体自身的转磷酸化、脂筏、蛋白酪氨酸激酶-酪氨酸磷酸酶相互作用3个当代模型[16]。如上所述,我们针对蛋白酪氨酸激酶-酪氨酸磷酸酶相互作用模型中,评价了蛋白酪氨酸激酶在脱颗粒中的作用和相互关系,如Fig 2所示。
|
| Fig 2 Relationship between SFKs and degranulation of mast cell |
SFKs是一类非受体型酪氨酸激酶,存在于多种细胞中,参与人体生长,分化,免疫等多种功能,在肥大细胞脱颗粒的信号传导中起着重要的作用。近年来研究发现了许多酪氨酸激酶抑制剂,为治疗过敏性疾病提供了新的方向。
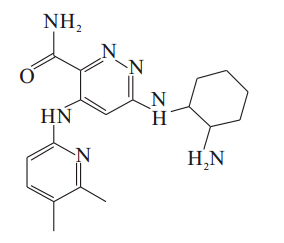
2.1.1 RO9021RO9021是罗氏公司开发的一种ATP竞争性抑制剂,口服生物利用度好,临床多用于类风湿性关节炎、多发性硬化症等,结构示意图见Fig 3。Liao等[17]研究发现,RO9021做为Syk抑制剂,可以阻断人单核细胞的FcγR受体信号和人肥大细胞的FcεRI受体信号。可以抑制组胺的释放,且呈浓度依赖性,其IC50为(22.8±1.7) nmol·L-1,为RO9021开展治疗过敏型疾病研究提供了很好的实验基础。
|
| Fig 3 RO9021 |
美国Rigel公司新型研制的鼻内制剂R112(见图 4),是一个Syk激酶抑制剂,已进入Ⅱ期临床,对季节性过敏性鼻炎具有极好的疗效。Rossi等[18]研究发现R112可以抑制脱颗粒的发生,防止脂质介质及细胞因子的产生,对在FcεRI介导的人肥大细胞脱颗粒可以快速、彻底的抑制。由此推断该化合物可能对多种过敏性疾病都有疗效。随后Rigel公司陆续开发了该系列的化合物R406、R788对类风湿性关节炎具有潜在作用。

|
| Fig 4 R112 |
塞卡替尼(saracatinib)(见图 5)是一种高选择性的Src/Abl激酶双重抑制剂,对卵巢癌有较好的潜在作用,目前正处于Ⅱ期临床试验阶段[19]。而de Wispelaere等[20]研究发现,塞卡替尼具有抗登革病毒(DV)感染的作用,其主要通过抑制Fyn激酶活性而阻止DV的复制,从而起到抗感染的作用。由此推断,塞卡替尼做为Fyn抑制剂,可能在抗过敏疾病中也有较好的作用。

|
| Fig 5 Saracatinib |
(见图 6)这是由日本新药株式会社(Nippon Shinyaku)开发的第二代酪氨酸酶抑制剂。主要用于治疗慢性粒细胞白血病和费城急性淋巴细胞白血病,是基于伊马替尼的化学结构修饰得到的化合物,同样为Abl抑制剂。同时其为Lyn激酶抑制剂。目前其做为B细胞慢性淋巴白血病和前列腺癌的治疗药正在进行Ⅱ期临床试验[21],在抗过敏性疾病作用尚不清楚。

|
| Fig 6 INNO-406 |
虽然目前市场上针对过敏性疾病的药物已经有很多,类似于糖皮质激素、抗组胺药、白三烯抑制剂等,但这些药物一般只能控制病情、治标不治本,且具有较多的副作用,对于改善患者生活质量无太大的帮助[22]。因此从中草药中寻找防治过敏性疾病的有效药物一直是人们关注的研究。研究发现,中药中欧当归内酯A、桑色素、白术内酯Ⅲ、白皮杉醇等具有抑制Src家族激酶的作用和抑制肥大细胞脱颗粒现象的发生,这为抗过敏药物的开发提供了新的方向。
2.2.1 欧当归内酯A(见图 7)欧当归内酯A(Levistilide A)是主要从川芎、当归提取分离获得。其药理学活性研究较少。我们最近的研究结果[23]表明,具有很强的抗炎作用,能够抑制TNF-α、MCP-1、IL-1β、IL-32的产生,能够阻断Syk和NF-κB活性。其直接抑制Syk激酶的酶活性IC50为0.129 μmol·L-1。

|
| Fig 7 Saracatinib |
桑色素(Morin)(见图 8)是黄酮类化合物的一种,在自然界中分布广泛,主要从桑叶、桑白皮和桑椹中提取得到,具有抗炎、抗肿瘤及抗氧化等作用。研究证明桑色素具有抑制肥大细胞激活的功能。Kim等[24]研究发现,桑色素能抑制TNF-α、IL-4的产生,抑制脱颗粒现象。其进行体外激酶实验,发现桑色素可抑制Fyn激酶,对Lyn、Syk无作用。由此推测,桑色素是一种Fyn的抑制剂,在IgE介导的过敏反应中通过抑制Fyn激酶起到抗过敏作用。

|
| Fig 8 Morin |
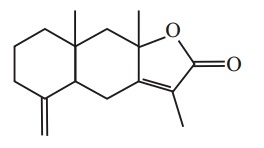
白术为菊科植物白术的根茎,其内酯类物质白术内酯Ⅰ 、Ⅱ、Ⅲ、Ⅳ具有抗炎、抗肿瘤的作用。Zhang等[25]研究发现白术内酯Ⅲ(见图 9)能抑制TNF-α、IL-4的产生,且效果较PP2好。另外其能抑制Lyn、Fyn、Syk、LAT、Gab2、Akt、p38和JNK的磷酸化。由此推断白术内酯Ⅲ是一种能广泛抑制Src家族激酶的化合物,在开发为过敏性疾病治疗药上有很好的前景。
|
| Fig 9 atractylenolide Ⅲ |
白皮杉醇(见图 10)是白藜芦醇的3’羟基化类似物,是Syk特异性抑制剂。它主要存在于大黄藓、大黄、葡萄和甘蔗中,是一种多酚类化合物,具有抗氧化、清除自由基等作用。Singh等[26]报道白皮杉醇可抑制离子霉素诱导的脱颗粒现象(非Sky调节)。由此推断,该化合物对于抑制脱颗粒具有多种分子靶点,可多方面抑制过敏反应。
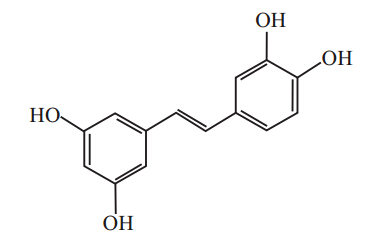
|
| Fig 10 piceatannol |
近年来的研究显示,发现多种中药成分对SFKs都具有抑制作用。Jelic等[27]发现迷迭香酸是一种新型的Fyn抑制剂。大黄素可抑制Syk的磷酸化,从而抑制肥大细胞活化,达到抗过敏的作用[28]。番石榴的乙酸乙酯提取物通过抑制Syk、LAT的磷酸化,而不是抑制Lyn的磷酸化达到抑制IgE介导的过敏反应的效果[29]。鱼腥草水提物能抑制Syk、Lyn的磷酸化[30],白藜芦醇抑制Syk的磷酸化[31]来发挥抑制肥大细胞脱颗粒的作用。
中草药中存在多种SFKs抑制剂,且大量被证实具有抗过敏作用,虽然这些SFKs抑制剂尚缺乏临床证据,但其作为多靶点的抗过敏天然活性物质,仍具有重要的研究价值和广泛的应用前景。
3 问题与展望综上所述,SFKs在FcεRI介导的人肥大细胞脱颗粒中起着重要的调节作用。Lyn激酶对肥大细胞脱颗粒具有双向调节作用,Fyn激酶对肥大细胞脱颗粒为正向调节作用,Syk激酶在驱动肥大细胞活化及传导细胞信号中起着核心作用。因此利用分子生物学技术把SFKs作为干预靶点,将为过敏性疾病的治疗提供新策略和新方法。目前,中药已经开展了抗过敏药物的研究,并且发现多种化合物可抑制SFKs活性,但是对其具体作用机制研究尚不明确。国内抗过敏药物的研究主要停留在药效学研究上,将其引入到SFKs抑制剂的研究上,为过敏性疾病的研究提供新的靶点,进行系统、深入的研究,对开发新一代抗过敏药物具有深远意义。
| [1] | Amin K. The role of mast cells in allergic inflammation[J]. Respirat Med, 2012, 106(1):9-14. |
| [2] | Galli S J, Tsai M, Piliponsky A M. The development of allergic inflammation[J]. Nature, 2008, 454(7203):445-54. |
| [3] | Gilfillan A M, Rivera J. The tyrosine kinase network regulating mast cell activation[J]. Immunol Rev, 2009, 228(1):149-69. |
| [4] | Stone K D, Prussin C, Metcalfe D D. IgE, mast cells, basophils, and eosinophils[J]. J Allergy Clin Immunol, 2010, 125(2):S73-S80. |
| [5] | Engen J R, Wales T E, Hochrein J M, et al. Structure and dynamic regulation of Src-family kinases[J]. Cell Mol Life Sci, 2008, 65(19):3058-73. |
| [6] | Okayama Y, Kashiwakura J I, Matsuda A, et al. The interaction between Lyn and FcεRIβ is indispensable for FcεRI-mediated human mast cell activation[J]. Allergy, 2012, 67(10):1241-9. |
| [7] | Alvarez-Errico D, Yamashita Y, Suzuki R, et al. Functional analysis of Lyn kinase A and B isoforms reveals redundant and distinct roles in FcεRI-dependent mast cell activation[J]. J Immunol, 2010, 184(9):5000-8. |
| [8] | Gomez G, Gonzalez-Espinosa C, Odom S, et al. Impaired FcεRI-dependent gene expression and defective eicosanoid and cytokine production as a consequence of Fyn deficiency in mast cells[J]. J Immunol, 2005, 175(11):7602-10. |
| [9] | Sanchez-Miranda E, Ibarra-Sanchez A, Gonzalez-Espinosa C. Fyn kinase controls FcεRI receptor-operated calcium entry necessary for full degranulation in mast cells [J]. Biochem Biophys Res Commun, 2010, 391(4):1714-20. |
| [10] | Lu Y, Son J K, Chang H W, Saucerneol F, a New Lignan Isolated from Saururus chinensis, Attenuates Degranulation via Phospholipase Cγ 1 Inhibition and Eicosanoid Generation by Suppressing MAP Kinases in Mast Cells[J]. Biomol Ther, 2012, 20(6):526. |
| [11] | Sanderson M P, Wex E, Kono T,et al. Syk and Lyn mediate distinct Syk phosphorylation events in FcεRI-signal transduction:implications for regulation of IgE-mediated degranulation[J]. Mol Immunol, 2010, 48(1):171-8. |
| [12] | Lee S H, Shin H J, Kim D Y, et al. Streptochlorin suppresses allergic dermatitis and mast cell activation via regulation of lyn/Fyn and syk signaling pathways in cellular and mouse models[J]. PloS One, 2013, 8(9):e74194. |
| [13] | 孙 丽,甘我挺,韩 欣,等.脾酪氨酸激酶-动脉粥样硬化新靶点及其药物研究[J].中国药理学通报,2012,28(5):608-612. Sun L, Gan W T, Han X, et al. Spleen tyrosine kinase, a new atherosclerosis target[J]. Chin Pharmacol Bull, 2012, 28(5):608-12. |
| [14] | Lee J H, Kim J W, Kim D K, et al. The Src family kinase Fgr is critical for activation of mast cells and IgE-mediated anaphylaxis in mice[J]. J Immunol, 2011, 187(4):1807-15. |
| [15] | Hong H, Kitaura J, Xiao W, et al. The Src family kinase Hck regulates mast cell activation by suppressing an inhibitory Src family kinase Lyn[J]. Blood, 2007, 110(7):2511-9. |
| [16] | Bugajev V, BambouskováM, DráberováL, Dráber P. What precedes the initial tyrosine phosphorylation of the high affinity IgE receptor in antigen-activated mast cell[J]. FEBS Lett, 2010, 584(24):4949-5495. |
| [17] | Liao C, Hsu J, Kim Y, et al. Selective inhibition of spleen tyrosine kinase (SYK) with a novel orally bioavailable small molecule inhibitor, RO9021, impinges on various innate and adaptive immune responses:implications for SYK inhibitors in autoimmune disease therapy[J]. Arthritis Res Ther, 2013, 15(5):R146. |
| [18] | Rossi A B, Herlaar E, Braselmann S, et al. Identification of the Syk kinase inhibitor R112 by a human mast cell screen[J]. J Allergy Clin Immunol, 2006, 118(3):749-55. |
| [19] | Liu K J, He J H, Su X D, et al. Saracatinib (AZD0530) is a potent modulator of ABCB1-mediated multidrug resistance in vitro and in vivo[J]. Internat J Cancer, 2013, 132(1):224-35. |
| [20] | De Wispelaere M, LaCroix A J, Yang P L. The small molecules azd0530 and dasatinib inhibit Dengue virus RNA replication via fyn kinase[J]. J Virol, 2013, 87(13):7367-81. |
| [21] | Santos F P, Kantarjian H, Cortes J, Quintas-cardama A. Bafetinib, a dual Bcr-Abl/Lyn tyrosine kinase inhibitor for the potential treatment of leukemia[J]. Curr Opin Investig Drugs (London, England:2000), 2010, 11(12):1450-65. |
| [22] | Cota B B, Bertollo C M, de Oliveira D M. Anti-allergic potential of herbs and herbal natural products-activities and patents [J]. Recent Pat Endocr Metab Immune Drug Discovery, 2013,7(1):26-56. |
| [23] | 孙 丽. 靶向NF-κB信号通路抑制剂的中药筛选及欧当归内酯-A体外抗炎作用机制的研究[D]. 上海中医药大学硕士论文,2013. Sun L. Screening of NF-κB Inhibitor and Anti-inflammatory Mechanism of Levistilide A in vitro[D].Shanghai University Traditional Chinese Medicine, Master's thesis,2013. |
| [24] | Kim J W, Lee J H, Hwang B Y, et al. Morin inhibits Fyn kinase in mast cells and IgE-mediated type I hypersensitivity response in vivo[J]. Biochem Pharmacol, 2009, 77(9):1506-12. |
| [25] | Zhang N, Park D K, Park H J. The inhibitory activity of atractylenolide Ⅲ, a sesquiterpenoid, on IgE-mediated mast cell activation and passive cutaneous anaphylaxis (PCA)[J]. J Ethnopharmacol, 2013, 145(1):278-85. |
| [26] | Singh R, Masuda E S,Payan D G. Discovery and development of spleen tyrosine kinase (SYK) inhibitors[J]. J Med Chem, 2012, 55(8):3614-43. |
| [27] | Jelic D, Mildner B, KoŠtrun S, et al. Homology modeling of human Fyn kinase structure:discovery of rosmarinic acid as a new Fyn kinase inhibitor and in silico study of its possible binding modes[J]. J Med Chem, 2007, 50(6):1090-100. |
| [28] | Lu Y, Yang J H, Li X, et al. Emodin, a naturally occurring anthraquinone derivative, suppresses IgE-mediated anaphylactic reaction and mast cell activation[J]. Biochem Pharmacol, 2011, 82(11):1700-8. |
| [29] | Han E H, Hwang Y P, Kim H G, et al. Ethyl acetate extract of Psidium guajava inhibits IgE-mediated allergic responses by blocking FcεRI signaling[J]. Food Chem Toxicol, 2011, 49(1):100-8. |
| [30] | Han E H, Park J H, Kim J Y, et al. Houttuynia cordata water extract suppresses anaphylactic reaction and IgE-mediated allergic response by inhibiting multiple steps of FcεRI signaling in mast cells[J]. Food Chem Toxicol, 2009, 47(7):1659-66. |
| [31] | Han S Y, Bae J Y, Park S H, et al. Resveratrol inhibits IgE-mediated basophilic mast cell degranulation and passive cutaneous anaphylaxis in mice[J]. J Nutrit, 2013, 143(5):632-9. |

