


2. 国家中医药管理局重点研究室(心脑血管络病), 河北 石家庄 050035;
3. 河北省络病重点实验室, 河北 石家庄 050035;
4. 河北医科大学附属以岭医院(国家中医药管理局中医络病学重点学科), 河北 石家庄 050035
2. Key Research Center of State Administration of Traditional Chinese Medicine, Shijiazhuang 050035, China;
3. Key Laboratory of Collateral Disease of Hebei Province, Shijiazhuang 050035, China;
4. Yiling Hospital Affiliated to Hebei Medical University, Shijiazhuang 050035, China
胰岛作为一个高度血管化的器官,含有丰富的具有独特窗孔结构的微血管内皮细胞(IMECs)。IMECs除了为胰岛输送氧气、提供营养及运送内分泌激素外,其分泌的细胞因子还能够刺激和诱导胰岛β细胞增殖和成熟,因而对胰岛功能的维持具有至关重要的作用[1, 2]。近年来IMECs作为胰岛微循环的主要屏障细胞在糖尿病胰岛病理生理机制中的作用日益得到重视,我们课题通过前期动物实验证实了津力达联合通心络能够通过保护胰岛微血管及血管内皮形态结构从而改善胰岛β细胞功能 ,但其具体作用机制尚不明确。因此本研究利用高糖诱导胰岛微血管内皮细胞MS-1损伤模型,探讨津力达联合通心络对IMECs的保护作用并初步分析其作用机制,为其在2型糖尿病胰岛微血管病变临床防治中的应用提供可靠的实验数据。
1 材料与方法 1.1 材料与仪器小鼠胰岛微血管内皮细胞(MS-1),购自中国科学院典型培养物保藏委员会细胞库(目录号:GNM20);津力达干粉由石家庄以岭药业股份有限公司提供;通心络超微粉由石家庄以岭药业股份有限公司提供;高糖(25 mmol·L-1)、低糖(5.6 mmol·L-1)DMEM培养基干粉购自美国Gibco公司;胎牛血清购自美国Corning公司;胰蛋白酶购自美国AMRESCO公司;D(+)葡萄糖购自美国Sigma公司;一氧化氮(NO)测试盒(硝酸还原酶法)、丙二醛(MDA)测试盒(TBA法)、超氧化物歧化酶(SOD)试剂盒(测总)(羟胺法)购自南京建成生物工程研究所;Endothelin-1 Quantikine ELISA购自美国R&D公司;Cellular ROS/Superoxide Detection Assay Kit购自美国Abcam公司。Forma 371细胞培养箱购自美国Thermo Scientific公司;Avant1 J-26XP台式离心机购自美国BECKMAN公司;多功能酶标仪购自美国BioTek公司;SACSC libur流式细胞仪购自美国BD公司。
1.2 方法 1.2.1 药物配制称取津力达干粉、通心络超微粉溶于无血清DMEM培养基,超声促溶1 h,6 500×g离心10 min,收集上清液,0.22 μm微孔滤器过滤除菌,同时将所得沉淀于60℃条件加热烘干,计算实际溶于无血清DMEM培养基药物量,分别制备成30 g·L-1津力达贮存液和17 g·L-1通心络贮存液,-20℃贮存备用。
1.2.2 MS-1细胞培养MS-1细胞接种到含有胎牛血清(体积比9 ∶ 1),1×108 U·L-1青霉素,1×108 U·L-1硫酸链霉素和5×107 U·L-1庆大霉素的高糖(25 mmol·L-1)DMEM培养基中,于37℃、5% CO2培养箱培养,常规胰蛋白酶消化传代,备用。
1.2.3 津力达、通心络及津力达+通心络对MS-1细胞增殖的作用采用MTS法检测津力达(JLD)、通心络(TXL)及津力达+通心络(JLD+TXL)对MS-1细胞增殖的影响。取对数生长期的MS-1细胞以1.0×108·L-1的细胞浓度接种于96孔培养板中,每组4个复孔,每孔加入100 μL细胞悬液。培养24 h后,吸去培养基,加入100 μL相应溶液,其中津力达终浓度分别为50、100、150、200、300 mg·L-1,通心络终浓度分别为50、100、150、200 mg·L-1,继续培养48 h。吸弃上清培养基,加入含有MTS的无血清培养基100 μL(MTS溶液 ∶ 无血清培养基=1 ∶ 5),避光孵育45 min,酶标仪检测490 nm波长处OD值。细胞存活率/%=(各孔测定值/正常组平均值)×100 %。根据上述单独给药结果,选取津力达终浓度50、100、150、200、300 mg·L-1及通心络终浓度100 mg·L-1分别进行联合给药,培养及给药方法同上述。以上实验均重复3次。
1.2.4 津力达、通心络及津力达+通心络对高糖损伤MS-1细胞存活率的影响取对数生长期细胞接种于96孔板中(细胞密度1.0×108·L-1),每组4个复孔。5% CO2培养箱培养24 h,吸弃上清培养基,加入含体积分数0.01胎牛血清的低糖(5.6 mmol·L-1)DMEM培养基同步化培养24 h后用于实验。将细胞分为以下5组:Normal(5‰血清低糖培养基)、Model(5‰血清高糖50 mmol·L-1培养基)、JLD(高糖50 mmol·L-1+200 mg·L-1津力达)、TXL(高糖50 mmol·L-1+100 mg·L-1通心络)、JLD+TXL(高糖50 mmol·L-1+200 mg·L-1津力达+100 mg·L-1通心络)。模型建立前,各药物干预组加入含体积分数0.01胎牛血清的低糖含药DMEM培养基预先给药4 h,吸弃上清培养基后按照上述分组分别进行干预,继续培养48 h、1周、2周,每隔36 h更换1次培养基。检测时吸弃上清培养基,加入含有MTS的无血清培养基100 μL(MTS溶液 ∶ 无血清培养基=1 ∶ 5),避光孵育45 min,酶标仪检测490 nm波长处OD值。细胞存活率/%=(各孔测定值/正常组平均值) ×100 % ,实验重复3次。
1.2.5 津力达、通心络及津力达+通心络对高糖损伤MS-1细胞内皮功能、细胞上清SOD、MDA及细胞内ROS含量的作用取对数生长期细胞接种于96孔板(或6 cm培养皿)中(细胞密度1.0×108·L-1),每组4个复孔,5% CO2培养箱中孵育24 h后按照上述分组进行给药干预,继续培养48 h后收集细胞上清液,1 000 r·min-1离心2 min去除细胞碎片,取上清液采用硝酸还原酶法和酶联免疫吸附法分别检测NO及ET-1含量,羟胺法及TBA法检测SOD、MDA含量,实验操作步骤严格按照说明书进行。吸弃剩余培养基,生理盐水清洗贴壁细胞2次,加入胰蛋白酶消化后收集细胞,离心弃去上清,Wash Buffer重悬,加入含有绿色活性氧荧光探针(Ex/Em:490/525 nm)和橙色超氧荧光探针(Ex/Em:550/620 nm),避光37℃孵育30 min,流式细胞仪检测。实验重复3次。
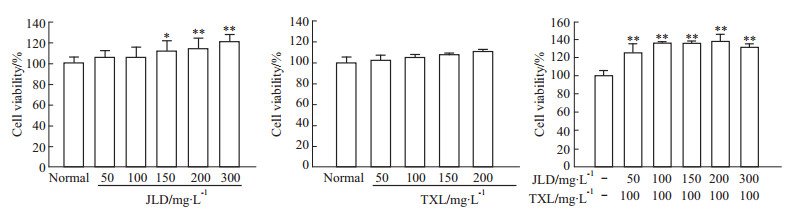
2 结果 2.1 JLD、TXL及JLD+TXL对MS-1细胞增殖的作用Fig1所示分别为JLD、TXL及JLD+TXL对MS-1细胞增殖的影响。由图中可以看出,MS-1细胞在不同浓度JLD、TXL及JLD+TXL作用下,细胞增殖率随药物浓度增加而逐渐升高,与正常组比较,JLD在150、200、300 mg·L-1浓度对MS-1细胞具有促增殖作用(P<0.05,P<0.01),JLD各浓度与TXL 100 mg·L-1联合给药对MS-1细胞均具有促增殖作用(P<0.01),其中以JLD 200 mg·L-1+TXL 100 mg·L-1作用最为明显(P<0.01)。TXL各浓度对MS-1细胞虽有一定促增殖作用,但与正常组比较无统计学意义。以上结果表明,JLD、JLD+TXL对MS-1细胞具有促增殖作用,并将JLD 200 mg·L-1、TXL 100 mg·L-1作为后续实验给药浓度。
|
Fig 1
Effect of JLD, TXL and JLD+TXL on proliferation of MS-1 cells ( ,n=4)
*P<0.05,**P<0.01 vs normal group ,n=4)
*P<0.05,**P<0.01 vs normal group
|
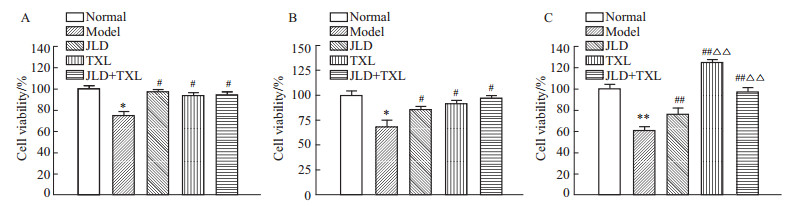
Fig2所示为JLD、TXL及JLD+TXL对高糖损伤MS-1细胞存活率的影响。与正常组比较,高糖诱导48 h、1周、2周模型组细胞存活率降低(P<0.05,P<0.01),且随着诱导时间延长细胞存活率逐渐降低。与模型组比较,JLD、TXL及JLD+TXL组升高48 h、1周、2周细胞存活率(P<0.05,P<0.01);与JLD组比较,培养至2周 TXL及JLD+TXL组细胞存活率升高(P<0.01)。
|
Fig 2
Effect of JLD, TXL, JLD+TXL on high glucose-induced injury of cell viability in MS-1 cells ( ,n=4)
A: Cell viability of each group after treated with high glucose for 48 h; B: Cell viability of each group after treated with high glucose for 1 w; C: Cell viability of each group after treated with high glucose for 2 w. *P<0.05, **P<0.01 vs normal group; #P<0.05, ##P<0.01 vs model group;△△P<0.01 vs JLD group ,n=4)
A: Cell viability of each group after treated with high glucose for 48 h; B: Cell viability of each group after treated with high glucose for 1 w; C: Cell viability of each group after treated with high glucose for 2 w. *P<0.05, **P<0.01 vs normal group; #P<0.05, ##P<0.01 vs model group;△△P<0.01 vs JLD group
|
与正常组比较,高糖诱导 48 h模型组细胞上清液NO含量降低,ET-1含量升高 (P<0.05,P<0.01),提示高糖诱导可引起内皮细胞功能损伤。JLD、TXL及JLD+TXL组升高细胞上清中NO含量,同时JLD、JLD+TXL组细胞上清液ET-1含量降低,且与模型组比较差异有显著性(P<0.05,P<0.01);与JLD、TXL组比较,JLD+TXL组NO含量升高,ET-1含量降低,且差异均具有统计学意义(P<0.01)。见Tab1。
 ,n=4)
,n=4)
 |
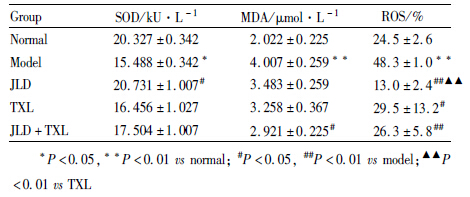
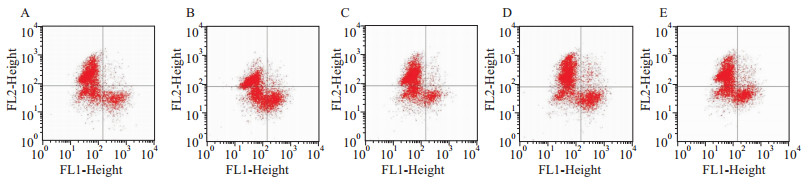
与正常组比较,高糖诱导48 h模型组细胞上清液SOD含量下降,同时上清液MDA含量及细胞ROS水平升高(P<0.05,P<0.01)。与模型组比较,各给药组不同程 度改善上述指标,其中JLD组升高细胞上清液SOD 含量(P<0.05);JLD+TXL组降低细胞上清液MDA含量(P<0.05);JLD、TXL及JLD+TXL组细胞内ROS水平均降低(P<0.05,P<0.01),与TXL组比较,JLD组细胞内ROS水平降低(P<0.01)。见Tab2、Fig3。
 ,n=4)
,n=4)
 |
|
| Fig 3 ROS levels of each group in MS-1 cells A: Normal group; B: Model group; C: JLD group; D: TXL group; E: JLD+TXL group. |
津力达颗粒是临床常用的治疗2型糖尿病的中药复方制剂,药用人参、黄精、麦冬、苍术等,既往临床及实验结果表明其具有有效控制血糖、调节脂质代谢、改善胰岛素抵抗、保护胰岛β细胞功能等作用[3, 4, 5, 6, 7]。而通心络胶囊作为通络药物的代表广泛应用于心脑血管疾病的防治,对于微血管损伤具有明显的保护作用,尤其是在保护微血管内皮细胞及其分泌功能方面显示出独特优势[8, 9, 10, 11, 12]。将二者联合应用于2型糖尿病胰岛微血管病变防治,将有可能为临床诊疗提供新的思路。本研究通过高糖诱导MS-1细胞损伤,并运用津力达联合通心络进行干预,初步探讨其保护MS-1细胞的作用及机制。
NO作为内皮细胞分泌的血管舒张因子,在神经信息传递、脏器血流调节、内分泌调节及机体防御和免疫应激等多方面发挥重要作用。生理状态下NO主要由内皮型一氧化氮合酶(eNOS)催化生成,主要作用是舒张血管和抑制血小板聚集。ET-1作为NO的拮抗剂,同样主要由血管内皮细胞分泌,主要维持血管基础张力,在心脑血管疾病及糖尿病血管并发症发病中发挥重要作用。本研究结果显示,经高糖损伤48 h IMECs细胞分泌NO减少,同时ET-1分泌增加,NO生物利用度下降,ET/NO之间动态平衡破坏,引起内皮细胞舒缩功能障碍。各给药组经干预后,JLD、TXL及JLD+TXL组细胞上清液中NO含量增加,JLD、JLD+TXL组上清中ET-1含量减少,其中以JLD+TXL组作用最为明显,且优于JLD及TXL组,表明津力达联合通心络能够有效改善高糖诱导的内皮细胞功能障碍。
既往观点认为高血糖导致血管病变主要通过多元醇通路、晚期糖基化终末产物途径、蛋白激酶C激活和己糖胺途径等4条经典途径。近年来氧化应激机制在糖尿病并发症中的重要作用备受关注,由于高糖长期作用引起线粒体呼吸链中氧自由基生成过多,导致PKC和NADPH氧化酶系统激活,引起组织细胞氧化应激损伤[13]。ROS作为氧元素在体内氧化还原反应的产物,当ROS产生增多、抗氧化物质减少及细胞自身修复能力降低时,IMECs由于氧化应激损伤而导致凋亡及坏死[14]。SOD作为生物体内重要的抗氧化酶,能够清除超氧阴离子自由基,对抗并阻断因氧自由基对细胞造成的损害。MDA是体内脂质过氧化的代表产物之一,能够间接反映细胞氧化损伤的程度。实验结果显示,高糖诱导模型细胞上清液中MDA含量及细胞内ROS水平升高,SOD含量降低,表明细胞存在明显氧化应激损伤。各给药组干预后细胞上清液中SOD、MDA含量及细胞内ROS水平均有不同程度改善,其中JLD组细胞上清SOD含量升高,同时细胞内ROS水平降低,TXL组细胞内ROS水平降低,但作用弱于JLD组,两药联合组细胞上清液MDA含量及细胞中ROS水平均降低。以上结果表明,津力达具有较强的抗氧化能力,能够有效清除氧自由基,同时减少细胞内ROS生成,通心络对高糖引起的细胞氧化应激损伤干预作用略显不足,但其在与津力达联合用药时可发挥协同效应,共同作用有效减轻细胞脂质过氧化损伤,减少ROS产生。综上,津力达联合通心络能够改善高糖诱导的氧化应激损伤,津力达在其中发挥着重要作用。
研究发现高糖导致内皮细胞损伤的机制主要涉及细胞内ROS和RNS水平的过度增高、线粒体功能紊乱、内质网应激过度激活、脂质过氧化、p-Akt 途径抑制及激活JNK、caspase-3等途径[15, 16, 17]。胞内氧化与抗氧化之间的平衡对维持细胞存活和功能发挥着至关重要的作用,当两者失衡将会导致大量ROS生成,诱导胞内相关信号通路发生改变,如基因调节、蛋白氧化损伤和脂质过氧化损伤等[18, 19]。本实验结果表明,津力达联合通心络能够改善高糖诱导胰岛微血管内皮细胞功能障碍,并通过减轻氧化应激损伤发挥细胞保护作用,其更深入的作用机制仍有待于进一步研究发现。
| [1] | Mattern H M, Hardin C D.Vascular metabolic dysfunction and lipotoxicity [J].Physiol Res, 2007, 56(2):149-58. |
| [2] | Artwohl M, Roden M, Waldhäusl W, et al.Free fatty acid strigger apoptosis and inhibit cell cycle progression in human vascular endothelial cells[J].FASEB J, 2004, 18(1):146-8. |
| [3] | 高玉芳, 冯书文, 平阳, 等.中药津力达丸与西药联合应用消除2型糖尿病高血糖毒性的临床观察[J].河北中医, 2006, 28(2):120-1. Gao Y F, Feng S W, Ping Y, et al.Clinical observation of traditional Chinese medicine Jinlida pill combine with western medicine on eliminating toxic of hyperglycemia in type 2 diabetes[J].Hebei J Tradit Chin Med, 2006, 28(2):120-1. |
| [4] | 高学东, 田野, 谷春华, 等.津力达颗粒对2型糖尿病胰岛素抵抗和胰岛β细胞功能的影响[C].石家庄:第九次全国中医糖尿病学术大会论文汇编, 2006:802-4. Gao X D, Tian Y, Gu C H, et al.Effect of Jinlida granule on insulin resistance and islet beta cell function in type 2 diabetes[C].Shijiazhuang:Proceedings of the ninth national diabetes academic conference of TCM, 2006:802-4. |
| [5] | 高怀林, 张建军, 吴以岭, 等.津力达颗粒对2型糖尿病胰岛β细胞功能的影响[J].时珍国医国药, 2010, 21(5):1119-20. Gao H L, Zhang J J, Wu Y L, et al.Effect of Jinlida granule on islet beta cell function in type 2 diabetes[J].Lishizhen Med Mat Med Res, 2010, 21(5):1119-20. |
| [6] | 吴以岭, 张会欣, 王宏涛, 等.津力达口服液对实验性2型糖尿病大鼠降糖作用及其机制的研究[C].石家庄:第九次全国中医糖尿病学术大会论文汇编, 2006:805-9. Wu Y L, Zhang H X, Wang H T, et al.Hypoglycemic effect and mechanism of Jinlida oral liquid on experimental type 2 diabetic rats[C].Shijiazhuang:Proceedings of the ninth national diabetes academic conference of TCM, 2006:805-9. |
| [7] | 史婧丽, 吴莹, 宋玉萍, 等.津力达颗粒对糖尿病大鼠胰岛B细胞的保护作用[J].第二军医大学学报, 2012, 33(4):385-9. Shi J L, Wu Y, Song Y P, et al.Protective effect of Jinlida granule on B cells in diabetic rats[J].Academ J Second Mil Med Univ, 2012, 33(4):385-9. |
| [8] | 吴以岭, 袁国强, 游佳华, 等.通心络超微粉对高脂饮食兔主动脉内皮保护机制的实验研究[J].中国病理生理杂志, 2007, 23(4):629-33. Wu Y L, Yuan G Q, You J H, et al.The protective effect of tongxinluo superfine powder on aorta endodermis in rabbits fed with fatty[J].Chin J Pathophysiol, 2007, 23(4):629-33. |
| [9] | Li X D, Yang Y J, Geng Y J, et al.Tongxinluo reduces myocardial no-reflow and ischemia-reperfusion injury by stimulating the phosphorylation of eNOS via the PKA pathway[J].Am J Physiol Heart Circ Physiol, 2010, 299(4):H1255-61. |
| [10] | 袁国强, 王玲玲, 杨海涛, 等.p38 MAPK通路在TNF-α诱导人脐静脉内皮细胞分泌ET-1与eNOS中的作用及通心络干预影响[J].中国药理学通报, 2009, 25(11):1415-20. Yuan G Q, Wang L L, Yang H T, et al.The role of p38MAPK signal pathway in the course of TNF-α inducing HUVEC to secrete ET-1 and eNOS and the effect of Tongxinluo[J].Chin Pharmacol Bull, 2009, 25(11):1415-20. |
| [11] | Liang J Q, Xu H B, Wu Y L, et al.Effect of serum from overfatigue rats on JNK/c-Jun/HO-1 pathway in human umbilical vein endothelial cells and the intervening effect of Tongxinluo superfine powder[J].Chin J Integr Med, 2009, 15(2):121-7. |
| [12] | 梁俊清, 徐海波, 陈小娟, 等.通心络通过PI-3K/Akt/HIF信号通路改善血管内皮细胞缺氧损伤[J].中国病理生理杂志, 2012, 28(5):846-51. Liang J Q, Xu H B, Chen X J, et al.Tongxinluo improves anti-hypoxia ability of vascular endothelial cells via PI-3K/Akt/HIF pathway[J].Chin J Pathophysiol, 2012, 28(5):846-51. |
| [13] | Brewnlee M.The pathobiology of diabetic complication:a unifying mechanism[J].Diabetes, 2005, 54(6):1615-25. |
| [14] | Ma Q, Fang H, Shang W, et al.Superoxide flashes:early mitochondrial signals for oxidative stress-induced apoptosis[J].J Biol Chem, 2011, 286(31):27573-81. |
| [15] | Symons J D, McMillin S L, Riehle C, et al.Contribution of insulin and Akt1 signaling to endothelial nitric oxide synthase in the regulation of endothelial function and blood pressure[J].Circ Res, 2009, 104(9):1085-94. |
| [16] | Favaro E, Miceli I, Bussolati B, et al.Hyperglycemia induces apoptosis of human pancreatic islet endothelial cells:effects of pravastatin on the Akt survival pathway[J].Am J Pathol, 2008, 173(2):442-50. |
| [17] | Gong L, Liu F Q, Wang J, et al.Hyperglycemia induces apoptosis of pancreatic islet endothelial cells via reactive nitrogen species-mediated Jun N-terminal kinase activation[J].Biochim Biophys Acta, 2011, 1813(6):1211-9. |
| [18] | Singh U, Jialal I.Oxidative stress and atherosclerosis[J].Pathophysiology, 2006, 13(3):129-42. |
| [19] | Shrilatha B, Muralidhara.Occurrence of oxidative impairments, response of antioxidant defences and associated biochemical perturbations in male reproductive milieu in the Streptozotocin-diabetic rat[J].Int J Androl, 2007, 30(6):508-18. |

