


2. 江苏省中医药研究院,江苏 南京 210028;
3. 南京中医药大学江苏省方剂高技术研究重点实验室,江苏 南京 210023
2. Jiangsu Provincial Academy of Traditional Chinese Medicine,Nanjing 210028,China;
3. Jiangsu Key Laboratory for High Technology Research of TCM Formulae,Nanjing University of Chinese Medicine,Nanjing 210023,China
甘遂始载于《神农本草经》,言其“味苦寒,主大腹疝瘕,腹满,面目浮肿,留饮宿食,破症坚积聚,利水谷道”。现行药典记载甘遂为大戟科(Euphobiaceae)大戟属(Euphorbia)植物甘遂(Euphorbia kansui,EK)的干燥块根,具有泻水逐饮的功能。用于水肿胀满、胸腹积水、痰饮积聚、气逆咳喘、二便不利[1]。毒性研究表明,过量使用易引起腹痛、腹泻,严重时会出现剧烈呕吐、血压下降、脱水和呼吸衰竭等症状。功效研究表明,甘遂化学成分具有抗癌抗肿瘤活性、抗病毒、抗胰腺炎等作用,亦可影响免疫系统的特异性[2]。
中药配伍禁忌概括为歌诀“本草名言十八反,半蒌贝蔹及攻乌,藻戟遂芫俱战草,诸参辛芍叛藜芦”最早见于金元时期张子和的《儒门事亲·卷十四·十八反》。“甘遂反甘草(Glycyrrhiza uralensis,GU)”为中药配伍禁忌之一,但从古到今,不断有医家报道配伍使用后无明显毒副作用,而实验研究的结果亦不尽相同[3, 4]。后世医家对其从各个角度进行了的实验验证。对大鼠心、肝、肾病理形态影响显示存在较明显毒性增强的情况[5]。
目前研究报道,甘遂主要化学成分主要为二萜类和三萜类化合物。活性研究也主要是针对二萜类和三萜类化合物的单体成分进行的。研究表明,二萜类化合物有较强的刺激作用,但也有抗肿瘤活性,提示其毒性成分与有效成分之间有一定的内在联系。三萜类成分也具有一定的药理活性,但其毒性方面的研究较少。甘遂本身所含巨大戟萜醇及其衍生物和一些二萜酯类如甘遂萜酯A、甘遂萜酯B均为毒性成分,具有激活EB病毒早期抗原活性、皮肤刺激及促进肿瘤发生作用[6]。所以,甘遂毒性成分的代谢可能影响其毒性作用。甘遂与甘草合用,可能影响了参与甘遂毒性成分代谢的酶,而使甘遂毒性成分代谢减慢,产生蓄积,导致毒性增强。本实验拟从甘草与甘遂合用对甘遂中毒性成份代谢的影响的角度入手,阐明二者合用增毒的可能原因。
1 材料与方法 1.1 试剂与仪器 1.1.1 仪器Waters Acquity UPLC(美国Waters公司),XevoTriple四极杆检测器(美国Waters公司),配置电喷射离子源(ESI),自动进样器,MS/MS检测器,MassLynx软件;METTER AL104电子天平(梅特勒—托利多仪器上海有限公司);XW-80A型漩涡混合器(上海沪西分析仪器厂有限公司);Milli-Q Gradient A10超纯水器(Millipore Inc. USA);AllegraTM 21R Centrifuge台式离心机(BECKMAN COULTERTM)。
1.1.2 试剂甘草水提物,甘遂95%醇提物由南京中医药大学江苏省方剂高技术研究重点实验室提供。甘遂萜酯A、甘遂萜酯B、甘草酸、甘草次酸由南京中医药大学江苏省方剂高技术研究重点实验室提供,红霉素、盐酸苯海拉明、苯溴马隆、西咪替丁和氟康唑购于中国药品检验所。
甘遂萜酯A、甘遂萜酯B的配制:精密称取KA、KB粉末各1 mg,加入200 μL DMSO溶解后,加PBS定容至1 mL。配制成1.0 g·L-1的储备液。
甘草酸和甘草次酸的配制:精密称取甘草酸1 mg,加热水溶解并定容至10 mL,终浓度为100 mg·L-1的应用液,临用现配,并置于热水浴中保持溶解性;精密称取甘草次酸1 mg,加入100 μL乙醇溶解后,加入PBS定容至1 mL浓度为1 g·L-1。红霉素、盐酸苯海拉明、苯溴马隆、西咪替丁和氟康唑的配制:均用PBS配制成1.0 g·L-1的溶液。
1.2 实验动物与分组健康♂ Sprague-Dawley大鼠,体质量180~200 g,由上海西普尔—必凯实验动物中心提供。自然昼夜环境饲养,给予标准饲料,自由摄食、饮水,室温保持(22±2)℃,相对湿度为50%~60%。动物实验由南京中医药大学动物伦理委员会批准实施。动物随机分组3组,分别为正常对照组、甘草组、甘遂与甘草合用组,每组6只。
1.3 给药方法与剂量按组别灌胃给予相应药物提取物,正常对照组给予0.25%的CMC-Na溶液。甘草组为10 g生药·kg-1,甘遂与甘草合用组为20 g生药·kg-1。连续灌胃给予各组提取物10 d,每天1次。于末次给药8 h后禁食16 h。
1.4 肝微粒体的制备采用差速离心法制备肝微粒体[7, 8]。动物于末次给药8 h后开始禁食,禁食16 h后,采用乙醚麻醉各组大鼠,股动脉放血后,颈椎脱臼处死,迅速取下肝组织,置于0~4℃冰板上。将肝组织剪碎,用0.15 mol·L-1 KCl-0.1 mol·L-1磷酸盐缓冲液反复冲洗3次,除去血红蛋白后加入上述磷酸盐缓冲液制成肝匀浆,在4℃下以9 000×g离心20 min后,取上清液,于4℃下以100 000×g 离心60 min,将粉红色沉淀物(微粒体)悬浮于含30%甘油的磷酸盐缓冲液中,使用Bradford法[9]测定试剂盒测定肝微粒体蛋白浓度,分装后置于-80℃冰箱内保存。
1.5 体外孵育法研究甘遂与甘草合用对甘遂中毒性成分KA、KB的影响KA、KB分别与正常对照组大鼠肝微粒体、甘遂处理组肝微粒体和甘草与甘遂合用组肝微粒体共孵育。反应体系中含NADPH再生系统(NADP 500 μmol·L-1,G-6-P 10 mmol·L-1,G-6-P-OH 1 kU·L-1,MgCl2 0.5 mmol·L-1),微粒体蛋白终浓度为1 g·L-1。先将反应体系置于37℃水浴预温孵5 min后,加入KA、KB启动反应,KA、KB的终浓度均为2.0 mg·L-1。孵育30 min后,加入50 μL乙腈中止反应。反应总体积为200 μL。
1.6 CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19的抑制剂对KA、KB代谢的影响取正常大鼠肝微粒体,反应体系中含微粒体蛋白终浓度为1 g·L-1、NADPH再生系统(NADP 500 μmol·L-1,G-6-P 10 mmol·L-1,G-6-P-OH 1 kU·L-1,MgCl2 0.5 mmol·L-1)。分别加入CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19的抑制剂红霉素、盐酸苯海拉明、苯溴马隆、西咪替丁和氟康唑,终浓度均为100 mg·L-1。于37℃预温孵5 min,加入KA、KB启动反应,温孵30 min后,加入50 μL乙腈中止反应。KA、KB的终浓度均为 2.0 mg·L-1。反应总体积为200 μL。
1.7 体外孵育法研究甘草酸、甘草次酸对KA、KB代谢的影响取正常大鼠肝微粒体,反应体系中含微粒体蛋白终浓度为1 g·L-1、NADPH再生系统(NADP 500 μmol·L-1,G-6-P 10 mmol·L-1,G-6-P-OH 1 kU·L-1,MgCl2 0.5 mmol·L-1)。分别加入甘草酸和甘草次酸,于37℃预温孵5 min,加入KA、KB启动反应,温孵30 min后,加入50 μL乙腈中止反应。KA、KB的终浓度均为 2.0 mg·L-1。甘草酸和甘草次酸的终浓度均为10 mg·L-1。反应总体积为200 μL。
1.8 色谱条件及MS质谱条件色谱柱为ACQUITY UPLC BEH C18 柱(100 mm×2.1 mm,1.7 μm);流动相为0.1%甲酸水-乙腈=40 ∶ 60;流速:0.4 mL·min-1;柱温:30℃;ESI-MS采用正离子检测的电喷雾电离方式;KA、KB的锥孔电压分别为44V和56V;去溶剂化温度为550℃;去溶剂化气流为1 000 L·h-1。在该色谱条件下,KA和KB的保留时间分别约为3.909 min和5.932 min (R>1.5),分离较好,且血浆中的内源性物质不干扰KA、KB的测定。
1.9 统计学处理采用SPSS 16.0软件包进行数据统计分析。实验数据以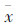 ± s表示,组间比较采用方差分析,组间两两比较采用t检验。
± s表示,组间比较采用方差分析,组间两两比较采用t检验。
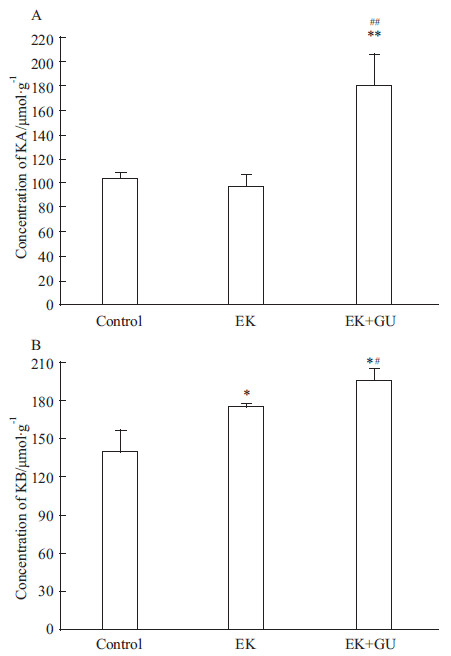
将甘遂中毒性成分KA、KB分别与正常对照组(Control)、甘遂组(EK)、甘遂与甘草合用组(EK+GU)微粒体体外共孵育,测定孵育后体系中KA、KB的浓度。KA、KB在各组中的浓度见Fig1。结果显示,甘遂组微粒体中KA的浓度与正常对照组间差异无显著性,而甘遂与甘草合用组微粒体 中KA的浓度明显高于正常对照组和甘遂组,表明合用使KA的代谢受到抑制;甘遂组微粒体中KB的浓度高于正常对照组,表明单独使用甘遂可使KB的代谢减慢,而甘遂与甘草合用组KB的浓度明显高于正常对照组与甘遂组,表明合用使KB的代谢受到抑制的程度增加。
|
| Fig.1 Concentration of KA (A) and KB (B) in hepatic microsomes of treated and control rats. Incubation mixture consisted of microsomal protein (1 g·L-1) Treated rats were prepared as described in Materials and Methods. Data represent the mean ± SD of two different preparations. *P<0.05, **P<0.01 vs control; #P<0.05,##P<0.01 vs EK. |
取正常大鼠肝微粒体,分别加入CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19的抑制剂红霉素、盐酸苯海拉明、苯溴马隆、西咪替丁和氟康唑,与KA、KB体外共孵育,测定孵育后体系中KA、KB的浓度。孵育后,KA、KB在各组中的浓度见Fig2。结果显示,各组微粒体中KA、KB的含量均明显高于空白对照组,表明CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19的活性受到抑制,KA、KB的代谢均减慢,CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19均可能参与了KA、KB的代谢,其中CYP2C9对KA代谢 的影响最为明显,CYP2C19对KB代谢的影响最为明显。由此可以推测,甘遂与甘草合用抑制了CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19等酶的活性,从而使甘遂中毒性成分KA、KB的代谢减慢,产生蓄积,最终导致甘遂毒性增加。这可能是甘遂与甘草合用增毒的原因之一。

|
| Fig.2 Concentration of KA (A) and KB (B) in hepatic microsomes with enzyme inhibitors of CYP3A4,CYP2D6,CYP2C9,CYP1A2 and CYP2C19 Incubation mixture consisted of microsomal protein (1 g·L-1). Treated rats were prepared as described in Materials and Methods. Data represent the mean ± SD of two different preparations. *P<0.05, **P<0.01 vs control. |
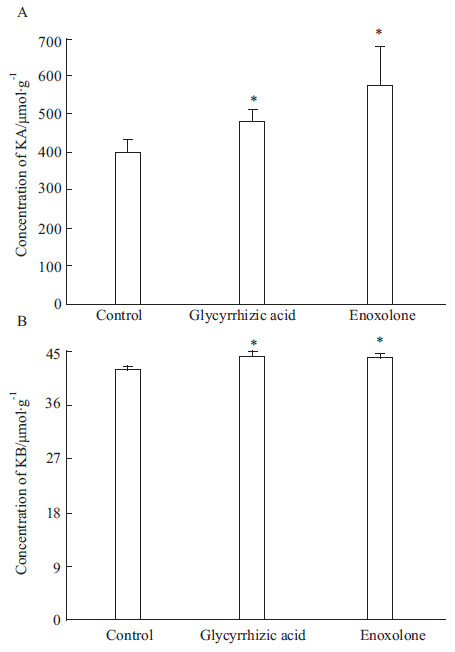
取正常大鼠肝微粒体,分别加入甘草酸和甘草次酸与KA、KB共孵育,测定孵育后体系中KA、KB的浓度。KA、KB在各组中的浓度见Fig3。结果显示,加入甘草酸和甘草次酸,温孵体系中KA、KB的浓度明显高于正常对照组,表明甘草酸和甘草次酸能够抑制KA、KB的代谢。
|
| Fig.3 Concentration of KA (A) and KB (B) in hepatic microsomal incubates with glycyrrhizic acid and enoxolone Incubation mixture consisted of microsomal protein (1 g·L-1). Treated rats were prepared as described in Materials and Methods. Data represent the mean ± SD of two different preparations. *P<0.05 vs control. |
本实验通过微粒体体外孵育的方法,研究甘遂与甘草合用对甘遂中毒性成分KA、KB代谢的影响,结果表明,甘遂与甘草合用使KA、KB的代谢受 到抑制;KA、KB分别与CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19的抑制剂红霉素、盐酸苯海拉明、苯溴马隆、西咪替丁和氟康唑体外共孵育,测定孵育后体系中KA、KB的浓度,以确定是哪种酶的亚型参与了KA、KB的代谢。结果表明,几种酶亚型均参与了KA、KB的代谢,以CYP2C9和CYP2C19影响最为明显。甘遂与甘草合用可能抑制了CYP3A4、CYP2D6、CYP2C9、CYP1A2、CYP2C19当中一种或几种酶的活性,从而使甘遂中毒性成分KA、KB的代谢减慢,产生蓄积,最终导致甘遂的毒性增加。这可能是甘遂与甘草不能合用的原因之一。
有研究表明,甘遂化学部位GS-3可明显促进脾淋巴细胞增殖,证明GS-3为甘遂致炎的毒性部位群。用HPLC-MSn色谱技术对GS-3部位进行化学组成分析,结果共鉴定了其中的12个二萜类化合物[10]。为进一步阐明甘遂毒效作用的物质基础,采用硅胶柱层析和制备液相等多种色谱手段对甘遂毒性部位进行了化学分离。结果共分离鉴定了8个化合物,甘遂萜酯A和甘遂萜酯B为其中两个。有文献报导二萜酯类如甘遂萜酯A、甘遂萜酯B均为毒性成分[6],故我们选择甘遂萜酯A、甘遂萜酯B为目标化合物,考察甘遂与甘草合用对KA、KB两个毒性物质代谢的影响,来阐明合用增毒的原因。
“甘草能解百药毒”、“十方九草”是中医方剂配伍解毒、调和药性之经典认识。然而,“十八反”则告诫人们海藻、大戟、甘遂、芫花与甘草相对立不宜伍用。研究表明,“藻戟遂芫俱战草”致毒、增毒效应可能的作用机制有:(1)诸药与甘草配伍后其有毒物质可能与甘草中的甘草酸通过氢键形成复合物,以及具有表面活性的甘草三萜酸均有助于毒性成分的溶出,使其在水煎剂中的含量增高;(2)甘草在一定条件下或可稳定大戟、甘遂毒性成分二萜醇(酯)和二萜原酸酯类成分的存在状态,或延缓其毒性成分在体内的消除速率而蓄积增毒。然而,甘草中主要成分甘草酸和甘草次酸对甘遂中毒性成分代谢的影响还未见报道。我们的实验采用体外微粒体温孵的方法考察甘草酸和甘草次酸对KA、KB代谢的影响,以从两味药单体成分相互作用这一角度阐明合用增毒的可能原因。
当然,中药成分非常复杂,对中药有效成分进行细胞色素P450酶多种亚型的研究及药物相互作用研究还不能够全面阐释中药相互作用的原因。中药间、中西药间及中药各成分间的相互作用尚需通过深入研究其对药物代谢酶系统的影响规律,进而阐明中药相互作用、毒副作用发生的分子机制及科学内涵,为中医药相互作用机制赋予现代的、科学的解释,为临床合理用药提供理论基础,提高中药使用的安全性和有效性[11]。
| [1] | 国家药典委员会.中国药典(一部)[S].北京:化学工业出版社, 2005:60.Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (Volume Ⅰ)[S]. Beijing:Chemical Industry Press, 2005:60. |
| [2] | 郭晓庄.有毒中草药大辞典[S].天津:天津科技翻译出版公司, 1992:739.Guo X Z. Toxic herbal Dictionary[S]. Tianjin:Tianjin Science and Technology Translation and Publishing Corporation, 1992:739. |
| [3] | 李兴玉.医学分子生物学[M].兰州:兰州大学出版社, 1999:290.Li X Y. Medical Molecular Biology[M]. Lanzhou:Lanzhou University Press, 1999:290. |
| [4] | 杨惠玲.高级病理生理学[M].北京:科学出版社, 1998:24-30.Yang H L. Advanced Pathophysiology[M]. Beijing:Science Press, 1998:24-30. |
| [5] | 黄文权, 程相岭, 肖鸿, 等.甘草甘遂伍用对大鼠心肝肾功能及形态的影响[J]. 第三军医大学学报, 2001, 23(12):1439-41.Huang W Q, Cheng X L, Xiao H, et al. Effect of licorice and kansui combination on functions and morphology of rat hearts, livers and kidneys[J]. Acta Acad Med Mil Tert, 2001, 23(12):1439-41. |
| [6] | 聂淑琴, 李泽琳, 梁爱华, 等.炮制对甘遂、牛膝、苦杏仁特殊毒性及药效的影响[J].中国中药杂志, 1996, 21(3):153-6.Nie S Q, Li Z L, Liang A H, et al. Effects of processing on specific toxieity and pharmaeodynamics of Radix Kansui, RadixAchyranthis Bidentae and Semen Armeniacae Amarum[J]. China J Chin Mat Med, 1996, 21(3):153-6. |
| [7] | Liu X Q. Metabolism and metabolic inhibition of clinipine in human hepatic microsomes[J]. Acta Pharmacol Sin, 2003, 24(1):263-8. |
| [8] | 王新敏, 彭蕴茹, 景欣悦, 等. HPLC法测定大鼠血浆、微粒体中非那西丁与其代谢物含量及其应用[J]. 中国药理学通报, 2013, 29(4):591-2.Wang X M, Peng Y R, Jing X Y, et al. HPLC determination of phenacetin and its metabolite in rat plasma and microsome and its application[J]. Chin Pharmacol Bull, 2013, 29(4):591-2. |
| [9] | Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J].Anal Biochem, 1976, 72:248-54. |
| [10] | Zhang L, Shu X Y, Ding A W, et al. LC-DAD-ESI-MS-MS separation and chemical characterization of the inflammatory fraction of the roots of Euphorbia kansui[J]. Chromatographia, 2009, 70 (5-6):805-10. |
| [11] | 韩永龙, 李 丹, 孟祥乐, 等.中药复方对细胞色素P450酶的调控研究进展[J].中药材, 2009, 32(10):1638-42. Han Y L, Li D, Meng X L, et al. Regulation of traditional Chinese medicine on the cytochrome P450 enzyme progress[J]. J Chin Med Mat, 2009, 32(10):1638-42. |

