文章信息
- 王一凡, 刘爽, 汪思齐, 李茂娟, 黄春华, 楼迪栋
- WANG Yifan, LIU Shuang, WANG Siqi, LI Maojuan, HUANG Chunhua, LOU Didong
- 急性马兜铃酸中毒小鼠肾损伤及Wnt7b/β-catenin/MMP-7的表达变化
- Renal injury and expression of Wnt7b/β-catenin/MMP-7 in mice with acute aristolochic acidosis
- 中国医科大学学报, 2023, 52(6): 505-511
- Journal of China Medical University, 2023, 52(6): 505-511
-
文章历史
- 收稿日期:2022-09-30
- 网络出版时间:2023-05-25 16:12:57
2. 贵州省法医中药毒理学特色重点实验室,贵阳 550000
2. Guizhou Provincial Key Laboratory of Forensic Medicine Toxicology, Guiyang 550000, China
马兜铃酸(aristolochic acids,AA) 是马兜铃科中药材的主要毒性成分,能引起肾损伤和纤维化[1]。其中AAⅠ的毒性最大[2],摄入含有AA的中草药引起的急性或慢性肾小管间质疾病被称为AA肾病(aristolochic acid nephropathy,AAN) [3-5]。临床上对含有AA中草药的使用有严格的规范,但相关中毒事件仍有发生[6],如未及时治疗会发展为慢性肾功能衰竭,最终形成终末期肾病[7]。
Wnt通路在机体发育、损伤修复过程中发挥着重要作用[8]。研究表明,Wnt7b能够促进肾脏发育过程中肾小管的增殖分化[9],参与斑马鱼肾脏损伤后的再生修复[10],但Wnt7b在哺乳动物致肾脏损害发展过程中的作用机制仍缺乏基础研究。本研究通过连续观察急性AAN不同时期和部位的肾脏病理改变及Wnt7b相关蛋白的表达变化,探讨急性AAN过程中的组织病理特征和Wnt7b通路作用机制,为明确AA的毒理机制提供参考依据。
1 材料与方法 1.1 药物和试剂AAⅠ标准品(纯度96%,四川省维克奇生物科技有限公司),溶于二甲基亚砜(北京索莱宝科技有限公司) 与0.4%羧甲基纤维素钠(上海展云化工有限公司) 中,制成2 mg/mL AAⅠ悬浊液。HE染色液(北京索莱宝科技有限公司),免疫组化(immunohistochemistry,IHC) SP试剂盒(北京中杉金桥生物技术有限公司),Wnt7b兔多克隆抗体(赛默飞世尔科技中国有限公司),β-catenin鼠多克隆抗体(武汉三鹰生物技术有限公司),基质金属蛋白酶-7 (matrix metalloproteinase-7,MMP-7) 兔多克隆抗体(武汉三鹰生物技术有限公司)。
1.2 实验动物雄性KM小鼠(长沙市天勤生物技术公司) 113只,8周龄,质量(32±5) g,于贵州中医药大学实验动物中心饲养,常温环境,自由摄食、饮水。实验过程严格按照《实验动物福利伦理审查指南(GB/T358922018) 》要求执行。
1.3 动物分组及给药将113只KM小鼠于笼中适应性喂养3 d,自由进食进水。
1.3.1 生存曲线给药方式将75只小鼠随机分为5组(n = 15),每组小鼠分别灌胃给药AAⅠ20 mg/(kg·d)、15 mg/(kg·d)、10 mg/(kg·d)、5 mg/(kg·d) 及0 mg/(kg·d) (溶剂对照)。
1.3.2 急性AAⅠ中毒模型给药方式将48只小鼠随机分为2组(n = 24),溶剂对照组小鼠灌胃给药AAⅠ 0 mg/(kg·2 d),模型组小鼠灌胃给药AAⅠ 5 mg/(kg·2 d)。
1.4 样本采集用药后,对照组和模型组的小鼠各随机取6只分别于第2、4、6和8天戊巴比妥钠腹腔注射麻醉,颈椎脱臼处死,摘眼球取血后,用PBS和固定液全身灌注,取双侧肾组织样本,沿矢状面分为2份,PBS冲洗,一份浸入4%多聚甲醛固定,另一份用2.5%戊二醛固定。
1.5 肾功能检测将采集的血液标本1 200 r/min 4 ℃离心10 min,取上清,用mindray生化免疫流水线检测其血肌酐和尿素氮含量。
1.6 组织病理学染色将4%多聚甲醛固定的肾脏组织经乙醇梯度脱水、二甲苯透明、浸蜡、包埋后切片(切片厚度2~4 µm),进行HE染色与Masson染色,光学显微镜下观察肾脏组织病理变化,并对肾小管损害指标等计数统计。
1.7 IHC染色切片样本放置于60 ℃烘箱中融蜡2 h,二甲苯脱蜡、乙醇梯度脱水。PBS冲洗后,置于100 ℃的柠檬酸缓冲液(pH6) 中,微波炉高火加热20 min,PBS浸洗。随后滴加内源性过氧化物阻断酶室温孵育,PBS浸洗。分别加入Wnt7b (1∶200)、β-catenin (1∶200) 和MMP-7 (1∶100) 3种蛋白的一抗,4 ℃冰箱孵育过夜,结束后用PBS浸洗。滴加生物素标记山羊抗小鼠/兔IgG,37 ℃孵育15 min,PBS浸洗,滴加辣根酶标记链霉素工作液,37 ℃孵育15 min,PBS浸洗。滴加DAB显色液,PBS浸洗终止染色,苏木素复染,酒精梯度脱水,二甲苯透明,封片。用ImageJ软件对IHC图像进行分析统计。
1.8 免疫电镜将组织从2.5%戊二醛固定后取出,乙醇梯度脱水,树脂渗透后进行包埋。超薄切片机切成70~80 nm超薄切片,超纯水悬浮5 min,进行复温后TBS清洗,用1%BSA封闭液室温封闭30 min,加入Wnt7b (1∶200) 和β-catenin (1∶200) 4 ℃过夜孵育,TBS清洗,加入4 nm胶体金羊抗鼠抗体(抗β-catenin) 和12 nm胶体金羊抗兔抗体(抗Wnt7b),37 ℃烘箱孵育1 h,TBS清洗。铀复染后用70%乙醇清洗,滤纸吸干后放入网板中,透射电子显微镜下观察并采集图像。
1.9 统计学分析Masson染色和IHC的图像参考DESHPANDE等[11]的方法,采用ImageJ软件对光密度平均值进行统计,用随机区域计数法对HE图像和IHC图像计数统计。采用SPSS 24.0软件进行统计分析,数据均以x±s表示,多组间统计学差异(方差齐性检验后) 采用单因素方差分析比较。P < 0.05为差异有统计学意义。
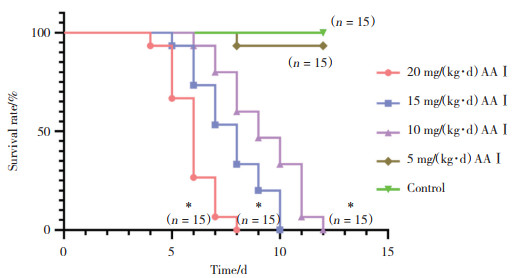
2 结果 2.1 AAⅠ与小鼠生存曲线将小鼠暴露于不同浓度的AAⅠ中,AAⅠ的浓度与小鼠生存时间呈负相关。当小鼠灌胃的AAⅠ浓度为20 mg/(kg·d) 时,小鼠表现出急性毒性效应,5~8 d出现高死亡率。当AAⅠ浓度降至10 mg/(kg·d) 时,小鼠的死亡率稍降低,当AAⅠ的浓度降至5 mg/(kg·d) 时,小鼠生存率显著上升;3组生存曲线与对照组相比有统计学差异(P均 < 0.05),见图 1。
|
| *P < 0.001 vs control group. 图 1 各组生存曲线 Fig.1 Survival curves of all groups |
2.2 小鼠肾脏生化指标
血清肌酐和尿素氮检测结果显示,模型组血清肌酐在小鼠暴露于AAⅠ 6~8 d时出现显著上升,8 d时为对照组的25倍,尿素氮也随着小鼠暴露于AAⅠ的时间增加,8 d时出现统计学差异(P < 0.05)。见表 1。
| Item | Control | Acute AAⅠ poisoning model groups | |||
| 2 d | 4 d | 6 d | 8 d | ||
| Creatinine (μmol/L) | 1.60±0.36 | 3.13±0.32 | 6.50±0.53 | 21.27±6.841) | 40.63±5.651) |
| Urea nitrogen (mmol/L) | 6.19±0.42 | 7.03±0.48 | 8.85±0.44 | 12.52±2.04 | 44.93±8.621) |
| 1) P < 0.05 vs control group. | |||||
2.3 小鼠肾脏组织病理学
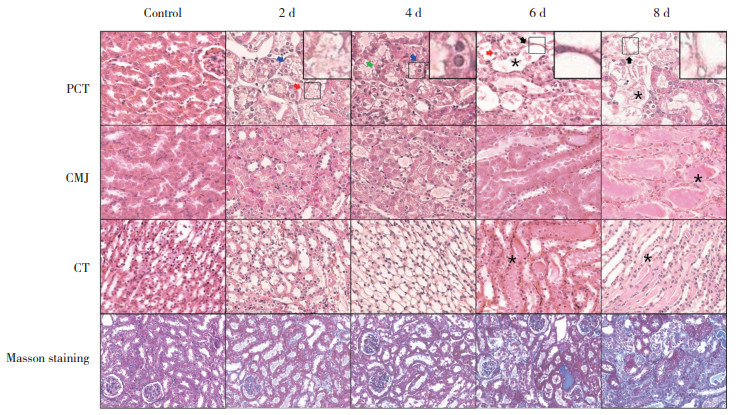
HE染色结果显示,小鼠肾小管损伤程度随着AAⅠ暴露时间增加而加重,肾小球无明显改变;暴露于AAⅠ 2 d后,50%以上近端小管(proximal convoluted tubule,PCT) 刷状缘破坏,伴部分上皮细胞水肿,空泡样变性;4 d时85%以上的PCTEC水肿,并出现少量坏死;6 d时坏死的PCT上皮细胞(proximal convoluted tubule epithelial cells,PCTEC) 逐渐从基底膜脱落;8 d时PCTEC坏死脱落增加,肾小管出现大量基底膜裸露,管型数量增加(P < 0.05)。皮髓交界(corticomedullary-junction,CMJ) 在暴露于AAⅠ 6~8 d时出现大量管型,远曲小管(distal convoluted tubule,DCT) 和集合管(collecting tubule,CT) 在8 d时出现少量水肿。Masson染色结果显示,AAⅠ暴露8 d后,肾皮质胶原容积分数(collagen volume fraction,CVF) 较对照组显著上升,有统计学差异(P < 0.01)。见图 2、表 2。
|
| Red arrows indicate the shedding of microvilli in the apical membrane of epithelial cells and the appearance of microvilli in the tubular lumen; blue arrows indicate cell edema and granular degeneration; green arrows indicate epithelial necrosis; black arrows indicate the exposed basement membrane, and asterisks indicate tubular shape. 图 2 HE和Masson染色代表性图像× 20 Fig.2 Representative images stained by HE and Masson × 20 |
| Item | Control | Acute AAⅠ poisoning model groups | |||
| 2 d | 4 d | 6 d | 8 d | ||
| Destruction of brush border of PCTEC | 0.000±0.000 | 0.520±0.0501) | 0.153±0.0211) | 0.082±0.005 | 0.091±0.0111) |
| Edema of PCTEC | 0.000±0.000 | 0.855±0.0231) | 0.440±0.0181) | 0.338±0.0851) | 0.150±0.0441) |
| Necrosis of PCTEC | 0.000±0.000 | 0.094±0.030 | 0.392±0.0471) | 0.385±0.0411) | 0.315±0.0711) |
| Basement membrane of PCT exposed | 0.000±0.000 | 0.000±0.000 | 0.016±0.006 | 0.203±0.0161) | 0.535±0.0891) |
| Distal tubule injury | 0.000±0.000 | 0.017±0.012 | 0.020±0.011 | 0.034±0.005 | 0.039±0.0201) |
| Tube cast | 0.000±0.000 | 0.538±0.0381) | 0.756±0.0601) | 0.836±0.0301) | 0.776±0.0841) |
| CVF | 0.058±0.012 | 0.077±0.036 | 0.072±0.010 | 0.098±0.025 | 0.306±0.0781) |
| 1) P < 0.01 vs control group. | |||||
2.4 小鼠肾脏Wnt7b、β-catenin和MMP-7 IHC结果
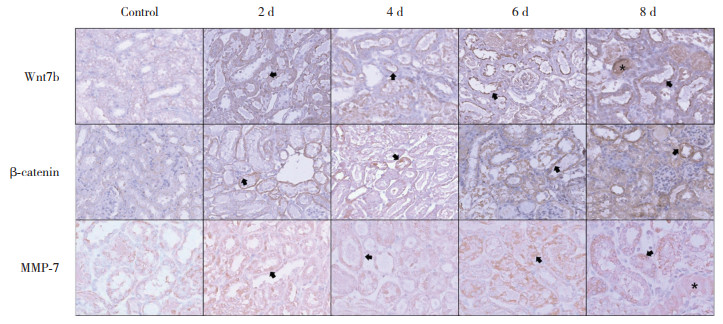
Wnt7b的IHC结果显示,模型组Wnt7b表达量上升,8 d时达到最高(主要聚集于刷状缘);暴露于AAⅠ8 d时,PCT、CMJ和CT处的Wnt7b的IHC平均光密度值增高,PCT的表达量增高至2 d时的2.5倍(P均 < 0.05);Wnt7b阳性的PCT比例增加,6~8 d时Wnt7b阳性小管数为70% (P均 < 0.05)。见图 3、表 3。
|
| Black arrows indicate proteins stained in the renal tubular epithelial cells. The asterisk indicates proteins in the lumen. 图 3 3种蛋白近端小管免疫组化染色代表性图像× 20 Fig.3 Representative images of immunohistochemical staining of three proteins in the proximal convoluted tubules × 20 |
| Item | Control | Acute AAⅠ poisoning model groups | |||
| 2 d | 4 d | 6 d | 8 d | ||
| PCT | 0.077±0.010 | 0.091±0.004 | 0.116±0.0171) | 0.173±0.0091) | 0.197±0.0231) |
| CMJ | 0.087±0.003 | 0.077±0.018 | 0.084±0.009 | 0.145±0.0121) | 0.139±0.0151) |
| CT | 0.076±0.014 | 0.081±0.010 | 0.073±0.006 | 0.071±0.025 | 0.126±0.0291) |
| Positive renal tubules | - | 0.475±0.074 | 0.691±0.0532) | 0.735±0.0572) | 0.716±0.0242) |
| 1) P < 0.01 vs control group;2) P < 0.01 vs 2 d. | |||||
β-catenin的IHC结果显示,模型组β-catenin表达量上升(PCT的近基底膜侧);第8天PCT、CMJ和CT处β-catenin的IHC平均光密度值和阳性小管与对照组相比明显增加,有统计学差异(P < 0.05)。见图 3、表 4。
| Item | Control | Acute AAⅠ poisoning model groups | |||
| 2 d | 4 d | 6 d | 8 d | ||
| PCT | 0.066±0.001 | 0.080±0.001 | 0.111±0.0101) | 0.124±0.0171) | 0.138±0.0141) |
| CMJ | 0.078±0.008 | 0.096±0.007 | 0.091±0.007 | 0.102±0.0121) | 0.087±0.010 |
| CT | 0.062±0.011 | 0.060±0.012 | 0.082±0.008 | 0.111±0.0141) | 0.093±0.0111) |
| Positive renal tubules | - | 0.357±0.049 | 0.471±0.0172) | 0.433±0.0222) | 0.675±0.0302) |
| 1) P < 0.01 vs control group;2) P < 0.01 vs 2 d. | |||||
MMP7的IHC结果显示,模型组MMP7在胞质内表达量上升;PCT、CMJ和CT处MMP7的IHC平均光密度值和阳性肾小管与对照组相比明显增加,有统计学差异(P < 0.05)。见图 3、表 5。
| Item | Control | Acute AAⅠ poisoning model groups | |||
| 2 d | 4 d | 6 d | 8 d | ||
| PCT | 0.051±0.001 | 0.056±0.002 | 0.053±0.008 | 0.060±0.005 | 0.089±0.0091) |
| CMJ | 0.052±0.004 | 0.122±0.0061) | 0.094±0.0171) | 0.093±0.0171) | 0.133±0.0201) |
| CT | 0.045±0.003 | 0.074±0.006 | 0.064±0.005 | 0.212±0.0221) | 0.223±0.0431) |
| Positive renal tubules | - | 0.448±0.015 | 0.551±0.042 | 0.582±0.0362) | 0.647±0.1042) |
| 1) P < 0.01 vs control group;2) P < 0.01 vs 2 d. | |||||
2.5 小鼠肾脏Wnt7b和MMP7免疫电镜结果
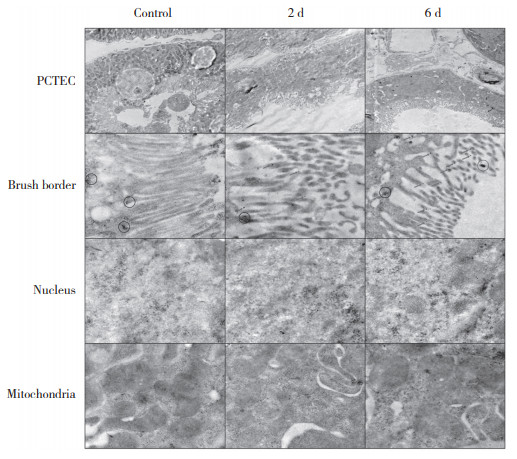
免疫电镜结果显示,对照组的PCTEC刷状缘绒毛排列整齐,线粒体嵴清晰,数量较多;暴露于AAⅠ 2 d后PCTEC刷状缘排列紊乱,线粒体数量减少;6 d时PCTEC空泡变性,刷状缘绒毛大量脱落,线粒体数量明显减少,呈“C”或“U”形。对照组未见Wnt7b胶体金颗粒,β-catenin胶体金颗粒主要聚集在细胞膜下;暴露于AAⅠ后,刷状缘出现成簇聚集的Wnt7b胶体金颗粒,β-catenin胶体金颗粒在细胞膜下逐渐减少,核内聚集增加。见图 4。
|
| The red arrows show Wnt7b protein. The red circles represent clusters of Wnt7b protein and the black circles represent clusters of β-catenin protein. The proximal convoluted tubule epithelium was magnified 2 000 times, while the brush border, nucleus, and mitochondria were magnified 15 000 times. 图 4 Wnt7b和β-catenin免疫电镜代表性图像 Fig.4 Representative immunoelectron microscopy images of Wnt7b and β-catenin proteins |
3 讨论
AA致肾损伤事件在非洲、亚洲和欧洲均有发生[12],而且大量不明原因慢性肾脏病被疑与含有AA的中草药有关[13]。因此,明确急性AAN早期的病理变化,阐明AAN的致病机制,对AAN的诊断和治疗有重要价值。
急性AAN的病理改变表现为肾小管受损,主要累及PCT [4],本研究连续观察了AAN的肾小管病理学改变,结果显示,AAN以PCT损害为主,且PCTEC的损伤呈时间和AAⅠ浓度依赖性;暴露于AAⅠ后,PCTEC刷状缘绒毛脱落,线粒体形态异常,数量减少,细胞水肿、坏死、脱落。急性AAN的肾脏间质CVF增加,细胞外基质紊乱,胶原纤维增多,呈纤维化改变[14]。DCT和CT的病理改变时间较晚,以细胞水肿为主,AAⅠ主要通过分布于PCT的阴离子选择通道蛋白进入细胞[15]。
目前研究[9]已经证明Wnt4和Wnt11参与肾纤维化过程,但Wnt信号通路在急性AAN过程中的机制并不清楚。巨噬细胞所分泌的Wnt7b在组织损伤诱导的炎症过程中,参与肾小管损伤后的的修复与再生[16-19]。Wnt通路激活后β-catenin在胞质聚集并转移到核内,激活下游基因表达(如参与细胞增殖和迁移的MMP-7) [20-21]。本研究结果显示,AAⅠ可诱导Wnt7b在PCTEC的刷状缘表达,β-catenin从膜下向胞质和细胞核内聚集,核内的表达量增高,MMP-7暴露于AAⅠ后表达量也逐渐升高。在6~8 d时PCTEC大量坏死,坏死细胞中表达的Wnt7b、β-catenin和MMP-7会随着细胞碎片在肾小管内聚集,使CMJ和CT处的蛋白表达增高,可能参与诱导启动肾祖细胞的增殖修复过程[22]。本研究结果显示,AAⅠ能够激活Wnt/β-catenin信号,可能参与肾小管上皮细胞损伤后的再生与修复过程。
急性AAⅠ中毒小鼠的肾脏损害,主要以PCT上皮坏死和脱落为主,与时间和AAⅠ浓度呈正相关;DCT和CT损伤较轻,以水肿为主;PCTEC的Wnt7b、β-catenin和MMP-7的表达量增高,可能参与肾小管上皮细胞的修复和再生过程。
| [1] |
贠凯祎, 徐志超, 宋经元. 含马兜铃酸中药及其检测研究进展[J]. 中国科学: 生命科学, 2019, 49(3): 238-249. DOI:10.1360/N052018-00274 |
| [2] |
PRIESTAP HA, TORRES MC, RIEGER RA, et al. Aristolochic acid Ⅰ metabolism in the isolated perfused rat kidney[J]. Chem Res Toxicol, 2012, 25(1): 130-139. DOI:10.1021/tx200333g |
| [3] |
ANGER EE, YU F, LI J. Aristolochic acid-induced nephrotoxicity: molecular mechanisms and potential protective approaches[J]. Int J Mol Sci, 2020, 21(3): 1157. DOI:10.3390/ijms21031157 |
| [4] |
REBHAN K, ERTL IE, SHARIAT SF, et al. Aristolochic acid and its effect on different cancers in uro-oncology[J]. Curr Opin Urol, 2020, 30(5): 689-695. DOI:10.1097/MOU.0000000000000806 |
| [5] |
ZHANG HM, ZHAO XH, SUN ZH, et al. Recognition of the toxicity of aristolochic acid[J]. J Clin Pharm Ther, 2019, 44(2): 157-162. DOI:10.1111/jcpt.12789 |
| [6] |
GROLLMAN AP. Aristolochic acid nephropathy: harbinger of a global iatrogenic disease[J]. Environ Mol Mutagen, 2013, 54(1): 1-7. DOI:10.1002/em.21756 |
| [7] |
NOGUEIRA A, PIRES MJ, OLIVEIRA PA. Pathophysiological mechanisms of renal fibrosis: a review of animal models and therapeutic strategies[J]. In Vivo, 2017, 31(1): 1-22. DOI:10.21873/invivo.11019 |
| [8] |
LIN JB, SENE A, WILEY LA, et al. WNT7A/B promote choroidal neovascularization[J]. Exp Eye Res, 2018, 174: 107-112. DOI:10.1016/j.exer.2018.05.033 |
| [9] |
YU J, CARROLL TJ, RAJAGOPAL J, et al. A Wnt7b-dependent pathway regulates the orientation of epithelial cell division and establishes the cortico-medullary axis of the mammalian kidney[J]. Development, 2009, 136(1): 161-171. DOI:10.1242/dev.022087 |
| [10] |
NUSSE R, CLEVERS H. Wnt/β-catenin signaling, disease, and emerging therapeutic modalities[J]. Cell, 2017, 169(6): 985-999. DOI:10.1016/j.cell.2017.05.016 |
| [11] |
DESHPANDE P, GOGIA N, CHIMATA AV, et al. Unbiased automated quantitation of ROS signals in live retinal neurons of Drosophila using Fiji/ImageJ[J]. BioTechniques, 2021, 71(2): 416-424. DOI:10.2144/btn-2021-0006 |
| [12] |
GÖKMEN MR, COSYNS JP, ARLT VM, et al. The epidemiology, diagnosis, and management of aristolochic acid nephropathy: a narrative review[J]. Ann Intern Med, 2013, 158(6): 469-477. DOI:10.7326/0003-4819-158-6-201303190-00006 |
| [13] |
YANG L, SU T, LI XM, et al. Aristolochic acid nephropathy: variation in presentation and prognosis[J]. Nephrol Dial Transplant, 2012, 27(1): 292-298. DOI:10.1093/ndt/gfr291 |
| [14] |
URATE S, WAKUI H, AZUSHIMA K, et al. Aristolochic acid induces renal fibrosis and senescence in mice[J]. Int J Mol Sci, 2021, 22(22): 12432. DOI:10.3390/ijms222212432 |
| [15] |
XUE X, GONG LK, MAEDA K, et al. Critical role of organic anion transporters 1 and 3 in kidney accumulation and toxicity of aristolochic acid I[J]. Mol Pharmaceutics, 2011, 8(6): 2183-2192. DOI:10.1021/mp100418u |
| [16] |
HALT K, VAINIO S. Coordination of kidney organogenesis by Wnt signaling[J]. Pediatr Nephrol, 2014, 29(4): 737-744. DOI:10.1007/s00467-013-2733-z |
| [17] |
ANASTAS JN, MOON RT. WNT signalling pathways as therapeutic targets in cancer[J]. Nat Rev Cancer, 2013, 13(1): 11-26. DOI:10.1038/nrc3419 |
| [18] |
SCHUNK SJ, FLOEGE J, FLISER D, et al. WNT-β-catenin signalling-a versatile player in kidney injury and repair[J]. Nat Rev Nephrol, 2021, 17(3): 172-184. DOI:10.1038/s41581-020-00343-w |
| [19] |
LIN SL, LI B, RAO S, et al. Macrophage Wnt7b is critical for kidney repair and regeneration[J]. Proc Natl Acad Sci USA, 2010, 107(9): 4194-4199. DOI:10.1073/pnas.0912228107 |
| [20] |
TAN RJ, LI YJ, RUSH BM, et al. Tubular injury triggers podocyte dysfunction by β-catenin-driven release of MMP-7[J]. JCI Insight, 2019, 4(24): e122399. DOI:10.1172/jci.insight.122399 |
| [21] |
KE B, FAN CQ, YANG LP, et al. Matrix metalloproteinases-7 and kidney fibrosis[J]. Front Physiol, 2017, 8: 21. DOI:10.3389/fphys.2017.00021 |
| [22] |
HULING J, YOO JJ. Comparing adult renal stem cell identification, characterization and applications[J]. J Biomed Sci, 2017, 24(1): 32. DOI:10.1186/s12929-017-0339-7 |
 2023, Vol. 52
2023, Vol. 52