文章信息
- 刘莹, 赵祥宇, 吴刘中, 曹灿
- LIU Ying, ZHAO Xiangyu, WU Liuzhong, CAO Can
- 超声清洗对钛种植体表面阳极氧化TiO2纳米阵列涂层不同深度氟元素含量的影响
- Effects of ultrasonic washing method on the fluoride content at different depths of post-anodized TiO2 nanotube array coatings of titanium implant
- 中国医科大学学报, 2022, 51(2): 160-162, 168
- Journal of China Medical University, 2022, 51(2): 160-162, 168
-
文章历史
- 收稿日期:2021-01-23
- 网络出版时间:2021-12-30 19:29
2. 沈阳市口腔医院综合急诊科, 沈阳 110002;
3. 沈阳市口腔医院牙周科, 沈阳 110002
2. Department of Oral Emergency, Shenyang Stomatological Hospital, Shenyang 110002, China;
3. Department of Periodontics, Shenyang Stomatological Hospital, Shenyang 110002, China
种植体表面阳极氧化纳米涂层在应用于生物环境前需经过清洗等手段处理[1]。研究[2-3]显示,阳极氧化纳米涂层制备后可采用超声震荡方式清洗,也可简单进行流水冲洗,也有在实验操作中省略了清洗步骤。阳极氧化后种植体表面不可避免会带有电解液中的各种成分[4],关于清洗后纳米管残留的氟元素分布的研究未见报道。
氟元素被证明在成骨过程中发挥重要的作用。体外实验表明不同浓度氟化钠均能刺激成骨细胞分泌骨钙素,并且与氟含量呈正相关[4-6]。本研究探讨了超声清洗对钛种植体表面阳极氧化TiO2纳米阵列涂层不同深度氟元素含量的影响。
1 材料与方法 1.1 主要材料、仪器和设备主要材料包括正方形纯钛试样(10 mm×10 mm×1 mm,购于西北有色金属研究院),SiC砂纸400、800、1200、2000目(韩国鹰牌砂纸公司),乙二醇、甲醇、乙醇、丙酮(天津富宇精细化工有限公司),去离子水(北部战区总医院药剂科),氟化铵(天津天力化学试剂有限公司)。主要仪器和设备包括稳流稳压直流电源(TPR6405D,香港LongWei公司)、磁力搅拌器(江苏金坛仪器设备厂)、超声波清洗机(UC-50,德国Whaledent公司)、场发射扫描电子显微镜(S-4800,日本Hitachi公司)、光电子能谱分析仪(荷兰ULVAC-Phi公司)。
1.2 TiO2纳米阵列涂层制备、分组及检测配制NH4F、乙二醇溶液作为阳极氧化电解液,以纯钛为阳极,以铂为阴极在40 V直流电下形成100 nm管径的TiO2纳米阵列涂层。
将制备好的TiO2纳米阵列涂层分为2组:清洗组(NT-W组,TiO2纳米阵列涂层经过丙酮、乙醇、去离子水顺次清洗10 min)、未清洗组(NT-UW组,TiO2纳米阵列涂层不做清洗处理,室温下自然干燥)。
沿纳米管长轴方向每500 nm进行刻蚀分析,应用X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)检测,分别得到2组XPS能谱数据。根据XPS能谱表截选结合能为685.0~685.9 a.u.作为氟元素的峰值区间。
1.3 统计学分析利用SPSS 26.0统计软件处理数据。计量资料采用x±s表示,组间比较采用Mann-Whitney U检验,组内比较采用单因素方差分析或配对t检验,P < 0.05为差异有统计学意义。
2 结果 2.1 扫描电镜下纳米管管口及侧壁形貌图40 V电压形成的纳米管管径约为80~100 nm,管壁厚5~8 nm,管与管之间间距5~20 nm。纳米管管长3~5 μm。扫描电镜可见经过阳极氧化处理后纯钛表面均形成均匀的纳米管阵列结构,见图 1。

|
| A, the top view of the anodized nanotube arrays; B, the side and bottom views of the anodized nanotube arrays. 图 1 阳极氧化形成的纳米阵列扫描电镜图 Fig.1 The microstructure of anodized nanotube arrays by field emission scanning electron microscopy |
2.2 2组氟含量比较
NT-W组、NT-UW组氟含量分别为(28 255.846±2 376.654)a.u.和(32 541.415±1 824.274)a.u.,2组比较差异有统计学意义(U = 8.375,P < 0.001)。
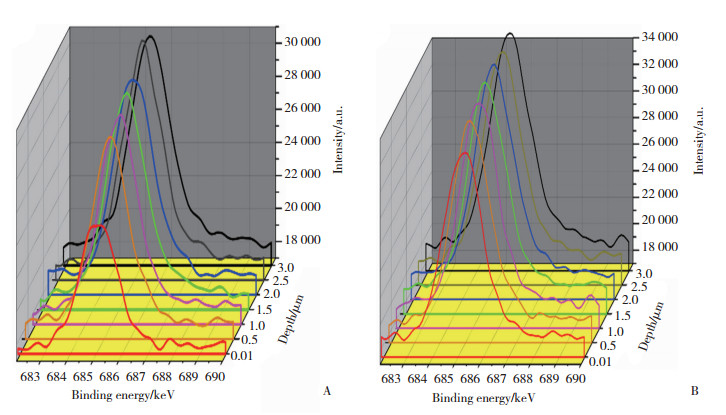
2.3 各组不同深度氟含量比较单因素方差分析结果显示,NT-W组不同深度氟含量差异显著(F = 25.231,P < 0.01)。配对t检验结果显示,0 μm深度氟含量与其他深度氟含量比较差异显著(P < 0.05),而其他各深度氟含量比较无统计学差异(均P > 0.05)。NT-UW组不同深度氟含量差异无统计学意义(F = 1.967,P = 0.086)。见表 1、图 2。
| Item | NT-W group | NT-UW group |
| 3 μm | 29 884.867±1 119.667 | 33 459.878±1 698.199 |
| 2.5 μm | 29 982.089±1 483.071 | 33 146.278±1 685.115 |
| 2.0 μm | 29 097.867±1 140.991 | 32 878.089±1 900.048 |
| 1.5 μm | 28 839.589±1 336.331 | 32 647.800±1 815.427 |
| 1.0 μm | 28 484.233±1 285.964 | 32 682.478±1 557.199 |
| 0.5 μm | 27 886.767±1 497.323 | 31 944.056±1 889.545 |
| 0 μm | 23 615.511±1 176.538 | 31 031.333±1 636.162 |
|
| A, NT-W group; B, NT-UW group. 图 2 氟元素不同深度刻蚀分析XPS能谱图 Fig.2 The XPS spectra of element of fluoride range after different depths etching |
3 讨论
纯钛在含氟电解液中发生阳极氧化反应可以生成纳米管阵列样结构[7-8]。本研究采用NH4F、乙二醇电解液,经过40 V电压处理后得到管径80 nm、管长3 μm的纳米管阵列。经过XPS元素刻蚀分析发现超声清洗过后的纳米管氟元素含量相比未清洗纳米管明显减少,但纳米管全长仍存在氟元素峰值,这说明氟元素结合能力极强,经过超声清洗处理仍不能彻底去除。
阳极氧化后残留的氟元素对应用种植体后的生物学行为存在潜在影响,包括刺激成骨细胞活性,干预钙、磷在骨内沉积[6-7]。本研究结果显示,超声清洗对于纳米管内部氟元素分布产生影响,经过清洗处理后纳米管管口位置的氟元素含量明显低于其他部位;而未经过清洗的纳米管各深度氟元素含量比较无统计学差异(P > 0.05),说明超声清洗对纳米管管口的氟元素去除效果显著,而较深位置氟元素去除效果明显小于管口位置。
综上所述,超声清洗可以明显减少TiO2纳米阵列涂层的氟元素含量,但不能彻底去除残留的氟元素。同时,超声清洗改变了管内氟元素分布,管口位置氟元素含量明显低于其他部位。本研究为氟元素在阳极氧化后TiO2纳米阵列涂层表面残留、分布及处理方式的相关研究提供依据。本研究局限于从材料学领域分析阳极氧化处理技术后氟元素残留及超声清洗对氟元素残留产生的影响,研究内容相对单一,量化分析较少。同时本研究缺乏残留后氟元素后期的释放及变化过程的追踪研究,关于纳米涂层残留氟元素在后期生物学行为中发挥的作用及机制等系统性研究工作需进一步开展。
| [1] |
ALIPAL J, LEE TC, KOSHY P, et al. Evolution of anodised titanium for implant applications[J]. Heliyon, 2021, 7(7): e07408. DOI:10.1016/j.heliyon.2021.e07408 |
| [2] |
BARJAKTAREVIĆ DR, CVIJOVIĆ-ALAGIĆ IL, DIMIĆ ID, et al. Anodization of Ti-based materials for biomedical applications: a review[J]. Metall Mater Eng, 2016, 22(3): 129-144. DOI:10.30544/209 |
| [3] |
LIM YP, YEO WH. The microstructure and mechanical properties of titanium dioxide nanotubes synthesized in the fluoride-based electrolyte[J]. Metall Mater Eng, 2018, 24(2): 83-92. DOI:10.30544/336 |
| [4] |
NIU DM, HAN AJ, CHENG H, et al. Effects of organic solvents in anodization electrolytes on the morphology and tube-to-tube spacing of TiO2 nanotubes[J]. Chem Phys Lett, 2019, 735: 136776. DOI:10.1016/j.cplett.2019.136776 |
| [5] |
JAIN S, WILLIAMSON RS, JANORKAR AV, et al. Osteoblast response to nanostructured and phosphorus-enhanced titanium anodization surfaces[J]. J Biomater Appl, 2019, 34(3): 419-430. DOI:10.1177/0885328219852741 |
| [6] |
KULKARNI M, MRAK-POLJŠAK K, FLAŠKER A. Fabrication of TiO2 nanotubes for bioapplications[J]. Mater Tehnol, 2015, 49(4): 635-637. DOI:10.17222/mit.2014.152 |
| [7] |
KIM SE, LIM JH, LEE SC, et al. Anodically nanostructured titanium oxides for implant applications[J]. Electrochimica Acta, 2008, 53(14): 4846-4851. DOI:10.1016/j.electacta.2008.02.005 |
| [8] |
MARENZI G, SPAGNUOLO G, SAMMARTINO JC, et al. Micro-scale surface patterning of titanium dental implants by anodization in the presence of modifying salts[J]. Materials, 2019, 12(11): 1753. DOI:10.3390/ma12111753 |
 2022, Vol. 51
2022, Vol. 51