文章信息
- 李扬, 刘贵朋, 杨清
- LI Yang, LIU Guipeng, YANG Qing
- 催乳素与子宫内膜腺癌的相关性
- Correlation between prolactin and endometrial adenocarcinoma
- 中国医科大学学报, 2020, 49(7): 646-650
- Journal of China Medical University, 2020, 49(7): 646-650
-
文章历史
- 收稿日期:2020-03-20
- 网络出版时间:2020-06-24 9:41
子宫内膜癌是妇科三大恶性肿瘤之一,其中腺癌为其主要分型。早期子宫内膜癌的5年生存率为75%~95%,但Ⅲ~Ⅳ期患者的预后情况不容乐观。如果诊断时癌症已经转移,尤其是远处转移患者[1],5年生存率大大降低。因此,预防和早期发现能够进一步减轻疾病负担。本课题组前期研究[2]发现,卵巢癌组织中催乳素(prolactin,PRL)的表达升高,而PRL与子宫内膜腺癌的关系国内外较少报道。
PRL是一种由垂体产生的激素,也是一种由多种炎症反应产生的自分泌性细胞因子。它除了具有促进乳汁分泌和性腺发育的作用,还可与PRL受体结合,通过Janus激酶、胞外信号调节激酶、信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)激活细胞内信号,发挥其他生物学作用,如免疫、应激、细胞的分裂和增殖等。以往的临床研究[3]显示,结肠癌患者血清PRL水平升高。也有研究[4]报道,PRL与一些妇科肿瘤的发生相关,PRL通过激活STAT5、哺乳动物雷帕霉素靶蛋白和丝裂原活化的胞外信号调节激酶,诱导和促进卵巢癌细胞增殖。本研究旨在通过检测血清PRL水平和癌组织中PRL的表达情况,探讨PRL与子宫内膜腺癌发生、发展的关系。
1 材料与方法 1.1 材料 1.1.1血清标本:选取2016年1月至2017年1月于中国医科大学附属盛京医院第一微创妇科经手术确诊的41例子宫内膜腺癌患者作为观察组,年龄44~72岁,平均(56.5 ±4.2)岁。同期选取38例健康女性志愿者作为对照组,年龄43~75岁,平均(57.5±4.8)岁。排除其他肿瘤等疾病患者。所有研究对象入组前3个月内未使用过激素治疗;观察组患者之前未接受任何治疗。手术前3~5 d采集血清样本。
1.1.2免疫组化标本:标本取自2015年1月至2017年1月中国医科大学附属盛京医院第一微创妇科收治患者的手术切除组织,其中分泌期正常子宫内膜组织和增生期正常子宫内膜组织取自因输卵管因素不孕的患者和因子宫脱垂而切除子宫的患者,各5例,子宫内膜不典型增生组织20例,子宫内膜腺癌组织57例。以上标本均经病理诊断证实。罹患其他疾病但具备正常子宫内膜组织患者,年龄32~50岁,平均(43.7±5.7)岁。子宫内膜不典型增生患者,年龄26~57岁,平均(47.5±4.2)岁。子宫内膜腺癌患者,年龄31~73岁,平均(55.7±7.8)岁;病理类型均为子宫内膜腺癌;国际妇产科联盟(International Federation of Gynecology and Obstetrics,FIGO)分期:Ⅰ+Ⅱ期29例,Ⅲ+Ⅳ期28例;组织学分级:高分化(G1)9例,中分化(G2)20例,低分化(G3)28例;浸润 < 1/2肌层37例,浸润≥1/2肌层20例;无淋巴结转移37例,有淋巴结转移20例。
1.2 方法 1.2.1血清PRL的检测:使用DIX800型全自动化学发光仪检测血清PRL水平,检测方法为化学发光免疫法,仪器和配套试剂由美国BECKMAN COULTER公司提供,按说明进行操作。
1.2.2免疫组化:采用免疫组化SP法,其中兔抗人PRL多克隆抗体(北京博奥森生物技术公司)浓度为1 : 400,按SP试剂盒的步骤操作,浓缩型二氨基联苯胺试剂盒进行显色,试剂盒均由北京中杉金桥公司提供,通过苏木素溶液复染,脱水完成后封片。将步骤中一抗替换为PBS作为对照。2位病理科医生判定病理结果,染色阳性表现为细胞内形成黄色着色。细胞染色强度评分:无色,0分;浅黄色,1分;棕黄色,2分;棕褐色,3分。显色细胞百分比评分:无显色细胞,0分;显色细胞比例 < 10%,1分;显色细胞比例10%~ < 50%,2分;显色细胞比例50%~ < 75%,3分;显色细胞比例≥75%,4分。将细胞染色强度、显色细胞百分比评分之积设定为总积分,总积分≤2分提示阴性(-),总积分≥3分提示阳性,其中总积分3~4分提示弱阳性(+),总积分5~8分提示中度阳性(++),总积分9~12分提示强阳性(+++)。将++~+++定义为PRL高表达。
1.3 统计学分析采用SPSS 22.0软件进行统计学分析,计量资料用x±s表示,采用t检验进行比较;计数资料采用χ 2检验或Fisher’s确切概率法以及秩和检验进行比较。P < 0.05为差异有统计学意义。
2 结果 2.1 观察组与对照组血清PRL水平的比较观察组和对照组血清PRL水平分别为(14.7±10.23)和(7.8±6.05)ng/mL,观察组明显高于对照组(P < 0.05),但二者均在正常值(3.34~26.72)ng/mL范围内。
2.2 PRL的表达与子宫内膜病变程度的关系秩和检验结果显示,正常子宫内膜组织、子宫内膜不典型增生组织和子宫内膜腺癌组织3组比较,PRL表达水平有统计学差异(P < 0.05)。PRL高表达率子宫内膜腺癌组织(64.9%,37/57)>子宫内膜不典型增生组织(25.0%,5/20)>正常子宫内膜组织(10.0%,1/10)。子宫内膜腺癌组织与正常子宫内膜组织、子宫内膜不典型增生组织比较,PRL高表达率的差异均有统计学意义(分别为P = 0.020和P = 0.040),但正常子宫内膜组织与子宫内膜不典型增生组织比较,PRL高表达率无统计学差异(P = 0.628)。见表 1、图 1。
| Endometrial lesion | n | PRL expression | High expression of PRL[n(%)] |
|||
| - | + | ++ | +++ | |||
| Normal endometrium | 10 | 8 | 1 | 1 | 0 | 1(10.0) |
| Atypical hyperplasia of endometrium | 20 | 3 | 12 | 4 | 1 | 5(25.0) |
| Endometrial adenocarcinoma | 57 | 4 | 16 | 13 | 24 | 37(64.9) |
|
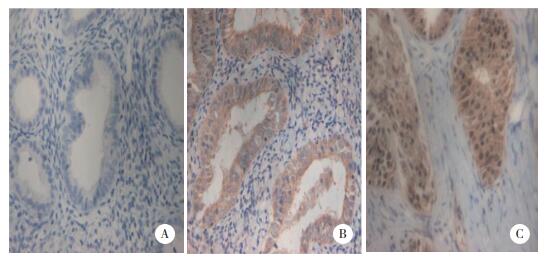
| A, normal endometrium; B, atypical hyperplasia of endometrium; C, endometrial adenocarcinoma. 图 1 不同子宫内膜病变中PRL的表达SP×200 Fig.1 Expression of PRL in different endometrial lesions SP×200 |
2.3 子宫内膜腺癌中PRL的表达水平与临床病理参数的关系
晚期(Ⅲ+Ⅳ期)子宫内膜腺癌患者的PRL高表达率(82.1%,23/28)明显高于早期(Ⅰ+Ⅱ期)患者(48.3%,14/29)(P < 0.05)。秩和检验结果显示,G1、G2和G3三组比较,PRL表达水平有统计学差异(P < 0.05)。G3中PRL高表达率明显高于G1(P = 0.001)和G2(P = 0.025),但G1与G2比较PRL高表达率无统计学差异(P > 0.05)。有淋巴结转移的子宫内膜腺癌中PRL高表达率明显高于无淋巴结转移的子宫内膜腺癌(P < 0.05)。PRL的表达与肌层浸润深度无关(P > 0.05)。见表 2。
| Clinicopathological characteristics | n | PRL expression | High expression of PRL [n(%)] | P | |||
| - | + | ++ | +++ | ||||
| Stage | 0.008 | ||||||
| Ⅰ+Ⅱ | 29 | 2 | 13 | 8 | 6 | 14(48.3) | |
| Ⅲ+Ⅳ | 28 | 2 | 3 | 5 | 18 | 23(82.1) | |
| Degree of differentiation | 0.001 | ||||||
| G1 | 9 | 3 | 4 | 1 | 1 | 2(22.2) | |
| G2 | 20 | 1 | 8 | 4 | 7 | 11(55.0) | |
| G3 | 28 | 0 | 4 | 8 | 16 | 24(85.7) | |
| Depth of myometrial invasion | 0.092 | ||||||
| < 1/2 | 37 | 3 | 13 | 5 | 16 | 21(56.8) | |
| ≥1/2 | 20 | 1 | 3 | 8 | 8 | 16(80.0) | |
| Lymph node metastasis | 0.023 | ||||||
| No | 37 | 3 | 14 | 11 | 9 | 20(54.1) | |
| Yes | 20 | 1 | 2 | 2 | 15 | 17(85.0) | |
3 讨论
PRL由脑垂体分泌,主要作用是刺激乳汁分泌。还有许多组织局部产生PRL,参与调节包括生殖、生长、发育、代谢和免疫调节在内的多种生理活动。PRL局部积累可能促进乳腺癌和结直肠癌等癌症的发生[3, 5]。PRL与PRL受体结合,促进细胞增殖和肿瘤形成。研究[5]报道,给患有乳腺癌的小鼠注射PRL抗血清可以抑制肿瘤或使肿瘤消退,再次注射PRL时乳腺癌又迅速生长。另外,最新研究[6]表明,PRL积累可以通过将p-STAT5转移到细胞核并与BRCA1形成抑制复合物,抑制乳腺癌细胞p21的肿瘤抑制活性。
本研究结果显示,虽然观察组和对照组血清PRL水平均在正常范围,但是子宫内膜腺癌患者血清PRL水平较健康人明显增高,与LEVINA等[7]的研究结果一致。但本研究缺乏子宫内膜腺癌患者术后血清PRL水平的随访,无法确切证实血清PRL水平在患病后确有升高。虽然已有研究[8]证明,血清PRL的敏感度可能比CA125高,但其特异度和子宫内膜腺癌患者血清水平的有效评价范围有待考证。
子宫内膜癌患者的发病年龄有降低趋势[9],女性生殖系统的生育功能和生理功能对年轻女性尤为重要,而子宫内膜癌主要病理类型以子宫内膜腺癌为主,故子宫内膜腺癌的早期诊断和治疗有重要意义。体外研究[7]显示,PRL可促进正常子宫内膜组织增殖并向恶性转化。本研究发现,PRL在子宫内膜腺癌组织中的高表达率明显高于子宫内膜不典型增生组织和正常子宫内膜组织,而子宫内膜不典型增生组织与子宫内膜正常比较PRL高表达率无明显差异。说明PRL可能在子宫内膜不典型增生组织向腺癌组织的转化中发挥了重要作用,PRL与肿瘤的发生、发展正相关,或许可以作为子宫内膜腺癌病理诊断的标志物之一。
癌细胞的分化程度可影响子宫内膜腺癌患者病情进展,细胞分化程度越低,其恶性程度越高,术后接受放化疗的概率越大[10]。结合临床病理资料,发现PRL在G1、G2、G3癌组织中的表达水平有差异,G3中的高表达率显著高于G1和G2,而G2中PRL高表达率虽高于G1,但差异无统计学意义。由此推测,子宫内膜腺癌恶性程度可能与PRL水平上调具有相关性,与前列腺癌研究[11]报道恶性病灶中PRL表达提高相互印证。本研究还发现,Ⅲ+Ⅳ期子宫内膜腺癌组织中PRL高表达率明显高于Ⅰ+Ⅱ期子宫内膜腺癌组织,有淋巴结转移的子宫内膜腺癌中PRL高表达率明显高于无淋巴结转移的子宫内膜腺癌,提示PRL表达的增加对子宫内膜腺癌转移有促进作用。PRL通过与PRL受体结合,刺激下游信号通路发挥作用,提高癌细胞复制和转移能力[8],从而促进肿瘤的侵袭和转移。另有研究[12-13]显示,PRL受体拮抗剂能够通过多种信号通路途径抑制乳腺癌细胞增殖,包括抑制AKT、HER2磷酸化,上调转化生长因子-β1,活化caspase-3等,抑制STAT5和STAT3活性,进一步反向确认PRL能够促进肿瘤发展。此外,PRL还可促进血管新生[14],保证肿瘤细胞的营养供给;提高细胞黏附能力[3, 7],促进肿瘤组织的增大和局部侵袭。既往研究[15]证实子宫内膜癌的转移与浸润深度有关,但PRL的表达与肌层浸润深度无相关性,这可能与本研究的病例不足有关。
关于子宫内膜腺癌与PRL相关性的研究还较少,免疫组化方法存在一定程度局限性,需进一步增大样本量,并进行基因水平研究,为子宫内膜腺癌发病机制、诊断和治疗的研究提供新的方向,实现对子宫内膜腺癌的早期诊断和靶向治疗。
| [1] |
SIEGEL RL, MILLER KD, JEMAL A. Cancer Statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34. DOI:10.3322/caac.21551 |
| [2] |
刘贵鹏, 张小围, 王爽, 等. 催乳素与卵巢癌的相关性分析[J]. 广东医学, 2012, 33(21): 3291-3293. DOI:10.3969/j.issn.1001-9448.2012.21.040 |
| [3] |
NERADUGOMMA NK, SUBRAMANIAM D, TAWFIK OW, et al. Prolactin signaling enhances colon cancer stemness by modulating Notch signaling in a Jak2-STAT3/ERK manner[J]. Carcinogenesis, 2014, 35(4): 795-806. DOI:10.1093/carcin/bgt379 |
| [4] |
KARTHIKEYAN S, RUSSO A, DEAN M, et al. Prolactin signaling drives tumorigenesis in human high grade serous ovarian cancer cells and in a spontaneous fallopian tube derived model[J]. Cancer Lett, 2018, 433: 221-231. DOI:10.1016/j.canlet.2018.07.003 |
| [5] |
CANBAY E, NORMAN M, KILIC E, et al. Prolactin stimulates the JAK2 and focal adhesion kinase pathways in human breast carcinoma T47-D cells[J]. Biochem J, 1997, 324(Pt 1): 231-236. DOI:10.1042/bj3240231 |
| [6] |
CHEN KH, WALKER AM. Prolactin inhibits a major tumorsuppressive function of wild type BRCA1[J]. Cancer Lett, 2016, 375(2): 293-302. DOI:10.1016/j.canlet.2016.03.007 |
| [7] |
LEVINA VV, NOLEN B, SU YY, et al. Biological significance of prolactin in gynecologic cancers[J]. Cancer Res, 2009, 69(12): 5226-5233. DOI:10.1158/0008-5472.CAN-08-4652 |
| [8] |
王颖, 孙会艳, 陈永莲. PRL及CA125在子宫内膜癌的表达及其与临床病理分期的关系[J]. 中国医疗前沿, 2012, 7(1): 44-45. DOI:10.3969/j.issn.1673-5552.2012.01.0028 |
| [9] |
张一琼, 于江燕, 朱元芳. 子宫内膜癌肿瘤微环境的研究进展[J]. 现代肿瘤医学, 2016, 24(16): 2651-2655. DOI:10.3969/j.issn.1672-4992.2016.16.042 |
| [10] |
BURKE WM, ORR J, LEITAO M, et al. Endometrial cancer:a review and current management strategies:partⅠ[J]. Gynecol Oncol, 2014, 134(2): 385-392. DOI:10.1016/j.ygyno.2014.05.018 |
| [11] |
DAGVADORJ A, COLLINS S, JOMAIN JB, et al. Autocrine prolactin promotes prostate cancer cell growth via Janus kinase-2-signal transducer and activator of transcription-5a/b signaling pathway[J]. Endocrinology, 2007, 148(7): 3089-3101. DOI:10.1210/en.2006-1761 |
| [12] |
ZHANG G, LI W, HOLLE L, et al. A novel design of targeted endocrine and cytokine therapy for breast cancer[J]. Clin Cancer Res, 2002, 8(4): 1196-1205. |
| [13] |
WENNBO H, GEBRE-MEDHIN M, GRITLI-LINDE A, et al. Activation of the prolactin receptor but not the growth hormone receptor is important for induction of mammary tumors in transgenic mice[J]. J Clin Invest, 1997, 100(11): 2744-2751. DOI:10.1172/JCI119820 |
| [14] |
FREEMAN ME, KANYICSKA B, LERANT A, et al. Prolactin:structure, function, and regulation of secretion[J]. Physiol Rev, 2000, 80(4): 1523-1631. DOI:10.1152/physrev.2000.80.4.1523 |
| [15] |
GARG G, GAO F, WRIGHT JD, et al. The risk of lymph node metastasis with positive peritoneal cytology in endometrial cancer[J]. Int J Gynecol Cancer, 2013, 23(1): 90-97. DOI:10.1097/IGC.0b013e318275afd2 |
 2020, Vol. 49
2020, Vol. 49