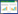文章信息
- 王宏娜, 许军
- WANG Hongna, XU Jun
- Oculus C-Quant散射光计量仪在视功能检查中的临床应用价值
- Clinical value of Oculus C-Quant straylight meter in visual function assessment
- 中国医科大学学报, 2020, 49(2): 165-169, 189
- Journal of China Medical University, 2020, 49(2): 165-169, 189
-
文章历史
- 收稿日期:2018-11-06
- 网络出版时间:2019-12-23 13:30
2. 沈阳爱尔卓越眼科医院眼科, 中南大学爱尔眼科学院, 沈阳 110001
2. Department of Ophthalmology, Shenyang Aier Excellence Eye Hospital, Aier School of Opthalmology, Central South University, Shenyang 110001, China
散射是由于屈光介质不均和不均等折射率结构引起的光线传播的异常, 可降低对比敏感度, 引起幕罩样眩光, 进而影响视觉质量[1]。失能眩光是指由于眼内散射光引起的视网膜上图像的对比度减弱[2-4]。国际照明委员会已经明确了失能眩光和眼内散射光的一致性, 即眼内散射光是形成失能眩光的基础[5]。在健康眼中, 失能眩光随着年龄的增长而增加[6-7]。在正常人眼的散射光中, 角膜、晶状体、视网膜源性散射分别约占30%、20%、20%[5]。视网膜散射光在40岁前相对恒定, 65岁后是40岁前的2倍, 而77岁后达到40岁前的3倍[8]。有屈光介质混浊时眼内散射光增加更为明显, 尤其常见于白内障患者[4-8]。早期白内障患者通常视力较好, 但是主观视功能感觉较差, 如光晕, 畏光, 视物模糊, 夜间驾驶能力较差, 色彩和对比度下降等, 因此, 眩光测试有助于白内障的早期诊断。正常情况下, 角膜并不是前向散射的重要来源, 但进行了角膜屈光手术后, 手术不仅改变了低阶像差而提高了视力, 同时也改变了角膜厚度、角膜表面形态和组织结构, 由此可能会引起散射的变化, 因此, 角膜屈光术前对散射光的评估以及对术中各项参数的合理设置有不容忽视的意义[9-10]。以前的眩光测试仪大部分都是测量有眩光条件下的视力或对比敏感度(contrast sensitivity, CS), 缺乏一种被广泛接受的标准。C-Quant散射光计量仪是以"补偿比较"的方法为基础, 精确客观地直接定量患者眼内散射光, 操作简单迅速, 可广泛用于视功能检查。
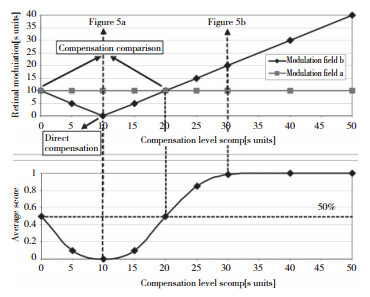
1 C-Quant测量原理 1.1 补偿比较C-Quant散射光计量仪(德国Oculus公司)由中央测试区和边缘散射光源2个部分组成。边缘散射光源闪烁时, 闪烁光会在晶状体和眼内的其他介质发生散射。由于散射光的存在, 受试者会觉得实际为黑色的中央测试区也在发生闪烁。C-Quant用"补偿比较"的方法把中央测试区分成左右2个测试区, 随机接受补偿光, 补偿光的闪烁时相与边缘散射光源的闪烁时相相反(图 1) [11-13]。受试者必须明确左右测试区哪个闪烁更强烈, 从而做出二进制的判断(0或1), 0代表受试者选择没有补偿光的一侧, 1代表受试者选择有补偿光的一侧。C-Quant的25次试验中包含7种"补偿比较"模式(图 2), 对于每种补偿模式重复试验后受试者会给出介于0~1间的平均反应值。C-Quant可以计算出中心测试区需要多大强度的光补偿散射光源发出的散射光。补偿光的强度是眼内散射光强度的2倍时, 重复试验后得到平均反应值为0.5, 此时中央测试区左右两侧闪烁强度相同。
|
| 图 1 C-Quant散射光计量仪测试原理 Fig.1 Testing fundamentals of Oculus C-Quant straylight meter |
|
| 图 2 7种"补偿比较"模式和心理测量函数曲线 Fig.2 "Compensation comparison" model and psychometric function curve |
1.2 心理测量函数(psychometric function, CF)和测试结果
CF被广泛应用于人类的感知觉功能, 根据患者的二进制反应值, CF能精确计算出受试者的散射光。C-Quant测得的眼内散射光测量结果取散射光强度的对数值[log straylight parameter, log (s)]。COPPENS等[11]对2 422名受试者用C-Quant进行了眩光测量的研究, 结果表明二进制反应值符合CF曲线(图 2)。
1.3 C-Quant具有更优的数据可靠性、可重复性与真实性由于C-Quant的测量是一种心理物理方法, 因此需要检查判断个体测量的可靠性, 故设置了可靠性参数(expected standard deviation, Esd)和质量参数Q来评价个体测量的准确性。COPPENS等[12]研究证明Esd能够有效的检测实验的可靠性, 在临床应用中可作为是否需要重复检测的标准。COPPENS等[14]采用蒙特卡罗模拟的方法评价了"补偿比较"方法的可靠性, 且用二项抽样法得出了精确的Esd值[Esd=0.07log (s)平均值]。当Esd < 0.008且Q > 1时, 可认为测量结果的可靠性高。PUELL等[15]应用C-Quant对29例青年(35.6岁±9.6岁)和23例老年人(61.8岁±8.7岁)进行散射光测量, 2次测量之间间隔1~3周, 结果表明, 青年组和老年组的平均视网膜散射光分别为(0.97±0.12)个对数单位和(1.21±0.21)个对数单位, 总体上测量值的重复性较高(MD= -0.003, COR = ±0.21), 青年组(MD=0.024, COR=±0.15)的重复性好于老年组(MD=-0.021, COR=±0.24), 但2次重复测量在每组和整个样本中均无显著差异, 表明C-Quant能够可重复且可靠地测量眼内的散射光, 患者的年龄不降低测量的可重复性。GUBER等[16]选取了45例正常人(年龄21~59岁), 其中正视14例, 近视16例, 远视8例, 散光7例, 应用C-Quant对其主视眼进行5次散射光重复测量发现, 年龄每增加10岁, 散射光平均增加0.10 (95%CI:0.04~0.16, P < 0.01), 不同屈光状态下(-5.25~+2.00 D)的散射光值差异无统计学意义, 表明C-Quant测量散射光具有较高的重现性, 适用于长期随访。VAN RIJN等[17]把112例受试者分成青年无眼病组、老年无眼病组、至少单眼患(早期)白内障组进行横断面队列研究, 用方差分析的方法研究3种散射光计量仪的可靠性、可重复性与真实性, 结果表明, 新型电脑控制的散射光计量仪可靠性、可重复性与真实性较Nyktotest (德国Rodenstock公司)和Mesotest (德国Oculus公司)散射光计量仪好。
2 C-Quant直接定量眼内散射光传统的眩光测试, 如Brightness Acuity Tester (BAT)、Berkeley Glare Test, 以及Mesotest Ⅱ、Nyktotest 300、Takaci-CGT-1000型自动眩光对比敏感度, 都是通过测量有眩光条件下的视力或CS来估量眩光对视功能的影响[2, 4, 18]。而Oculus C-Quant Straylight Meter是以"补偿比较"为原理, 通过CF精确、有效地测量有眩光条件下投射到视网膜上的散射光, 将散射光的大小作为眩光对视功能影响的定量评价, 更好地反映了散射光引起的视网膜上图像的对比度下降, 且可靠性、可重复性及真实性好[17]。
3 C-Quant测量的散射光比其他视功能检查更精准有效视力可反映黄斑区对高对比(100%黑白对比)精细目标的分辨能力, 而整个视网膜对低对比度目标的分辨能力却无法用视力衡量, CS在视角与对比度结合的基础上, 测定人眼对不同空间频率、不同对比度图形的分辨能力, 但也不能反映强烈的光线入眼时, 由于眼内光学系统存在的缺陷而使入射光发生散射对成像质量的影响。像差反映实际工作中光学系统所成的像与近轴光学(高斯光学)所获得的结果的偏离, 同样不能反映入射光发生散射对成像质量的影响。眩光敏感度(glaret sensitivity, GS)是检测散射光在眼内引起散射使视网膜成像对比度下降而引起的CS下降效应, 旨在检测受试者在强光源下看清视标的能力。眩光对比敏感函数(glare contrast sensitivity funcion, GSF)测定以CSF变化作为基础, 加上眩光作用, 通过功能负荷, 更敏感化[19]。ADAMSONS等[20]指出早期白内障患者视觉质量的精细改变可以通过CS, 尤其是GS检查发现, 用多重回归的方法分析眩光对视力的影响(P > 0.7), 得出眩光与视力的相关性检验不具有统计学意义, 而早期白内障患者的CS和GS均不同程度地下降。SUPERSTEIN等[21]提出白内障的不同发展阶段均导致眼内散射, 引起失能眩光, 检查白内障患者GS的敏感性高于CS, 而视力检查低估了混浊晶状体引起的视功能损失。
GS是通过CS的下降效应来反映眩光对视功能的影响, 并未直接反映出患者眼内的散射光情况, C-Quant恰恰可以添补这一空缺, 能够精确、有效地测量有眩光条件下有多少光在视网膜上形成了散射, 为眼科医生定量患者眼内的散射光提供了更加简捷、直观、方便的途径。
4 Oculus C-Quant临床应用 4.1 诊断早期白内障 4.1.1 散射光是评价白内障患者晶体混浊程度的最有效指标MICHAEL等[22]用C-Quant测量了20~89岁的2 422名欧洲司机的眼内散射光, 对患有白内障的患者采用晶状体混浊分类标准(lens opacities classification system Ⅲ, LOCS Ⅲ)进行分类, 建立LOCS Ⅲ与视力、CS、眼内散射光的对数回归方程, 结果显示眼内散射光对LOCS Ⅲ评分的偏回归系数最大(P < 0.01), 标准化β=0.44, 眼内散射光对LOCS Ⅲ的R2=0.27, 最佳矫正视力和CS对LOCS Ⅲ的R2均为0.10, 说明眼内散射光与晶状体混浊程度的相关性强于视力和CS, 表明眼内散射光是评价白内障患者晶状体混浊程度的最有效指标。ADAMSONS等[20]用BAT和Berkeley Glare Test 2种方法测试早期白内障患者(视力 > 20/40)的眩光评分, 均得出后囊膜下白内障的眩光最强, 皮质性白内障的眩光次之, 核性白内障的眩光最弱的结论。邢晓杰等[23]应用C-Quant测量不同类型年龄相关性白内障眼内散射光值后发现, 后囊下白内障产生眼内散射光最高, 其次为混合性, 核性白内障组眼内散射光值随着年龄的增加而增大; 混合性和后囊下白内障眼内散射光值与最佳矫正视力(best corrected visual acuity, BCVA)相关性均不明显, 而核性白内障和皮质性白内障组眼内散射光值与BCVA均呈负相关。
4.1.2 眼内散射光测量可解释早期白内障主观视觉较差的原因临床中常见到有些早期白内障患者(无其他眼病)主观感觉和客观测得的视力、CS不匹配, 尤以有驾车需求者为甚, 表现为视力下降不明显, 但在强烈的光线下有严重的视觉质量下降的主诉, 如光晕, 畏光, 视物模糊, 夜间驾驶能力较差, 色彩和对比度下降等[18]。这可以从散射光的角度来解释。晶状体的生理形态随年龄发生改变, 是眼内散射光呈年龄相关性的主要原因。当光线通过透明的晶状体时, 造成大约40%的眼内散射[24], 研究[20]表明, 强烈的光线通过混浊的晶状体时会产生更大的散射, 散射光在眼内形成较强的光幕, 使投射在视网膜上的影像叠加在一起, 造成光幕性视网膜照明, 视网膜敏感性部分或全部降低, 引起物像的对比度大幅下降, 从而使患者感觉视物模糊。当早期白内障患者的晶状体混浊尚未侵害视轴时, 对视力无明显影响[8, 25], 此时最先表现出的是强烈光线下眼内散射光引起的视功能下降。因此, 散射光的检查对于视力变化不明显的早期白内障患者有重要的临床意义[26]。
4.1.3 早期白内障患者手术的依据DE VRIES等[27]用C-Quant研究了66只植入AcrySof ReSTOR SA60D3人工晶状体(intraocular lens, IOL)和40只植入AcrySof SA60AT IOL的眼术后6个月的散射光, 并以与上述2组受试者年龄相符的非白内障患者作为对照组, 测量对照组受试者的眼内散射光, 结果表明, 2组IOL眼的散射光均低于同年龄非白内障患者的眼内散射光(P < 0.001)。VAN DEN BERG等[8]对2 422名司机的横断面研究也表明白内障超声乳化吸除联合IOL植入术后的受试者眼内散射光低于白内障患者眼内散射光。由于眩光对白内障患者的主观视觉影响较大, 而白内障超声乳化吸除联合IOL植入术能有效地改善晶状体混浊引起的视网膜散射光, 改善患者的视觉质量, JAFFE [25]曾提出将眩光作为白内障的手术指征。ADAMSONS等[28]认为对于轻度视力下降却有失能眩光的早期白内障患者, 手术可以消除症状。因此主张将眩光作为白内障的手术指征之一。
C-Quant用于术前散射光计量, 可预测哪些患者更有可能得到主观视觉改善, 同时也可将散射光的计量作为白内障手术的指征, 但关于散射光计量log (s)参考值范围是多少时为白内障手术的合适手术时机, 仍需要大样本的多中心临床试验探讨论证。
4.2 评估IOL的性能C-Quant可以用于单焦点和多焦点IOL及不同材料IOL的性能评估。DE VRIES等[27]用C-Quant研究了66只植入AcrySof ReSTOR SA60D3 IOL和40只植入AcrySof SA60AT IOL的IOL眼术后6个月的散射光, 结果得出多焦点晶状体组的log (s) =1.20±0.16, 单焦点晶状体组的log (s) =1.10± 0.19, 当矫正了年龄对2组数值的影响后, 单焦点组比多焦点组散射光平均下降0.078 log (s)单位(P = 0.026)。HOFMANN等[29]的结果与前者不同, 他们用C-Quant对IOL植入术后18个月的患者进行眼内散射光测量, 40例植入AcrySof ReSTOR IOL (SA60D3), 40例植入AcrySof SA60AT IOL, 75%植入ReSTOR SA60D3 IOL和80%植入AcrySof SA60AT IOL的患者术后眼内散射光降低, 但没有统计学差异(P = 0.079), 而问卷调查则显示植入ReSTOR SA60D3 IOL组在各种光条件下(白天, 暗光和夜晚)抱怨评分更高(P < 0.001)。TANG等[30]应用C-Quant对70例植入TecnisZA 9003 IOL、SensarAR40e IOL、SA60AT IOL、XLSTABI ZO IOL或Akeros AO IOL术后3~4周的IOL眼进行散射光测量发现, 正常瞳孔下, 疏水性IOL的散射光明显高于亲水性IOL (P < 0.05)。瞳孔扩张后, 非球面IOL的散射光明显高于球面IOL (P < 0.05)。
4.3 评估激光角膜屈光矫正术的预后角膜屈光矫正术后同样存在眩光的问题[9, 31]。BARRETO等[3]应用C-Quant测量比较了波前像差引导的准分子激光原位角膜磨镶术(wavefront-guided laser in situ keratomileusis, WFG-LASIK)和波前像差引导的准分子激光角膜表面切削术(wavefront-guided photorefractive keratectomy, WFG-PRK) 2种术式矫正屈光后眼内散射光值的变化, 结果显示, WFG-LASIK和WFG-PRK术后1年眼内散射光值均较术前无明显增加, 且2种术式之间没有统计学差异(P = 0.306)。李晶等[32]用C-Quant测量机械法准分子激光上皮瓣下角膜磨镶术(epipolis laser in situ keratomileusis, Epi-LASIK)和LASIK术前及术后1、4、10个月的散射光值, 发现散射光值在术后早期显著增加, 但随时间的推移而部分降低。刘洋辰等[33]研究了飞秒LASIK手术前后散射光的变化, 发现术后1个月内散射光计量值增加, 术后6个月恢复正常。徐路路等[34]对比分析了微小切口基质透镜切除术(small incision lenticule extraction, SMILE)与飞秒LASIK矫治屈光后眼内散射光计量值的变化, 同样发现飞秒LASIK术后眼内散射光计量值增加, 尤以早期最为显著, 而SMILE手术前后术眼内散射光计量值变化不明显, 2种手术后的散射光计量值随时间的延长逐渐恢复。
4.4 评估配戴角膜接触镜后的视觉质量有研究[35]称使用角膜接触镜能增加眼内的散射光, 沉着物和葡萄疮是散射光增加的主要原因。FORTUIN等[36]采用随机双盲交叉对照研究了2种硬性高透氧性角膜接触镜(rigid gas permeable contact lens, RGP)和镜片表面清洁剂对眼内散射光的影响, 将30例患者(60眼)随机分成2组, 分别使用Miraflow和Boston 2种清洁剂, 交叉配戴Boston XO和Comfort O2 (ONSI-56)材料的镜片, 分别用C-Quant测量使用镜片时眼内散射光及不使用镜片时眼内散射光, 结果表明, 配戴RGP会使眼内散射光增加, Comfort O2和Boston XO 2种镜片引起的眼内散射光无统计学差异(P < 0.05)。
4.5 筛查其他眼科病变玻璃体混浊[37]、角膜营养不良[38]及视网膜病变, 如黄斑变性、视网膜色素变性、青光眼等, 都会使眼内散射光增加, C-Quant同样可以作为这些疾病的辅助检查。
综上所述, Oculus C-Quant散射光计量仪采用"补偿比较"的方法, 通过CF精确定量眼内的散射光, 测得的散射光计量可估量晶状体的混浊程度, 能够发现眩光、光晕和夜间视力差的原因, 可广泛用于视功能检查。C-Quant尤其适用于早期白内障患者, 可结合裂隙灯检查对主观视觉下降而客观视力下降不明显的早期白内障患者进行诊断, 也可用于白内障超声乳化联合IOL植入术术后视觉质量的评价, 还可用于不同材料IOL及晶状体异位的研究、角膜屈光手术的预后评价, 同时, 对其他眼科疾病也有一定的诊断价值。
| [1] |
黄锦海, 林施施, 王勤美, 等. C-Quant散射光计量仪测量散射光的重复性和再现性研究[J]. 中华实验眼科杂志, 2012, 30(2): 160-163. DOI:10.3760/cma.j.issn.2095-0160.2012.02.017 |
| [2] |
VAN DEN BERG TJTP, FRANSSEN L, KRUIJT B, et al. History of ocular straylight measurement:a review[J]. Zeitschrift Für Medizinische Physik, 2013, 23(1): 6-20. DOI:10.1016/j.zemedi.2012.10.009 |
| [3] |
BARRETO J JR, BARBONI MT, FEITOSA-SANTANA C, et al. Intraocular straylight and contrast sensitivity after contralateral wavefront-guided LASIK and wavefront-guided PRK for myopia[J]. J Refract Surg, 2010, 26(8): 588-593. DOI:10.3928/1081597X-20090930-01 |
| [4] |
VAN DER MEULEN IJE, ENGELBRECHT LA, VAN VLIET JMJ, et al. Straylight measurements in contact lens wear[J]. Cornea, 2010, 29(5): 516-522. DOI:10.1097/ico.0b013e3181c11e29 |
| [5] |
黄锦海, 郑博, 王勤美. 眼内散射光的临床意义及测量方法的研究进展[J]. 中华实验眼科杂志, 2012, 30(12): 1139-1143. DOI:10.3760/cma.j.issn.2095-0160.2012.12.022 |
| [6] |
PUTNAM CM, BLAND PJ, BASSI CJ. Influence of macular pigment optical density spatial distribution on intraocular scatter[J]. J Optom, 2017, 10(1): 63-68. DOI:10.1016/j.optom.2015.10.001 |
| [7] |
VOS JJ. On the cause of disability glare and its dependence on glare angle, age and ocular pigmentation[J]. Clin Exp Optom, 2003, 86(6): 363-370. DOI:10.1111/j.1444-0938.2003.tb03080.x |
| [8] |
VAN DEN BERG TJ, VAN RIJN LJ, MICHAEL R, et al. Straylight effects with aging and lens extraction[J]. Am J Ophthalmol, 2007, 144(3): 358-363. DOI:10.1016/j.ajo.2007.05.037 |
| [9] |
王雁, 郝维婷. 有效控制角膜屈光手术后光学并发症以不断提高手术后视觉质量[J]. 中华实验眼科杂志, 2017, 35(6): 481-485. DOI:10.3760/cma.j.issn.2095-0160.2017.06.001 |
| [10] |
刘洋辰, 王雁. 人眼散射光研究进展[J]. 中华眼科杂志, 2016, 52(1): 73-76. DOI:10.3760/cma.j.issn.0412-4081.2016.01.019 |
| [11] |
COPPENS JE, FRANSSEN L, VAN RIJN LJ, et al. Reliability of the compensation comparison stray-light measurement method[J]. J Biomed Opt, 2006, 11(3): 34027. DOI:10.1117/1.2209555 |
| [12] |
FRANSSEN L, COPPENS JE, VAN DEN BERG TJ. Compensation comparison method for assessment of retinal straylight[J]. Invest Ophthalmol Vis Sci, 2006, 47(2): 768-776. DOI:10.1167/iovs.05-0690 |
| [13] |
VAN DEN BERG TJ, FRANSSEN L, COPPENS JE. Straylight in the human eye:testing objectivity and optical character of the psychophysical measurement[J]. Ophthalmic Physiol Opt, 2009, 29(3): 345-350. DOI:10.1111/j.1475-1313.2009.00638.x |
| [14] |
COPPENS JE, FRANSSEN L, VAN DEN BERG TJ. Reliability of the compensation comparison method for measuring retinal stray light studied using Monte-Carlo simulations[J]. J Biomed Opt, 2006, 11(5): 054010. DOI:10.1117/1.2357731 |
| [15] |
PUELL M, BARRIO AR, ANTONA B. The repeatability of straylight measurements using the C-Quant in young and older adults[J]. Acta Ophthalmol, 2015, 93: S255. DOI:10.1111/j.1755-3768.2015.0457 |
| [16] |
GUBER I, BACHMANN LM, GUBER J, et al. Reproducibility of straylight measurement by C-Quant for assessment of retinal straylight using the compensation comparison method[J]. Albrecht Von Graefes Arch Fur Klinische Und Exp Ophthalmol, 2011, 249(9): 1367-1371. DOI:10.1007/s00417-011-1704-y |
| [17] |
VAN RIJN LJ, NISCHLER C, GAMER D, et al. Measurement of stray light and glare:comparison of Nyktotest, Mesotest, stray light meter, and computer implemented stray light meter[J]. Br J Ophthalmol, 2005, 89(3): 345-351. DOI:10.1136/bjo.2004.044990 |
| [18] |
卢奕, 叶鸿飞. 白内障与眼内散射光[J]. 中华眼科杂志, 2013(8): 765-768. DOI:10.3760/cma.j.issn.0412-4081.2013.08.020 |
| [19] |
周晓东, 汪芳润. 青年人的眩光失能测定[J]. 眼科新进展, 1999, 19(5): 312-313. DOI:10.13389/j.cnki.rao.1999.05.004 |
| [20] |
ADAMSONS I, RUBIN GS, VITALE S, et al. The effect of early cataracts on glare and contrast sensitivity. A pilot study[J]. Arch Ophthalmol, 1992, 110(8): 1081-1086. DOI:10.1001/archopht.1992.01080200061025 |
| [21] |
SUPERSTEIN R, BOYANER D, OVERBURY O. Functional complaints, visual acuity, spatial contrast sensitivity, and glare disability in preoperative and postoperative cataract patients[J]. J Cataract Refract Surg, 1999, 25(4): 575-581. DOI:10.1016/s0886-3350(99)80059-5 |
| [22] |
MICHAEL R, VAN RIJN LJ, VAN DEN BERG TJ, et al. Association of lens opacities, intraocular straylight, contrast sensitivity and visual acuity in European drivers[J]. Acta Ophthalmol, 2009, 87(6): 666-671. DOI:10.1111/j.1755-3768.2008.01326.x |
| [23] |
邢晓杰, 汤欣, 宋慧. 不同类型年龄相关性白内障眼内散射光的检测及其临床意义[J]. 中华实验眼科杂志, 2013, 31(4): 386-389. DOI:10.3760/cma.j.issn.2095-0160.2013.04.017 |
| [24] |
ABRAHAMSSON M, THAUNG J, SJÖSTRAND J. Dim the light! Glare problems in a world with ever increasing demands on visual acuity[J]. Lakartidningen, 1997, 94(41): 3607-3611. |
| [25] |
JAFFE NS. Glare and contrast:indications for cataract surgery[J]. J Cataract Refract Surg, 1986, 12(4): 372-375. DOI:10.1016/s0886-3350(86)80098-0 |
| [26] |
NEUMANN AC, MCCARTY GR, LOCKE J, et al. Glare disability devices for cataractous eyes:a consumer' s guide[J]. J Cataract Refract Surg, 1988, 14(2): 212-216. DOI:10.1016/s0886-3350(88)80098-1 |
| [27] |
VRIES NED, FRANSSEN L, WEBERS CAB, et al. Intraocular straylight after implantation of the multifocal AcrySof ReSTOR SA60D3 diffractive intraocular lens[J]. J Cataract Refract Surg, 2008, 34(6): 960-962. |
| [28] |
ADAMSONS IA, VITALE S, STARK WJ, et al. The association of postoperative subjective visual function with acuity, glare, and contrast sensitivity in patients with early cataract[J]. Arch Ophthalmol, 1996, 114(5): 529-536. DOI:10.1001/archopht.1996.01100130521004 |
| [29] |
HOFMANN T, ZUBERBUHLER B, CERVINO A, et al. Retinal straylight and complaint scores 18 months after implantation of the AcrySof monofocal and ReSTOR diffractive intraocular lenses[J]. J Refract Surg, 2009, 25(6): 485-492. DOI:10.3928/1081597X-20090512-02 |
| [30] |
TANG Y, SONG H, CHEN J, et al. Comparison of pseudophakic retinal straylight in spherical/aspherical and hydrophobic/hydrophilic intraocular lens[J]. Int J Ophthalmol, 2015, 8(6): 1146-1150. DOI:10.3980/j.issn.2222-3959.2015.06.12 |
| [31] |
TORRICELLI AA, PAREDE TR, NETTO MV, et al. Intraocular straylight before and after low myopic photorefractive keratectomy with and without mitomycin C[J]. Arq Bras Oftalmol, 2016, 79(2): 88-91. DOI:10.5935/0004-2749.20160027 |
| [32] |
李晶, 王雁, 左彤, 等. 准分子激光角膜屈光手术后散射的变化及其相关因素分析[J]. 中华眼科杂志, 2011, 47(7): 589-595. DOI:10.3760/cma.j.issn.0412-4081.2011.07.004 |
| [33] |
刘洋辰, 王雁, 李晶, 等. 飞秒激光角膜原位磨镶术手术前后散射变化及其影响因素分析[J]. 中华实验眼科杂志, 2012, 30(12): 1096-1099. DOI:10.3760/cma.j.issn.2095-0160.2012.12.012 |
| [34] |
徐路路, 王雁, 刘洋辰, 等. SMILE与FS-LASIK术后散射变化特性的比较[J]. 中华实验眼科杂志, 2015, 33(2): 159-164. DOI:10.3760/cma.j.issn.2095-0160.2015.02.013 |
| [35] |
COUPLAND SG, KIRKHAM TH. Improved contrast sensitivity with antireflective coated lenses in the presence of glare[J]. Can J Ophthalmol, 1981, 16(3): 136-140. |
| [36] |
FORTUIN MF, SCHILPEROORT J, EVANS BJ, et al. Randomised controlled trial of the effects of two rigid gas permeable (RGP) contact lens materials and two surface cleaners on straylight values[J]. Ophthalmic Physiol Opt, 2009, 29(5): 497-508. DOI:10.1111/j.1475-1313.2009.00660.x |
| [37] |
CASTILLA-MARTI M, VAN DEN BERG TJ, DE SMET MD. Effect of vitreous opacities on straylight measurements[J]. Retina (Philadelphia, Pa), 2015, 35(6): 1240-1246. DOI:10.1097/IAE.0000000000000456 |
| [38] |
CASTAÑO-MARTÍN B, GROS-OTERO J, MARTÍNEZ J, et al. Study of light scattering using C-Quant® in patients with Fuchs' endothelial dystrophy:a pilot study[J]. Arch Soc Esp Oftalmol, 2017, 92(11): 516-520. DOI:10.1016/j.oftal.2016.12.017 |
 2020, Vol. 49
2020, Vol. 49