文章信息
- 赵桂敏, 刁兰萍, 刘丽宏, 吴晓琳, 高哲, 高玉环
- ZHAO Guimin, DIAO Lanping, LIU Lihong, WU Xiaolin, Gao Zhe, GAO Yuhuan
- f101基因3’端非翻译区微小RNA结合位点单核苷酸多态性与非霍奇金淋巴瘤患者预后的关系
- Single nucleotide polymorphism at the microRNA binding site in the 3'-untranslated region of the f101 gene and prognosis of non-Hodgkin lymphoma
- 中国医科大学学报, 2020, 49(12): 1101-1105
- Journal of China Medical University, 2020, 49(12): 1101-1105
-
文章历史
- 收稿日期:2020-03-04
- 网络出版时间:2020-12-03 10:27
非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)是全世界第五大最常见癌症相关死亡病因[1],造成全球约20万的年死亡病例[2]。美国癌症登记处指出,NHL的发病率在过去的几十年中呈倍数增长趋势[3]。NHL是以B或T和NK淋巴细胞单克隆增殖为特点的一组异质性免疫系统肿瘤[4-5]。以往研究[6-8]表明,不同亚型的NHL生存模式不同,而且有不同的预后危险因素。国际预后指数(international prognostic index,IPI)模型1993年被应用于侵袭性NHL患者的预后预测,在IPI模型中临床特征对于预后至关重要[9]。但IPI评分一样的患者也可能显示不同的生存和预后。研究[10]发现遗传因素可以预测NHL的生存和预后。微小RNA (microRNA,miRNA)参与多种生物活动包括发育、分化、凋亡、生存、衰老、翻译抑制,并促进信使RNA的降解和代谢[11-12]。miRNA在肿瘤中扩增或过表达,通过结合靶基因3’端非翻译区(3’ untranslated regions,3’-UTRs)的互补序列沉默靶基因从而促进肿瘤发展[13]。在3’-UTRs靶位点的基因多态性改变miRNA和靶基因之间亲和力,从而影响靶基因的表达并修改致癌作用[14]。然而,迄今为止miRNA相关单核苷酸多态性(miRNA related single nucleotide polymorphism,miR-SNPs)和NHL的研究报告很少。本研究中选择f101 rs4901706来评估其对NHL癌症风险和预后的作用。
1 材料与方法 1.1 标本来源选取2006年1月1日至2015年10月1日于河北医科大学第四医院血液科治疗的258例患者作为病例组。所有患者均来自中国北方地区。其中,男152例,女106例,年龄14~87岁,中位年龄为50岁。将患者按照造血与淋巴组织肿瘤WHO分类: (1)惰性淋巴瘤(50例),包括黏膜相关淋巴组织类型淋巴瘤、滤泡淋巴瘤、淋巴浆细胞淋巴瘤,小淋巴细胞性淋巴瘤/慢性淋巴细胞白血病和T大颗粒淋巴细胞白血病;(2)侵袭性淋巴瘤(165例),包括弥漫型大B细胞淋巴瘤,套细胞淋巴瘤,外周T细胞淋巴瘤,间变性大细胞淋巴瘤,血管免疫母T细胞淋巴瘤;(3)高度侵略性淋巴瘤(32例),包括T和B淋巴母细胞白血病,鼻腔NK/T细胞淋巴瘤,伯基特淋巴瘤。其余11例患者为不明亚型。选取2011年1月1日至2016年1月1日于河北医科大学第四医院健康体检者110例作为对照。本研究获得河北医科大学第四医院伦理委员会批准(2016MEC066),所有参与者均知情同意。
1.2 DNA提取和f101基因分型基因组DNA应用向导基因组DNA提取工具提取。miRNA结合位点f101 (rs4901706)的单核苷酸多态性(single nucleotide polymorphism,SNP)应用连接酶检测反应方法进行基因分型。引物序列为F:5’-AAACTAAGTCATCTCCCAGATA-3’;R:5’-GTCATCTGGTGAAAGACTGGA-3’。扩增DNA片段根据NCBI数据库(http://www.ncbi.nlm.nih.gov/snp)。聚合酶链反应应用PCR混合试剂盒按照制造商的说明进行(Promega)。DNA产品应用ABI 3730XL基因分析仪分离。连接用探针为S1 (5’-TTTTTTTTTTAATGGGGTATTCAGTGACTAAGA-3’),S2 (5’-TTTTTTTTTTTTTAATGGGGTATTCAGTGACTAAGG-3’),S3 (5’-TCTGCTATTTATGCAAAATTCTGTTTTTTTT-3’)。多态性被证实基于rs4901706不同等位基因的长度差异。
1.3 统计学分析采用SPSS 18.0软件包进行统计分析。应用log-rank检验及Kaplan-Meier法计算3年总生存率。多因素生存分析采用Cox比例风险模型。P < 0.05为差异有统计学意义。
2 结果 2.1 随访结果258例患者的随访时间为10~36个月,随访率为100%。期间169例患者死亡,死亡原因分别为疾病进展(121例)、感染(25例)、出血(9例)和其他(14例)。3年生存率为34.5% (89/258)。
2.2 临床病理特征与NHL患者生存率之间的关系单因素分析结果显示,B细胞型患者高于T细胞型患者(P = 0.005);骨髓非浸润患者高于骨髓浸润患者(P = 0.001);无B症状患者高于有B症状患者(P = 0.001);乳酸脱氢酶(lactic dehydrogenase,LDH)水平正常患者高于LDH水平偏高患者(P < 0.001);肿瘤惰性患者高于侵袭性和高度侵袭性患者(P均 < 0.05),肿瘤侵袭性患者高于高度侵袭性患者(P = 0.023);Ann Arbor分期为Ⅰ、Ⅱ期的患者高于分期为Ⅲ、Ⅳ期的患者(P < 0.001);原发部位为结外和淋巴结的患者高于原发病为白血病的患者(P < 0.001);IPI评分为低危的患者高于低中危、中高危和高危的患者(P均 < 0.05);T细胞亚型为AA型的患者高于AG/GG型患者(P = 0.025),见表 1。
| Clinical characteristics | n | 3-year survival rate (%) | P |
| Immunohistochemical subtype | 0.005 | ||
| B cell type | 160 | 50.5 | |
| T cell type | 98 | 32.8 | |
| Bone marrow infiltration | 0.001 | ||
| No | 206 | 48.1 | |
| Yes | 52 | 26.3 | |
| B symptoms | 0.001 | ||
| No | 108 | 60.1 | |
| Yes | 150 | 35.3 | |
| LDH level | < 0.001 | ||
| Normal | 168 | 58.2 | |
| On the high side | 90 | 18.9 | |
| Invasive | 0.023 | ||
| Invasive | 165 | 46.3 | |
| Inert | 50 | 70.1 | |
| High invasiveness | 32 | 21.7 | |
| Ann Arbor staging | < 0.001 | ||
| Ⅰ-Ⅱ | 84 | 65.6 | |
| Ⅲ-Ⅳ | 174 | 34.8 | |
| The primary site | < 0.001 | ||
| Outside the junction | 113 | 48.4 | |
| Lymph node | 132 | 45.5 | |
| Leukemia | 13 | 8.8 | |
| IPI score | < 0.001 | ||
| Low-risk | 91 | 67.1 | |
| Low-to moderate-risk | 99 | 38.8 | |
| Moderate-to high-risk | 52 | 21.6 | |
| High-risk | 16 | 0.0 | |
| f101 genotyping | 0.017 | ||
| AA | 27 | 65.9 | |
| AG/GG | 231 | 34.8 | |
| T cell subtype | 0.025 | ||
| AA | 8 | 56.0 | |
| AG/GG | 77 | 15.0 |
2.3 f101基因型的分布及其与NHL患者生存率之间的关系
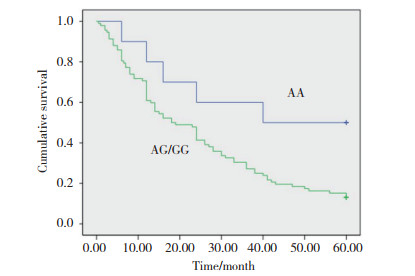
f101基因型与NHL患者临床特征(Ann Arbor分期、LDH水平、IPI评分、肿瘤侵袭性)的相关性通过χ2检验进行评估,未发现相关性,见表 2。f101基因型为AA型的患者27例(10.5%),AG/GG基因型的患者为231例(89.5%)。f101基因型为AA型患者的3年生存率高于基因型为AG/GG型的患者(P = 0.017),见图 1。
| Clinical characteristics | f101 | P | |
| AA | AG/GG | ||
| Ann Arbor staging | 0.457 | ||
| Ⅰ/Ⅱ | 15 | 108 | |
| Ⅲ/Ⅳ | 12 | 123 | |
| LDH | 0.241 | ||
| Normal | 17 | 95 | |
| On the high side | 10 | 136 | |
| IPI score | 0.373 | ||
| Low-risk | 9 | 40 | |
| Low-to moderate-risk | 6 | 55 | |
| Moderate-to high-risk | 7 | 62 | |
| High-risk | 5 | 74 | |
| Invasive | 0.382 | ||
| Invasive | 9 | 77 | |
| Inert | 11 | 60 | |
| High invasiveness | 7 | 94 | |
|
| 图 1 rs4901706基因型与TCL生存相关性 Fig.1 Correlation between the rs4901706 genotype and survival of TCL patients |
2.4 NHL患者f101基因型及临床病理特征与患者生存率之间的关系
将上述单因素纳入多因素Cox比例风险回归模型分析显示,f101 AG/GG基因型可作为NHL患者的独立预后指标,与患者的生存率(RR:1.768,95%CI:1.045~2.997,P = 0.035)密切相关;同时患者的年龄、侵袭性、原发部位和IPI评分也与患者生存率密切相关(P < 0.05),见表 3。
| Clinical characteristics | The relative risk | 95%CI | P |
| Age (year) | 0.001 | ||
| > 60 | 1 | ||
| ≤60 | 2.287 | 0.967-0.989 | |
| Invasive | 0.022 | ||
| Inert | 1 | ||
| Invasive | 1.817 | 1.088-3.034 | |
| The primary site | 0.020 | ||
| Outside the junction | 1 | ||
| Lymph node | 1.629 | 1.080-2.456 | |
| Leukemia | 5.577 | 2.176-14.292 | |
| IPI score | < 0.001 | ||
| Low-risk | 1 | ||
| Low-to moderate-risk | 2.084 | 1.593-4.936 | |
| Moderate-to high-risk | 5.434 | 2.369-12.467 | |
| High-risk | 37.397 | 11.465-121.988 | |
| f101 genotyping | 0.035 | ||
| AA | 1 | ||
| AG/GG | 1.768 | 1.045-2.997 |
3 讨论
本研究对258例NHL患者选择f101基因rs4901706位点的miR-SNP进行分析,评估其与NHL癌症风险和预后的相关性。结果发现rs4901706基因多态性与NHL癌症风险无关。f101 rs4901706 AA基因型患者的生存时间比AG/GG基因型更长。多因素分析表明,f101 rs4901706 AA基因型是NHL生存的一个独立预后变量。结果同样适用于TCL亚组。
miRNA途径已成为调控肿瘤发生的关键系统。miRNA途径相关的SNP,被称为miR-SNPs,依据其位置以不同的方式调节miRNA的功能,可以直接影响miRNA的表达水平或影响miRNA与目标的相互作用[15]。研究miR-SNPs可以打开新的癌症生物学和临床肿瘤学研究领域,尤其是在危险分层、对治疗的反应等[16]。BRADSHAW等[17]首次报道MIR143中的miRSNP与高加索人的NHL风险降低相关。PECKHAM-GREGORY等[18]研究表明,一些miRNA-SNP与AIDS-NHL风险有关,并可能调节miRNA的表达。FU等[19]发现miR-618参与滤泡性淋巴瘤的发生,确定miR-618是滤泡性淋巴瘤的潜在危险生物标志物,并阐明了miR-618调控的淋巴瘤发生途径。本研究评估rs4901706 SNP对NHL癌症风险的预测能力,结果显示两者没有关联。YU等[20]使用许多类型的癌症作为一个整体研究对象,确定rs4901706 SNP与癌症风险有关,说明miRSNP癌症风险相关性趋势可能存在于某些特定的癌症患者。研究发现rs4901706的等位基因A与某些特定癌症风险相关,而本课题组前期研究发现该等位基因A提示NHL患者预后良好,说明参与NHL病因的miRNA-SNP未必影响患者预后,而影响预后的miRNA-SNP未必参与其中。
本研究结果显示,miRNA结合位点SNP影响癌症总生存。f101的3’端非翻译区rs4901706 SNP改变了其与miRNA的亲和力,从而影响它的表达;rs4901706 A→G过渡可能破坏miRNA结合位点的A:T键,调整f101表达。然而,本研究的结果还需要进一步验证。
总之,miRNA结合位点f101的SNP被发现是NHL总体生存的一个独立预后标志。miRNA结合位点的基因多态性分析可能有助于识别患者预后较差的亚组,从而为NHL患者制定治疗方案提供依据。
| [1] |
JEMAL A, SIEGEL R, XU J, et al. Cancer statistics, 2010[J]. CA:A Cancer J Clin, 2010, 60(5): 277-300. DOI:10.3322/caac.20073 |
| [2] |
JEMAL A. Global burden of cancer:opportunities for prevention[J]. Lancet, 2012, 380(9856): 1797-1799. DOI:10.1016/S0140-6736(12)61688-2 |
| [3] |
CULTRERA JL, DALIA SM. Diffuse large B-cell lymphoma:current strategies and future directions[J]. Cancer Control, 2012, 19(3): 204-213. DOI:10.1177/107327481201900305 |
| [4] |
DOTAN E, AGGARWAL C, SMITH MR. Impact of rituximab (Rituxan) on the treatment of B-cell non-Hodgkin's lymphoma[J]. P T, 2010, 35(3): 148-157. |
| [5] |
VIJAI J, KIRCHHOFF T, SCHRADER KA, et al. Susceptibility loci associated with specific and shared subtypes of lymphoid malignancies[J]. PLoS Genet, 2013, 9(1): e1003220. DOI:10.1371/journal.pgen.1003220 |
| [6] |
CHEN WL, TSAI WC, CHAO TY, et al. The clinicopathological analysis of 303 cases with malignant lymphoma classified according to the World Health Organization classification system in a single institute of Taiwan[J]. Ann Hematol, 2010, 89(6): 553-562. DOI:10.1007/s00277-009-0870-z |
| [7] |
LUMINARI S, CESARETTI M, RASHID I, et al. Incidence, clinical characteristics and survival of malignant lymphomas:a population-based study from a cancer registry in northern Italy[J]. Hematol Oncol, 2007, 25(4): 189-197. DOI:10.1002/hon.826 |
| [8] |
ABDELHAMID T, SAMRA M, RAMADAN H, et al. Clinical prognostic factors of diffuse large B cell non-Hodgkin lymphoma:a retrospective study[J]. J Egypt Natl Cancer Inst, 2011, 23(1): 17-24. DOI:10.1016/j.jnci.2011.07.003 |
| [9] |
INTERNATIONAL NON-HODGKIN'S LYMPHOMA PROGNOSTIC FACTORS PROJECT. A predictive model for aggressive non-Hodgkin's lymphoma[J]. N Engl J Med, 1993, 329(14): 987-994. DOI:10.1056/NEJM199309303291402 |
| [10] |
ZHANG Y, CHEN MB, ZHOU XY, et al. Lymphotoxin alpha (LTA) polymorphism is associated with prognosis of non-Hodgkin's lymphoma in a Chinese population[J]. PLoS One, 2013, 8(6): e66411. DOI:10.1371/journal.pone.0066411 |
| [11] |
BARTEL DP. MicroRNAs:target recognition and regulatory functions[J]. Cell, 2009, 136(2): 215-233. DOI:10.1016/j.cell.2009.01.002 |
| [12] |
AMBROS V. The functions of animal microRNAs[J]. Nature, 2004, 431(7006): 350-355. DOI:10.1038/nature02871 |
| [13] |
VENTURA A, JACKS T. MicroRNAs and cancer:short RNAs go a long way[J]. Cell, 2009, 136(4): 586-591. DOI:10.1016/j.cell.2009.02.005 |
| [14] |
LANDI D, GEMIGNANI F, NACCARATI A, et al. Polymorphisms within micro-RNA-binding sites and risk of sporadic colorectal cancer[J]. Carcinogenesis, 2007, 29(3): 579-584. DOI:10.1093/carcin/bgm304 |
| [15] |
SCHUETZ JM, DALEY D, GRAHAM J, et al. Genetic variation in cell death genes and risk of non-Hodgkin lymphoma[J]. PLoS One, 2012, 7(2): e31560. DOI:10.1371/journal.pone.0031560 |
| [16] |
NAVARRO A, MUNOZ C, GAYA AN, et al. MiR-SNPs as markers of toxicity and clinical outcome in Hodgkin lymphoma patients[J]. PLoS One, 2013, 8(5): e64716. DOI:10.1371/journal.pone.0064716 |
| [17] |
BRADSHAW G, HAUPT LM, AQUINO EM, et al. Single nucleotide polymorphisms in MIR143 contribute to protection against non-Hodgkin lymphoma (NHL) in caucasian populations[J]. Genes (Basel), 2019, 10(3): 185. DOI:10.3390/genes10030185 |
| [18] |
PECKHAM-GREGORY EC, THAPA DR, MARTINSON J, et al. MicroRNA-related polymorphisms and non-Hodgkin lymphoma susceptibility in the multicenter AIDS cohort study[J]. Cancer Epidemiol, 2016, 45: 47-57. DOI:10.1016/j.canep.2016.09.007 |
| [19] |
FU AL, HOFFMAN AE, LIU R, et al. Targetome profiling and functional genetics implicate miR-618 in lymphomagenesis[J]. Epigenetics, 2014, 9(5): 730-737. DOI:10.4161/epi.27996 |
| [20] |
YU ZB, LI Z, JOLICOEUR N, et al. Aberrant allele frequencies of the SNPs located in microRNA target sites are potentially associated with human cancers[J]. Nucleic Acids Res, 2007, 35(13): 4535-4541. DOI:10.1093/nar/gkm480 |
 2020, Vol. 49
2020, Vol. 49