文章信息
- 张娇, 于紫燕, 赵江月
- ZHANG Jiao, YU Ziyan, ZHAO Jiangyue
- Doxycycline诱导表达Msx2-GFP的鼠晶状体上皮Alpha-TN4细胞株的建立
- Establishment of Alpha-TN4 Cell Line Expressing Msx2-GFP Induced by Doxycycline
- 中国医科大学学报, 2019, 48(6): 499-501, 506
- Journal of China Medical University, 2019, 48(6): 499-501, 506
-
文章历史
- 收稿日期:2018-12-24
- 网络出版时间:2019-05-24 17:35
肌节同源盒基因同系物2(msh homobox 2,Msx2)作为肌节同源框基因家族的一员,其编码的转录抑制蛋白可调控细胞的存活与凋亡[1]。它多表达在间充质细胞与上皮细胞的交界处以及细胞增殖的区域,在体内控制着细胞的增殖和分化,与心血管、骨骼、眼耳鼻等组织发育密切相关,Msx2的表达异常或突变会对机体产生不良影响[2-3]。
在眼发育学研究领域,国外有研究[4]结果显示,在Msx2转基因鼠中发现小眼球畸形及视网膜发育缺陷。先前的研究[5]中也发现Msx2表达异常,通过抑制FoxE3基因并上调Prox1的表达来调控晶状体的发育。同时,敲除Msx2基因可通过激活Casp3/Casp8凋亡信号通路,引起晶状体组织中凋亡增加[6]。晶状体细胞凋亡是导致白内障发生的机制之一,因此,把Msx2作为靶因子导入晶状体上皮细胞,抑制细胞增殖和分化,触发凋亡,可能成为基因治疗晶状体及白内障相关疾病的一个突破性进展。
本研究利用基因开关调节系统(Tet-on),拟建立由doxycycline调控表达的Msx2诱导细胞株,探索其差异表达基因(differentially expressed genes,DEGs),为进一步的临床研究奠定基础。
1 材料与方法 1.1 实验材料细胞:实验组选取doxycycline诱导表达Msx2的Alpha-TN4细胞株M8;空载体细胞株T9作为对照。
1.2 细胞培养及诱导细胞株M8空载体T9在含胎牛血清的细胞培养液(dulbecco’s modified eagle’s medium,DMEM)过夜培养。经doxycycline(1 μg/mL)处理后,24 h后共聚焦荧光显微镜观察,并收集细胞。
1.3 蛋白提取及浓度测定培养的细胞用预冷的PBS洗3遍,加入适量(200 μL/60 mm皿)裂解液,细胞刮收取蛋白至EP管每次超声15 s,重复5次,放置30 min,4 ℃离心12 000 r/min,15 min,取上清。考马斯亮蓝蛋白测定试剂盒(北京吉美生物有限公司)测定样本液蛋白浓度。
1.4 二维凝胶电泳配制CyDye DIGE工作液(400 pmol/μL),根据蛋白定量结果,标本及1份混合内标各取50 μg加入1 μL浓度为400 pmol/μL的CyDye DIGE染料,避光。漩涡震荡,彻底混合,12 000 g 4 ℃离心10 min,收集底部标记混合物,在黑暗中冰上反应30 min。加入1 μL 10 mmol/L赖氨酸终止标记反应。充分混合,在黑暗中置于冰上10 min。每份样品加入同体积的补充液(7 mol/L尿素、2 mol/L硫脲、4%CHAPS、2%DTT、2% IPG Buffer),用再水化液(7 mol/L尿素、2 mol/L硫脲、18 mmol/L DTT、2% CHAPS、0.5% IPG Buffer)将样品体积补至340 μL,将18 cm IPG胶条(pH 3~pH 10,NL)置于胶条槽内,上样后在IPGphor固相pH梯度等电聚焦仪上行等电聚焦。整个过程避光。灌制12%SDS-PAGE胶,脱氧并保证胶面平齐。将IPG胶条置放在两低荧光玻璃板间的凝胶面上,用0.5%低融点琼脂糖溶液包埋。恒温20 ℃,行SDS-PAGE电泳(15 mA/胶,30 min;30 mA/胶,4 h)。整个过程避光,最后行考马斯亮蓝染色。
1.5 扫描及图像分析电泳所得凝胶用MilliQ冲洗后用Typhoon 9400荧光扫描仪在不同激发光下扫描成像,所使用波长如下:Cy2-488/520,Cy3-532/580,Cy5-633/679。所得的蛋白质组图谱用DeCyder 2-D凝胶图像分析软件进行检测、自动分析,光斑体积的差异作为实验组与对照组蛋白表达水平变化的衡量指标,采用Mann Whitney U-test进行统计学检验,P < 0.05为差异有统计学意义。
2 结果 2.1 建立由doxycycline诱导稳定表达Msx2的鼠晶状体上皮细胞株经过扩增培养后,G418筛选出明显由doxycycline调控诱导表达Msx2-GFP的Alpha-TN4细胞株,为M8克隆。同时,以空载体细胞株T9作为阴性对照。细胞株M8在无doxycycline存在的条件下不表达Msx2-GFP,在加入doxycycline(1 μg/mL)10 h后,Msx2-GFP开始有微量表达,随着时间增加,Msx2-GFP的表达量随之增高。细胞株M8和T9在doxycycline(1 μg/mL)处理24 h后,以共聚焦显微镜检测可见细胞株M8有Msx2-GFP明显表达,见图 1。

|
| A and B, M8 cell line; C and D, T9 cell line of the control group. 图 1 doxycycline处理24 h后诱导细胞株M8及T9 ×100 Fig.1 Induction of M8 and T9 cell lines by a 24-h doxycycline treatment ×100 |
2.2 二维电泳分析M8及T9细胞株蛋白质
由诱导的细胞株M8和空载体T9阴性对照样品分别获得二维凝胶电泳图谱,每组样品重复3次。经图像分析分别在实验组M8检测到5 460个点,对照组T9检测到5 389个点。其中M8与T9之间差异点有31个,见图 2。

|
| A, M8;B, T9. 图 2 二维电泳分析晶状体上皮细胞蛋白质 Fig.2 Two-dimensional gel electrophoresis of lens epithelial cell proteins |
2.3 RNA微阵列分析和array结果的分析
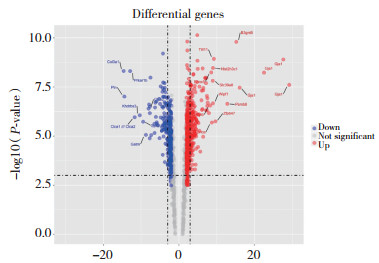
对M8及T9 2组细胞进行了基因表达微阵列分析。通过SAS统计软件筛选DEGs。结果显示,在Alpha-TN4细胞系中存在712个多于2倍的表达变化的DEGs,其中454个基因被上调,258个基因被下调。在下调的基因中,Col3α1基因下调明显,见图 3。对2组细胞进行实时PCR分析,检测到M8组mRNA的相对表达量为7.91±0.35,T9组mRNA的相对表达量为4.08±0.26。Col3α1表达量明显下降,此结果与上述结论保持一致。
|
| Fold change 图 3 M8及T9细胞株DEGs Fig.3 Differentially expressed genes in M8 and T9 cells |
3 讨论
Msx2是新近发现的参与调控细胞凋亡的关键蛋白。以往研究[7-8]多集中在Msx2对心血管、骨骼等组织发育的影响上,本研究利用基因开关调节系统(Tet-on),首次建立由doxycycline调控表达的Msx2诱导晶状体上皮细胞株。该系统利用改良的大肠杆菌E.coli的调节系统,靶基因的表达受四环素的衍生物doxycyclin精确调节,故具有低毒性、特异性、高敏感性,且不影响细胞内其他基因活性的特点[9]。在诱导细胞株中,Msx2受doxycycline的精确调节,使诱导细胞株建系成功。Msx2诱导细胞株的建立为研究Msx2功能提供了良好的细胞模型。
本研究采用比较蛋白质组学的理论和方法,对诱导细胞株M8和阴性对照细胞株T9蛋白质组进行分析和比较,检测差异明显的蛋白质。经过基因表达微阵列分析,分析出明显下调及上调的基因。并对其中在Msx2过表达细胞株M8中下调明显的Col3α1进行实时PCR分析验证,结果显示,过表达Msx2基因的晶状体上皮细胞与正常细胞相比,Col3α1的表达量明显下降,该结果与基因表达微阵列分析结果保持一致。
Col3α1作为一种Ⅲ型胶原,主要存在于细胞外基质中,尤其在人的血管内膜、肌肉等结缔组织中含量丰富[10]。在晶状体中,胶原纤维的异常增生会加速晶状体上皮细胞纤维化,加速细胞移行,从而导致晶状体浑浊。已知后发性白内障(posterior capsular opacification,PCO)的发生与晶状体囊膜的纤维化和基质的积聚和收缩有关[11]。其中晶状体囊膜由晶状体上皮细胞核纤维产生,富含Ⅳ型胶原蛋白,也含有Ⅰ型和Ⅲ型胶原及细胞外基质成分。研究发现正常情况下Ⅳ型胶原纤维均匀分布于晶状体囊全层,同时还存在Ⅰ型和Ⅲ型胶原,其中Ⅲ型胶原因具有特异性而使晶状体囊区别于眼球内其他基底膜组织[12-13]。而胶原纤维以及细胞外基质的异常沉积是PCO发生的重要病理机制[14]。本研究中Msx2过表达引起的Col3α1下调可能是晶状体上皮细胞发生凋亡的一个潜在机制,这一发现为PCO的基因治疗提供了新的研究思路。但Msx2与Col3α1之间是否存在直接联系,以及Col3α1如何影响Msx2,从而促发细胞凋亡,仍需进一步研究。
| [1] |
张登勇, 鲁正. MSX2基因与肿瘤关系的研究进展[J]. 中华临床医师杂志(电子版), 2013, 7(17): 138-139. DOI:10.3877/cma.j.issn.1674-0785.2013.17.063 |
| [2] |
SHAO JS, CHENG SL, PINGSTERHAUS JM, et al. Msx2 promotes cardiovascular calcification by activating paracrine Wnt signals[J]. J Clin Invest, 2005, 115(5): 1210-1220. DOI:10.1172/JCI24140 |
| [3] |
SATOKATA I, MA L, OHSHIMA H, et al. Msx2 deficiency in mice causes pleiotropic defects in bone growth and ectodermal organ formation[J]. Nat Genet, 2000, 24(4): 391-395. DOI:10.1038/74231 |
| [4] |
WU LY, LI M, HINTON DR, et al. Microphthalmia resulting from MSX2-induced apoptosis in the optic vesicle[J]. Invest Ophthalmol Vis Sci, 2003, 44(6): 2404-2412. DOI:10.1167/iovs.02-0317 |
| [5] |
于紫燕, 于雯婷, 刘佳, 等. 小鼠肌节同源盒基因同系物2条件性敲除在先天性白内障发生中的作用[J]. 中华眼视光学与视觉科学杂志, 2018, 20(1): 14-18. DOI:10.3760/cma.j.issn.1674-845X.2018.01.003 |
| [6] |
ZHAO J, WU X, WU D, et al. Embryonic surface ectoderm-specific mitofusin 2 conditional knockout induces congenital cataracts in mice[J]. Sci Rep, 2018, 8(1): 1522. DOI:10.1038/s41598-018-19849-2 |
| [7] |
SATOKATA I, MA L, OHSHIMA H, et al. Msx2 deficiency in mice causes pleiotropic defects in bone growth and ectodermal organ formation[J]. Nat Genet, 2000, 24(4): 391-395. DOI:10.1038/74231 |
| [8] |
CHENG SL, SHAO JS, CHARLTON-KACHIGIAN N, et al. Msx2 promotes osteogenesis and suppresses adipogenic differentiation of multipotent mesenchymal progenitors[J]. J Biol Chem, 2003, 14(46): 45969-45977. DOI:10.1074/jbc.M306972200 |
| [9] |
夏焱, 苏浩彬, 马国川, 等. 建立doxycycline诱导表达Xaf1的肿瘤细胞株[J]. 中山大学学报(医学科学版), 2005, 26(5): 528-532. DOI:10.3321/j.issn:1672-3554.2005.05.011 |
| [10] |
葛明旭, 朱玉方, 庞琦, 等. Ⅲ型胶原蛋白COL3A1基因多态性与颅内动脉瘤的关系[J]. 中国脑血管病杂志, 2008, 5(12): 560-562. DOI:10.3969/j.issn.1672-5921.2008.12.008 |
| [11] |
包秀丽, 刘婷婷, 王艳艳, 等. Wnt3a诱导人晶状体上皮细胞细胞外基质合成和胶原凝胶收缩的机制研究[J]. 中华实验眼科杂志, 2016, 34(7): 597-601. DOI:10.3760/cma.j.issn.2095-0160.2016.07.005 |
| [12] |
武惠, 石珍荣. 老年性白内障晶体囊和囊下上皮的超微结构[J]. 中华眼科杂志, 1990, 26(3): 168-170. |
| [13] |
DARK AJ, STREETEN BW. Precapsular film on the aging human lens:precursor of pseudoexfoliation?[J]. Br J Ophthalmol, 1990, 74(12): 717-722. DOI:10.1136/bjo.74.12.717 |
| [14] |
解芳, 钟洪珊, 张林. 后发性白内障发生机制研究进展[J]. 现代生物医学进展, 2008, 8(4): 754-756. DOI:10.3969/j.issn.1673-6273.2008.04.052 |
 2019, Vol. 48
2019, Vol. 48