文章信息
- 李茹, 刘爽, 张立敏, 马春燕, 杨军
- LI Ru, LIU Shuang, ZHANG Limin, MA Chunyan, YANG Jun
- 组织运动瓣环位移评价缩窄性心包炎和限制性心肌病患者左心室收缩功能及其在鉴别诊断中的价值
- Tissue Motion of Annular Displacement in the Evaluation of Left Ventricular Function and Differentiation between Constrictive Pericarditis and Restrictive Cardiomyopathy
- 中国医科大学学报, 2019, 48(5): 390-392, 397
- Journal of China Medical University, 2019, 48(5): 390-392, 397
-
文章历史
- 收稿日期:2018-11-30
- 网络出版时间:2019-05-13 10:38
研究[1]表明,尽管许多心脏疾病左心室射血分数(left ventricular ejection fraction,LVEF)仍在正常范围,但左心室收缩功能已出现不同程度的减低。组织运动瓣环位移(tissue motion of annular displacement,TMAD)能快速而准确的评估心脏疾病患者潜在的收缩功能异常,因而受到越来越多的关注。缩窄性心包炎(constrictive pericarditis,CP)与限制型心肌病(restrictive cardiomyopathy,RCM)的临床症状及血流动力学改变相似,而两者发病机制不同,治疗方法各异[2]。因此,通过超声新技术准确鉴别CP及RCM,对临床治疗具有重要的指导意义。虽然传统超声心动图及组织多普勒成像可以为临床诊断提供有价值的信息,但当患者合并严重二尖瓣钙化或心肌损伤等病变时,准确鉴别两者存在一定的局限性[3]。因此,本研究的目的是应用TMAD评价CP及RCM患者左心室收缩功能的改变及其在两者鉴别诊断的应用价值,为临床准确鉴别及治疗提供更多有意义的参考信息。
1 材料与方法 1.1 研究对象选取2014年2月至2017年2月在我院经手术证实的CP患者34例,其中男性22例,女性12例。所有患者术前均行经胸超声心动图检查,其中21例患者舒张早期血流速度随呼吸变化增加25%,8例超声心动图提示心包钙化。所有CP患者心电图均为窦性心律,超声心动图提示患者不合并其他心脏疾病。34例CP患者中,17例病因为结核性心包炎,10例为病毒性,7例为非特异性。同期选取32例RCM患者,其中男性15例,女性17例。32例RCM患者中,22例病因为心脏淀粉样变,经活检证实,10例为非特异性。超声诊断RCM:双房增大、LVEF > 50%、舒张期左心室容积减少和左心室舒张功能减低。同时选取35例健康人作为对照组,其中男性23例,女性12例。对照组排除心血管疾病史及器质性心脏病,普通检查如心电图、胸片和化验等均提示正常。对照组、CP组和RCM组患者性别、体质量、身高、血压、心率等基本临床资料无统计学差异。所有患者均签署知情同意书。
1.2 仪器与方法受检者采取左侧卧位,胸前连接心电图,使用Philips IE 33超声诊断仪,S5探头采集超声图像,频率为1.0~3.0 MHz。所有患者于平静呼吸时记录心电图及采集图像。二维超声切面常规数据测量参照美国超声心动图协会指南,并采用组织多普勒成像测量二尖瓣瓣环间隔和侧壁舒张早期峰值速度(Ea-sep和Ea-lat)。随后采集心尖四腔心切面的二维动态图像存储,帧频52~65 fps。TMAD分析采用QLAB 9.0工作站,在心尖四腔心切面中分别选择二尖瓣瓣环间隔及左心室侧壁,将另一点固定在心尖,运行软件后自动测量出二尖瓣瓣环相对心尖的位移,得出间隔和侧壁的二尖瓣瓣环位移(Dlat和Dsep)、平均位移(Dmid)及平均位移率(TMADmidpt%),TMADmidpt%=Dmid/左心室舒张末期长径。
1.3 统计学分析采用SPSS 17.0软件进行统计分析,计量资料采用
CP组与对照组相比,LVEF无统计学差异(P > 0.05),左心室内径变小,而RCM组较对照组和CP组LVEF降低,左心室壁心肌厚度增加(P < 0.05)。CP组患者Ea-sep较对照组和RCM组显著增加(P < 0.05),RCM组Ea-lat较对照组和CP组均减低(P < 0.05)。见表 1。
| Parameter | Control group(n = 35) | CP group(n = 34) | RCM group(n = 32) |
| Left ventricular end-diastolic diameter(mm) | 45.72±3.93 | 41.29±3.401) | 48.41±5.35 |
| Left ventricular end-systolic diameter(mm) | 32.58±3.41 | 28.01±3.571) | 37.66±5.052) |
| Interventricular septal thickness(mm) | 7.61±0.73 | 7.04±1.06 | 11.53±1.971),2) |
| Left ventricular posterior wall thickness(mm) | 7.52±0.82 | 7.69±0.97 | 11.35±2.021),2) |
| LVEF(%) | 63.06±4.22 | 64.31±5.09 | 56.21±7.041),2) |
| Ea-lat(cm/s) | 14.70±4.16 | 12.35±3.79 | 4.18±2.951),2) |
| Ea-sep(cm/s) | 9.72±2.39 | 12.11±2.471) | 4.54±1.991),2) |
| Dsep(mm) | 12.56±1.72 | 11.34±2.02 | 5.31±2.521),2) |
| Dlat(mm) | 13.49±2.46 | 9.02±2.711) | 4.89±2.431),2) |
| Dmid(mm) | 13.33±2.71 | 10.79±2.171) | 5.22±2.061),2) |
| TMADmidpt% | 17.21±3.17 | 14.16±2.821) | 5.36±2.741),2) |
| 1)P < 0.05 vs control group;2)P < 0.05 vs CP group. | |||
2.2 TMAD参数
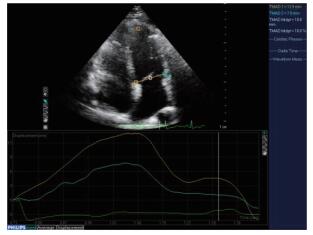
CP组患者Dlat较对照组减低(P < 0.05),而Dsep未见明显减低(P > 0.05),见图 1。RCM组Dsep、Dlat、Dmid及TMADmidpt%较对照组均减低(P < 0.05)。与CP组患者相比,RCM组Dsep、Dlat、Dmid及TMADmidpt%均减低,差异有统计学意义(P < 0.05)。见表 1。相关性分析显示,LVEF与Dsep的相关性较好(r = 0.69,P < 0.001)。
|
| Dlat(blue curve)in patients with CP was significantly lower than Dsep(yellow curve). 图 1 TMAD测量CP患者二尖瓣瓣环位移曲线图 Fig.1 TMAD-derived mitral annular displacement curve in patients with CP |
2.3 超声心动图参数鉴别CP和RCM的特异度和敏感度
ROC曲线显示,与其他参数相比,Ea-sep、Dsep、TMADmidpt%曲线下面积较大。Ea-sep的截点值为8 mm时,灵敏度为96.9%,特异度为90.2%(AUC=0.982,P < 0.001)。Dsep的截点值为8.45 mm时,灵敏度为95.6%,特异度为92.4%(AUC=0.976,P < 0.001)。此外,TMADmidpt%的截点值为10%时,灵敏度为82.3%,特异度为90.5%(AUC=0.967,P < 0.001)。
3 讨论LVEF是评价左心室收缩功能常用指标之一,也是大多数心脏疾病患者临床治疗预后的可靠预测指标。然而,通过超声心动图准确评估LVEF耗时较长,且容易受图像质量影响[4]。研究[5]表明,许多心脏疾病在LVEF减低之前,左心室收缩功能已受损。因此,准确评估患者心脏收缩功能具有重要的临床意义。TMAD是通过检测二尖瓣瓣环的运动及相对运动反映左心室收缩功能的超声技术,该技术无需清晰识别心内膜即可准确评价潜在的心脏功能受损,通过人工标记二尖瓣瓣环,自动追踪和测量,相对简单、方便,因此受到广泛关注。研究[6]发现,不同人群二尖瓣瓣环平面产生的位移与心脏每搏输出量的比例具有极好的相关性,且与磁共振等测量结果一致性良好。研究[7]表明,左心室内径对二尖瓣位移的测量有显著影响,然而TMAD可以通过左心室长轴来标化。
本研究中CP组患者与对照组相比LVEF无明显差异,但TMAD值明显较低,提示病变早期左心室收缩功能已经受到影响。此外,CP组患者Dlat较Dsep明显减低,提示心包粘连导致左心室纵向功能减低,侧壁运动受损较明显。与CP组和对照组相比,RCM组二尖瓣瓣环纵向位移明显降低,提示RCM患者左心室收缩功能减低比CP患者更明显。统计学分析显示Dsep与LVEF相关性良好,提示TMAD可用于早期评价左心室收缩功能,及时进行临床干预。
临床工作中准确鉴别CP和RCM相对困难,因为两者临床、血流动力学和超声心动图特点类似。本研究对CP和RCM患者二尖瓣瓣环位移进行了评估,并推测TMAD定量分析可能对上述疾病鉴别有重要的临床指导意义。本研究发现,当Ea-sep < 8 cm/s时可用于鉴别CP和RCM,与MAHMOUD等的研究[8]一致。但部分CP患者由于病程较长,常伴有瓣环显著钙化或心肌损伤,使Ea-sep敏感度下降。本研究中,Dsep、TMADmidpt%曲线下面积较大,敏感度较高。当患者Ea-sep > 8 cm/s时,Dsep和TMADmidpt%可以为CP和RCM鉴别提供参考信息。研究[9]表明,TMADmidpt%在评价左心室收缩功能方面优于瓣环位移。本研究发现,尽管CP组患者与对照组相比LVEF无显著差异,但CP组二尖瓣瓣环收缩期速度除纵向位移外均有所减低,这可能是由于心包运动受限和二尖瓣瓣环钙化影响瓣环附着位点活动所致。
本研究也有一定局限性,如样本量相对较少,期待临床大规模研究证实。且本研究中所有对象均为窦性心律,以排除心房颤动等心律不齐对结果造成的影响。此外,原发性RCM患者发病率较低,本研究中RCM患者病因较局限,大多数为心肌淀粉样变所致。
综上所述,本研究结果表明CP和RCM患者左心室收缩功能均减低,CP患者左心室收缩功能减低可能与心包粘连有关,而RCM患者减低更明显,可能与心肌僵硬度增加有关。TMAD可用于鉴别CP及RCM,为两者鉴别诊断提供更多更准确的参考信息,为临床诊断及治疗提供新的可靠的应用指标。
| [1] |
刘振林, 韩江涛, 杨启才, 等. 组织运动二尖瓣环位移评价急性前壁心肌梗死患者左室整体收缩功能的临床价值[J]. 中国循证心血管医学杂志, 2016, 8(11): 1341-1344. DOI:10.3969/j.issn.1674-4055.2016.11.16 |
| [2] |
HABIB G, BUCCIARELLI-DUCCI C, CAFORIO ALP, et al. Multimodality imaging in restrictive cardiomyopathies:an EACVI expert consensus document in collaboration with the "Working Group on myocardial and pericardial diseases" of the European Society of Cardiology Endorsed by The Indian Academy of Echocardiography[J]. Eur Heart J Cardiovasc Imaging, 2017, 18(10): 1090-1121. DOI:10.1093/ehjci/jex034 |
| [3] |
刘爽, 任卫东, 马春燕, 等. 左房节段二维应变参数鉴别缩窄性心包炎和限制型心肌病的价值[J]. 中国超声医学杂志, 2016, 32(2): 140-142. DOI:10.3969/j.issn.1002-0101.2016.02.016 |
| [4] |
HOMMA Y, HAYABUCHI Y, TERADA T, et al. Early diastolic left ventricular relaxation in normal neonates is influenced by ventricular stiffness and longitudinal systolic function[J]. Int Heart J, 2018, 59(1): 149-153. DOI:10.1536/ihj.17-125.S |
| [5] |
YOLDAŞ T, ÖRÜN UA, SAGSAK E, et al. Subclinical left ventricular systolic and diastolic dysfunction in type 1 diabetic children and adolescents with good metabolic control[J]. Echocardiography, 2018, 35(2): 227-233. DOI:10.1111/echo.13887 |
| [6] |
SEEMANN F, PAHLM U, STEDING-EHRENBORG K, et al. Time-resolved tracking of the atrioventricular plane displacement in cardiovascular magnetic resonance(CMR)images[J]. BMC Med Imaging, 2017, 17(1): 19. DOI:10.1186/s12880-017-0189-5 |
| [7] |
GRUE JF, STORVE S, DALEN H, et al. Automatic measurements of mitral annular plane systolic excursion and velocities to detect left ventricular dysfunction[J]. Ultrasound Med Biol, 2018, 44(1): 168-176. DOI:10.1016/j.ultrasmedbio.2017.09.002 |
| [8] |
MAHMOUD A, BANSAL M, SENGUPTA PP. New cardiac imaging algorithms to diagnose constrictive pericarditis versus restrictive cardiomyopathy[J]. Curr Cardiol Rep, 2017, 19(5): 43. DOI:10.1007/s11886-017-0851-0 |
| [9] |
ROBERSON DA, CUI W. Tissue doppler imaging measurement of left ventricular systolic function in children:mitral annular displacement index is superior to peak velocity[J]. J Am Soc Echocardiogr, 2009, 22(4): 376-382. DOI:10.1016/j.echo.2009.01.008 |
 2019, Vol. 48
2019, Vol. 48