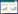文章信息
- 武晶晶, 孔令慧, 贾茹
- WU Jingjing, KONG Linghui, JIA Ru
- 小鼠Na+-K+-2Cl-共转运蛋白基因启动子克隆及20-HETE对其转录活性的影响
- Cloning of the Murine Na+-K+-2Cl- Cotransporter Gene Promoter and the Effect of 20-HETE on Its Transcriptional Activity
- 中国医科大学学报, 2019, 48(1): 29-33
- Journal of China Medical University, 2019, 48(1): 29-33
-
文章历史
- 收稿日期:2018-05-23
- 网络出版时间:2019-01-02 09:21
2. 中国医科大学生命科学学院生物科学系, 沈阳 110122
2. Department of Biological Science, School of Life Sciences, China Medical University, Shenyang 110122, China
Na+-K+-2Cl-共转运蛋白(Na+-K+-2Cl- cotransporter,Nkcc2)基因编码的呋塞米敏感的Na+-K+-2Cl-共转运蛋白是溶质转运体超家族成员之一,因此编码该蛋白的基因也被称为SLC12A1[1-2]。NKCC2蛋白主要分布在肾脏髓袢升支粗段,可将2个Cl-、1个Na+和1个K+同向转运到细胞内,参与肾脏近30% Na+的重吸收[3],是重要的高血压候选基因之一。
细胞色素P450 4F2编码的ω-羟化酶,可将花生四烯酸代谢生成二十羟基二十炭四烯酸(20-hydroxyeicosatetraenoic acid,20-HETE)[4],是重要的血压调节因子。前期本课题组成功地构建了CYP4F2转基因小鼠,并证明转基因小鼠肾脏CYP4F2蛋白表达增加,20-HETE合成增多,是研究20-HETE对血压调控机制的重要动物模型[5]。在对转基因小鼠的研究[6]中发现,转基因小鼠肾脏Nkcc2蛋白和mRNA表达均显著低于野生型小鼠,推测20-HETE在基因转录水平对Nkcc2存在调控作用。本研究通过构建小鼠Nkcc2基因启动子萤光素酶报告基因载体,利用20-HETE刺激转染了Nkcc2启动子报告基因载体的HEK-293T细胞,检测该报告基因的转录活性,初步分析20-HETE对Nkcc2基因启动子活性的影响,为阐明20-HETE对Nkcc2基因调节作用的分子机制奠定实验基础。
1 材料与方法 1.1 材料与试剂大肠杆菌JM109感受态细胞、pMD18-T Vector、Taq DNA polymerase、LA Taq DNA polymerase、DNA marker、T4 DNA连接酶、KpnⅠ和Hind Ⅲ限制性内切酶、琼脂糖均购自日本Takara公司,DMEM高糖培养基、胎牛血清购自美国HyClone公司,人类胚胎肾细胞系HEK293T细胞购自中国科学院上海细胞生物学研究所,胰蛋白酶购自美国Biosharp公司,萤光素酶报告基因载体pGL3-Basic、海参萤光素酶载体pRL-TK、Dual-GloTM双萤光素酶检测系统购自美国Promega公司,胰蛋白胨、酵母提取物、琼脂粉购自美国Sigma-Aldrich公司,胶回收、质粒制备试剂盒购自美国Axygen公司,脂质体LipofectamineTM2000购自美国Invitrogen公司,20-HETE购自美国Cayman公司,引物合成由中国南京金斯瑞生物科技有限公司完成,DNA测序由中国沈阳优唯生物科技有限公司完成。
1.2 方法 1.2.1生物信息学分析:应用生物信息学软件ALiBaba 2.1和TRANSFAC TESS,对小鼠Nkcc2基因启动子区-1 474 bp~+1 bp序列进行预测,比对2个软件的分析结果,寻找潜在的顺式作用元件。
1.2.2 小鼠Nkcc2基因启动子的克隆: 1.2.2.1 小鼠基因组DNA提取与引物设计取FVB/N小鼠鼠尾,常规方法提取小鼠基因组DNA,-20℃保存。根据Gen Bank数据库获得小鼠Nkcc2基因启动子的DNA序列,利用primer 5.0设计一对特异性引物P1和P2,PCR产物的长度为1 502 bp(-1 462 bp ~+40 bp)。设计引物:上游引物5'-GTCACCAATTTACCTTTCCCTT-3';下游引物5'-ACTTACCGCCCCATCCAG-3'。
1.2.2.2 启动子片段扩增及TA克隆以小鼠基因组DNA为模板进行PCR扩增。PCR产物经电泳鉴定,并利用胶回收纯化试剂盒回收纯化,纯化后的PCR产物连接到pMD-18T载体,16 ℃连接过夜。连接产物转化JM109型感受态细胞,涂布于LB琼脂板,进行蓝白斑筛选。挑取白色克隆于含有氨苄西林的LB培养液中扩增,经菌液PCR鉴定DNA片段插入方向,质粒提取试剂盒提取质粒,经DNA双向测序验证,正确的重组载体命名为pMD18-Nkcc2。
1.2.2.3 小鼠Nkcc2启动子萤光素酶报告基因载体的构建pMD18-Nkcc2重组载体经KpnⅠ和Hind Ⅲ双酶切,酶切产物经电泳鉴定,并利用胶回收纯化试剂盒回收纯化后,插入到pGL3-Basic载体,16 ℃连接过夜,转化JM109型感受态细胞,挑取单克隆菌落于含有Amp的LB培养液中扩增,试剂盒提取质粒经双酶切及双向测序鉴定,正确的重组载体命名为pGL3-Nkcc2。
1.2.3 小鼠Nkcc2基因启动子活性检测: 1.2.3.1 细胞培养及处理人类胚胎肾细胞系HEK293T细胞常规培养于含10%胎牛血清,100 U /mL青霉素,100 U /mL链霉素的DMEM高糖培养基中,37 ℃、5% CO2及饱和湿度的条件下培养,用含0.1%胰蛋白酶的消化液消化传代。
1.2.3.2 转染转染前1 d,用无抗生素培养基接种HEK293T细胞于24孔培养板中,接种密度以24 h后细胞增长至50%~70%为宜,分别用无血清无抗生素的培养基配置质粒DNA(小鼠Nkcc2启动子萤光素酶报告基因质粒及海参萤光素酶对照质粒)和脂质体LipofectamineTM2000,两者混合后室温孵育20 min,加入24孔培养板培养基中转染HEK293T细胞。细胞转染24 h后,用终浓度为1 μmol/L 20-HETE刺激2 h。
1.2.3.3 Dual-GloTM双萤光素酶检测系统检测荧光素酶活性依据试剂盒说明书PBS洗涤细胞后,加入100 μL 1×PLB裂解细胞,室温震荡15 min,将10 μL细胞裂解液移入萤光素酶检测管中,每管加入35 μL LAR Ⅱ,利用生物发光仪检测萤火虫萤光强度值,每管再加入35 μL Stop-reagent,检测海参萤光强度值,计算相对荧光值。
1.3 统计学分析实验数据均由3次独立实验结果的x±s表示,采用SPSS 17.0软件进行统计学分析,P < 0.05为差异有统计学意义。
2 结果 2.1 小鼠Nkcc2基因启动子区的生物信息学分析登录美国国家生物技术信息中心Gen Bank下载小鼠Nkcc2基因启动子区1 474 bp序列,应用生物信息学软件AliBaba2.1和TRANSFAC TESS分析小鼠Nkcc2基因启动子区结构(-1 474 bp~+1 bp),该区域存在多个顺式作用元件,其中NF-κB、AP-1等均与20-HETE调控靶基因转录活性相关,是20-HETE调控Nkcc2基因的潜在作用元件,见图 1。

|
| 图 1 小鼠Nkcc2基因启动子区潜在转录因子结合位点 Fig.1 Transcription factor binding site of the murine Nkcc2 gene promoter region |
2.2 Nkcc2基因启动子萤光素酶报告基因载体的构建
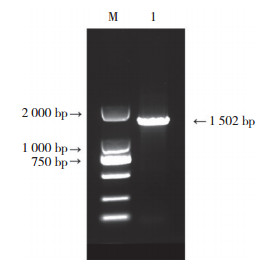
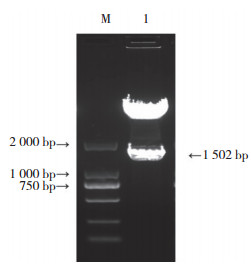
以小鼠基因组DNA为模板,利用PCR扩增小鼠Nkcc2基因启动子片段(-1 462 bp ~ +40 bp),PCR产物经琼脂糖凝胶电泳检测,片段大小与预期相符(图 2)。将PCR产物克隆至中间载体pMD18-T vector中,经PCR、双向测序及BLAST比较分析,鉴定出与GenBank序列一致的pMD18-Nkcc2重组载体,经限制性内切酶KpnⅠ和HindⅢ双酶切,回收目的短片段,插入到经KpnⅠ和HindⅢ双酶切的无启动子萤光素酶报告基因载体pGL3-Basic上。重组载体pGL3-Nkcc2经Kpn I和Hind Ⅲ双酶切,琼脂糖凝胶电泳分析,可见1 502 bp的阳性插入片段(图 3),且测序结果(图 4)与GenBank序列一致,证明用于分析Nkcc2启动子活性的萤光素酶报告基因载体构建成功。
|
| M, DL2000 marker; 1, PCR product. 图 2 小鼠Nkcc2基因启动子PCR产物电泳图 Fig.2 Agarose gel electrophoresis of the PCR-amplified murine Nkcc2 gene promoter fragmen |
|
| M, DL2000 marker; 1, the plasmid digested by KpnⅠand HindⅢ. 图 3 重组质粒双酶切鉴定电泳图 Fig.3 Agarose gel electrophoresis of the recombinant plasmid digested by restriction endonuclease |
|
| A, forward sequencing of the recombinant plasmid (-1 462 bp--701 bp); B, reverse sequencing of the recombinant plasmid (-732 bp-+40 bp). 图 4 重组质粒双向测序结果 Fig.4 Bidirectional sequencing of the recombinant plasmid |
2.3 20-HETE对Nkcc2基因启动子活性的影响
为验证20-HETE对Nkcc2基因启动子转录活性的调控作用,将pGL3-Nkcc2萤光素酶报告基因载体瞬时转染到HEK293T细胞24 h后,用1 μmol/L 20-HETE刺激2 h,并利用萤光素酶报告基因系统检测Nkcc2基因启动子转录活性。与对照组相比,20-HETE处理组Nkcc2基因启动子转录活性下降了27.5%(P < 0.05),说明20-HETE可有效下调Nkcc2基因启动子转录活性,初步验证了假设。
3 讨论原发性高血压是当今医学领域最具挑战性的心血管疾病之一,也是全球范围内重大公共问题。血压调节是一个多系统多环节的复杂过程,其中肾小管Na+重吸收作用通过调节机体水钠代谢,参与血压调节。Nkcc2基因编码的Na+-K+-2Cl-共转运体主要分布在肾脏髓袢升支粗段,参与肾小管Na+的重吸收,因此该基因是重要的高血压候选基因。
CYP4F2是另一个重要的高血压候选基因,该基因编码的ω-羟化酶是人类肾脏产生20-HETE最重要的酶之一。20-HETE主要由髓袢升支粗段生成,通过抑制Nkcc2发挥利尿钠作用,然而其具体机制尚不清楚。有报道[7-8]称20-HETE通过抑制ROMK活性,减少Nkcc2转运所需K+浓度差的势能,间接抑制Nkcc2的活性。本课题组前期利用4% NaCl的高盐饲料喂养具有高20-HETE水平的CYP4F2转基因小鼠,发现20-HETE与高盐有协同作用,通过经典的泛素-蛋白酶体系统降解肾脏Nkcc2蛋白,证明了20-HETE通过翻译后调控机制参与肾脏Nkcc2蛋白表达的调控。本研究中还发现,正常饮食CYP4F2转基因小鼠肾脏Nkcc2蛋白和mRNA表达均低于同组野生型小鼠,推测20-HETE在基因转录水平对Nkcc2表达亦存在调节作用。虽然,目前尚未有直接证据证明20-HETE对Nkcc2基因表达存在调控作用,但仍有一些报道从侧面支持本研究的结论。在对盐敏感性高血压动物模型Dahl盐敏感性大鼠的研究[9-12]中发现,Dahl盐敏感性大鼠内源性20-HETE水平较低是引起盐敏感性高血压的主要原因;对Dahl盐敏感性大鼠肾脏水钠代谢相关通道蛋白表达谱的研究[13]发现,Dahl盐敏感性大鼠肾脏Nkcc2蛋白表达及活性均高于其他种类大鼠;而利用Clofibrate外源性诱导20-HETE合成增加可恢复Dahl盐敏感性大鼠肾脏Nkcc2至正常水平[9-10],以上结论均间接说明了20-HETE对Nkcc2的表达存在调控作用。
结合本课题组的前期工作基础和其他实验室关于20-HETE对Nkcc2作用机制的研究,推测20-HETE在转录水平存在对Nkcc2基因表达的调节作用。为探讨20-HETE对Nkcc2基因转录调控的作用机制,利用生物信息学软件分析小鼠Nkcc2基因启动子区-1 474 bp ~+1 bp序列,发现该区域存在多个20-HETE调控基因转录的潜在作用元件,如NF-κB、AP-1等。进一步构建了小鼠Nkcc2基因启动子区萤光素酶报告基因载体pGL3-Nkcc2。20-HETE刺激转染了pGL3-Nkcc2载体的HEK293T细胞后,通过萤光素酶报告基因系统检测Nkcc2基因启动子转录活性,结果显示,20-HETE能有效减少pGL3-Nkcc2重组载体转录活性,初步判断20-HETE在转录水平下调Nkcc2基因的表达。
综上所述,本研究成功构建了小鼠Nkcc2基因启动子区重组报告基因载体pGL3-Nkcc2,为进一步探究20-HETE对Nkcc2基因的调控机制提供了有利的研究工具。同时,本研究发现20-HETE对pGL3-Nkcc2重组载体转录活性存在抑制作用,为进一步鉴定20-HETE对Nkcc2基因表达调控的分子机制奠定了实验基础。
| [1] |
DELPIRE E, GAGNON KB. Na+-K+-2Cl- Cotransporter (NKCC) physiological function in nonpolarized cells and transporting epithelia[J]. Compr Physiol, 2018, 8(2): 871-901. DOI:10.1002/cphy.c170018 |
| [2] |
VERGINE G, FABBRI E, PEDINI A, et al. Bartter syndrome Type 1 presenting as nephrogenic diabetes insipidus[J]. Case Rep Pediatr, 2018, 2018: 9175271. DOI:10.1155/2018/9175271 |
| [3] |
BAZUAV S, CASTAN BM, GAMBA G. Physiological role of SLC12 family members in the kidney[J]. Am J Physiol Renal Physiol, 2016, 311: F131-F144. DOI:10.1152/ajprenal.00071 |
| [4] |
GARCIA V, SCHWARTZMAN ML. Recent developments on the vascular effects of 20-hydroxyeicosatetraenoic acid[J]. Curr Opin Nephrol Hypertens, 2017, 26(2): 74-82. DOI:10.1097/MNH.0000000000000302 |
| [5] |
LIU X, ZHAO Y, WANG L, et al. Overexpression of cytochrome P4504F2 in mice increases 20-hydroxyeicosatetraenoic acid production and arterial blood pressure[J]. Kidney Int, 2009, 75: 1288-1296. DOI:10.1038/ki.2009.281 |
| [6] |
WU J, LIU X, LAI G, et al. Synergistical effect of 20-HETE and high salt on NKCC2 protein and blood pressure via ubiquitin-proteasome pathway[J]. Hum Genet, 2013, 132(2): 179-187. DOI:10.1007/s00439-012-1238-3 |
| [7] |
WANG W, LU M. Effect of arachidonic acid on activity of the apical K+ channel in the thick ascending limb of the rat kidney[J]. J Gen Physiol, 1995, 106(4): 727-743. DOI:10.1085/jgp.106.4.727 |
| [8] |
STEC DE, MATTSON DL, ROMAN RJ. Inhibition of renal outer medullary 20-HETE production produces hypertension in Lewis rats[J]. Hypertension, 1997, 29(1 Pt 2): 315-319. |
| [9] |
ROMAN RJ, MA YH, FROHICH B, et al. Clofibrate prevents the development of hypertension in Dahl salt-sensitive rats[J]. Hypertension, 1993, 21(6 Pt 2): 985-988. |
| [10] |
ITO O, ROMAN RJ. Role of 20-HETE in elevating chloride transport in the thick ascending limb of Dahl SS/Jr rats[J]. Hypertension, 1999, 33(1 Pt 2): 419-423. |
| [11] |
ROMAN RJ, HOAGLAND KM, LOPEZ B, et al. Characterization of blood pressure and renal function in chromosome 5 congenic strains of Dahl S rats[J]. Am J Physiol Renal Physiol, 2006, 290(6): F1463-F1471. DOI:10.1152/ajprenal.00360.2005 |
| [12] |
HOAGLAND KM, FLASCH AK, ROMAN RJ. Inhibitors of 20-HETE formation promote salt-sensitive hypertension in rats[J]. Hypertension, 2003, 42(4): 669-673. DOI:10.1161/01.HYP.0000084634.97353.1A |
| [13] |
HOAGLAND KM, FLASCH AK, DAHLY-VERONO AJ, et al. Elevated BSC-1 and ROMK expression in Dahl salt-sensitive rat kidneys[J]. Hypertension, 2004, 43(4): 860-865. DOI:10.1161/01.HYP.0000120123.44945.47 |
 2019, Vol. 48
2019, Vol. 48