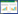文章信息
- 王月, 徐振华, 苏荣健
- WANG Yue, XU Zhenhua, SU Rongjian
- 外分泌葡萄糖调节蛋白78对肝细胞癌侵袭的影响
- Effects of Exocrine Glucose-regulated Protein 78 on Invasion of Hepatocellular Carcinoma
- 中国医科大学学报, 2018, 47(7): 589-592
- Journal of China Medical University, 2018, 47(7): 589-592
-
文章历史
- 收稿日期:2017-10-18
- 网络出版时间:2018-06-28 9:42
2. 锦州医科大学附属第一医院病理科, 辽宁 锦州 121001;
3. 锦州医科大学生命科学研究院, 辽宁 锦州 121001
2. Department of Pathology, The First Affiliated Hospital, Jinzhou Medical University, Jinzhou 121001, China;
3. Institution of Life Science, Jinzhou Medical University, Jinzhou 121001, China
肝细胞癌(hepatocellular carcinoma,HCC)是一种常见的恶性肿瘤,病死率高[1],临床上具有起病隐匿、早期即发生侵袭和转移的特点,侵袭和转移是HCC患者致死的重要原因。因此研究HCC侵袭和转移的机制,探寻新的抗侵袭和转移方法对于改善患者临床疗效具有重要意义。葡萄糖调节蛋白78(glucose-regulated protein 78,GRP78)在恶性肿瘤细胞中过表达,而在正常细胞中低表达甚至不表达[2]。随着对GRP78功能认识的不断深入,研究[3-4]发现GRP78除了驻留在内质网中发挥分子伴侣作用外,还可以分布在细胞质、细胞膜上,在肿瘤侵袭、转移和耐药性形成中发挥关键的调节作用。近年研究[5]发现GRP78还可以被肺癌等肿瘤细胞分泌到细胞外,肿瘤细胞分泌的GRP78可以促进肿瘤细胞增殖和新生血管形成。前期研究[6]证实HCC细胞也可以分泌GRP78,HCC分泌的GRP78通过与细胞表面表皮生长因子受体(epidermal growth factor receptor,EGFR)结合,促进肿瘤细胞增殖,降低对索拉非尼敏感性[7]。本研究应用GRP78原核重组蛋白处理HCC细胞(SMMC7721和PLC5),观察其对肿瘤细胞侵袭的影响,以期为HCC治疗提供新的线索。
1 材料与方法 1.1 材料HCC细胞(SMMC7721和PLC5)购自中科院细胞库,大肠杆菌GST重组蛋白(GST-GRP78)为本实验室分离和纯化。Cortactin和磷酸化Cortactin Y421抗体购于英国Abcam公司。FAK、磷酸化FAK(Y397)、Src和磷酸化Src(Y416)、EGFR购自美国Cell Signaling公司。TRITC标记的毒伞素购于美国Sigma公司。HRP标记二抗购自中山公司。ECL发光试剂购自碧云天公司。
1.2 方法 1.2.1细胞培养与GST-GRP78处理:SMMC7721和PLC5在含10%胎牛血清(fetal bovine serum,FBS)和1%青霉素/链霉素的DMEM(dulbecco’s modified eagle medium)培养基中,37 ℃,5%CO2环境下培养。2~3 d更换1次培养液。在GST-GRP78处理前血清饥饿3 h,然后用不同浓度GRP78重组蛋白无血清条件下培养24 h。
1.2.2侵袭实验:应用xCELLigence RTCA DP无标记细胞功能分析系统检测GRP78重组蛋白对肿瘤细胞侵袭能力的影响,操作严格按说明书进行。应用无血清培养液将SMMC7721和PLC5细胞稀释至1×105/mL,接种于16孔Transwell培养板上层,100 μL/孔,加入不同浓度GRP78重组蛋白。下层加入完全培养液,以表皮生长因子(epidermal growth factor,EGF)作为阳性对照,以无血清培养液为阴性对照。在37 ℃,5%CO2的环境下培养24 h,观察细胞侵袭能力。
1.2.3免疫荧光及细胞骨架染色:将SMMC7721细胞接种于共聚焦显微镜专用的培养皿中,12 h后加入GRP78重组蛋白处理24 h,PBS漂洗,3.7%甲醛固定30 min,0.2%Triton-X-100透化5 min,1% BSA封闭30 min,一抗(兔源抗Cortactin)温育1 h,FITC标记的羊抗兔IgG和TRITC标记的毒伞素温育30 min,共聚焦显微镜下观察。
1.2.4免疫印迹实验:将GRP78重组蛋白处理的SMMC7721细胞用放射免疫沉淀测定(radio-immunoprecipitation assay,RIPA)缓冲液[1% NP-40、0.5%脱氧胆酸钠、1%十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、0.1%苯甲基磺酰氟(phenylmethanesulfonyl fluoride,PMSF)]裂解,小牛血清白蛋白(bovine serum albumin,BSA)法定量,SDS-PAGE电泳,转膜,1% BSA封闭,一抗(1: 1 000稀释)4 ℃杂交过夜,PBST洗膜后加入辣根过氧化物酶(horseradish peroxidase,HRP)标记的二抗室温温育1 h,ECL显色。
1.3 统计学分析采用SPSS 17.0统计软件进行分析,多组比较采用单因素方差分析,2组比较采用t检验。P < 0.05为差异有统计学意义。
2 结果 2.1 重组GRP78促进HCC细胞(SMMC7721和PLC5)侵袭如图 1所示,重组GRP78对SMMC7721和PLC5侵袭能力具有促进作用,随着重组蛋白浓度增加促进作用逐渐增强,400 ng/mL促进作用最明显,呈现浓度依赖性的关系;400 ng/mL处理组与空白对照组(0 ng/mL)比较有统计学差异(P < 0.01)。
|
| A, SMMC7721;B, PLC5. 图 1 重组人GRP78促进肝细胞癌细胞侵袭 Fig.1 Recombinant human GRP78 promotes the invasion of hepatocellular carcinoma cells lines |
2.2 重组GRP78促进侵袭伪足形成
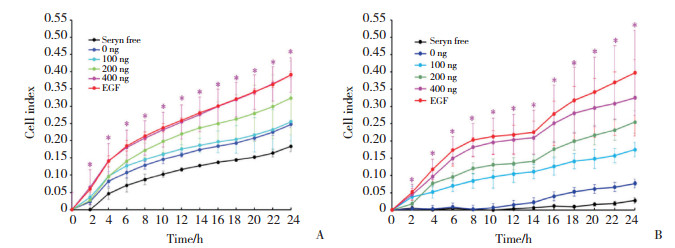
共聚焦显微镜观察抗Cortactin(绿色)和F-actin(红色)共染色结果显示,重组GRP78处理后的SMMC7721和PLC5细胞中黄色荧光斑点明显增加(图 2A、2B),显示重组GRP78可以促进HCC细胞侵袭伪足形成。
|
| A, SMMC7721;B, PLC5. 图 2 重组人GRP78促进HCC细胞侵袭伪足形成×630 Fig.2 Recombinant human GRP78 facilitates the formation of invadopodia in hepatocellular carcinoma cells ×630 |
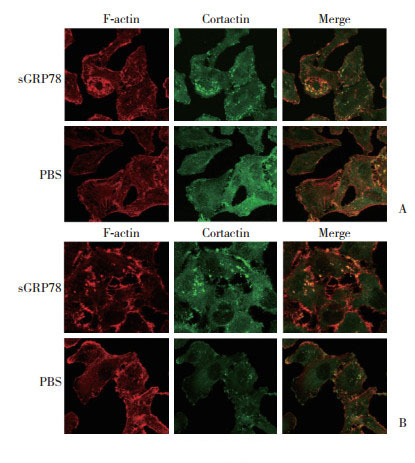
SMMC7721细胞中检测重组GRP78对Cortactin磷酸化的影响,结果显示,重组GRP78可以促进Cortactin磷酸化,而对其表达没有影响。见图 3A。
|
| A, Cortactin; B, FAK and Scr. 图 3 重组人GRP78促进Cortactin、FAK和Src磷酸化 Fig.3 Recombinant human GRP78 enhances the phosphorylation of cortactin, FAK, and c-Src protein kinase |
2.3 重组GRP78蛋白促进FAK和Src磷酸化
免疫印迹实验结果显示在重组GRP78处理的SMMC7721中,FAK和Src磷酸化水平明显高于未处理细胞,而在重组GRP78处理细胞和未处理细胞中,FAK和Src的表达没有差异,这提示重组GRP78可以促进FAK和Src的磷酸化,而对其表达没有影响。见图 3B。
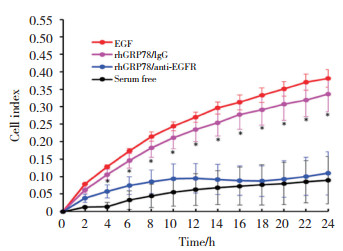
2.4 抗体封闭细胞表面EGFR阻断外分泌GRP78介导的HCC侵袭应用抗-EGFR抗体预处理SMMC7721细胞,封闭细胞表面EGFR。结果发现与未预处理的细胞比较,EGFR抗体预处理细胞经重组GRP78处理后,其侵袭能力明显减弱(P < 0.05)。提示EGFR在重组GRP78促进HCC细胞侵袭过程中具有重要作用。见图 4。
|
| 图 4 阻断细胞表面EGFR抑制重组GRP78促进侵袭作用 Fig.4 Blockade of cell surface EGFR inhibits the stimulatory activity of rhGRP78 on hepatocellular carcinoma cells |
3 讨论
侵袭和转移是HCC患者死亡的重要原因,目前HCC侵袭和转移机制尚不清楚。GRP78是内质网合成的一种分子伴侣,属于热休克蛋白70家族。GRP78在肿瘤细胞过表达,对肿瘤细胞增殖、侵袭和转移等生物学特性具有重要调节作用[8]。最近研究[9]显示GRP78不仅定位在内质网、细胞质和细胞膜,还可以被肿瘤细胞分泌到细胞外。有报道[10]指出在恶性肿瘤患者血清样品中GRP78含量显著高于非肿瘤患者,可以作为恶性肿瘤诊断的标志物。也有研究[11]指出,肿瘤细胞外分泌的GRP78可以激活PI3K/Akt信号通路,促进肿瘤细胞增殖。本课题组前期研究[6, 12]表明HCC外分泌的GRP78可以通过激活EGFR/Src/STAT3信号通路,导致HCC细胞对索拉非尼反应性降低。
本研究结果发现GRP78可以明显促进HCC的侵袭。侵袭伪足是肿瘤细胞在侵袭过程中形成的一种特化结构,在肿瘤细胞的侵袭过程中发挥关键作用,本研究显示重组GRP78可以促进侵袭伪足形成,并促进侵袭伪足关键蛋白Cortactin磷酸化。本研究表明重组人GRP78可以促进FAK和Src磷酸化。研究[13-14]显示FAK-Src信号通路是肿瘤细胞内的重要信号通路,不仅促进肿瘤细胞侵袭,还参与肿瘤细胞增殖、耐药性形成。当该通路被细胞内外信号激活后,FAK第397位酪氨酸磷酸化水平增加,促进Src激酶第416位酪氨酸磷酸化激活Src,促进肿瘤细胞侵袭。本研究应用EGFR单克隆抗体封闭细胞表面EGFR,结果发现重组GRP78对HCC侵袭的促进作用被明显抑制。这提示EGFR在HCC外分泌GRP78促进侵袭过程中也具有重要作用。以往研究[6]显示外分泌GRP78可以与EGFR结合,导致HCC对索拉非尼耐药。本研究结果显示外分泌GRP78可以促进HCC细胞侵袭。这些进一步说明EGFR可能是抑制HCC侵袭和逆转索拉非尼耐药性的重要靶点。
综上所述,HCC细胞外分泌GRP78可以促进HCC侵袭,EGFR在该过程中可能发挥重要作用,为临床上抑制HCC侵袭和索拉非尼耐药性及HCC治疗提供了新的线索。但本研究为体外研究,尚缺乏动物实验和临床实验的支持,对机制探讨也不够深入。今后的研究将在动物水平进一步探讨外分泌GRP78促进HCC侵袭的效果,并对机制进行深入研究。
| [1] |
TORRE LA, BRAY F, SIEGEL RL, et al. Global cancer statistics, 2012[J]. CA, 2015, 65(2): 87-108. |
| [2] |
LEE AS. Glucose-regulated proteins in cancer:molecular mechanisms and therapeutic potential[J]. Nat Rev Cancer, 2014, 14(4): 263-276. DOI:10.1038/nrc370 |
| [3] |
GIFFORD JB, HILL R. GRP78 influences chemoresistance and prognosis in cancer[J]. Current Drug Targets, 2018, 19(6): 701-708. DOI:10.2174/1389450118666170615100918 |
| [4] |
KAMIL M, HAQUE E, IRFAN S, et al. ER chaperone GRP78 regulates autophagy by modulation of p53 localization[J]. Frontiers Biosci, 2017, 9(1): 54. DOI:10.2741/e785 |
| [5] |
LOUESSARD M, BARDOU I, LEMARCHAND E, et al. Activation of cell surface GRP78 decreases endoplasmic reticulum stress and neuronal death[J]. Cell Death Differ, 2017, 24(9): 1518-1529. DOI:10.1038/cdd.2017.35 |
| [6] |
RUI L, Gu YJ, HE WB, et al. Secreted GRP78 activates EGFR-SRCSTAT3 signaling and confers the resistance to sorafeinib in HCC cells[J]. Oncotarget, 2017, 8(12): 19354-19364. DOI:10.18632/oncotarget.15223 |
| [7] |
MACHIHARA K, TANAKA H, HAYASHI Y, et al. Questiomycin A stimulates sorafenib-induced cell death via suppression of glucose-regulated protein 78[J]. Biochem Biophys Res Comm, 2017, 492(1): 33-40. DOI:10.1016/j.bbrc.2017.08.042 |
| [8] |
贾鹏宇, 何苗, 魏敏杰. GRP78在肿瘤发生发展及干性形成中的研究进展[J]. 生命的化学, 2015, 35(4): 559-564. DOI:10.13488/j.smhx.20150416 |
| [9] |
YIN Y, CHEN C, CHEN J, et al. Cell surface GRP78 facilitates hepatoma cells proliferation and migration by activating IGF-IR[J]. Cell Signal, 2017, 35: 154-162. DOI:10.1016/j.cellsig.2017.04.003 |
| [10] |
ZHANG JY, TAN EM. Autoantibodies to tumor-associated antigens as diagnostic biomarkers in hepatocellular carcinoma and other solid tumors[J]. Expert Rev Mol Diagn, 2010, 10(3): 321-328. DOI:10.1586/erm.10.12 |
| [11] |
ZHENG NQ, ZHENG ZH, XU HX, et al. Glucose-regulated protein 78 demonstrates antiviral effects but is more suitable for hepatocellular carcinoma prevention in hepatitis B[J]. Virol J, 2017, 14(1): 77. DOI:10.1186/s12985-017-0747-z |
| [12] |
GU Y, LI H, ZHAO L, et al. GRP78 confers the resistance to 5-FU by activating the c-Src/LSF/TSAxisinhepatocellularcarcinoma[J]. Oncotarget, 2015, 6(32): 33658-33674. DOI:10.18632/oncotarget.5603 |
| [13] |
LIU S, YAMASHITA H, WEIDOW B, et al. Laminin-332-beta1 integrininteractions negatively regulate invadopodia[J]. J Cell Physiol, 2010, 223(1): 134-142. DOI:10.1002/jcp.22018 |
| [14] |
CHATZIZACHARIAS NA, GIAGINIS C, GATZIDOU E, et al. Expression and clinical significance of FAK and Src proteins in human endometrial adenocarcinoma[J]. Pathol Oncol Res, 2011, 17(2): 277-285. DOI:10.1007/s12253-010-9310-6 |
 2018, Vol. 47
2018, Vol. 47