文章信息
- 王荣, 覃海媚, 陆玉兰, 黄华佗, 蓝艳, 王俊利, 韦叶生
- WANG Rong, QIN Haimei, LU Yulan, HUANG Huatuo, LAN Yan, WANG Junli, WEI Yesheng
- 广西人群miR-17-92基因簇启动子区rs1491033A/C和rs1813389A/G多态性研究
- Study of the Polymorphisms rs1491033A/C and rs1813389A/G in the miR-17-92 Gene Cluster Promoter Region in a Guangxi Population
- 中国医科大学学报, 2018, 47(2): 114-118
- Journal of China Medical University, 2018, 47(2): 114-118
-
文章历史
- 收稿日期:2017-03-23
- 网络出版时间:2018-01-08 10:54
2. 右江民族医学院附属医院皮肤科, 广西 百色 533000
2. Department of Dermatology, Affiliated Hospital of Youjiang Medical University for Nationalities, Baise 533000, China
微小RNA(microRNA,miRNA)是由19~25个核苷酸构成的非编码小RNA分子,通过和靶mRNA的3’非编码区序列结合后降低mRNA的稳定性或抑制翻译,从而在基因表达中发挥重要的调控作用[1]。近些年来,研究者对miRNA与疾病的关系产生了浓厚的兴趣,最具有代表性的是miR-17-92基因簇。它由6种成熟的miRNA(miR-17、miR-18a、miR-19a、miR-20a、miR-19b-1和miR-92a-1)组成。研究[2]发现,miR-17-92基因簇在宫颈癌、子宫内膜癌及卵巢癌多种细胞系中表达,而且在生物学行为不同的同种肿瘤细胞系中也存在差异表达。在实体肿瘤组织中,miR-17-92在B细胞淋巴瘤及直肠癌等中呈不同的表达状态,提示miR-17-92或可作为潜在的肿瘤预防和治疗的新分子靶标[3-4]。miRNA基因启动子区多态性可影响miRNA的转录,调控基因的表达,从而影响miRNA相关疾病的发生和发展。但是,尚未见文献报道关于miR-17-92基因簇启动子区遗传多态性的研究。因此,本研究采用多重单碱基延伸和DNA测序技术,检测miR-17-92基因簇启动子区的rs1491033A/C位点和rs1813389A/G位点的基因型,并分析其多态性在不同正常人群中的差异。
1 材料与方法 1.1 研究对象选取我院体检中心275例健康体检者,其中男98例,女177例,年龄17~78岁。排除肝、肾、心脏及肿瘤史等疾病,各临床及实验室检查均正常。研究对象均是来自广西的无亲缘关系个体。研究方案经我院医学伦理委员会审批后进行,研究对象均知情且签署同意书。
1.2 方法 1.2.1 样本DNA制备采用EDTAK2抗凝采血管抽取研究对象静脉血3 mL。取200 μL血液按照北京天根公司的全血液基因组DNA提取试剂盒说明书提取样本DNA,置于-20 ℃保存待用。
1.2.2 引物合成参考miR-17-92基因簇启动子区rs14911033a/c位点和rs1813389a/g位点的核苷酸序列,采用primer3.0引物在线设计软件(http://primer3.ut.ee/)设计针对本研究的特异性引物,交由上海天昊生物科技有限公司合成。rs14911033A/C位点上游引物:5’-TGGGGTTTCTTCAGGGGATAAT TG-3’,下游引物:5’-TGTTCTGAGTGGAGGGCCCTT AT-3’,延伸引物:5’-TTTTTTTTTTTTTTTTTTTTTTT TTTTTTTTTGTAAACTAAGCTTTGTTTTGCCTGTT-3’;RS1813389A/G位点上游引物:5’-TCGGGGGAGAATA AACGAGAGG-3’,下游引物:5’-TCGCCAGTGCATT AAGCCCTAC-3’,延伸引物:5’-TTTTTTTTTTTTTTT TTTTTTTTTTTTCAGCCAGAGTGGATCAACCTT-3’。
1.2.3 基因分型PCR扩增反应体系总共20 μL,包括1.0 μL样本DNA、2.0 μL缓冲液、2.0 μL dNTPs、1 U TapDNA聚合酶及上、下游引物各1.0 μL,剩余体积添加灭菌的双蒸水。使用热启动Taq聚合酶(Hotstar Taq,德国Qiagen公司)进行多重PCR扩增。获得PCR产物经虾碱酶(SAP,日本Promega公司)和核酸外切酶Ⅰ(EXO1,美国Epicentre公司)纯化后用美国ABI公司的SNaPshot Multiplex kit进行延伸反应,延伸产物采用SAP纯化后在ABI 3730XL上样,并用Gene Mapper 4.1(美国Applied Biosystems公司)分析。运用DNA测序法验证上述分型结果。
1.3 统计学分析采用SPSS 17.0统计学软件分析数据。直接计数法统计各位点的基因型及等位基因频率。采用χ2检验比较各组基因多态性分布差异,P < 0.05为差异有统计学意义。采用Hardy-Weinberg遗传平衡法则验证样本人群是否有代表性。
2 结果 2.1 rs1491033A/C和rs1813389A/G基因分型经检验2个位点的基因型分布符合Hardy-Weinberg遗传平衡定律(P = 0.287,P = 0.084),说明本研究选取的样本人群有代表性。rs1491033A/C位点和rs1813389A/G位点的扩增长度分别为232 bp、281 bp。分型结果显示,rs1491033A/C有AA、AC、CC 3种基因型,频率分别为21.1%、53.1%、25.8%;rs1813389A/G有AA、AG、GG 3种基因型,频率分别为40.0%、50.2%、9.8%。测序结果充分证实了上述分型结果(图 1、2)。

|
| The inverted triangles of panels in A, B, and C indicated AA, AC, and CC genotypes, respectively. 图 1 miR-17-92基因簇rs1491033A/C位点测序图 Fig.1 Sequencing map of the genotype for the rs1491033A/C site in the miR-17-92 gene cluster |
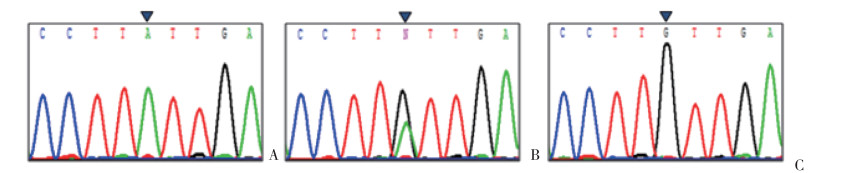
|
| The inverted triangles of panels in A, B, and C indicated AA, AG, and GG genotypes, respectively. 图 2 miR-17-92基因簇rs1813389A/G位点测序图 Fig.2 Sequencing map of the genotype for the rs1813389A/G site in the miR-17-92 gene cluster |
2.2 广西人群中2个位点的基因多态性分布
rs1491033A/C位点AA、AC、CC基因型及A、C等位基因频率分布在男女间比较无统计学差异(P > 0.05)。rs1813389A/G位点AA、AG、GG基因型及A、G等位基因频率分布在男女间比较无统计学差异(P > 0.05)。见表 1。
| Site | n | Genotype [n (%)] | P | Allele [n (%)] | P | |||
| AA (AA) | AC (AG) | CC (GG) | A (A) | C (G) | ||||
| rs1491033A/C | ||||||||
| Male | 98 | 22 (22.4) | 49(50.0) | 27(27.6) | 0.747 | 93(47.4) | 103(52.6) | 0.948 |
| Female | 177 | 36(20.3) | 97(54.8) | 44(24.9) | 169(47.7) | 185(52.3) | ||
| Total | 275 | 58(21.1) | 146(53.1) | 71(25.8) | 262(47.6) | 288(52.4) | ||
| rs1813389A/G | ||||||||
| Male | 98 | 41(11.2) | 50(54.1) | 7(34.7) | 0.533 | 132(67.3) | 64(32.7) | 0.409 |
| Female | 177 | 69(39.0) | 88(49.7) | 20(11.3) | 226(63.8) | 128(36.2) | ||
| Total | 275 | 110(40.0) | 138(50.2) | 27 (9.8) | 358(65.1) | 192(34.9) | ||
2.3 各位点与其他人群的基因多态性比较
广西人群rs1491033A/C位点基因型和等位基因分布频率与欧洲人、非洲人相比,差异均有统计学意义(P < 0.05),与北京人和日本人相比,差异无统计学意义(P > 0.05)。广西人群rs1813389A/G位点基因型及等位基因分布频率与欧洲人、非洲人、北京人及日本人相比,差异均有统计学意义(P < 0.05)。见表 2。
| Site | n | Genotype [n (%)] | P | Allele [n (%)] | P | |||
| AA (AA) | AC (AG) | CC (GG) | A (A) | C (G) | ||||
| rs1491033A/C | ||||||||
| Guangxi | 275 | 58 (21.1) | 146(53.1) | 71(25.8) | 262(47.6) | 288(52.4) | ||
| HapMap-CEU | 118 | 0 (0.0) | 36(30.5) | 82(69.5) | < 0.001 | 36 (15.3) | 200(84.7) | < 0.001 |
| HapMap-HCB | 88 | 20(22.7) | 46 (52.3) | 22(25.0) | 0.947 | 86(48.9) | 90(51.1) | 0.777 |
| HapMap-JPT | 90 | 14 (15.6) | 48 (53.3) | 28(31.1) | 0.416 | 76(42.2) | 104(57.8) | 0.206 |
| HapMap-YRI | 118 | 2 (1.7) | 50 (42.4) | 66(55.9) | < 0.001 | 54(22.9) | 182(77.1) | < 0.001 |
| rs1813389A/G | ||||||||
| Guangxi | 275 | 110(40.0) | 138(50.2) | 27(9.8) | 358(65.1) | 192(34.9) | ||
| HapMap-CEU | 120 | 14(11.7) | 50(41.7) | 56(46.6) | < 0.001 | 78(32.5) | 162(67.5) | < 0.001 |
| HapMap-HCB | 90 | 26(28.9) | 46(51.1) | 18(20.0) | 0.019 | 98(54.4) | 82(45.6) | 0.010 |
| HapMap-JPT | 88 | 20(22.7) | 42(47.7) | 26(29.6) | < 0.001 | 82(46.6) | 94(53.4) | < 0.001 |
| HapMap-YRI | 120 | 4(3.3) | 26(21.7) | 90(75.0) | < 0.001 | 34(14.2) | 206(85.8) | < 0.001 |
3 讨论
miRNA-17-92基因簇位于人类第13号染色体上(13q31-32),C13orf25基因的第3个内含区,其转录前体含有6个串联茎环发卡结构,属于高度保守的基因[5]。在人体的正常生长发育中,miRNA-17-92基因簇参与机体的免疫系统、心肺和血管生长等分化过程。在肿瘤的发生和发展过程中,它主要是通过抑制细胞周期调控基因和抑癌基因的表达实现的。抑癌基因p53以及信号转导和转录激活因子3(signal transduction and activator of transcription 3,STAT3)均可与miR-17-92基因簇启动子区结合,激活miR-17-92基因簇转录,通过抑制其靶基因引发肿瘤[6-7]。最新研究[8]发现,其家族成员可通过对细胞周期负向调节因子p21蛋白的抑制而增强白血病干细胞的增殖能力,从而在混合谱系白血病的发生中起关键作用。此外,miR-17-92基因簇还可通过抑制抑癌基因PTEN和促凋亡蛋白基因Bim的表达促进细胞增殖、抑制凋亡,这些作用由转化生长因子β信号通路介导[9],这些研究表明miR-17-92基因簇在肿瘤发生发展中扮演着重要的作用。
单核苷酸多态性(single nucleotide polymorphism,SNP)是指在基因组DNA序列中由于单个核苷酸(A、G、C、T)替换而引起的多态性,是人类可遗传变异中最常见的一种,占所有已知多态性的90%以上。启动子是RNA聚合酶特异性识别和结合的DNA序列,调控基因转录起始时间和表达的程度。启动子区SNP可影响基因的转录,导致与之相关疾病的发生[10-11]。本研究采用SNaPshot SNP分型技术和DNA测序法检测275例广西人群rs1491033A/C位点和rs1813389A/G位点,并将所得结果与HapMap公布的不同人群比较,分析不同种族、地区人群间2个位点多态性的分布差异。结果表明,广西人群rs1491033A/C位点和rs1813389A/G位点的基因型和等位基因频率在不同性别间比较差异均无统计学意义(P > 0.05),表明广西人群中这2个位点的多态性与性别无关。进一步将2个位点结果与HapMap公布的不同人群比较发现,rs1491033A/C基因型和等位基因频率广西人群与欧洲人和非洲人比较差异均有统计学意义(P < 0.01),而与北京人和日本人比较差异无统计学意义(P > 0.05)。rs1813389A/G位点基因型和等位基因频率广西人群与欧洲、北京、日本和非洲人群比较,差异均有统计学意义(P < 0.05)。广西人群中miR-17-92基因簇rs1491033A/C位点和rs1813389A/G位点多态性与其他种族、地区人群存在不同程度的差异。这种差异可能与本地区饮食习惯、生活环境和自然选择等因素有关。这也体现了不同的遗传背景下,其多态性存在着不同的多态性差异。
总之,本研究首次开展对广西人群miR-17-92基因簇rs1491033A/C位点和rs1813389A/G位点多态性的研究,并和不同地区、人群进行比较,不仅为miR-17-92基因簇多态性的群体遗传学普查提供了资料,同时为其与相关疾病的研究奠定了遗传学方面的基础。国内学者陶陶等[12]关于microRNA在卵巢浆液性癌化疗耐药及敏感组织的差异表达的研究中发现,miR-17-92基因簇与卵巢浆液性癌化疗耐药有关。而基因多态性差异影响疾病的发病率和耐药性。因此,今后应进一步研究miR-17-92基因簇多态性和疾病的关系。
| [1] |
PAUL P, CHAKRABORTY A, SARKAR D, et al. Interplay between miRNAs and human diseases[J]. J Cell Physiol, 2018, 233(3): 2007-2018. DOI:10.1002/jcp.25854 |
| [2] |
接智慧, 吴建磊, 陶陶, 等. miR-17~92基因簇在宫颈癌、子宫内膜癌与卵巢癌多种细胞系中的表达及意义[J]. 中国医科大学学报, 2013, 42(3): 209-213. DOI:10.3969/j.issn.0258-4646.2013.03.005 |
| [3] |
ROBAINA MC, FACCCION RS, MCAZZOCCOLI L, et al. miR-17-92 cluster components analysis in Burkitt lymphoma:overexpression of miR-17 is associated with poor prognosis[J]. Ann Hematol, 2016, 95(6): 881-891. DOI:10.1007/s00277-016-2653-7 |
| [4] |
张丽静, 赵增仁, 张志勇, 等. 直肠腺癌组织中microRNA差异表达谱分析[J]. 肿瘤防治研究, 2014, 41(6): 602-605. DOI:10.3971/j.issn.1000-8578.2014.06.020 |
| [5] |
OTA A, TAGAWA H, KARNAN S, et al. Identification and characterization of a novel gene, C13orf25, as a target for 13q31-q32 amplification in malignant lymphoma[J]. Cancer Res, 2004, 64(9): 3087-3095. DOI:10.1158/0008-5472.CAN-03-3773 |
| [6] |
MAO S, LI X, WANG J, et al. miR-17-92 facilitates neuronal differentiation of transplanted neural stem/precursor cells under neuroinflammatory conditions[J]. 2016, 13(1): 208-222. DOI: 10.1186/s12974-016-0685-5.
|
| [7] |
TAVAKOLI R, VAKILIAN S, LANGROUDI L, et al. The role of miR-17-92 cluster in the expression of tumor suppressor genes in unrestricted somatic stem cells[J]. Biologicals, 2017, 46: 143-147. DOI:10.1016/j.biologicals.2017.02.006 |
| [8] |
WONG P, IWASAKI M, SOMERVAILLE TC, et al. The miR-17-92 microRNA polycistron regulates MLL leukemia stem cell potential by modulating p21 expression[J]. Cancer Res, 2010, 70(9): 3833-3842. DOI:10.1158/0008-5472.CAN-09-3268 |
| [9] |
WANG Y, FRANK DB, MORLEY MP, et al. HDAC3-dependent epigenetic pathway controls lung alveolar epithelial cell remodeling and spreading via miR-17-92 and TGF-beta signaling regulation[J]. Dev Cell, 2016, 36(3): 303-315. DOI:10.1016/j.devcel.2015.12.031 |
| [10] |
LIU Q, YANG G, SONG XL, et al. Association between rs4938723 functional polymorphism in the promoter region of miR-34b/c gene and cancer risk[J]. Clin Res Hepatol Gastroenterol, 2015, 39(4): 526-533. DOI:10.1016/j.clinre.2014.10.007 |
| [11] |
WANG S, CAO X, DING B, et al. The rs767649 polymorphism in the promoter of miR-155 contributes to the decreased risk for cervical cancer in a Chinese population[J]. Gene, 2016, 595(1): 109-114. DOI:10.1016/j.gene.2016.10.002 |
| [12] |
陶陶, 王敏. 化疗耐药及敏感卵巢癌细胞差异表达microRNA的筛查与组织鉴定[J]. 中国医科大学学报, 2013, 42(2): 118-122. DOI:10.3969/j.issn.0258-4646.2013.02.006 |
 2018, Vol. 47
2018, Vol. 47