文章信息
- 李阳, 吴酬飞, 吴小芹, 叶建仁, 张立钦.
- LI Yang, WU Chou-fei, WU Xiao-qin, YE Jian-ren, ZHANG Li-qin.
- Cry3a杀虫蛋白基因的合成优化及在JK-SH007中高效表达
- Gene Synthesis of Bacillus thuringiensis Cry3Aa and High-level Expression in Burkholderia pyrrocinia JK-SH007 as a Biopesticide
- 中国生物工程杂志, 2017, 37(6): 70-77
- China Biotechnology, 2017, 37(6): 70-77
- http://dx.doi.org/DOI:10.13523/j.cb.20170611
-
文章历史
- 收稿日期: 2017-03-15
- 修回日期: 2017-05-26
2. 湖州师范学院 湖州 313000
2. College of Life Sciences, Huzhou Teachers College, Huzhou 313000, China
苏云金芽孢杆菌Bacillus thuringiensis(BT)分泌的杀虫晶体蛋白(ICPS)因其对害虫具有高度专一毒杀作用,且对环境和人畜安全,成为世界上应用最广泛的一类微生物杀虫剂[1].根据杀虫晶体蛋白氨基酸序列的同源性,可将他们划分为17群94亚类[2],目前已报道的编码Cry蛋白的基因达300多个,其中Cry1类的表达产物对鳞翅目昆虫有特异毒性,而Cry3类的表达产物对鞘翅目昆虫有特异毒性[3-4]。1987年, 研究者[5-6]克隆了第一个对鞘翅目害虫有毒性的Cry3Aa基因,随后发现对鞘翅目昆虫具有专一毒性蛋白的基因还有Cry5、Cry7、Cry8和Cry18A等[7]。但又以Cry3Aa基因专一性和毒性最高,其从细胞营养期即可不依赖芽孢的产生进行较长时间表达,且表达的蛋白多肽易被昆虫肠液降解为55kDa的毒性多肽,因此国内外一般都优先选用Cry3Aa基因作为抗虫基因转入微生物,构建具有抗鞘翅目昆虫杀虫活性的BT工程菌[8-9]。Cry3Aa基因的工程菌剂于1991年投放市场, 在马铃薯甲虫的防治中发挥了巨大作用[10-11]。本研究构建了一个吡咯伯克霍尔德氏菌B. pyrrocinia T7表达系统,利用人工密码子优化重新合成Cry3Aa基因,同时将T7表达系统重组到PHKT2表达载体上,通过将Cry3A杀虫蛋白基因插入T7启动子后,让T7表达系统启动表达T7RNA聚合酶后表达Cry3Aa杀虫蛋白,最后将重组表达质粒转入本实验室前期自行分离并保存的吡咯伯克霍尔德氏菌B. pyrrocinia JK-SH007中[12-13]。宿主菌JK-SH007,是由本实验室近年分离自野外杨树林,此菌对拟茎点霉(Phomopsis macrospore)、金黄壳囊孢菌(Cytospora chrysosperma)、七叶树壳梭孢菌(Fusicoacum aesculi)三种主要病原菌具有83%以上的抑菌率[12],生态价值重大。此次构建的工程菌经过PCR、SDS-PAGE蛋白电泳、West blot及室内生测分析,结果显示重组工程菌成功表达了Cry3Aa杀虫蛋白,对鞘翅目幼虫有一定杀虫活性。随着人工和天然林的逐渐增长,森林病虫害仍将是一个较大威胁。此次研究通过转基因技术开发成新的生物工程菌,具有较大的生防潜力和经济价值,为进一步开发生物农药奠定基础。
1 材料和方法 1.1 菌株,害虫,载体,培养基及试剂B. pyrrocinia JK-SH007(中国典型培养物保藏号:M209028) 分离并保存于本实验室,Cry3Aa-Pet30a质粒、大肠杆菌XL10-GOLD购自Stratagene公司,大肠杆菌BL21(DE3) 购自默克密理博公司。
原核表达载体PHKT2由本实验室保存,大肠杆菌购自ABM生物公司,供试榆蓝叶甲由浙江农林大学生物农药高效制备技术国家地方联合工程实验室提供。所有的细菌菌株都于37℃培养于Luria bertani(LB)中。鼠单克隆抗6×HIS IgG抗体和羊抗鼠IgG(辣根过氧化物酶标记)购自生工生物工程有限公司。质粒及DNA胶回收试剂盒购自全式金生物技术有限公司,Tryptone和Yeast extract购自生工生物工程有限公司,引物合成、高保真聚合酶,DNA Marker等常规生化分子试剂购自大连宝生物工程有限公司,甲氧苄啶抗生素(TP)购自南京博巧生物科技有限公司, 所有其他试剂为分析纯(除非另有说明)。
1.2 Cry3Aa的人工合成及优化Cry3Aa的密码子序列来自于苏云金芽孢杆菌Bacillus thuringiensis[GenBank ID: M84650.1],加上N末端6×His标签,根据大肠杆菌密码子偏好进行优化[14],通过DNA work软件进行引物设计,合成DNA(https://hpcwebapps.cit.nih.gov/cgi-bin/dnaworks)。Cry3Aa核苷酸序列利用引物通过重叠PCR技术拼接而成[15]。
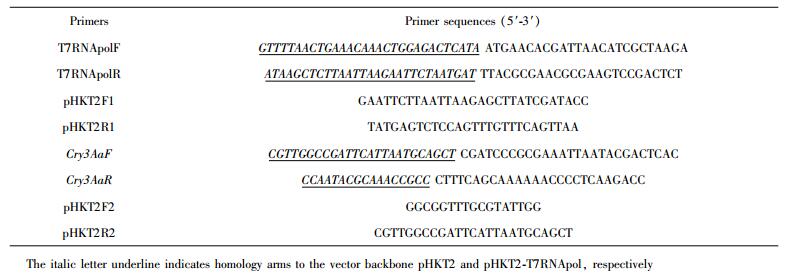
1.3 重组质粒构建为了实现T7启动子在JK-SH007中对Cry3Aa基因的表达,首先将T7 RNA聚合酶基因利用同源重组的方式连接到PHKT2载体上[16-17],载体骨架片段通过反向的PCR技术从PHKT2中扩增而来[18],引物为pHKT2F1/R1(表 1),T7 RNA聚合酶[产品编号:P001509]通过引物T7RNApolF/R(表 1) 从大肠杆菌BL21(DE3) 扩增得到, 然后将扩增的目的片段和载体按照1:3(100 ng载体:300 ng DNA片段)的比例混合[19], 然后转移到大肠杆菌XL-10 Gold感受态细胞中,重组质粒通过测序确定为pHKT2-T7RNA pol。
吡咯伯克霍尔德氏菌B. pyrrocinia-Cry3Aa表达载体质粒构建方法同上,利用引物Cry3aF/R、pHKT2F2/R2(表 1) 分别扩增目的片段和载体片段,其中pBluescript SK(+)载体利用反向PCR扩增出T7 promoter-6×his-Cry3Aa-T7 tel DNA结构, 重组质粒通过测序鉴定确定为pHKT2-Cry3Aa。
1.4 Cry3Aa基因在吡咯伯克霍尔德氏菌B. pyrrocinia JK-SH007中的表达将重组pHKT2-Cry3Aa质粒导入B. pyrrocinia JK-SH007感受态细胞, 然后涂布于浓度为50μg /ml含甲氧苄啶抗生素的LB抗性平板上,30 ℃过夜培养.将新重组菌株命名为B. pyrrocinia JK-SH007(pHKT2-Cry3Aa). Cry3Aa蛋白表达通过将重组菌接于LB培养基,采用30 ℃,220r/min摇培,待OD600=0.8时, 加终浓度为0.1mmol/L IPTG, 并迅速升温到42 ℃,继续培养4h,然后取工程菌液(6000×g, 10 min)离心,再将沉淀重悬于PBS (100 mmol/L, pH 7.8) 缓冲液, 利用超声波破碎(10℃, 120w, 15min),离心收集细胞裂解液进行SDS-PAGE分析。
1.5 SDS-PAGE和蛋白浓度测定蛋白样品采用4%~12%(w/v)SDS聚丙烯酰胺凝胶电泳(SDS-PAGE)分离。通过考马斯亮蓝R-250染色检测目标蛋白条带。用Bradford蛋白浓度试剂盒测定蛋白质浓度。
1.6 蛋白质印迹Western blot蛋白质样品在4%~12% Tris-glycine凝胶分离,然后转移到硝酸纤维素膜,膜浸泡在10毫升TBST(20mmol/L Tris-HCl,150mol/L Mnacl, 0.05%吐温20) 和10%(w/v)脱脂奶中,室温1h。Western blot分析采用了一抗(单克隆抗-6×His IgG抗体,1:3 000稀释)和二抗羊抗鼠IgG-HRP(辣根过氧化物酶标记,1:5 000稀释)。采用ECL发光液检测底物;信号经X光压片、洗片记录。
1.7 异源蛋白表达的质谱分析将SDS-PAGE电泳凝胶、经硝酸银染色,然后切下目标条带,37℃与胰蛋白酶消化过夜,蛋白质采用基质辅助激光解析飞行时间质谱(UltraFlex Ⅱ MALDI-TOF/TOF质谱)正离子反射模式(布鲁克·道尔顿公司)鉴定。利用Biotools软件分析肽段分子量指纹图谱,同时采用mascot软件在NCBI搜寻非冗余蛋白质库进行比对鉴定(http://www.matrixscience.com)。
1.8 生物毒杀活性生物毒性测定采用发酵液浸泡过的榆树叶对2龄榆蓝叶甲幼虫进行饲喂。B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)诱导蛋白表达方法如前1.4所述。B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)致死中浓度(LC50)计算方法如Sharma所描述[20], 通过采用5个梯度稀释的发酵工程菌液浸泡同样大小的榆树叶15min[21],然后20℃风干30min, 转移到装有灭菌滤纸的培养皿内,再将2龄的榆蓝叶甲幼虫放入皿中孵育,置于25℃恒温箱中。第二天记录幼虫的死亡率,每个实验设计三个重复,同时利用B.pyrrocinia JK-SH007(pHKT2-T7RNApol)作为对照组。进一步分析榆蓝叶甲幼虫生存曲线,首先将JK-SH007以及工程菌JK-SH007(pHKT2-Cry3Aa)菌液(6000×g, 10 min)离心,取中位浓度0.83 g/L湿重菌重悬于PBS (100 mmol/L, pH 7.8) 缓冲液,再将榆树叶浸泡(如前所述)。死亡率采用每隔8h记录一次,直到96h调查死亡结果[22],最后利用Graphpad Prism 6软件绘制榆蓝叶甲幼虫生存率曲线。
2 结论与分析 2.1 Cry3Aa基因合成与优化Cry3Aa基因序列全长1 794 bp, 编码蛋白大小为67.7 kDa.本研究根据大肠杆菌密码子偏好对Cry3Aa进行优化,其中包括一个6×His标签。通过设计54条引物(表 2),实验通过重叠PCR技术[23-24]合成了T7启动子-6×his-Cry3Aa -T7终止子的DNA结构。将此结构克隆到pBluescript SK(+)载体上,并导入大肠杆菌菌株BL21(DE3) 时,Cry3Aa基因转录可以被T7启动子及终止子启动和终止。

|
2.2 构建Cry3A蛋白表达载体pHKT2-Cry3Aa
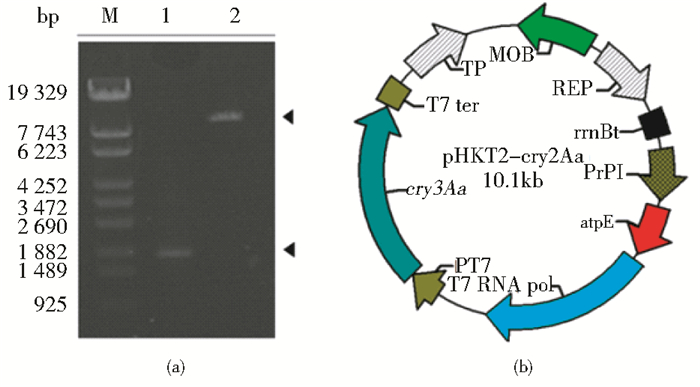
首先,通过反向PCR以及体内同源重组技术构建重组质粒pHKT2-T7RNApol,方法为通过将3.0 kb的T7 RNA聚合酶基因插入到pHKT2载体骨架,得到pHKT2-T7RNApol (图 1)。T7 RNA聚合酶基因转录依赖prpL启动子, 实验利用一个25bp以及17bp的同源臂将一个2.0 kb大小的T7启动子Cry3Aa-T7终止子基因克隆进pHKT2-T7RNApol中。重组菌通过菌落PCR筛选,将带有Cry3Aa基因以及T7启动子和终止子序列的菌株送上海生工测序鉴定,确定为pHKT2-Cry3Aa(图 2)。

|
| 图 1 B. pyrrocinia T7表达载体pHKT2-T7RNA pol的构建 Figure 1 Construction of the B. pyrrocinia T7 expression vector pHKT2-T7RNApol (a)The electrophoresis analysis of T7 RNApol and linear vector of pHKT2 M: Molecular weight marker; 1: T7 RNA pol; 2: Linear vector of pHKT2 (b) The physic map of plasmid pHKT2-T7RNApol Tp: Dihydrofolate reductase; MOB: Gene for plasmid mobilization; rep: Gene for plasmid replication; rrnBT: Transcriptional terminator; prpL: Lambda phage transcriptional promoters; atpE: Translation initiation region; T7 RNA pol: T7 DNA directed RNA polymerase |
|
| 图 2 pHKT2-Cry3Aa表达载体的构建 Figure 2 Construction of the Cry3Aa ICP expression vector pHKT2-Cry3Aa (a) The electrophoresis analysis of T7 Cry3Aa and linear vector of pHKT2-T7RNApol M: Molecular weight marker; 1: T7P-Cry3Aa-T7T; 2: Linear vector of pHKT2-T7RNApol (b) The physic map of plasmid pHKT2-Cry3Aa PT7: T7 RNA polymerase binding promoter; Cry3Aa: Gene encoding Bacillus thuringiensis tenebrionis Cry3Aa crystal toxin protein; T7 ter: T7 RNA polymerase transcriptional terminator |
通过电转将pHKT2-Cry3Aa质粒导入B. pyrrocinia strain JK-SH007。重组菌通过DNA提取及PCR验证(图 3).将阳性克隆子放于LB平板上进行传代培养,待其长到对数期, 将工程菌转接诱导培养4h以便产生蛋白。将5ml培养菌液等分进行SDS-PAGE和Western blot蛋白免疫鉴定分析。结果清晰显示工程菌PHKT2-Cry3Aa在野生吡咯伯克霍尔德氏菌中成功表达分子量为70 kDa的蛋白(图 4)。将此条带割胶,进一步通过基质辅助激光解吸离子飞行质谱分析,确定其为Cry3Aa杀虫蛋白.使用Bradford法对蛋白定量,获得约3.05 g/L的总蛋白浓度, 通过定量计算得到在诱导蛋白表达中,诱导表达的Cry3Aa杀虫蛋白约占15.6%。
|
| 图 3 B. pyrrocinia JK-SH007 (pHKT2-Cry3Aa)重组菌的PCR鉴定 Figure 3 Identification of the recombinant B. pyrrocinia strain JK-SH007 by PCR screening (a) Agarose gel electrophoresis of plasmid DNA extracted from B. pyrrocinia JK-SH007 M: Molecular weight marker; N: pHKT2-T7RNApol DNA isolated from B. pyrrocinia JK-SH007; 1~8: pHKT2-Cry3Aa DNA isolated from 8 independent B. pyrrocinia JK-SH007 colonies (b) Identification of recombinant B. pyrrocinia strain JK-SH007 by PCR assay N: Negative control using PHKT2-T7RNApol template; 1~8 were positive recombinants, PCR amplification used primers Cry3a F/R |

|
| 图 4 B. pyrrocinia JK-SH007表达Cry3Aa融合蛋白SDS-PAGE和蛋白质印迹分析 Figure 4 SDS-PAGE and Western blotting analysis of Cry3Aa fusion protein expressed in B. pyrrocinia strain JK-SH007 M: Protein molecular mass markers (the corresponding sizes are indicated 1: The total cell lysates from B. pyrrocinia strain JK-SH007(pHKT2-T7RNApol) induced by 42℃ temperature shifting; 2: The total cell lysates from B. pyrrocinia JK-SH007(pHKT2-Cry3Aa) induced by 42℃ temperature shifting; The arrow indicates Cry3Aa (about 70 kDa) |
为检验工程菌JK-SH007(pHKT2-Cry3Aa)毒杀二龄榆蓝叶甲幼虫活性,实验选取了0.21~3.32 g/L 5个不同梯度湿重的发酵菌液浸泡榆树叶, 每个稀释浓度接种15条二龄榆蓝叶甲幼虫,实验做三个重复。结果发现对照组B. pyrrocinia JK-SH007(pHKT2-T7RNApol)死亡率为0,而相同的剂量重组菌B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)对榆蓝叶甲幼虫致死效果明显,尤其当浓度为3.32 g/L时,B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)工程菌对榆蓝叶甲幼虫致死率高达88.89%。随着工程菌浓度的稀释,杀虫活性也表现出下降(图 5)。通过计算得出,B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)的致死中浓度LC50为0.63(0.48~0.82) g/L(表 3)。同时实验对比了工程菌B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)与野生菌B. pyrrocinia JK-SH007在中位发酵浓度为0.83 g/L时对二龄榆蓝叶甲幼虫的存活周期(图 6)。以上结果证明工程菌B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)对榆蓝叶甲幼虫具有显著杀虫活性[24]。
|
| 图 5 B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)发酵液经PBS缓冲液稀释后不同梯度对榆蓝叶甲幼虫的致死率 Figure 5 Lethal rate of Pyrrhalta aenescens larvae using different doses of induced B. pyrrocinia JK-SH007(pHKT2-Cry3Aa) Bacteria were diluted with PBS (100 mmol/L, pH 7.8). Measurements were performed in triplicates. Error bars denote SD |

|

|
| 图 6 B.pyrrocinia JK-SH007重组菌液对榆蓝叶甲幼虫的毒杀存活率 Figure 6 Characterization of recombinant B.pyrrocinia JK-SH007 living bacteria on the survival rates of P. aenescens larvae Groups of P. aenescens larvae were treated with 0.83 g/L wet weight B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)or B. pyrrocinia JK-SH007(Control) (n = 15) |
榆树是多种天然林的重要组成部分。在我国,许多品种用作道路观赏、花园装饰、土壤保护而广泛种植。然而,近几十年,许多成年榆树死于虫害。对此,许多森林保护者和研究人员在这一森林病害的防治上做了大量的工作,并开发出许多用于昆虫防治的化学和生物制剂。然而,许多化学杀虫剂,如有机磷农药、有机氯农药,已被证明对环境和人类健康造成危害。为了对环境和人类健康的影响更加友好,生物农药被广泛使用,其中苏云金芽孢杆菌使用最广泛,因Bacillus thuringiensis的孢子形成过程中,能够产生多种杀虫成分[20, 25],其中Cry3Aa杀虫蛋白被证明对鞘翅目害虫具有最高的特异性细胞毒性。为了达到生物农药的高产以及对鞘翅目甲虫处理过程的优化,本研究合成优化了Cry3Aa基因,同时采用T7表达系统来表达Cry3Aa杀虫蛋白。此次实验Cry3Aa的表达具有一个相对较高的表达水平(0.48 g/L, 总蛋白的15.6%)。根据以往的研究报道,当T7启动子表达基因时,几乎所有的细胞资源都用来参与靶蛋白的表达,这也可能导致此次外源基因的高效表达。此次研究首次报道在野生B. pyrrocinia JK-SH007内生菌中。利用T7表达系统高效表达外源基因Cry3A杀虫蛋白。成功地使具有抑菌功效的植物内生菌吡咯伯克霍尔德氏菌JK-SH007表达了Cry3A蛋白。通过生测实验证明工程菌B. pyrrocinia JK-SH007(pHKT2-Cry3Aa)对榆树甲虫幼虫的控制是有效的。此次实验建立了以吡咯伯克霍尔德氏菌为宿主的苏云金芽孢杆菌杀虫蛋白的表达系统,将有助于我们开发,具有相当的生防潜力[26]环保的生物农药。
| [1] | Schnepe E, Crickmore N, Lereculus D. Bacillus thuringiensis and its pesticidal crystal proteins. Microbiol Mol Biol Rev, 1998, 62 : 775–806. |
| [2] | Tabashnik B E, Carriere Y, Dennehy T J, et al. Insect resistance to transgenic Bt crops:lessons from the laboratory and field. J. Econ Entomol, 2003, 96 : 1031–1038. DOI:10.1093/jee/96.4.1031 |
| [3] |
Seker V, Thompson D A, Maroney M J, et al. Proc Natl Acad Sci UAS.1987.84:7036-7040 |
| [4] | Whiteley H R, Schnepf H. E. The molecular biology of parasporal crystal body formation in Bacillus thuringiensis. Annual Review of Microbiology, 1986, 40(1) : 549–576. DOI:10.1146/annurev.mi.40.100186.003001 |
| [5] | Herrnstadt C, Gilroy T E, Sobieski D A, et al. Nucleotide sequence and deduced amino acid sequence of a coleopteran-active delta-endotoxin gene from Bacillus thuringiensis subsp. Sandiego. Gene, 1987, 57(1) : 37–46. DOI:10.1016/0378-1119(87)90174-0 |
| [6] | Park Y, Abdullah M A, Taylor M D, et al. Enhancement of Bacillus thuringiensis Cry3Aa and Cry3Bb toxicities to coleopteran larvae by a toxin-binding fragment of an insect cadherin. Appl Environ Microbiol, 2009, 75 : 3086–3092. DOI:10.1128/AEM.00268-09 |
| [7] | Park Y, Hua G, Taylor M D, et al. A coleopteran cadherin fragment synergizes toxicity of Bacillus thuringiensis toxins Cry3Aa, Cry3Bb, and Cry8Ca against lesser mealworm, Alphitobius diaperinus (Coleoptera:Tenebrionidae). J. Invertebr Pathol, 2014, 123 : 1–5. DOI:10.1016/j.jip.2014.08.008 |
| [8] | Hua G, Park Y, Adang M J. Cadherin Adcad1 in Alphitobius diaperinus larvae is a receptor of Cry3Bb toxin from Bacillus thuringiensis. Insect Biochem Mol Biol, 2014, 45 : 11–17. DOI:10.1016/j.ibmb.2013.10.007 |
| [9] | Crickmore N, Zeugler D R, Feitelson J, et al. Revision of the nomenclature for the Bacillus thuringiensis pesticidal Crystal progeins. Microbilogy and Molecular Biology Reviews, 1998 : 807–813. |
| [10] | Abbott W S. A method of computing the effectiveness of an insecticide. Journal of the American Mosquito Control Association, 1987, 3(2) : 302–303. |
| [11] | Nicholas D, Stephen E. Transgenic Plant and Insect Pests Bio-control. JohnWiley & Sons Press, 1997 : 1–18. |
| [12] |
任嘉红, 班虎栋, 叶建仁, 等.
吡咯伯克霍尔德氏菌JK-SH007的发酵条件及其对杨树溃疡病的防治效果. 中国生物防治学报, 2010, 26(3) : 300–306.
Ren J H, Ban H D, Ye J R, et al. Fermentation conditions of antagonistic strain Burkholderia pyrrocinia JK-SH007and its control effect on poplar canker disease. Chinese Journal of Biological Control, 2010, 26(3) : 300–306. |
| [13] | Zhao T H, Cai Q N, Luo K, et al. Research on insect-resistant cotton endophytic bacterium. In:Progress of Research on Chinese Plant Protection, 1996 : 684. |
| [14] |
张杰, 宋福平. 对鞘翅目害虫高毒力Bt基因cry3Aa7的分离克隆及表达研究. 中国农业科学, 2003, 21: 1493-1497 Zhang J, Song F P, Li C Y, et al. Cloning and expression of cry3Aa7 Gene from Bacillus thuringiensis strain toxic to Coleopteran pests. Scientia Agricultura Sinica, 2002, 35(6):650-653. |
| [15] |
杨波, 张绍勇, 陈振, 等.
新化合物天维菌素的杀虫杀螨活性. 农药学学报, 2016, 18(1) : 124–129.
Yang B, Zhang S Y, Chen Z, et al. Insecticidal and acaricidal activity of novel compound tenvermectin. Chinese Journal of Pesticide Science, 2016, 18(1) : 124–129. |
| [16] | Zhu D, Zhong X, Tan R, et al. High-throughput cloning of human liver complete open reading frames using homologous recombination in Escherichia coli. Anal Biochem, 2010, 397(2) : 162–167. DOI:10.1016/j.ab.2009.10.018 |
| [17] | Shivakumar A G. Vegetative expression of the δ-endotoxin genes of Bacillus thuringiensis subsp.kustaki in Bacillus subtilis. J Bacteriol, 1986, 166 : 194–204. DOI:10.1128/jb.166.1.194-204.1986 |
| [18] | Tomlin K L, Clark S R, et al. Green and red fluorescent protein vectors for use in biofilm studies of the intrinsically resistant Burkholderia cepacia complex. J Microbiol Methods, 2004, 57 : 95–106. DOI:10.1016/j.mimet.2003.12.007 |
| [19] | Liu Y, Zhang L, Zhang Y, et al. Functional analysis of rnai suppressor p19 on improving baculovirus yield and transgene expression in sf 9 cells. Biotechnology Letters, 2015, 37(11) : 1–8. |
| [20] | Li J J, Zhang G, Yu J H, et al. Molecular cloning and characterization of caffeic acid 3-o-methyltransferase from the rhizome of ligusticum chuanxiong. Biotechnology Letters, 2015, 37(11) : 2295–2302. DOI:10.1007/s10529-015-1917-y |
| [21] |
熊海燕, 王为国, 曾东方, 等.
介绍测量菌液浓度的一种方法. 食品信息与技术, 2004(3) : 59–59.
Xiong H Y, Wang W G, Wang C W, et al. A method of determining the cell concertration. Sichuan Food and Fermentation, 2004(3) : 59–59. |
| [22] | Ferre J, Van Rie J. Biochemistry and genetics of insect resistance to Bacillus thuringiensis. Annu Rev Entomol, 2002, 47 : 501–533. DOI:10.1146/annurev.ento.47.091201.145234 |
| [23] | Vadlamudi R K, Weber E, Ji I, et al. Cloning and expression of a receptor for an insecticidal toxin of Bacillus thuringiensis. J Biol Chem, 1995, 270 : 5490–5494. DOI:10.1074/jbc.270.10.5490 |
| [24] |
冯书亮, 付韵琴, 范秀华, 等.
几株高效苏云金杆菌菌株对玉米螟、棉铃虫、粘虫和黄地老虎的毒力测定. 中国生物防治学报, 1995, 11(1) : 22–25.
Feng S L, Fu Y Q, Fan X H, et al. A study on bioassay for toxicities of several highly effective strains of Bacillus thuringiensis to four species of lepidopterous larvae. Chinese Journal of Biological Control, 1995, 11(1) : 22–25. |
| [25] | Zhao J Z, Cao J, Li Y, et al. Transgenic plants expressing two Bacillus thuringiensis toxins delay insect resistance evolution. Nat Biotechnol, 2003, 21 : 1493–1497. DOI:10.1038/nbt907 |
| [26] | Harwood C R, Cutting S M. Molecular biological methods for Bacillus. Febs Letters, 1990, 287(1-2) : 227. |
 2017, Vol. 37
2017, Vol. 37