文章信息
- 王旭静, 张欣, 刘培磊, 王志兴
- WANG Xu-jing, ZHANG Xin, LIU Pei-lei, WANG Zhi-xing
- 复合性状转基因植物的应用现状与安全评价
- The Application and Safety Assessment of Stacked Transgenic Plant
- 中国生物工程杂志, 2016, 36(4): 18-23
- China Biotechnology, 2016, 36(4): 18-23
- http://dx.doi.org/10.13523/j.cb.20160403
-
文章历史
- 收稿日期: 2016-01-13
- 修回日期: 2016-01-27
2. 农业部科技发展中心 北京 100122
2. Development Center of Science and Technology, Ministry of Agriculture of the People's Republic of China, Beijing 100122, China
通过分子复合或育种复合的方式,将两种或两种以上的基因或性状导入同一植物中并使其稳定遗传给后代,这种含有两个或两个以上基因或新性状的转基因植物称为复合性状转基因植物。与单性状转基因植物相比,复合性状转基因植物具有集成创新、节省资源,聚合多个优良性状、满足种植者多元化需求,以及提高资源利用效率等优势[1]。
复合性状转基因植物可以通过共转化、再转化和育种复合三种途径获得[2]。国际上把共转化和再转化获得的复合性状转基因植物作为新的转化体看待,其安全评价同样按照新转化体的要求提供全面系统数据。对育种复合获得的复合性状转基因植物,不同国家采取了适合本国国情的安全评价模式。本文对育种复合性状转基因植物的研发应用现状、国际上对育种复合转基因植物的安全评价进行了综述,并提出了我国对育种复合转基因植物安全评价的建议,以期为我国复合性状转基因植物安全评价提供理论依据。
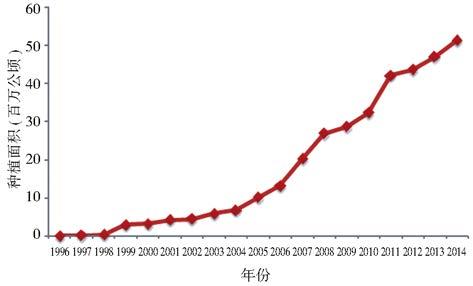
1 复合性状转基因植物的应用现状转基因植物商业化种植20年后,伴随着单性状产品的逐渐丰富和研发单位的相互授权,复合性状已成为转基因植物发展的一个重要趋势。据ISAAA统计,复合性状转基因植物的种植面积持续增加,2014年全球复合性状转基因植物种植面积达5 140万公顷,比2013年增长9%,占转基因植物总种植面积的28%,成为当前发展最快的转基因植物类型(图 1)。在28个转基因植物种植国家中,美国、巴西、阿根廷、加拿大、菲律宾等13个国家种植了复合性状转基因植物(图 2)。其中美国复合性状转基因玉米和棉花的种植面积分别占玉米和棉花总种植面积的76%和78%[3]。而且,复合性状转基因植物商业化种植将进一步飞速发展。
|
| 图 1 1996~2014年复合性状转基因植物的种植面积 Fig. 1 The planting area of stacked transgenic plant between 1996 and 2014 |
当前,已有约120个育种复合转化体批准商业化应用,复合的性状以抗虫抗除草剂、多基因抗虫复合为主,涉及的作物包括棉花、玉米、大豆、油菜(表 1)。其中SmartStaxTM是一种复合了8个基因的转基因玉米,它具有抗地上和地下害虫、及抗除草剂三种性状,2010年在美国和加拿大批准商业化应用[4]。

|
| 图 2 2014年复合性状转基因植物的种植国家及种植面积 Fig. 2 The planting country and area of stacked transgenic plant in 2014 (million hectares) |
目前,国际上对育种复合转基因植物的安全评价没有统一标准,世界卫生组织、粮农组织和国际植保协会(Croplife International) 等国际组织认为育种复合与传统育种具有实质等同性,如果单性状亲本证明是安全的,那么其育种复合产品也是安全的[5, 6, 7, 8]。美国和加拿大等国家与这些国际组织的看法一致,对育种复合转基因植物采取了比较宽松的评价模式。但因为受技术发展水平、经济利益、公众接受程度等各种因素的影响,不同国家对复合性状转基因植物采取了不同的评价模式,所要求提供的资料和数据也大相径庭。
| 复合转基因植物名称 | 复合的基因 | 复合的性状 | 商业化种植时间 |
| 油菜MS8×RF3×GT73 | bar,barnase,cp4-epsps,goxv247 | 抗除草剂和育性控制 | 2012 |
| GHB614×LLCotton25×MON15985 | cry1Ac,cry2Ab2,bar,2mepsps,nptII,aad,uidA | 抗虫抗除草剂 | 2011 |
| GHB614×T304-40×GHB119 | 2mepsps,cry1Ab,cry2Ae,bar | 抗虫抗除草剂 | 2012 |
| T304-40×GHB119 | cry1Ab,cry2Ae,bar | 抗虫抗除草剂 | 2011 |
| 5307×MIR604×Bt11×TC1507×GA21 | ecry3.1Ab,mcry3A,cry1Ab,pat,cry1Fa2,mepsps,pmi | 抗虫抗除草剂 | 2012 |
| 5307×MIR604×Bt11×TC1507×GA21×MIR162 | ecry3.1Ab,mcry3A,cry1Ab,pat,cry1Fa2,mepsps,vip3Aa20,pmi | 抗虫抗除草剂 | 2012 |
| BT11×59122×MIR604×TC1507×GA21 | Pat,cry1Ab,cry34Ab1,cry35Ab1,mcry3A,pmi,mepsps,cry1Fa2 | 抗虫抗除草剂 | 2011 |
| Bt11×MIR162×MIR604×GA21 | cry1Ab,vip3Aa20,pat,pmi,mcry3A,mepsps | 抗虫抗除草剂 | 2012 |
| BT11×MIR162×MIR604×TC1507×GA21 | cry1Ab,vip3Aa20,cry1Fa2,pat,mepsps,pmi ,mcry3A | 抗虫抗除草剂 | 2011 |
| Bt11×MIR162×TC1507×GA21 | cry1Ab,vip3Aa20,cry1Fa2,pat,pmi,mepsps | 抗虫抗除草剂 | 2011 |
| BT11×MIR604 x GA21 | cry1Ab,pat,mcry3A,pmi,mepsps | 抗虫抗除草剂 | 2011 |
| MON87427×MON89034×MON88017 | cp4 -epsps,cry2Ab2,cry1A.105,cry3Bb1 | 抗虫抗除草剂 | 2013 |
| MON87427×MON89034×NK603 | cp4 -epsps ,cry2Ab2,cry1A.105 | 抗虫抗除草剂 | 2013 |
| MON87460×MON89034×MON88017 | cspB,cry1A.105,cry2Ab2,cry3Bb1,cp4- epsps,nptII | 抗虫抗除草剂和非生物逆境 | 2012 |
| MON87460×MON89034 x NK603 | cp4-epsps,cry2Ab2,cry1A.105,cspB,nptII | 抗虫抗除草剂和非生物逆境 | 2012 |
| MON87460×NK603 | cp4 -epsps,cspB,nptII | 抗除草剂和非生物逆境 | 2012 |
| TC1507×59122×MON810×MIR604 x NK603 | cry1Fa2,cp4-epsps,pat,cry34Ab1,cry35Ab1,cry1Ab,mcry3A,pmi | 抗虫抗除草剂 | 2012 |
| TC1507×59122×MON810 x NK603 | cry1Fa2,cp4-epsps,pat,cry34Ab1,cry35Ab1,cry1Ab | 抗虫抗除草剂 | 2011 |
| TC1507 ×MIR604×NK603 | cry1Fa2,cp4-epsps,pat,mcry3A,pmi | 抗虫抗除草剂 | 2011 |
| TC1507×MON810 | cry1Fa2,cry1Ab,pat | 抗虫抗除草剂 | 2011 |
| TC1507×MON810×NK603 | cry1Fa2,cry1Ab,pat,cp4-epsps | 抗虫抗除草剂 | 2011 |
| DP305423×GTS 40-3-2 | gm-hra,gm-fad2-1 (partial sequence),cp4 epsps | 抗除草剂和品质改良 | 2012 |
| MON87708×MON89788 | dmo,cp4-epsps | 抗2种除草剂 | 2013 |
这种模式对复合性状转基因植物的安全评价比较宽松,主要依据单个转化体来管理育种复合的转基因植物。一般来说,如果单性状亲本已经批准商业化应用,其育种复合后代被认为也是安全的,不需要单独进行审批。
美国转基因植物的管理部门包括农业部、食品药品局和环保署。三部门对育种复合转基因植物均不进行评价。农业部对育种复合转基因植物不进行监管;食品药品局要求事先告知,研发商需向食品安全与营养中心提交复合转基因植物的生物技术报告;环保署会对多个抗虫基因复合的转基因植物进行安全评价,评价内容主要包括单个转化体亲本在复合转基因植物中的存在和遗传稳定性,以及基因间的相互作用[9]。
加拿大对复合性状转基因植物的安全评价与美国相同,只针对单个转化体。研发商需要在复合性状转基因植物商业化应用前自己完成安全评价报告,并告知食品检验局,食品检验局根据研发商提供的评价资料确定是否需要进行其它的评价试验[10, 11]。迄今加拿大还没有一例复合性状转基因植物要求进行额外的评价试验。
2.2 澳大利亚/新西兰模式澳大利亚和新西兰对复合性状转基因植物的评价模式本质上与美国和加拿大相同,对复合性状转基因植物不进行评价和审批,只需要研发商事先向澳新食品标准局提交上市报告[12]。但因其特殊的地理位置,要求对环境安全性进行风险评估,评估时充分考虑单性状亲本的安全性,重点评价基因互作可能带来的环境风险,评价指标基本与美国环保署的要求相同[1]。
2.3 日本/韩国模式日本基于单转化体中对植物代谢的影响将转基因植物分成3类。第一类为没有改变受体植物的代谢途径,第二类为改变受体植物代谢途径,导致内源代谢产物的增加或减少,第三类为改变受体植物代谢途径,并引入新的代谢产物。复合性状转基因植物的管理根据其含有的单性状亲本来进行分级管理[13]。对只含有第一类的复合产品在不改变性状和用途的前提下,采取豁免审批的政策,但需要通知管理部门;对于含有第二类和第三类的复合性状转基因植物需要依据个案分析的原则进行安全评价。
韩国负责复合性状转基因植物安全评价的部门是食品药品局,采用事前告知制度。复合性状转基因植物的安全评价程序分为豁免和非豁免两类。对于未改变目标蛋白表达水平、无亚种间杂交、不改变人类消费水平、植物取食部位和用途的复合性状转基因植物采取豁免评价程序,只需要提供目标性状有效存在的生物学测定数据。其他类型的复合性状转基因植物采取非豁免评价程序,需要进行严格的安全评价。
2.4 阿根廷/菲律宾模式阿根廷和菲律宾对复合性状转基因植物的商业化应用需要附加审批,审批时以单性状转基因亲本为基准,采用补充相关数据的方法进行评估。要求在评估单个转化体的基础上,提供单性状在育种复合转基因植物中存在和遗传稳定性,以及基因间相互作用的数据和资料,并根据这些资料来对复合性状植物进行评估。
2.5 欧盟模式欧盟对复合性状转基因植物的安全评价采取与单性状转化体相同的评价程序,申报资料的要求也基本相同。欧洲食品安全局颁布的安全评价手册指出,复合性状转基因植物分为两类,一类为其亲本已批准,一类为亲本未批准应用。前者的安全评价应以亲本的安全性资料和评价方法为基准,重点评价目标基因的完整性、表型的稳定性和基因间互作,而后者作为新性状重新评价[14, 15, 16]。虽然欧盟的安全评价指南提出基于亲本的安全性资料和评价方法对复合性状转基因植物进行安全评价,但其评价内容涵盖了单转化体的全部资料和程序。
3 育种复合转基因植物安全性的考虑传统育种其实是已知或未知基因的聚合过程。植物育种大约起始于1万年前[17],最早的植物育种是人们保留表现好的植物种子,并在下一生长季进行种植。随着1900年孟德尔遗传规律的发现[18],人们开始通过杂交育种、基因渐渗、突变、双倍体等传统育种技术来培育产量、营养和农艺性状等优良的新品种。在此过程中,通过基因渐渗和基因聚合将抗病、高产、耐胁迫、和品质改良等许多优异性状从野生种中转入栽培种。20年内,19种作物中有111个基因从野生种转入了栽培种,其中80%与抗病有关[19, 20]。
在品种选育过程中,育种家利用杂种优势、基因及其产品间的非叠加效应来培育性状优良的作物新品种[21, 22]。近年来,研究者们分析了一些可能与杂种优势有关的分子参数,结果表明杂交育种过程中发生了成千的基因间的非叠加效应,甚至有时基因间的互作会导致基因沉默,只不过这些材料会在育种过程中被淘汰[23]。
育种复合转基因植物的培育实质上是常规杂交育种过程,通过在不同环境下的多代筛选而获得目标性状稳定遗传的品种。在选育过程中,育种者通过分析植物的表型特征来推测其可能产生的一些非预期效应,并帮助其选择食用/饲用产品的安全性和品质不会发生变化的后代进行培育[24, 25]。
传统育种培育的新品种不需要进行安全评价而被认为是安全的,其安全性是基于原有的作物品种具有长期安全食用/饲用的历史。转基因植物育种复合所用单性状亲本已经过全面的安全评价,与其受体品种一样安全,而复合过程等同于杂交育种,在食用和饲用安全性方面不会比常规育种产生更多的风险[26, ]。因此,认为利用已批准商业化应用的单性状转化体育种复合获得的转基因植物也是安全的,不需要再进行重新评价。
综上所述,虽然不同国家对育种复合转基因植物的安全评价采取了不同的模式,但其安全评价的焦点都集中在遗传稳定性和基因互作两个方面。目前国际上已进行了大量的这方面研究。对于遗传稳定性方面,Weber等从植物基因组的可塑性、基因沉默、基因重组等多方面分析了育种复合对基因组稳定性的影响,最终得出结论认为育种复合不会对植物基因组的稳定性产生影响[27]。我们实验室利用基因芯片技术分析了育种复合后代与其亲本的SNP差异,结果发现育种复合造成的SNP差异小于不同品种间的SNP差异,说明不会对基因组稳定性产生影响。对于基因互作,Wayne Parrott等认为评价基因互作时应从基因间的直接互作、基因表达模式和代谢途径的参与三方面来考虑,并提出了复合性状转基因植物安全评价模型(图 3),认为评价时应采取个案分析[28]。

|
| 图 3 复合性状转基因植物安全评价模型 Fig. 3 Safety assessment model of stacked transgenic plant |
在转基因新品种培育重大专项的引领下,我国已形成单一性状和复合性状兼顾的转基因植物研发格局,而且美国、巴西等国家也有复合性状转基因植物申请出口我国。为了保证我国复合性状转基因植物的产业化进程健康有序发展,结合上述分析和吸取其他国家的评价经验,对我国复合性状转基因植物的安全评价提出以下建议:(1)采取个案分析、分类管理的原则。(2)需进行安全审批,审批时提供以下数据:①复合性状转基因植物的分子特征:包括目标基因在植物基因组中整合的稳定性、目标基因表达稳定性、外源插入片段的完整性、及目标性状遗传稳定性等方面的数据分析。②基因间互作:通过分析单性状转化体的基本信息,包括目标基因同源性、表达调控元件及标记基因、整合位点、目标蛋白的作用机制等,确定基因间互作的可能性,并进行分类。目标基因间不存在基因互作时,则只需要提供证明目标基因育种复合后稳定存在的数据,不必再进行其他方面的安全评价。目标基因间存在基因互作的可能性时,需要评价基因互作对食品和环境安全性产生的影响。对于多基因抗虫复合转基因植物,应通过等级测试和分层次评价来分析复合性状转基因植物与单性状亲本对非靶标生物影响的差异。
| [1] | 刘培磊,李宁,程金根. 不同国家和地区复合性状转基因植物安全评价管理的比较. 农业科技管理, 2008, 27(3): 23-27. Liu P L, Li N, Cheng J G. Comparison of safety assessment of stacked transgenic plant in different country and region. Management of Agricultural Science and Technology, 2008, 27(3): 23-27. |
| [2] | Halpin C. Gene stacking in transgenic plants——the challenge for 21st century plant biotechnology. Plant Biotech J, 2005, 3 : 141-155. |
| [3] | James Clive. 2014年全球生物技术/转基因植物商业化发展态势. 中国生物工程杂志, 2015, 35(1): 1-14. James C. Global status of commercialized biotech/GM crops in 2014.China Biotech, 2015, 35(1): 1-14. |
| [4] | James Clive. 2011年全球生物技术/转基因植物商业化发展态势. 中国生物工程杂志, 2012, 32(1): 1-14. James C. Global status of commercialized biotech/GM crops in 2011. China Biotech, 2012, 32(1): 1-14. |
| [5] | World Health Organization. Application of the Principles of Substantial Equivalence to the Safety Evaluation of Foods or Food Components from Plants Derived by Modern Biotechnology. Geneva: World Health Organization 1995/FNU/FOS/95.1. |
| [6] | CropLife International. Regulation of plant biotechnology products containing two or more traits combined by conventional plant breeding. 2005, . |
| [8] | International Seed Federation. Genetically modified crops and plant breeding. . |
| [9] | EPA. Biopesticides registration action document ——Bacillus thuringiensis plant-incorporated Protectants. http: //www.epa. gov/oppbppd1/biopesticides/pips/bt-brad. htm. |
| [10] | Canadian Food Inspection Agency. Directive 94-08 (Dir 94-08): Assessment Criteria for Determining Environmental Safety of Plants With Novel Traits. http://www.inspection.gc.ca/plants/plants-with-novel-traits/applicants/directive-94-08/eng/1304475469806/1304475550733. |
| [11] | Canadian Food Inspection Agency. Regulating the Environmental Release of Stacked Plant Products in Canada. http://www.inspection.gc.ca/plants/plants-with-novel-traits/approved-under-review/stacked-traits/eng/1337653008661/1337653513037. |
| [12] | Office of the Gene Technology Regulator of Australia. Policy on Licensing of Plant GMOs in which Different Genetic Modifications have been Combined (or 'Stacked') by Conventional Breeding. http://www.ogtr.gov.au/internet/ogtr/publishing.nsf/Content/gmstacking08-htm. |
| [13] | Food Safety Commission. Regarding safty assessment of crossing of genetically modified plants. 2004-1-29. http://www.fsc.go.jp/senmon/idensi/gm_kangaekata.pdf. |
| [14] | EFSA. Guidance document of the scientific panel on genetically modified organisms for the risk assessment of genetically modified plants and derived food and feed. The EFSA Journal, 2004,99:1-94. |
| [15] | The European Association for Bioindustries. Safety assessment of GM crops: Document 5- Evaluation of crops containing GM events combined by traditional breeding . http://www.europabio.org/relatedinfo/CP12.pdf. |
| [16] | Anon. Risk Assessment of Plants Containing Genetic Modification Events Combined by Crossing- for public consultation. http://www.efsa.europa.eu/science/ gmo/gmo_consultations/1035_en.html. |
| [17] | McCouch S. Diversifying selection in plant breeding. PLoS Biolology, 2004, 2: 1507-1512. |
| [18] | Duvick D N. Plant breeding, an evolutionary concept. Crop Sci, 1996, 36: 539-548. |
| [19] | Hajjar R, Hodgkin T. The use of wild relatives in crop improvement: a survey of developments over the last 20 years. Euphytica, 2007, 156: 1-13. |
| [20] | Fernie A R, Tadmor Y, Zamir D. Natural genetic variation for improving crop quality. Curr Opin Plant Biol, 2006, 9:196-202. |
| [21] | Groszmann M, Greaves I K, Albertyn Z I, et al. Changes in 24-nt siRNA levels in Arabidopsis hybrids suggest an epigenetic contribution to hybrid vigor. Proc Natl Acad Sci USA, 2011, 108: 2617-2622. |
| [22] | Xu X, Pan S, Cheng S, et al. Genome sequence and analysis of the tuber crop potato. Nature, 2011, 475: 189-195. |
| [23] | Parrott W, Chassy B, Ligon J, et al. Application of food and feed safety assessment principles to evaluate transgenic approaches to gene modulation in crops. Food Chem Toxicol, 2010, 48: 1773-1790. |
| [24] | Cellini F, Chesson A, Colquhoun I, et al. Unintended effects and their detection in genetically modified crops. Food Chem Toxicol, 2004, 42: 1089-1125. |
| [25] | National Research Council. Safety of Genetically Engineered Foods: Approaches to Assessing Unintended Health Effects. Washington, DC, USA: National Academies Press, 2004. |
| [26] | Pilacinski W, Crawford A, Downey R, et al. Plants with genetically modified events combined by conventional breeding: an assessment of the need for additional regulatory data. Food Chem Toxicol, 2011, 49(1):1-7. |
| [27] | Weber N, Halpin C, Hannah L C, et al. Editor's choice: Crop genome plasticity and its relevance to food and feed safety of genetically engineered breeding stacks. Plant Physiol, 2012, 160(4):1842-1853. |
| [28] | Steiner H Y, Halpin C, Jez J M, et al. Editor's choice: Evaluating the potential for adverse interactions within genetically engineered breeding stacks. Plant Physiol, 2013, 161(4):1587-1594. |
 2016, Vol. 36
2016, Vol. 36




