文章信息
- 王东波, 马义, 王孝丽, 赵绍军, 韩磊, 洪岸
- WANG Dong-Bo, MA Yi, WANG Xiao-Li, ZHAO Shao-Jun, HAN Lei, HONG An
- 基因重组PACAP27衍生多肽RP2制备及促角膜上皮细胞增殖研究
- Preparation of Recombinant PACAP 27-derived Peptide RP2 and Its Effects on Promoting Corneal Epithelial Cell Proliferation
- 中国生物工程杂志, 2015, 35(3): 61-65
- China Biotechnology, 2015, 35(3): 61-65
- http://dx.doi.org/10.13523/j.cb.20150309
-
文章历史
- 收稿日期:2015-01-28
- 修回日期:2015-02-02
垂体腺苷酸环化酶激活肽(pituitary adenylate cyclase activating polypeptide,PACAP)是促胰液素/胰高血糖素/血管活性肽(VIP)家族中的一员,具有的较强的AC(腺苷酸环化酶)激活活性。主要以PACAP 38及PACAP 27(PACAP 38氨基末端1~27位aa序列)两种形式存在,并被证实来源于一个共同176个aa组成的前体蛋白[1]。PACAP及其受体不仅分布在中枢神经系统、周围神经系统,而且在周围组织、器官也广泛分布。
PACAP作为一种神经递质和神经营养因子在神经系统的发育中起着重要作用[2]。PACAP有三类特异的G蛋白偶联受体:PAC1、VPAC1和VPAC2,然而PAC1受体主要分布在中枢神经系统中[3]。在眼部PACAP及其受体主要分布在角膜、虹膜、睫状神经节、视网膜等[4]。角膜的敏感性、透光性与间质细胞和上皮细胞的完整性密不可分[5, 6]。现有研究表明,PACAP与角膜上皮细胞的损伤修复存在密切的关系[7, 8];同时,PACAP可有效促进三叉神经节细胞突触再生及损伤修复,而角膜有大量三叉神经末梢分布,是角膜视觉敏感性的生理基础[9]。所以PACAP在角膜的损伤修复中可发挥重要作用。前期研究表明,野生型PACAP 27在体外的稳定性较低,而在PACAP 27的N末端添加一个氨基酸(His)以及突变一个氨基酸(V19L)得到的重组多肽,可具有更高的稳定性[10, 11]。本研究利用基因重组技术及新型高效的表达载体pTXB1-MCS,表达和制备PAC1型受体特异激动剂RP2,并进一步优化表达纯化条件[12],以提高重组肽的产量和纯度,并利用重组表达和制备的RP2,研究其促进角膜上皮细胞损伤修复的生物学效应,为其药用研发提供实验基础。 1 材料与方法 1.1 材 料 1.1.1 菌株与试剂
高效质粒表达载体pTXB1、大肠杆菌ER2566(美国New England Biolab 公司)小鼠角膜上皮细胞(ATCC细胞库);Chitin-Beads(美国New England Biolabs公司);限制性核酸内切酶Nde I和BspQ I(美国New England Biolabs公司);T4 DNA连接酶(美国New England Biolabs公司);PCR 片段纯化 Kit、切胶回收 Kit(日本TaKaRa公司);乙腈(上海安普公司);三氟乙酸(美国Merck公司);引物合成及DNA测序由艾基基因公司完成;MTT等试剂均为国产分析纯。 1.1.2 主要仪器设备
高速冷冻离心机(德国Sigma公司);微量移液器(德国Eppendorf); PCR仪(美国BIO-RAD公司);5L发酵罐(无锡东盛石化装备有限公司);超声破碎仪(中国广州聚能生物科技有限公司);冷冻干燥机(北京悦诚嘉业科技有限公司); C18反相柱(上海月旭材料科技有限公司);HPLC系统Waters e2695(美国Waters公司);恒温培养箱(美国Thermo scientific);核酸蛋白分析仪(日本日立公司)。 1.2 方 法 1.2.1 重组质粒pTXB1-RP2的构建与鉴定
选用大肠杆菌偏爱密码子设计引物,利用重叠延伸PCR技术合成RP2全基因序列,并插入质粒载体pTXB1-MCS的NdeⅠ和BspQⅠ酶切位点之间,构建重组表达质粒pTXB1-RP2,然后,转化大肠杆菌ER2566,转化菌接种在涂有氨苄青霉素的平板上,挑取单菌落培养并抽取质粒,进行DNA测序验证。 1.2.2 融合蛋白RP2-intein-CBD的表达和目的肽RP2的制备和鉴定
表达工程菌pTXB1-RP2/ER2566在含有50 mg/ml氨苄青霉素的5 ml LB液体培养基中,37℃摇菌过夜,再转接至含50 mg/ml氨苄青霉素300 ml LB培养基的摇瓶中培养2~3 h,菌种转入5 L发酵罐中培养,培养至OD600=1.5,加入IPTG至终浓度为0.7 mmol/L,30 ℃诱导表达4 h。发酵产物4℃,7 000g离心10 min,弃上清收集菌体,用含20 mmol/L HEPES,500 mmol/L NaCl,1 mmol/L EDTA的Buffer 1(pH=8)重悬菌体,用超声破碎仪进行破碎,破碎产物4℃,15 000g离心40min,上清液过Chitin-Beads柱纯化,流速为0.5 ml/min,整个纯化过程在层析冷柜(4℃)中进行;过柱完成后,使用Buffer 1快速洗柱,流速为3 ml/min,洗脱20倍柱体积;洗柱完成后用含有20 mmol/L HEPES,500 mmol/L NaCl,1 mmol/L EDTA,40 mmol/L DTT的切割缓冲液Buffer 2(pH=8)快速过柱,流速5 ml/min,洗脱3个柱体积;洗脱完成后停止洗脱,取柱子中的Chitin-Beads,用于鉴定融合蛋白的结合效率;将结合有融合蛋白的Chitin-Beads柱与Buffer 2在4℃孵育48 h,以诱导内含肽自剪切;切割完成后收集切割缓冲液利用HPLC进一步纯化和制备RP2,并分析其纯度,HPLC分析条件如表 1所列(乙腈和超纯水中均含有0.1%的三氟乙酸TFA)。制备的重组肽进一步经SDS-PAGE鉴定和质谱鉴定。
| 时间min | 流速ml/min | 流动相A | 流动相B |
| 乙腈(%) | 超纯水(%) | ||
| 0 | 1.23 | 3 | 97 |
| 5 | 1.23 | 3 | 97 |
| 25 | 1.23 | 60 | 40 |
| 30 | 1.23 | 60 | 40 |
培养的小鼠角膜上皮细胞,分别用RP2、PACAP 27、PBS处理24 h和48 h。然后采用MTT法测量角膜上皮细胞增殖率,并采用SPSS 13.0统计学软件进行统计分析,P<0.05为差异有统计学意义,P<0.01为差异极显著。 2 结果与分析 2.1 重组质粒pTXB1-RP2的构建与鉴定
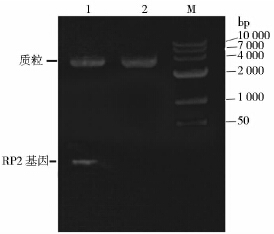
设计引物F1、F2和F3,使用重叠延伸PCR技术扩增,收获含有内切酶Nde I 和BspQI 酶切位点的RP2基因;经双酶切后插入由Nde I 和BspQI 双酶切后的pTXB1-MCS载体中,T4 DNA连接酶连接,获得重组表达质粒pTXB1-RP2,该质粒双酶切验证如图 1;之后重组质粒转化至表达菌ER2566中,构建成表达工程菌pTXB1-RP2/ER2566。
|
| 图 1 重组质粒pTXB1-RP2鉴定 Fig. 1 Identification of recombinant plasmid pTXB1-RP2 1: The RP2 recombinant plasmid double digested;2:The RP2 recombinant plasmid M:High molecular DNA Maker |
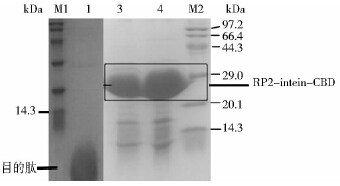
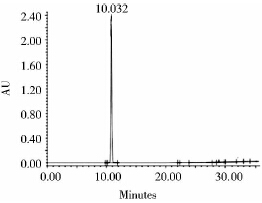
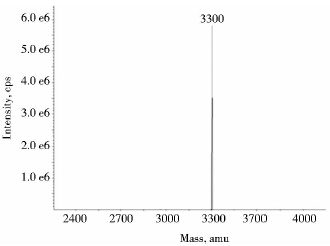
表达工程菌pTXB1-RP2/ER2566在35℃、0.7 mmol/L IPTG诱导浓度下诱导表达4 h,表达产物为融合蛋白RP2-intenin-CBD。收获的菌体超声破碎,破碎液在4℃、15 000g离心20 min,取上清液,即为含有融合蛋白的粗提液(图 2)。粗提液经Chitin-Beads柱亲和吸附(图 2),由DTT诱导intein自剪切而释放重组肽RP2,收集得到含有RP2多肽的切割液,经由HPLC分离、制备得到含有RP2的溶液,冻干后获得干粉;经SDS-PAGE鉴定(图 2) 重组肽RP2的条带位置与理论分子量相符合,用C18反相柱HPLC系统分析制备的RP2,出峰时间是10.032 min,获得的干粉制剂纯度大于96%(图 3)。进一步利用质谱鉴定制备的重组肽RP2的分子量为3.3 kDa,与理论值相符合(图 4);并且重组肽RP2的产量可达40mg/L(每升发酵液)。
|
| 图 2 重组RP2-inteni-CBD融合蛋白的表达与目的多肽RP2 Fig. 2 Expression of fusion protein RP2-intenin-CBD and recombinant peptide RP2 M1:Low molecular protein Maker; 1: Recombinant peptide RP2 after purification; 2:Protein bound to the chitin beads;3: The supernatant of the extracts after induced expression; M2:Low molecular protein Maker |
|
| 图 3 重组肽RP2的HPLC分析 Fig. 3 HPLC analysis of recombinant peptide RP2 |
|
| 图 4 重组肽 RP2 的质谱鉴定 Fig. 4 MS identification of recombinant peptide RP2 |
培养的小鼠角膜上皮细胞,分别使用PACAP 27、RP2、PBS培养24 或48 h,通过MTT法测量细胞增殖率,实验结果如表 2所示,在处理细胞24 h时,RP2处理组的细胞增殖率达到49.6%,是PACAP 27处理 组的1.71倍,是PBS处理组的2.46倍;处理细胞48 h时,RP2处理组的细胞增殖率是PACAP 27 处理的1.18倍,是PBS处理组的2.27倍。经统计学处理,差异极显著(P< 0.01)。实验结果表明,重组肽 RP2可明显促进角膜上皮细胞的增殖,且生物学效应明显高于PACAP 27。
| n | 24h | 48h | |
| RP2 | n=3 | (49.6±3.1)% | (93.0±1.7)% |
| PACAP27 | n=3 | (29.0±2.4)% | (78.8±2.6)% |
| Control | n=3 | (20.2±1.1)% | (40.9±3.3)% |
| P | P<0.01 | P<0.01 | |
PACAP作为一种重要的神经多肽,是近年来的研究热点之一。Schafer等证实大鼠脑细胞上有丰富的PACAP受体存在,并提出PACAP受体复合物与GTP结合蛋白有关系[13]。PACAP与受体的相互作用是快速、可逆和可饱和的,并受温度、pH和作用时间影响。PACAP不仅可在表达存在的局部发挥作用,而且可发挥激素样的“远距”作用。PACAP最基本的作用是激活AC(腺苷酸环化酶),使细胞内、外cAMP蓄积增加;PACAP作为一种神经营养因子,在促进垂体激素及相关基因表达,胰岛素分泌、生殖细胞发生、神经信号传导等方面发挥重要作用[14]。
角膜是眼睛最前面的透明部分,从外向内由5层结构组成:上皮细胞层、前弹力层、基质层、后弹力层和内皮细胞层。角膜有大量十分敏感的神经末梢分布,主要通过透过泪液及房水获取养份及氧气。角膜的完整性对于正常视力是必不可少的。角膜上皮细胞层作为最外层,易受到各种侵害,有研究表明,PACAP能够促进角膜上皮的损伤修复[8]。
由于稳定性差,野生型PACAP在体内的半衰期较短,阻碍了其体内生物学作用的发挥。前期研究表明,PACAP 27的N末端添加一个氨基酸(His)以及突变一个氨基酸(V19L)得到的重组多肽,可显著增加对PAC1受体的特异激动性,且在体内半衰期可以得到明显延长。本研究通过基因重组及DTT诱导自剪切技术制备PACAP衍生多肽RP2[15, 16],通过反相色谱进一步纯化,得到的重组多肽RP2的纯度可达到96%以上,产量可达到40毫克/(每升发酵液),从而,实现了RP2的高效制备,同时,本研究建立的表达纯化技术也能够用于PACAP其他衍生多肽及其类似物的纯化和制备。细胞学实验表明,PACAP 27重组多肽RP2对小鼠角膜上皮细胞增殖有明显的促进作用,且生物学作用明显强于野生型PACAP 27,这主要是因为改构后,与野生型PACAP 27相比较,重组肽RP2具有更高稳定性和PAC1受体激活活性。
因此,利用本研究建立的纯化制备技术制备的重组多肽RP2可用于角膜损伤修复研究,其促角膜上皮细胞增殖及神经细胞修复的分子机制还有待进一步的深入研究。
| [1] | Miyata A, Arimura A, Dahl R , et al. Isolation of a novel 38 residue-hypothalamic polypeptide which stimulates adenylate cyclase in pituitary cells. Biochemical and biophysical research communications, 1989,164(1): 567-574. |
| [2] | White C M, Ji S, Cai H,et al.Therapeutic potential of vasoactive intestinal peptide and its receptors in neurological disorders. CNS & neurological disorders drug targets, 2010,9(5): 661. |
| [3] | Farnham M M, Lung M S, Tallapragada V J, et al. PACAP causes PAC1/VPAC2 receptor mediated hypertension and sympathoexcitation in normal and hypertensive rats. American Journal of Physiology-Heart and Circulatory Physiology, 2012,303(7): H910-H917. |
| [4] | Troger J, Kieselbach G, Teuchner B, et al. Peptidergic nerves in the eye, their source and potential pathophysiological relevance. Brain research reviews, 2007,53(1): 39-62. |
| [5] | Ehlers N, HjortDa L.The cornea: epithelium and stroma. Advances in organ biology, 2005,10: 83-111. |
| [6] | Pellegrini G, Traverso C, Tito FranziA, et al. Long-term restoration of Da.maged corneal surfaces with autologous cultivated corneal epithelium. The Lancet, 1997,349(9057): 990-993. |
| [7] | Kenchegowda S, Bazan N G, Bazan H E.EGF stimulates lipoxin A4 synthesis and modulates repair in corneal epithelial cells through ERK and p38 activation. Investigative ophthalmology & visual science, 2011,52(5): 2240-2249. |
| [8] | Jiang X Y, McClellan S A, Elizabeth A B et al. VIP and growth factors in the infected cornea. Investigative ophthalmology & visual science, 2011,52(9):6154-6161. |
| [9] | Nakajima E, Walkup R D, Fujii A, et al. Pituitary adenylate cyclase-activating peptide induces neurite outgrowth in cultured monkey trigeminal ganglion cells: Involvement of receptor PAC1. Molecular vision, 2013,19: 174. |
| [10] | Li, H , Zhou, T, Ma Y, et al. An integrated strategy for improving plasma half-life of therapeutic peptides. Biopolymers, 2009, 92(4):363. |
| [11] | Ma Y, Ma M, Dai Y, Hong A, et al. Expression, identification and biological effects of a novel VPAC2-specific agonist with high stability and bioactivity. Acta biochimica et biophysica Sinica, 2010, 42(1): 21-29. |
| [12] | 徐文娜, 马义, 叶祖禄,等. 垂体腺苷酸环化酶激活肽衍生多肽 RHMP 的重组制备及促角膜损伤修复的初步研究. 中国生物工程杂志, 2013,33(2):65-69. Xu W N, Ma Y, Ye Z L, et al. Study on recombination and preparation of PACAP-derived polypeptide RHMP and its effects on promoting corneal wound healing.China Biotechnology, 2013,33(2): 65-69. |
| [13] | Schäfer H, Schwarzhoff R, Creutzfeldt W, et al. Characterization of a guanosine-nucleotide-binding-coupled receptor for pituitary adenylate cyclase activating polypeptide on plasma membranes from rat brain.Eur J Biochem,1991,202:951. |
| [14] | Arimura A. Perspectives on pituitary adenylate cyclase activating polypeptide (PACAP) in the neuroendocrine, endocrine, and nervous systems. The Japanese Journal of Physiology, 1998,48(5): 301-331. |
| [15] | Perler F B, Davis E O, Dean G E, et al. Protein splicing elements: inteins and exteins—a definition of terms and recommended nomenclature. Nucleic Acids Research, 1994,22(7): 1125. |
| [16] | Shah N H, Dann G P, Vila-Perelló M, et al. Ultrafast protein splicing is common among cyanobacterial split inteins: implications for protein engineering. Journal of the American Chemical Society,2012,134(28): 11338-11341. |
 2015, Vol. 35
2015, Vol. 35




