扩展功能
文章信息
- 陈宏宇, 张雅明, 张文佳, 于洋, 高晓丽, 王玥
- CHEN Hong-yu, ZHANG Ya-ming, ZHANG Wen-jia, YU Yang, GAO Xiao-li, WANG Yue
- 高温环境对德国小蠊基因表达的影响
- Effect of high temperature on gene expression of Blattella germanica
- 中国媒介生物学及控制杂志, 2020, 31(1): 62-65
- Chin J Vector Biol & Control, 2020, 31(1): 62-65
- 10.11853/j.issn.1003.8280.2020.01.013
-
文章历史
- 收稿日期: 2019-08-27
- 网络出版时间: 2019-12-30 09:37
昆虫是变温动物,环境温度对昆虫的生长、发育、繁殖和分布有重要影响。当温度升高到一定程度时,昆虫体内细胞会受到损害甚至死亡[1-2]。德国小蠊(Blattella germanica)是能传播多种疾病的世界性卫生害虫[3],其生长发育、种群繁殖及活动分布明显受到环境温度的影响[4-5]。为了初步推测德国小蠊的高温应答分子机制,本实验利用RNA-Seq转录组学方法,对40 ℃高温处理组和25 ℃常温对照组的德国小蠊成虫进行了差异表达基因识别、基因功能富集和代谢通路分析,从基因表达和调控角度分析了德国小蠊受高温胁迫后的基因反应。
1 材料与方法 1.1 试虫饲养与处理德国小蠊由本实验室提供。在25 ℃人工气候箱中饲养,随机选取个体大小相似,雌、雄各半的20只成虫,置于40 ℃人工气候箱作为高温处理组,同时随机选取个体大小相似,雌、雄各半的20只成虫,置于25 ℃人工气候箱作为对照,处理2 h后迅速将所有试虫置于液氮速冻,然后保存在-80 ℃冰箱备用。
1.2 RNA提取与测序利用TRIzol试剂盒(Invitrogen)提取试虫总RNA,利用RQ1 DNase(Promega)去除其中的DNA。利用SmartSpec Plus Spectrophotometer(Bio-Rad)和1.5%琼脂糖凝胶电泳检查总RNA的质量和纯度,合格后反转录纯化和扩增cDNA,取150~200 bp的PCR产物用于高通量测序,测序使用Illumina Genome Analyzer Iix。
1.3 测序数据分析去除测序结果中的接头序列、5′或3′末端质量值<20或者含N的碱基、“trim”以及读序长度<75 bp的序列,整理成备用原始数据。利用HISAT2(v2.0.1)和BLAST程序进行德国小蠊的基因组定位和基因注释,该基因组数据库注册德国小蠊基因28 774个[6]。利用GO(Gene Ontology database)和KEGG(Kyoto Encyclopedia of Genes and Genomes)数据库进行基因功能富集和代谢通路分析。利用RPKM值(reads per kilobase of exon model per million mapped reads)计算基因表达量[7]。利用DESeq2(V1.6.3)[8]和edgeR(V3.4.6)[9]软件计算识别差异表达基因,即高温应答基因。
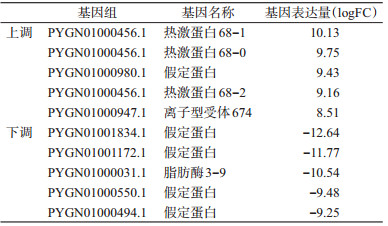
2 结果 2.1 测序与差异表达基因过滤测序数据后,分别得到46 436 578个对照组读序和47 289 134个处理组读序,读序平均长度分别为148.35和148.27 bp。将读序比对到德国小蠊基因组,对照组比对36 670 628个(约占78.97%)、高温处理组比对37 449 027个(约占79.19%)。对照组中,多比对位置和唯一比对位置的读序所占比例分别为5.14%和73.83%;高温处理组中,多个比对位置和唯一比对位置的读序所占比例分别为5.15%和74.04%。通过计算RPKM值获得基因相对表达量,表达差异>2倍且FDR(false discovery rate)值<0.05为显著差异表达基因。结果计算得到上调表达基因(即高温诱导表达基因)524个、下调表达基因(即高温抑制表达基因)525个。表 1中列举了高温应答程度最大的5个诱导表达基因和5个抑制表达基因。上调表达基因中有3个热激蛋白Hsp68-1、Hsp68-0和Hsp68-2。
|
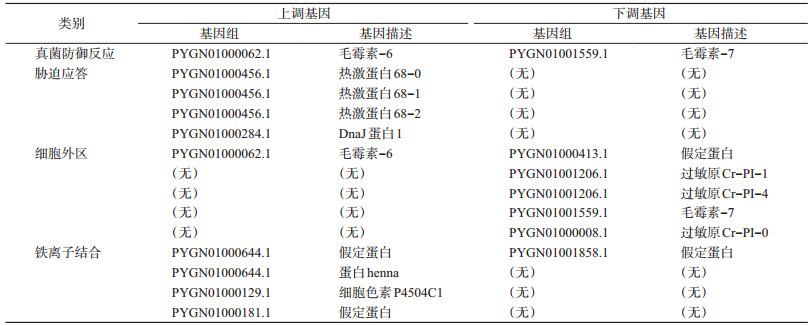
利用GO数据库进行功能富集分析,结果德国小蠊高温应答基因共分为14个小类。包括真菌防御反应、胁迫应答、苯丙氨酸4单加氧酶活性、L苯丙氨酸分解代谢、细胞外区、色氨酸5单加氧酶活性、芳香化酶活性、铁离子结合、氨基酸结合、膜结合细胞器、内质网膜、氧化还原酶活性、羧酸酯水解酶活性和信息素应答等。表 2中列举了真菌防御反应、胁迫应答、细胞外区和铁离子结合4个分类中所包含的高温应答基因。真菌防御反应类别中包含了1个上调表达的果蝇霉素基因6(Drs-6)和1个下调表达的果蝇霉素基因7(Drs-7),这些基因均属于抗菌肽类蛋白基因。胁迫应答类别中包含了4个上调表达的热激蛋白基因Hsp68-0、Hsp68-1、Hsp68-2和DnaJ(即Hsp40)。
|
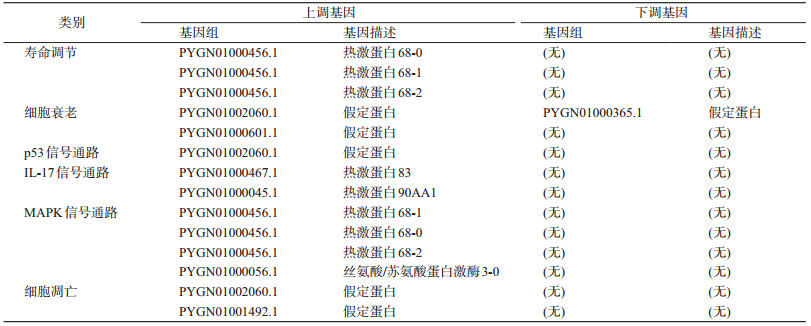
利用KEGG数据库进行代谢通路分析,结果发现甲流疾病应答、寿命调节、雌激素信号、有丝分裂、麻疹应答、NF-kappa B信号通路、抗原应答、细胞衰老、孕酮介导的卵母细胞成熟、脂肪酸合成、p53信号通路、IL-17信号通路、癌症转录失调、坏死、非洲锥虫病应答、植物病原互作、Th17细胞分化、MAPK(mitogen-activated protein kinase)信号通路、弓形虫病应答、前列腺癌、铂抗药性、糖胺聚糖生物合成硫酸肝素、同源重组、花生四烯酸代谢、内质网蛋白质加工、军团菌病应答、结节样受体信号、细胞凋亡、叶酸和Epstein-Barr病毒感染应答共30个代谢通路途径。表 3列举了寿命调节、细胞衰老、p53信号通路、IL-17信号通路、MAPK信号通路和细胞凋亡6个代谢通路中所包含的差异表达基因。
|
已有研究表明,环境温度变化能影响很多生物体内的生物化学调控及相应的基因表达变化[10]。2016年,Etges等[11]对果蝇(Drosophila melanogaster)在高温和低温环境下的基因表达进行了研究,结果发现3 294个与温度变化应答有关的基因。其中高温胁迫引起上调基因806个、下调基因1 045个。2018年,单艳敏[12]对沙葱萤叶甲幼虫温度胁迫应答基因进行识别,结果有1 265个基因与高温胁迫应答有关。本实验中,共识别得到德国小蠊高温应答上调基因524个、下调基因525个。短期40 ℃高温环境对德国小蠊无致命伤害,但是暴露在该温度下2 h可以使德国小蠊体内基因表达发生较强烈变化,说明德国小蠊能迅速感知外界温度变化并通过基因表达调控产生高温耐受机制。此外,本实验中不仅识别了很多德国小蠊高温应答上调表达基因,而且识别了近乎相同数量的下调表达基因,说明下调基因可能与上调基因一样发挥重要细胞保护作用。GO是基因或蛋白产物功能描述的分子生物学数据库,主要用于分析基因间的功能相似性。果蝇是重要的模式昆虫,研究发现果蝇高温应答基因主要集中在温度应答、阳离子结合、核糖体和糖酵解等[11]。类似的研究包括沙葱萤叶甲幼虫的高温响应机制,其高温应答基因主要在DNA复制和代谢、大分子代谢、初级代谢、分子功能催化活性、核酸结合、神经形成、ATP(adenosine triphosphate)结合、水解酶活性、微管相关复合体等功能类别[12]。本实验中,德国小蠊高温应答基因的功能富集主要在真菌防御反应、胁迫应答、苯丙氨酸4单加氧酶活性、L苯丙氨酸分解代谢、细胞外区、色氨酸5单加氧酶活性、芳香化酶活性、铁离子结合、氨基酸结合、膜结合细胞器、内质网膜、氧化还原酶活性、羧酸酯水解酶活性、信息素应答等,说明德国小蠊可能在这些方面应对高温胁迫。与果蝇和沙葱萤叶甲相比,德国小蠊的高温适应机制既有相同点,也有独特的基因调控过程。
3.2 高温应答基因热激蛋白(heat-shock protein genes)是一类普遍存在于原核生物和真核生物中,在进化上高度保守的蛋白质,在生物体或细胞受环境胁迫后大量合成,在昆虫抗逆境环境胁迫中起重要作用[13]。热激蛋白如Hsp68、Hsp70和Hsp90等通常作为分子伴侣保护细胞免受高温带来的损伤。本实验中,受高温环境影响,有6个热激蛋白Hsp68-1、Hsp68-0、Hsp68-2、Hsp83、Hsp90AA1和DnaJ蛋白(Hsp40)上调表达,说明德国小蠊与其他生物类似,通过热激蛋白保护受损细胞。锌指蛋白(zinc finger protein)基因在抗逆基因表达调控中起重要作用,利用其空间结构,与DNA分子相互作用进行转录调控[14]。德国小蠊受高温影响后,AN1- type zinc finger protein 2B(Zfand2b)、PR domain zinc finger protein 4(PRDM4)和Zinc finger protein 226(ZNF226)基因表达显著上调,Zinc finger protein 26(Zfp26_3)、Zinc finger protein 583(Znf583)和Zinc finger protein 726(ZNF726)基因表达显著下调,说明锌指蛋白也参与德国小蠊高温适应机制。细胞色素P450(Cytochrome P450)是数量庞大的基因家族,属于解毒代谢酶,广泛存在于动、植物和微生物中,参与有毒物质代谢和防御反应,也参与多种激素合成。本实验中,细胞色素P450 CYP4C1-1、CYP6K1-2和Cyp6a14-4为3个高温诱导上调表达基因,CYP4C1-0、CYP4C1-13、CYP4C1-9、CYP6J1-1、CYP6K1-3和CYP9E2-13为6个高温诱导下调表达基因,推测细胞色素P450基因参与德国小蠊高温适应。此外,例如高温诱导差异表达的18个参与嗅觉受体的离子型受体基因Ionotropic receptor 145、Ionotropic receptor 146和Ionotropic receptor 211等,以及高温诱导下调表达的2个脂肪酶基因Lipase 3-1和Lipase 3-9等,推测这些基因可能参与了德国小蠊应对高温胁迫的重要过程。
| [1] |
杜尧, 马春森, 赵清华, 等. 高温对昆虫影响的生理生化作用机理研究进展[J]. 生态学报, 2007, 27(4): 1565-1572. Du Y, Ma CS, Zhao QH, et al. Effects of heat stress on physiological and biochemical mechanisms of insects:a literature review[J]. Acta Ecol Sin, 2007, 27(4): 1565-1572. DOI:10.3321/j.issn:1000-0933.2007.04.037 |
| [2] |
王艳敏, 仵均祥, 万方浩. 昆虫对极端高低温胁迫的响应研究[J]. 环境昆虫学报, 2010, 32(2): 250-255. Wang YM, Wu JX, Wan FH. Response of insects to extreme high and low temperature stresses[J]. J Environ Entomol, 2010, 32(2): 250-255. DOI:10.3969/j.issn.1674-0858.2010.02.018 |
| [3] |
齐欣, 孙耘芹. 德国小蠊生物学特性及综合治理[J]. 中国媒介生物学及控制杂志, 2004, 15(1): 73-75. Qi X, Sun YQ. Biological characteristics and comprehensive control of Blattella germanica[J]. Chin J Vector Biol Control, 2004, 15(1): 73-75. DOI:10.3969/j.issn.1003-4692.2004.01.031 |
| [4] |
杜云静, 潘义, 冯丹, 等. 不同温度下的德国小蠊实验种群生命表[J]. 中国媒介生物学及控制杂志, 1991, 2(4): 241-244. Du YJ, Pan Y, Feng D, et al. The life diagram of the Blattella germanica in the experimental population under different temperature[J]. Chin J Vector Biol Control, 1991, 2(4): 241-244. |
| [5] |
霍京, 苗明升. 温度和光周期对德国小蠊生长发育、繁殖及生活史节律的影响[J]. 中国媒介生物学及控制杂志, 2012, 23(2): 114-117. Huo J, Miao MS. Effect of temperature and photoperiod on growth, reproduction and life-cycle rhythm of Blattella germanica[J]. Chin J Vector Biol Control, 2012, 23(2): 114-117. |
| [6] |
Harrison MC, Jongepier E, Robertson HM, et al. Hemimetabolous genomes reveal molecular basis of termite eusociality[J]. Nat Ecol Evol, 2018, 2(3): 557-566. DOI:10.1038/s41559-017-0459-1 |
| [7] |
Mortazavi A, Williams BA, McCue K, et al. Mapping and quantifying mammalian transcriptomes by RNA-Seq[J]. Nat Methods, 2008, 5(7): 621-628. DOI:10.1038/nmeth.1226 |
| [8] |
Love MI, Anders S, Huber W. Differential analysis of count data-the DESeq2 package[J]. Genome Biol, 2014, 15: 550. DOI:10.1186/s13059-014-0550-8 |
| [9] |
Robinson MD, McCarthy DJ, Smyth GK. edgeR:a Bioconductor package for differential expression analysis of digital gene expression data[J]. Bioinformatics, 2010, 26(1): 139-140. DOI:10.1093/bioinformatics/btp616 |
| [10] |
MacMillan HA, Knee JM, Dennis AB, et al. Cold acclimation wholly reorganizes the Drosophila melanogaster transcriptome and metabolome[J]. Sci Rep, 2016, 6: 28999. DOI:10.1038/srep28999 |
| [11] |
Etges WJ, De Oliveira CC, Rajpurohit S, et al. Effects of temperature on transcriptome and cuticular hydrocarbon expression in ecologically differentiated populations of desert Drosophila[J]. Ecol Evol, 2017, 7(2): 619-637. DOI:10.1002/ece3.2653 |
| [12] |
单艳敏.沙葱萤叶甲幼虫对温度胁迫响应的转录组学研究[D].呼和浩特: 内蒙古农业大学, 2018. Shan YM. Transcriptomal study on the Galeruca daurica larvae in response to thermal stress[D]. Huhehaote: Inner Mongolia Agricultural University, 2018. |
| [13] |
张天浩, 张仙红. 昆虫热激蛋白的研究进展[J]. 山西农业大学学报:自然科学版, 2019, 39(1): 35-40. Zhang TH, Zhang XH. Research progress of heat shock protein in insect[J]. J Shanxi Agric Univ (Nat Sci Ed), 2019, 39(1): 35-40. DOI:10.13842/j.cnki.issn1671-8151.201806017 |
| [14] |
Nekludova L, Pabo CO. Distinctive DNA conformation with enlarged major groove is found in Zn-finger-DNA and other protein-DNA complexes[J]. Proc Natl Acad Sci USA, 1994, 91(15): 6948-6952. DOI:10.1073/pnas.91.15.6948 |
 2020, Vol. 31
2020, Vol. 31


