扩展功能
文章信息
- 吴海莲, 吴海生, 何建, 杨晓艳, 辛有全, 李存香, 靳娟, 李胜, 张琪, 代瑞霞, 祁芝珍
- WU Hai-lian, WU Hai-sheng, HE Jian, YANG Xiao-yan, XIN You-quan, LI Cun-xiang, JIN Juan, LI Sheng, ZHANG Qi, DAI Rui-xia, QI Zhi-zhen
- 青海省果洛藏族自治州鼠疫耶尔森菌病原学分析及耐药相关基因检测
- Etiological analysis and determination of antibiotic resistance-related genes of Yersinia pestis in Guoluo Tibetan autonomous prefecture, Qinghai province, China
- 中国媒介生物学及控制杂志, 2019, 30(2): 167-171
- Chin J Vector Biol & Control, 2019, 30(2): 167-171
- 10.11853/j.issn.1003.8280.2019.02.012
-
文章历史
- 收稿日期: 2018-10-17
- 网络出版时间: 2019-03-01 08:56
果洛藏族自治州(果洛州)地处青藏高原腹地,黄河源头,位于青海省的东南部。现辖玛沁、玛多、甘德、达日、班玛和久治6县,总面积7.6万km2,总人口约12.9万人,其中藏族11.2万人。果洛州平均海拔在4 000 m以上,具有典型的高原大陆性气候特征。分别在1978和1979年,玛多和玛沁县用细菌学方法被判定为鼠疫自然疫源县,之后久治、达日和甘德县用血清学方法也被证实为鼠疫自然疫源县,疫源地面积达9 396.0 km2,属于青藏高原喜马拉雅旱獭鼠疫自然疫源地[1]。1978-1985年间果洛州鼠疫流行呈活跃态势,其中人间鼠疫发生9起,发病22例,死亡12例[1]。尽管在1986-2016年果洛州未检出鼠疫菌,但仍需严防鼠疫的复燃和远距离传播,防控形势依然严峻。
抗生素的应用使人类对鼠疫的治疗有了根本性进展,鼠疫患者在获得及时治疗的情况下死亡率大大降低[2-3]。以链霉素为代表的传统抗生素在治疗鼠疫方面起着举足轻重的作用,但越来越多的事实表明,耐药率不断上升的问题正日益引起人们的重视[4],在马达加斯加报道了1株对多种抗生素(包括用于预防和治疗鼠疫的链霉素、磺胺类等)具有耐药性的鼠疫菌[5],为全世界敲响了警钟。全球范围内革兰阴性多耐药菌株在持续增加[4],因此,鼠疫菌的耐药也是一个不容忽视的问题。
我国迄今为止尚无耐药鼠疫菌株的报道,本研究对1978-2016年分离自果洛州的13株鼠疫菌进行了病原学分析以及耐药相关基因检测,可为该地区制订科学有效的鼠疫防治对策提供依据,现将结果报道如下。
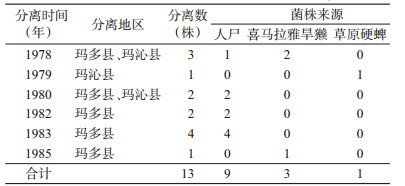
1 材料与方法 1.1 材料 1.1.1 菌株选取1978-2016年在果洛州不同宿主和媒介昆虫体内分离的13株鼠疫菌株作为实验对象,其中,分离自喜马拉雅旱獭(Marmota himalayana)3株,分离自人尸9株,分离自草原硬蜱(Ixodes crenulatus)1株,均由青海省国家鼠疫菌种保藏中心提供。耐药基因strA、strB、tem、ctx-m、sul1、sul2的阳性模板DNA(A1234)由中国疾病预防控制中心(CDC)传染病预防控制所馈赠。13株鼠疫菌的宿主、媒介及地区分布见表 1。
实验动物为标准化昆明系小白鼠,体质量控制在18~20 g,实验动物由青海省地方病预防控制所(青海地方病所)实验动物中心提供。实验动物使用许可证号:SYXK(青)2016-0001,本实验经青海地方病所实验动物伦理委员会批准符合实验动物伦理要求。
1.1.3 主要试剂及培养基Taq DNA聚合酶、dNTPs、DL2000、琼脂糖购自北京欣经科生物技术有限公司。培养基由青海地方病所培养基室提供。
1.1.4 引物参照美国国立生物信息中心(NCBI)公布的耐氨基糖苷类链霉素strA、strB基因、耐β-内酰胺类抗菌药物tem、ctx-m基因,耐磺胺类药物sul1、sul2基因序列,利用Primer 5.0进行引物设计,引物序列见表 2。引物由生工生物工程(上海)股份有限公司合成。

|
超微量核酸蛋白测定仪购自美国GE公司,型号NaNovue;PCR扩增仪购自德国Eppendorf公司,型号Mastercycler proS;凝胶成像仪购自英国Syngene公司,型号GBOX-F3;多用电泳仪购自北京六一仪器厂,型号DYY-12。
1.2 方法 1.2.1 生化及糖醇类酵解试验被试菌株于琼脂培养基28 ℃培养24 h后,用1%蛋白胨水制备成约2×1013个菌/ml的菌悬液,分别接种于阿胶糖、鼠李糖、麦芽糖、蜜二糖、甘油、脱氮培养基中,混匀后放置37 ℃温箱培养,连续观察7 d,然后在21 ℃的温度下再连续观察7 d,记录发酵情况。
1.2.2 毒力因子检测用抗鼠疫血清培养基检测荚膜抗原(F1),用鼠疫杆菌素Ⅰ(PstⅠ)培养基检测PstⅠ,用草酸镁培养基检测毒力抗原因子(VW);用氯化血红素培养基检测色素沉着因子(Pgm)。
生化及糖醇类酵解试验和毒力因子检测的结果判定均以鼠疫强毒标准菌株141和假结核菌PTB5分别作为阳性和阴性对照。结果判定方法请参见文献[6]。
1.2.3 毒力测定被试菌株于琼脂培养基37 ℃培养24 h后,用灭菌生理盐水制备成菌悬液,用标准比浊管法比浊后稀释为2×101、2×102、2×103、2×104、2×105、2×106、2×107个菌/ml的菌悬液,分别取0.5 ml皮下注射小白鼠鼠鼷部,5只为1组,共7组,分笼饲养14 d。动物死亡后解剖取淋巴、肝、脾、肺、心组织进行细菌培养,以分离出鼠疫菌为特异性死亡,并计算半数致死量(LD50),毒力测定方法和判定标准参见文献[6]。
1.2.4 质粒提取及分析细菌质粒提取方法参见文献[7],质粒DNA相对分子质量(Mr)的测定采用标准质粒对照法[7]。
1.2.5 鼠疫菌DNA的提取细菌DNA提取按照常规的十二烷基硫酸钠裂解,酚-氯仿抽提法进行[8]。用超微量核酸蛋白测定仪对DNA进行含量测定,DNA终浓度稀释至2 ng/μl备用。
1.2.6 差异区段(different region,DFR)分型利用23对DFR(DFR01~DFR23)分型引物和质粒验证引物(pMT1),检索包含909株鼠疫菌自然分离株的DFR分型数据库[8],按照文献[9]的方法,以13株鼠疫菌的DNA为模板进行PCR扩增,82009和620024菌株DNA的等量混合物作为阳性对照,以去离子水作为阴性对照,引物序列及结果分析参见文献[8]。根据DFR分型结果,确定13株鼠疫菌的基因组型。
1.2.7 耐药基因检测以鼠疫菌DNA为模板逐一进行耐药基因扩增,引物序列见表 2。PCR反应体系:10×buffer 2.5 μl,10 mmol/L dNTP 0.2 μl,5 U/μl Taq DNA聚合酶0.5 μl,正、反向引物(2 μmol/L)各0.5 μl,模板DNA(2 ng/μl)5.0 μl,用去离子水补足至25.0 μl。PCR扩增条件:95 ℃预变性4 min;95 ℃变性40 s,56 ℃退火40 s,72 ℃延伸40 s,30个循环;72 ℃终延伸4 min。因tem引物的产物长度较长,延伸时间为70 s,其他条件不变。电泳:取PCR产物7.5 μl,2﹪琼脂糖凝胶电泳,电压为80~100 V,电泳时间为15~30 min,利用凝胶成像系统拍照并记录结果。
2 结果 2.1 试验菌株生化特性13株鼠疫菌均有分解阿胶糖和甘油的能力,脱氮反应也均为阳性;对鼠李糖和蜜二糖均不能酵解;9株能酵解麦芽糖,4株不能。13株鼠疫菌的生物型均为古典型,其中9株的生态型为青藏高原型,4株为祁连山型,见表 3。
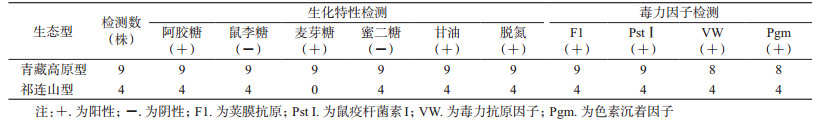
|
被试菌株均能产生鼠疫菌F1和PstⅠ;VW阳性和Pgm阳性的菌株均占92.31%(12/13);4个毒力因子都具备的菌株占84.62%(11/13),见表 3。
2.3 菌株毒力13株鼠疫菌的毒力测定结果,11株菌的LD50为(1~99)个菌/ml,2株菌的LD50为(100~999)个菌/ml,按鼠疫菌株毒力等级分类[6],以上13株均属于强毒株。
2.4 菌株的质粒种类在被鉴定的13株鼠疫菌中,共携带有4种质粒,Mr分别为6×106、45×106、52×106和65×106。4种质粒组成2种质粒谱,6×106、45×106、52×106和6×106、45×106、65×106。
2.5 基因分型结果对13株鼠疫菌进行DFR分型,共发现有5型7株、8型4株、36型和01b各有1株,均为青藏高原喜马拉雅旱獭鼠疫自然疫源地所有的基因组型,其中5型和8型为主要基因组型,36型和01b型为次要基因组型[9],见表 4、图 1。

|

|
| 注:M. Marker;1~23.鼠疫菌23个差异片段(DFR01~DFR23);pMT1.质粒验证引物 图 1 青海省果洛州13株鼠疫菌基因组分型PCR产物电泳结果 Figure 1 Electrophoretogram of PCR amplification for genotyping of the 13 Yersinia pestis strains in Guoluo prefecture, Qinghai province |
| |
13株鼠疫菌DNA均未在目的基因处扩增出条带,未发现具有耐链霉素strA、strB基因、耐磺胺类药物sul1、sul2基因及耐β-内酰胺类抗菌药物tem、ctx-m基因的菌株。
3 讨论1977年果洛州玛多县扎陵湖乡发生人间鼠疫(由剥食藏系绵羊感染),相关部门进一步加强了该地的鼠疫监测工作,果洛州被证实属于青藏高原喜马拉雅旱獭鼠疫自然疫源地。之后经过长期查源工作,新的鼠疫疫源地和自然染疫动物被陆续发现,果洛地区鼠疫疫源地面积不断增大,疫点分布多,旱獭密度较高,旱獭的主要体外寄生蚤—斧形盖蚤(Callopsylla dolabris)和谢氏山蚤(Oropsylla silantiewi),不仅能自然感染鼠疫,且有较高的媒介效能,充分说明果洛州境内有暴发鼠疫的潜在风险。
本研究中的13株鼠疫菌分别属于青藏高原型和祁连山型2个生态型;基因组型为青藏高原喜马拉雅旱獭鼠疫自然疫源地所有的基因组型;2株菌分别缺失了VW抗原和Pgm位点,但该2株的基因组型均为青藏高原喜马拉雅旱獭鼠疫自然疫源地所有的主要基因组型(8型),可能由表型特征分型法自身分辨率低或稳定性不足所致;13株菌均为强毒鼠疫菌。上述结果表明该地区分离的鼠疫菌株具备青藏高原喜马拉雅旱獭鼠疫自然疫源地分离菌株的特点[9-13]。
本研究检测结果显示,果洛州1978-2016年分离的13株鼠疫菌中尚未发现耐链霉素、β-内酰胺类、磺胺类抗菌药物相关基因的菌株。但在1995年,Galimand等[14]首次报道了1株多重耐药鼠疫菌株,此菌株含有自转移质粒(pIP1202),带有7种耐药基因,对链霉素、氯霉素、氨苄西林、壮观霉素、卡那霉素、四环素和磺胺类药物具有高抗性。2001年Guiyoule等[15]在马达加斯加报道了1株质粒介导的对链霉素具有高抗性的鼠疫菌株(菌株名为16/95),该菌株携带自转移质粒(pIP1203),该质粒仅带有strA、strB耐药基因,能高频结合到其他鼠疫菌,提示自然条件下携带耐药基因的质粒可能会整合到鼠疫菌基因组,鼠疫菌很有可能向具有多重耐药性方向发展。因此,应该将鼠疫菌耐药基因的检测纳入到鼠疫常规监测工作中,以便为鼠疫患者提供及时有效的救治方案,同时也为制订精细化的鼠疫防控策略提供科学依据。
在20世纪七八十年代,青海省各州县交通比较闭塞,医疗条件相对差,加上青藏高原高寒的恶劣环境,鼠疫患者往往得不到及时诊断和救治,隔离措施采取不及时,首发病例死亡率较高,感染率也高。通过科学监测,灭獭拔源,有效控制鼠类、蚤类密度及其数量,开展鼠防知识宣传教育等多种防制措施[16],在之后的1986-2016年间,该地区未检出鼠疫菌,但随着大武机场的通航,果洛州特有的旅游项目不断被开发,鼠疫远距离传播的危险性也可能会增加,周边疫源地向果洛州地区输入鼠疫疫情现象也应引起高度重视[17-18],要严防该地区鼠疫复燃。
| [1] |
李存香, 靳娟, 吴海莲, 等. 1978-2014年青海省果洛州鼠疫流行病学分析[J]. 中国病原生物学杂志, 2017, 12(7): 651-653. DOI:10.13350/j.cjpb.170714 |
| [2] |
张贵, 张贵军, 刘振才. 抗生素治疗鼠疫的现状及进展[J]. 中国地方病学杂志, 2006, 25(6): 729-730. DOI:10.3760/cma.j.issn.1000-4955.2006.06.056 |
| [3] |
唐新元, 王梅, 田富彰, 等. 链霉素单独和联合环丙沙星治疗鼠疫的疗效比较[J]. 中国媒介生物学及控制杂志, 2015, 26(3): 317-319. DOI:10.11853/j.issn.1003.4692.2015.03.026 |
| [4] |
Galimand M, Carniel E, Courvalin P. Resistance of Yersinia pestis to antimicrobial agents[J]. Antimicrob Agents Chemother, 2006, 50(10): 3233-3236. DOI:10.1128/AAC.00306-06 |
| [5] |
Welch TJ, Fricke WF, McDermott PF, et al. Multiple antimicrobial resistance in plague:an emerging public health risk[J]. PLoS One, 2007, 2(3): e309. DOI:10.1371/journal.pone.0000309 |
| [6] |
祁芝珍, 罗志丹巴, 段勇军, 等. 四川省德格县2株疑似喜马拉雅旱獭鼠疫菌株的鉴定[J]. 中国地方病学杂志, 2009, 28(1): 48-53. DOI:10.3760/cma.j.issn.1000-4955.2009.01.013 |
| [7] |
李敏, 于晓涛, 金丽霞, 等. 我国鼠疫菌大质粒的特性及其流行病学意义[J]. 中国地方病学杂志, 1994, 13(4): 223-225. |
| [8] |
Li YJ, Dai EH, Cui YJ, et al. Different region analysis for genotyping Yersinia pestis isolates from China[J]. PLoS One, 2008, 3(5): e2166. DOI:10.1371/journal.pone.0002166 |
| [9] |
杨晓艳, 魏柏青, 靳娟, 等. 中国鼠疫耶尔森菌差异区段分型及其地理分布特征[J]. 中华流行病学杂志, 2014, 35(8): 943-948. DOI:10.3760/cma.j.issn.0254-6450.2014.08.015 |
| [10] |
祁芝珍, 李超, 王丽, 等. 青海省三江源地区鼠疫病原学分析[J]. 中华流行病学杂志, 2009, 30(1): 55-57. DOI:10.3760/cma.j.issn.0254-6450.2009.01.016 |
| [11] |
李梅玉, 王国钧, 于守鸿, 等. 原发性肺鼠疫肺水肿肺大泡1例报告[J]. 中国地方病学杂志, 2011, 30(3): 322. DOI:10.3760/cma.j.issn.1000-4955.2011.03.025 |
| [12] |
崔百忠. 2001-2011年青海省人间鼠疫流行病学分析[J]. 中华地方病学杂志, 2013, 32(5): 520-522. DOI:10.3760/cma.j.issn.2095-4255.2013.05.013 |
| [13] |
戴瑞霞, 杨永海, 于守鸿, 等. 2004年青海省人间鼠疫菌生物学特性及流行病学分析[J]. 中国地方病学杂志, 2006, 25(2): 216. DOI:10.3760/cma.j.issn.1000-4955.2006.02.040 |
| [14] |
Galimand M, Guiyoule A, Gerbaud G, et al. Multidrug resistance in Yersinia pestis mediated by a transferable plasmid[J]. N Engl J Med, 1997, 337(10): 677-680. DOI:10.1056/NEJM199709043371004 |
| [15] |
Guiyoule A, Gerbaud G, Buchrieser C, et al. Transferable plasmid-mediated resistance to streptomycin in a clinical isolate of Yersinia pestis[J]. Emerg Infect Dis, 2001, 7(1): 43-48. DOI:10.3201/eid0701.700043 |
| [16] |
王梅, 唐新元, 王祖郧, 等. 青海省鼠疫疫源地分布特征的研究[J]. 中国媒介生物学及控制杂志, 2015, 26(2): 194-195. DOI:10.11853/j.issn.1003.4692.2015.02.023 |
| [17] |
赵秋芳, 尹家祥. 我国鼠疫流行形势分析及其防治策略探讨[J]. 中国热带医学, 2016, 16(7): 733-735. DOI:10.13604/j.cnki.46-1064/r.2016.07.29 |
| [18] |
陈洪舰, 王虎, 王祖郧. 青海省青藏铁路沿线鼠疫防治思考[J]. 中国媒介生物学及控制杂志, 2010, 21(2): 150-152. |
 2019, Vol. 30
2019, Vol. 30