扩展功能
文章信息
- 杨仁东, 房元圣, 张荣娜, 梁作如, 戚晓鹏
- YANG Ren-dong, FANG Yuan-sheng, ZHANG Rong-na, LIANG Zuo-ru, QI Xiao-peng
- 中国疟疾防控技术能力调查
- An investigation of technical capabilities for malaria control in China
- 中国媒介生物学及控制杂志, 2023, 34(1): 94-100
- Chin J Vector Biol & Control, 2023, 34(1): 94-100
- 10.11853/j.issn.1003.8280.2023.01.017
-
文章历史
- 收稿日期: 2022-08-20
2 中国疾病预防控制中心全球公共卫生中心, 北京 102206;
3 珠海市疾病预防控制中心应急管理办公室, 广东 珠海 519060
2 Center for Global Public Health, Chinese Center for Disease Control and Prevention, Beijing 102206, China;
3 Emergency Management Office, Zhuhai Center for Disease Control and Prevention, Zhuhai, Guangdong 519060, China
近年来,我国以共建“一带一路”倡议积极践行“人类命运共同体”理念[1],对外医疗援助不断增加,大国形象和文化软实力得到进一步提升[2-3]。在与疟疾斗争的70多年期间,我国积累了大量的防控技术和经验,使得疟疾防控成为我国对外医疗援助领域中的重要组成部分[4]。2021年6月30日世界卫生组织(WHO)宣布中国消除疟疾。在此时间节点,本研究对我国各类疟疾防控机构的疟疾防控技术能力进行梳理和评价,以期有助于消除疟疾后时代防控工作的延续,同时为其他传染病的消除提供借鉴,为我国对外医疗援助事业助力。
1 材料与方法参照彭张林[5]推荐的“O-C-W-I-S-D”六大科学性原则,针对各大疟疾防控机构筛选出关键性技术能力指标,采用定量和定性相结合的方式进行梳理和评价。具体包括以下内容。
1.1 问卷调查自制2套调查问卷,调查省级疾病预防控制中心(疾控中心)和寄生虫病防治研究所(寄研所)。一套调查24个疟疾流行省(即有疟疾再传播风险省份)[6-7]的疟疾防控能力,即除去北京市、天津市、黑龙江省、吉林省、宁夏回族自治区、青海省、内蒙古自治区、香港特别行政区(港)、澳门特别行政区(澳)、台湾省(台)等10个省级行政区(为了叙述方便,以下统称为省)之外,调查内容包括疟疾防控人员基本情况、关键岗位(实验室和流行病学调查)人数、关键技术能力(比如镜检)具备情况、课题项目获批情况。另一套调查除港、澳、台之外的大陆31个省份的蚊媒监测能力,调查内容包括蚊媒监测点数量、实验室和养蚊室数量、工作人员数量、常规监测和深入研究开展情况。
1.2 监测数据分析从中国疾病预防控制信息系统中导出2017年1月-2021年5月期间报告的疟疾病例个案数据,分析不同类型的医疗卫生机构报告疟疾病例种类、病例数等指标。
1.3 文献情报资料研究查阅相关机构官网,搜集通过WHO预认证(PQ)、国家药品监督管理局(国家药监局)批准注册的抗疟产品及对应的企业名单,并搜集企业的生产研发情况。查阅文献,对全国疟疾诊断参比实验室网络、全国疟疾诊断网络、疫苗与药物研发等进行梳理、论述。
1.4 专家咨询和访谈采用目标抽样和滚雪球抽样相结合的方式,选取专家开展咨询和访谈,收集以上3种方法不宜获取的资料,主要用于WHO、海关、基金会、民间社会组织、行业团体组织等其他机构或组织的调查。
2 结果 2.1 疾控中心和寄研所 2.1.1 全国疟疾诊断参比实验室网络国家以疟疾传播潜在风险大的重点省份为主,建立省级疟疾诊断参比实验室,由中国疾控中心寄生虫病预防控制所每2年对各省疟疾诊断参比实验室的检验人员进行培训,并组织参加WHO镜检技能评估[7-8]。截止2019年底,全国24个有再传播风险省份全部建立了省级疟疾诊断参比实验室。全国有30个省份共47人获得WHO镜检技能评估证书,其中获得一级证书19人、二级15人、三级7人、四级6人[8]。
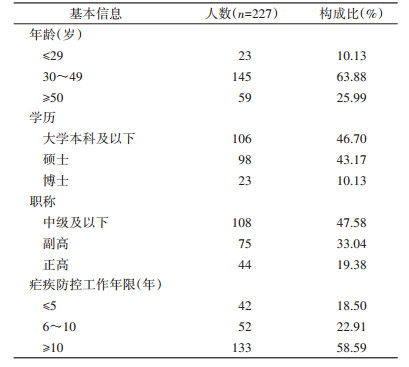
2.1.2 疟疾防控人员基本情况24个有再传播风险省份的省级机构共有从事疟疾防控工作人员227人,平均9.45人/省。年龄以30~49岁为主,占63.88%。学历水平以大学本科及以下和硕士居多,分别占46.70%和43.17%。职称方面以高级职称偏多,正、副高级职称合计占52.42%。从事疟疾防控相关工作10年及以上的人数超过一半,占58.59%。见表 1。
|
24个省级机构共有从事疟疾相关实验室工作人员132人,平均5.50人/省;共有从事疟疾流行病学调查工作人员105人,平均4.38人/省;少部分人员同时开展这两项工作。24个省份均具备疟原虫血涂片镜检能力和核酸检测能力,具备能力的技术人员分别有95和86人,平均有3.95和3.58人/省。其中16个省份(占66.67%)具备疟原虫基因测序或生物信息分析能力,共有技术人员41人,平均1.71人/省。只有8个省份(占33.33%)具备疟原虫培养及体外药敏能力,共有技术人员16人,平均0.67人/省。24个省份都有疟疾相关实验室,共有145间,平均6.04间/省;共有实验室面积6 122.60 m2,中位数面积133.30 m2,平均42.22 m2/间。
2.1.4 疟疾相关课题项目2011年以来,24个省级机构共有16个获批援外项目、省部级及以上课题项目,共获批56项,包括援外4项、国家级19项、省部级33项。研究范围覆盖全部4种人类疟疾,其中恶性疟11项、间日疟4项、卵形疟3项、三日疟1项。研究地域覆盖全球三大洲,其中亚洲(与云南省接壤境外地区)4项、非洲(坦桑尼亚、刚果)2项、大洋洲(巴布亚新几内亚)2项。研究领域主要涉及输入性疟疾(12项)、传播风险评估与模型构建(11项)、青蒿素抗药性或杀虫剂抗性(10项)、消除疟疾(9项)、分子机制与功能研究(9项)、实验室检测与病例诊断(8项)、基因多态性或关联性研究(6项)、按蚊等传播媒介(5项)。
2.1.5 蚊媒监测国家在全国各地设置了国家级病媒生物监测点共166个,平均5.35个/省。除个别省份外,30个省份都开展了蚊媒监测工作,其中28个省级机构设有蚊媒实验室,共65间,平均2.09间/省。26个省级机构设有养蚊室,共43间,平均1.38间/省。31个省级机构共有从事蚊媒监测工作人员178人,平均5.74人/省。83.87%(26/31)的省份开展了蚊媒密度监测、蚊媒种群和生态学研究等常规监测工作。部分省份开展深入研究工作,其中87.09%(27/31)的省份开展了杀虫剂种类和抗性研究,70.96%(22/31)的省份开展了蚊媒习性和宿主偏好研究,38.71%(12/31)的省份开展了蚊媒基因测序研究。
2.2 医疗机构 2.2.1 全国疟疾诊断网络和重症疟疾救治网络国家建立了由省、市、县的各级综合医院、部分民营医院和乡镇医院(社区卫生服务中心)等具备疟疾诊断能力的医疗机构组成的全国疟疾诊断网络,承担疟原虫的实验室检测和诊断工作[8]。目前,24个有再传播风险的省份均依法指定至少1所三级甲等综合医院或传染病专科医院承担重症疟疾治疗任务,并对其他医疗机构开展重症疟疾治疗进行指导[9]。
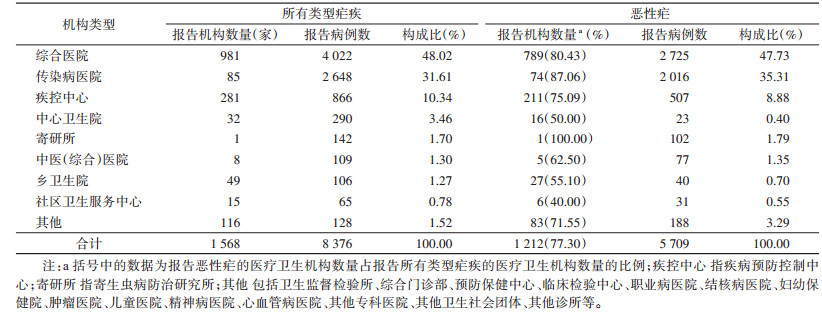
2.2.2 疟疾诊疗能力疟疾(尤其是恶性疟)的报告病例数可以间接反映医疗卫生机构的诊疗能力。近5年来,全国共1 568家医疗卫生机构报告疟疾病例,累计报告8 376例;其中1 212家(占77.30%)曾报告过恶性疟病例,共报告5 709例。无论是恶性疟还是所有类型疟疾,都主要由综合医院和传染病医院报告,两者报告病例数占总病例数的80.00%左右。见表 2。
|
截止2021年6月,通过国家药监局批准注册的产品共有89种,来自48家企业,具体包括:磷酸氯喹(26家,35种)、蒿甲醚(7家,14种)、青蒿琥酯(6家,11种)、磷酸伯氨喹(7家,7种)、磷酸哌喹(7家,7种)、复方药物(6家,7种)、青蒿琥酯阿莫地喹(1家,3种)、双氢青蒿素哌喹片(1家,2种)、青蒿素哌喹(1家,2种)和磷酸咯萘啶(1家,1种)。
截止2021年6月,我国共有5家企业的13种产品申请了WHO疟疾快速诊断试剂(RDT)评估,但还没有产品通过评估。通过WHO原料药预认证的产品55种,来自26家企业。通过WHO制剂药预认证的企业只有1家,共有产品24种。通过WHO疟疾病媒控制-长效防虫蚊帐预认证的企业共3家。
据不完全统计,目前化学农药制剂生产企业主要有6家,其中1家获得WHO室内滞留喷洒预认证;生物农药生产企业主要有3家;生物杀虫剂(苏云金芽孢杆菌和球形芽孢杆菌等)生产企业主要有4家。
2.4 高校和科研机构中国中医科学院中药研究所的屠呦呦教授及其团队在抗疟药领域做出了重大贡献,其提取的青蒿素是WHO唯一认可的抗疟特效药,也是中国第1个符合国际标准并拥有自主知识产权和国际专利的原创性药物[10]。2003年,我国创制的青蒿素、蒿甲醚、青蒿琥酯、双氢青蒿素的原料药及其制剂被列入WHO《国际药典》第3版,青蒿素类药物单一用药和以青蒿素为基础的复合治疗逐步推广应用于全球主要疟区[11]。
我国多个高校一直积极开展疟疾疫苗研发工作,PfCP-2.9抗原获批进入临床试验,PfCP-2.9和PfCSP-2组成的多价多期疟疾疫苗,以及以疟原虫特异性B细胞表位为基础构建的新型多表位人工抗原疟疾疫苗均已进入临床前研究。此外,在疟疾DNA疫苗和重组蛋白疫苗研究方面也取得不同程度的进展[12]。
2.5 海关海关构建“境外、口岸、境内”三道防线助力消除疟疾,其口岸媒介监测也被纳入中国媒介监测网络。截止2020年底,中国海关在口岸设立蚊媒生物监测点数量达到1 091个[13]。2010-2019年共31个海关口岸截获或检测到疟疾传播媒介按蚊(Anopheles)11种。国内42个隶属海关实验室积极参加国家认监委、原卫生部临床检验中心、国际旅行卫生保健中心、疾控中心等组织的各项能力验证或室间比对,其中北京、上海、杭州、福州等4个海关口岸通过了美国病理家学会组织的疟原虫快速检测能力验证[8]。
2.6 其他机构或组织WHO、基金会、民间社会组织、行业团体组织等机构或组织在我国消除疟疾历程中也发挥着难以替代的作用。
WHO与中国疾控中心寄研所、江苏省寄防所、云南省寄研所等3个机构建立合作中心,开展媒介生物监测与管理、消除疟疾研究与培训、新型疟疾防治工具研发与诊断治疗培训等工作。选派专家参与多个省、市的消除疟疾评估,为我国培养符合国际标准的镜检技术人员,邀请中国专家参加国际会议学习先进经验和分享中国经验[8]。
全球基金在2003-2012年期间为我国提供了第1、5、6、10轮和国家策略全球基金疟疾项目,先后在10省47县(第1轮,2003-2008年)、6省121县(第5轮,2006-2010年)、1省12县(第6轮,2006-2010年)、20省762县(国家策略项目,2010-2012年)实施,资助中部及边境等重点疟疾流行区1.16亿美元经费[14-15]。比尔及梅琳达盖茨基金支持中国抗疟产品申请WHO预认证,支持提升抗疟产品技术及质量标准和管理水平,加强中国疟疾防控的国际交流[16]。
英国健康扶贫行动于1993年进入中国,与云南等10个省份开展合作,开展中国疟疾控制和消除、艾滋病等传染病健康促进项目。1994年进入缅甸,帮助完善和落实中缅边境地区疟疾防控工作[17]。该组织是中国全球基金疟疾项目第5、6和10轮项目的第二执行机构[17]。
中华预防医学会于2016-2019年期间组织专家参与多个省、市的消除疟疾评估;其寄生虫分会举办学术研讨会,培养青年专家队伍。中国医药保健品进出口商会对医药保健品贸易与投资及相关活动进行协调、规范,维护对外贸易秩序,为促进医药保健品贸易与投资健康发展做出重大贡献[8]。
3 讨论在与疟疾斗争的70多年间,我国建立了一套符合国情的防控机制和工作网络,在全国范围内建立了疟疾诊断、诊断参比实验室、重症疟疾救治、病媒生物监测等多套工作网络,构建了疾控、医院、海关、企业、高校、非政府组织等多个机构或组织共同参与的联防联控机制,这些工作机制对于其他传染病的防控和消除具有很好的借鉴意义[18-20]。同时,我国在多个关键技术岗位积累了专业水准较高的防控队伍,例如,30个省份均有人员获得WHO镜检技能评估证书,防控队伍中的高级职称、工作10年及以上的人数占比均超过一半,24个有再传播风险省份都具备疟原虫血涂片镜检和核酸检测能力,且其中2/3的省份具备疟原虫基因测序或生物信息分析能力,这些经验丰富、专业水平过硬的人员,在国内可以通过“传、帮、带”在疟疾消除后时代发挥作用,在国外可以通过对外医疗援助发挥专业特长[21-22]。此外,我国在关键研发领域也投入了较大成本,取得了突破性成绩,例如,2/3的有再传播风险的省份获批重要课题项目,研究的范围全、地域广、领域多;研制的青蒿素及其衍生物成为WHO唯一认可的抗疟特效药,通过WHO预认证的抗疟产品覆盖原料药、制剂药、长效防虫蚊帐、室内滞留喷洒等4大类,这些研究成果和产品对于我国防范疟疾再传播,对外系统性输出防控经验、技术和成果,将防控关口往外前移具有重要的战略意义[17, 21-23]。
不过,我国在疟疾防控领域仍存在一些短板。例如,防控队伍中,低年龄组占比仅为10.13%,工作5年及以下人数占比不足20.00%,只有8个省份具备疟原虫培养及体外药敏实验能力,以上提示人员可能出现断层、部分技术能力可能在下降,且有可能进一步加剧[23-27]。因此,从国家生物安全的战略层面考虑,建立疟疾消除后时代的能力维持机制,储备战略性防控人才很有必要,建立长期的对外医疗援助合作机制是值得积极探索的方向[17, 20, 22-27]。
另外,我国开展疫苗研发20多年,仍面临机制研究不深、合适的动物评价模型和佐剂缺乏等诸多困难,至今尚无成熟产品推入市场[12]。通过WHO预认证的国产抗疟产品整体占比较低,通过制剂药和杀虫剂预认证的只有1家企业,作为未来疟疾诊断发展方向的RDT产品[28],目前还没有通过预认证的中国产品。我国在境外正式注册的疟疾相关非政府组织数量极少,无法像全球基金、英国扶贫行动等组织一样产生影响力[18]。建议有关部门积极合作,与WHO等国际机构开展协商、对话,帮助企业通过预认证[29];积极与疟疾流行国家和地区开展对话,组织利益相关方搭建交流和信息共享平台,帮助企业“走出去”[22]。同时,通过政府引导,促进非政府组织在境外展开民间外交活动,持续性获得资助,发挥优势互补作用[18, 30]。
利益冲突 无
| [1] |
赵可金. 通向人类命运共同体的"一带一路"[J]. 当代世界, 2016(6): 9-13. Zhao KJ. The Belt and Road: A path to community of shared future for mankind[J]. Contemp World, 2016(6): 9-13. DOI:10.3969/j.issn.1006-4206.2016.06.003 |
| [2] |
梁晓诗, 李娜玲. "一带一路"倡议背景下我国援外医疗工作现状及对策研究: 以广东省援外医疗工作为例[J]. 卫生软科学, 2021, 35(7): 31-34. Liang XS, Li NL. Study on status quo and countermeasures of China's foreign medical aid under the background of "the Belt and Road Initiative": Taking Guangdong's foreign aid medical work as an example[J]. Soft Sci Health, 2021, 35(7): 31-34. DOI:10.3969/j.issn.1003-2800.2021.07.007 |
| [3] |
刘再起, 王曼莉. "一带一路": 中国软实力的"西游"之路[J]. 江汉论坛, 2016(6): 48-52. Liu ZQ, Wang ML. "The Belt and Road": The "journey to the west" of China's soft power[J]. Jianghan Trib, 2016(6): 48-52. DOI:10.3969/j.issn.1003-854X.2016.06.007 |
| [4] |
陈夏茹. 新世纪中国对非医疗援助研究[D]. 济南: 山东师范大学, 2018. Chen XR. The study on China's medical aid to African countries in new century[D]. Ji'nan: Shandong Normal University, 2018. (in Chinese) |
| [5] |
彭张林. 综合评价过程中的相关问题及方法研究[D]. 合肥: 合肥工业大学, 2015. Peng ZL. Research on some specific problems and the solution methods of comprehensive evaluation[D]. Hefei: Hefei University of Technology, 2015. (in Chinese) |
| [6] |
卫生部. 关于印发《中国消除疟疾行动计划(2010-2020)》的通知[EB/OL]. (2010-05-26)[2022-06-16]. http://www.nhc.gov.cn/wjw/gfxwj/201304/15a4cc7a40b0452191fe409590ca99d8.shtml. Ministry of Health, People's Republic of China. Action plan malaria eradication in China (2010-2020 years)[EB/OL]. (2010-05-26)[2022-06-16]. http://www.nhc.gov.cn/wjw/gfxwj/201304/15a4cc7a40b0452191fe409590ca99d8.shtml. (in Chinese) |
| [7] |
国家卫生健康委员会. 关于印发防止疟疾输入再传播管理办法的通知[EB/OL]. (2021-01-06)[2022-06-16]. http://www.nhc.gov.cn/jkj/s3577/202101/1c8b2c40c76a4815acd703f13dba0b83.shtml. Nation Health Commission of the People's Republic of China. Notice on printing and distributing the measures for the management of preventing reestablishment of imported malaria[EB/OL]. (2021-01-06)[2022-06-16]. http://www.nhc.gov.cn/jkj/s3577/202101/1c8b2c40c76a4815acd703f13dba0b83.shtml. (in Chinese) |
| [8] |
国家卫生和计划生育委员会. 国家消除疟疾报告[M]. 北京: 人民卫生出版社, 2022: 64, 81-82. Nation Health and Family Planning Commission of the People's Republic of China. Chinese report on malaria elimination programme[M]. Beijing: People's Medical Publishing House Co., LTD, 2022: 64, 81-82. |
| [9] |
国家卫生健康委员会. 关于印发全国消除疟疾工作方案(2016-2020年)的通知[EB/OL]. (2016-09-01)[2022-06-16]. http://www.nhc.gov.cn/jkj/s5873/201609/2e89de24dfdf4f2899a00daecbdae690.shtml?from=timeline. Nation Health Commission of the People's Republic of China. The malaria eradication programme in China (2016-2020)[EB/OL]. (2016-09-01)[2022-06-16]. http://www.nhc.gov.cn/jkj/s5873/201609/2e89de24dfdf4f2899a00daecbdae690.shtml?from=timeline. (in Chinese) |
| [10] |
邢少文. 中国青蒿素, 40年徘徊在WHO门外[J]. 现代经济信息, 2007(11): 73-75. Xing SW. Artemisinin in China has been lingering outside WHO for 40 years[J]. Mod Econ Inf, 2007(11): 73-75. |
| [11] |
袁亚男, 姜廷良, 周兴, 等. 青蒿素的发现和发展[J]. 科学通报, 2017, 62(18): 1914-1927. Yuan YN, Jiang TL, Zhou X, et al. Discovery and development of Artemisinin[J]. Chin Sci Bull, 2017, 62(18): 1914-1927. DOI:10.1360/N972017-00320 |
| [12] |
张冬梅, 潘卫庆. 我国疟疾疫苗研究进展及前景[J]. 中国寄生虫学与寄生虫病杂志, 2009, 27(5): 390-393. Zhang DM, Pan WQ. Research and development of malaria vaccine in China[J]. Chin J Parasitol Parasit Dis, 2009, 27(5): 390-393. |
| [13] |
海关总署. 中国海关构建三道防线助力消除疟疾[EB/OL]. (2021-08-02)[2022-06-16]. http://www.customs.gov.cn/customs/ztzl86/302414/302415/gmfc40/2813466/3815599/index.html. General Administration of Customs of the People's Republic of China. China customs builds three lines of defense to help eliminate malaria[EB/OL]. (2021-08-02)[2022-06-16]. http://www.customs.gov.cn/customs/ztzl86/302414/302415/gmfc40/2813466/3815599/index.html. (in Chinese) |
| [14] |
苏婕, 李红梅, 丁玮, 等. 中国消除疟疾的督导与评估: 政治、经济、社会和技术分析[J]. 中国寄生虫学与寄生虫病杂志, 2018, 36(3): 286-290. Su J, Li HM, Ding W, et al. Supervision and evaluation of malaria elimination in China: A political, economic, social and technological analysis[J]. Chin J Parasitol Parasit Dis, 2018, 36(3): 286-290. |
| [15] |
张庆锋, 王汝波, 郑彬, 等. 2003-2013年中国全球基金疟疾项目实施效果分析[J]. 中华预防医学杂志, 2017, 51(5): 427-431. Zhang QF, Wang RB, Zheng B, et al. Analysis on the performance evaluation of the Global Fund Malaria Programme in China from 2003 to 2013[J]. Chin J Prev Med, 2017, 51(5): 427-431. DOI:10.3760/cma.j.issn.0253-9624.2017.05.011 |
| [16] |
李红梅, 丁玮, 周晓农, 等. 两个国际对华大型卫生援助项目分析[J]. 中国公共卫生管理, 2018, 34(2): 148-151. Li HM, Ding W, Zhou XN, et al. Features of two large-scale international health assistance programs for China[J]. Chin J Public Health Manag, 2018, 34(2): 148-151. DOI:10.19568/j.cnki.23-1318.2018.02.002 |
| [17] |
苏婕. 中国与缅甸疟疾防治体系比较研究[D]. 北京: 中国疾病预防控制中心, 2018. Su J. The comparative study of China and Myanmar's malaria control system[D]. Beijing: Chinese Center for Disease Control and Prevention, 2018. (in Chinese) |
| [18] |
黄晓勇, 蔡礼强, 何辉, 等. 中国社会组织报告-2019[M]. 北京: 社会科学文献出版社, 2019: 257-279. Huang XY, Cai LQ, He H, et al. Report on social organization in China-2019[M]. Beijing: Social Sciences Academic Press (China), 2019: 257-279. |
| [19] |
丰俊, 周水森. 从控制走向消除: 我国疟疾防控的历史回顾[J]. 中国寄生虫学与寄生虫病杂志, 2019, 37(5): 505-513. Feng J, Zhou SS. From control to elimination: The historical retrospect of malaria control and prevention in China[J]. Chin J Parasitol Parasit Dis, 2019, 37(5): 505-513. DOI:10.12140/j.issn.1000-7423.2019.05.001 |
| [20] |
夏志贵, 周水森, 汤林华. 中国消除疟疾的历程、意义、主要经验及消除后策略与展望[J]. 传染病信息, 2022, 35(1): 39-45, 59. Xia ZG, Zhou SS, Tang LH. History, impacts and experience of malaria elimination in China and strategies and prospects after elimination[J]. Infect Dis Inf, 2022, 35(1): 39-45, 59. DOI:10.3969/j.issn.1007-8134.2022.01.003 |
| [21] |
刘光奇, 曹俊, 于孟轲, 等. 中国参与全球消除疟疾行动的优势和挑战: 基于抗疟技术专家观点的一项定性研究[J]. 中国卫生政策研究, 2020, 13(10): 62-67. Liu GQ, Cao J, Yu MK, et al. Advantages and challenges of China's participation in global malaria control and elimination: A qualitative research based on malarial experts' opinions[J]. Chin J Health Policy, 2020, 13(10): 62-67. DOI:10.3969/j.issn.1674-2982.2020.10.010 |
| [22] |
朱国鼎, 高琪, 曹俊. 中国防止疟疾输入再传播面临的挑战和应对策略[J]. 中国血吸虫病防治杂志, 2021, 33(1): 7-9, 21. Zhu GD, Gao Q, Cao J. Challenges and countermeasures in prevention of re-establishment of imported malaria in China[J]. Chin J Schist Control, 2021, 33(1): 7-9, 21. DOI:10.16250/j.32.1374.2021008 |
| [23] |
申晓君, 周思园, 廖瑜, 等. 长沙市2015-2019年输入性疟疾疫情分析[J]. 中国热带医学, 2021, 21(1): 88-93. Shen XJ, Zhou SY, Liao Y, et al. Analysis of imported malaria epidemic in Changsha, 2015-2019[J]. China Trop Med, 2021, 21(1): 88-93. DOI:10.13604/j.cnki.46-1064/r.2021.01.20 |
| [24] |
丰俊, 张丽, 夏志贵, 等. 中国消除疟疾: 重要里程碑意义及消除后的挑战[J]. 中国寄生虫学与寄生虫病杂志, 2021, 39(4): 421-428. Feng J, Zhang L, Xia ZG, et al. Malaria elimination in China: An eminent milestone in the anti-malaria campaign and challenges in the post-elimination stage[J]. Chin J Parasitol Parasit Dis, 2021, 39(4): 421-428. DOI:10.12140/j.issn.1000-7423.2021.04.001 |
| [25] |
李倩. 福建省疟疾消除后防止输入再传播风险分析[D]. 福州: 福建医科大学, 2021. DOI: 10.27020/d.cnki.gfjyu.2021.001063. Li Q. Risk analysis of preventing re-transmission after malaria elimination in Fujian province[D]. Fuzhou: Fujian Medical University, 2021. DOI: 10.27020/d.cnki.gfjyu.2021.001063.(in Chinese) |
| [26] |
高琪. 输入性疟疾对巩固消除疟疾成果防止再传播的挑战和对策[J]. 中国热带医学, 2021, 21(1): 1-4. Gao Q. Challenge and response of imported malaria for preventing malaria re-establishment[J]. China Trop Med, 2021, 21(1): 1-4. DOI:10.13604/j.cnki.46-1064/r.2021.01.01 |
| [27] |
曹俊, 刘耀宝, 曹园园, 等. 中国消除疟疾的持续挑战: 输入性疟疾[J]. 中国寄生虫学与寄生虫病杂志, 2018, 36(2): 93-96. Cao J, Liu YB, Cao YY, et al. Sustained challenge to malaria elimination in China: Imported malaria[J]. Chin J Parasitol Parasit Dis, 2018, 36(2): 93-96. |
| [28] |
王敬军. 疟疾快速免疫诊断技术的应用研究进展[J]. 黑龙江医学, 2021, 45(6): 669-670. Wang JJ. Research progress in the application of rapid immunodiagnostic technology for malaria[J]. Heilongjiang Med J, 2021, 45(6): 669-670. DOI:10.3969/j.issn.1004-5775.2021.06.044 |
| [29] |
戚淑叶, 许明哲. 基于世界卫生组织认证分析我国医药行业国际化的机遇与挑战[J]. 中国药事, 2021, 35(1): 1-9. Qi SY, Xu MZ. On internationalization of Chinese pharmaceutical industries based on the WHO prequalification program: Opportunities and challenges[J]. Chin Pharm Aff, 2021, 35(1): 1-9. DOI:10.16153/j.1002-7777.2021.01.001 |
| [30] |
徐红芬. 国际非政府组织在地方治理中的作用: 以云南省为例[D]. 湘潭: 湘潭大学, 2009. Xu HF. International non-governmental organizations in the role of local governance: Yunnan province as an example[D]. Xiangtan: Xiangtan University, 2019. (in Chinese) |
 2023, Vol. 34
2023, Vol. 34


