扩展功能
文章信息
- 郭慧, 柳静, 毛伟平, 丁浩, 武茜茜, 周良才, 吴丽群, 陈晓敏
- GUO Hui, LIU Jing, MAO Wei-ping, DING Hao, WU Qian-qian, ZHOU Liang-cai, WU Li-qun, CHEN Xiao-min
- 武汉市2018-2021年媒介伊蚊生态学监测结果分析
- Ecological monitoring of Aedes vector in Wuhan, Hubei province, China, 2018-2021
- 中国媒介生物学及控制杂志, 2023, 34(1): 48-52
- Chin J Vector Biol & Control, 2023, 34(1): 48-52
- 10.11853/j.issn.1003.8280.2023.01.009
-
文章历史
- 收稿日期: 2022-07-01
2 武汉市疾病预防控制中心消毒与病媒生物防制所, 湖北 武汉 430022;
3 武汉市青山区疾病预防控制中心, 湖北 武汉 430080
2 Institute for Disinfection & Vector Control, Wuhan Center for Disease Control and Prevention, Wuhan, Hubei 430022, China;
3 Qingshan District Center for Disease Control and Prevention, Wuhan, Hubei 430080, China
伊蚊(Aedes)是登革热、基孔肯雅热、黄热病和寨卡病毒病等虫媒传染病的重要媒介,在全球范围内造成了严重的健康负担和经济损失[1]。其中,登革热是目前全球分布最广的虫媒传染病,由于气候变暖、环境城市化以及国际商旅增加,目前低风险或无本土病例的地区也面临越来越大的登革热传播和暴发风险[2-3]。武汉市自1945年后一直未出现登革热本地病例,居民对登革热普遍易感,而近年湖北黄冈[4]、重庆万州[5]、浙江杭州[6]等同纬度地市均发生了登革热本地暴发疫情,在新型冠状病毒肺炎(以下简称新冠肺炎)疫情防控背景下,武汉市在防范国内外登革热输入性病例引起本土传播上面临严峻挑战[7-9]。由于缺乏有效的疫苗及抗病毒药物,蚊媒控制是当前预防登革热传播的主要措施。而武汉市属亚热带季风性湿润气候区,历年均监测到白纹伊蚊(Ae. albopictus)繁衍孳生。为进一步掌握武汉市媒介伊蚊孳生和消长情况,现将2018-2021年媒介伊蚊生态学监测结果进行分析,为登革热传播风险预警及科学防控提供依据。
1 材料与方法 1.1 资料来源资料来源于2018-2021年武汉市登革热媒介伊蚊专项监测点上报的数据。
1.2 监测方法参照中国疾病预防控制中心下发的《全国病媒生物监测实施方案》(2016版),按照定时、定点、定人的原则,分别选择中心城区(青山区)和远城区(东西湖区)同时开展幼蚊和成蚊监测。
1.2.1 幼蚊监测采用布雷图指数(BI)法,选择青山区31街坊、104街坊和东西湖区颐和家园社区的居民区为监测地点,每月中旬监测1次。按不同方位,各城区每次走访调查100户。每个家庭、集体宿舍/单位办公室酒店的2个房间、农贸市场/花房/外环境/室内公共场所等每30 m2定义为1户。检查记录室内外所有小型积水和积水容器(以下统称积水容器),收集阳性容器中的幼蚊或带回实验室饲养至成蚊进行种类鉴定,计算幼蚊密度的BI,公式如下:

|
采用双层叠帐法,选择青山区31街坊居民区、104街坊废品站、南干渠公园和东西湖区颐和家园居民区、金银潭废旧轮胎堆放点、银潭路竹林为监测地点,每月上、下旬于15:00-18:00各监测1次。各区每处生境设2顶专用蚊帐,两帐间隔100 m以上,诱集者在内层封闭蚊帐中暴露两条小腿,收集者在外层利用电动吸蚊器收集停落在蚊帐上的伊蚊,持续30 min,将收集的成蚊放入-20 ℃冰箱冷冻处死,剔除雄蚊后,计算帐诱指数,公式如下:

|
除2020年4月受新冠肺炎疫情影响未能开展监测外,其余年份均为每年4-11月开展监测。
1.4 登革热传播风险评估标准参考《登革热媒介伊蚊监测指南》,帐诱指数>2只/(顶∙h)或5 < BI≤10有传播风险,10 < BI≤20有暴发风险,BI > 20有区域流行风险。
1.5 统计学分析采用Excel 2010软件进行数据整理,SPSS 20.0软件进行统计分析,P < 0.05为差异有统计学意义。通过χ2检验比较BI的组间差异,通过方差分析(正态分布)或Kruskal-Wallis检验(偏态分布)分析比较帐诱指数的组间差异。
2 结果 2.1 幼蚊密度监测 2.1.1 基本情况2018-2021年共调查6 200户,阳性户数224户,其中积水容器1 445个,白纹伊蚊幼蚊阳性容器279个,BI为4.50(表 1)。其中,48.75%(136/279)为闲置容器(碗/瓶/缸/罐),其次是盆景/水生植物和贮水池/缸/盆,分别占15.05%(42/279)和14.34%(40/279)。武汉市监测未发现埃及伊蚊(Ae. aegypti)。
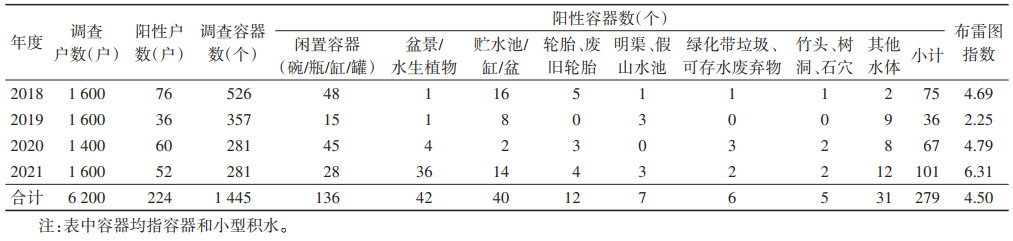
|
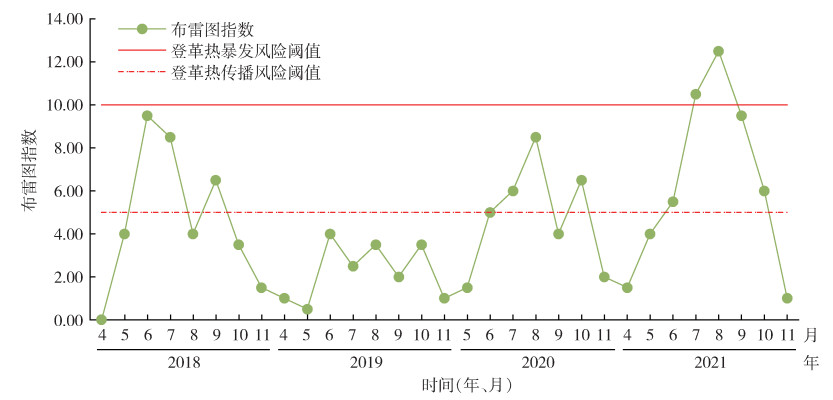
不同年份间BI差异有统计学意义(χ2=31.476,P < 0.001),经两两比较后发现,2019年幼蚊密度(BI=2.25)与其他各年份间差异有统计学意义(P < 0.05),显著偏低。且2020-2021年的密度(BI=5.60)明显高于2018-2019年(BI=3.47),差异有统计学意义(χ2=16.366,P < 0.001)。季节消长方面,不同月份间BI差异有统计学意义(χ2=74.035,P < 0.001),峰值出现在6-8月。其中,除2019年各监测月的BI值均 < 5外,2018年(6-7、9月)、2020年(7-8、10月)、2021年(6-10月)均存在登革热传播风险;其中7月的频次最高,2021年7-8月首次达到登革热暴发阈值(BI≥10)。见图 1。
|
| 图 1 2018-2021年武汉市伊蚊幼蚊密度指数与登革热传播风险 Figure 1 Density index of Aedes larvae and risk of dengue fever transmission in Wuhan, Hubei, China, 2018-2021 |
| |
2018-2022年共布设744帐次,捕获白纹伊蚊雌蚊909只,平均帐诱指数为2.44只/(顶∙h)。其中,居民区、公园、旧轮胎堆放地3种生境的帐诱指数依次为3.42、2.57和1.34只/(顶∙h)(表 2)。经Kruskal-Wallis检验不同生境间的帐诱指数差异有统计学意义(H=18.952,P < 0.001),居民区的帐诱指数高于旧轮胎堆放地(H=29.468,P < 0.001)。

|
2019年的帐诱指数最低,2020年的帐诱指数最高,但不同年份间的成蚊帐诱指数差异无统计学意义(F=1.207,P=0.326)。季节消长方面,不同月份间帐诱指数差异有统计学意义(H=22.944,P=0.002),峰值出现在7-8月。其中,除2019年外,其余年份平均帐诱指数均超阈值,具有登革热传播风险的月份主要集中在6-9月。见图 2。

|
| 图 2 2018-2021年武汉市伊蚊成蚊密度指数与登革热传播风险 Figure 2 Density index of Aedes adults and risk of dengue fever transmission in Wuhan, Hubei, China, 2018-2021 |
| |
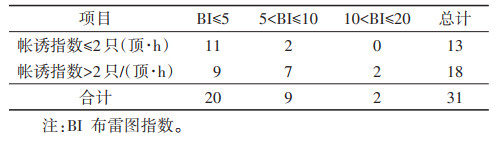
2018-2021年共计开展监测31个月,BI > 5或帐诱指数 > 2只/(顶∙h)的月份有20个,即64.52%(20/31)的监测月有登革热传播风险。见表 3。
|
近年来,登革热在我国的暴发呈地域扩散、甚至向高纬度扩散态势[8]。2019年已在13个省(自治区、直辖市)发生了登革热本地疫情,达到了新中国成立以来登革热本地病例发生省份数最高水平[9]。2020-2021年由于我国新冠肺炎疫情施行严格的出入境人员管控措施,登革热发病水平明显回落[10]。而登革热传播媒介伊蚊具有较强的生态可塑性,其丰度和分布受当地的生态环境和人类活动影响[11]。封控措施将人类限制在室内环境而减少户外活动暴露时,也限制了常规媒介生物控制措施的开展,两者对媒介伊蚊分布的综合影响尚不明确[12-13]。当全球登革热传播的持续高水平叠加我国新冠肺炎常态化防控,武汉市作为登革热非流行地区,通过伊蚊生态学监测做好登革热风险预测至关重要。
传统的伊蚊监测依赖于幼蚊和蛹的调查,其中BI是最常用的指数,但有研究认为它们与成蚊的丰度相关性较差[14],从卵到成蚊的发育过程中死亡率通常很高[15],最准确的监测方法是捕获吸血的雌性成蚊[16]。因此本调查同时采用BI法和双层叠帐法开展媒介伊蚊密度监测,并综合伊蚊幼蚊和成蚊的孳生情况进行登革热风险评估。监测结果显示,2018-2021年武汉市每年均监测到白纹伊蚊,平均BI为4.50,平均帐诱指数为2.44只/(顶∙h),提示武汉市登革热传播风险持续存在。
BI监测中90%以上的调查容器均为居民区户外容器,入户难问题持续存在,尤其是在新冠肺炎疫情防控期间,室内阳性容器可能被遗漏,因此幼蚊密度可能存在低估。年际消长方面,伊蚊密度在2019年出现明显低谷后,在2020-2021年新冠肺炎疫情出现后呈上升趋势,这可能是由于2019年武汉市举办第七届世界军人运动会,结合夏秋季爱国卫生运动集中开展了广泛的除害防病行动,如相关重点区域5-8月每月至少全覆盖1次、9-10月每周全覆盖,大量消减了蚊虫孳生环境,而新冠肺炎疫情防控严格的场所管控及紧张的卫生资源使病媒生物防制工作受阻,2020年4月甚至未能开展常规监测,除四害工作更是全面停滞,致使伊蚊孳生出现反弹。此外,居民区的帐诱指数明显高于旧轮胎堆放地,与甘肃省天水市[17]的结果相反,可能与不同地区的城镇化治理程度不同有关,旧轮胎堆放地常在偏远无人处,而武汉市居民区内生态环境丰富、人口密度大,更适宜伊蚊吸血繁殖。季节消长方面,武汉市伊蚊的幼蚊和成蚊高峰分别出现在6-8和7-8月,与广西壮族自治区[18]的监测结果一致。这提示我们不同月份可根据伊蚊的生态特点开展更精准的蚊媒控制措施,如在6-8月应以清除幼蚊孳生地为重点进行室内外的环境治理,同时7-8月应注重外环境成蚊的杀灭工作。同时,参照我国登革热风险评估标准,2018-2021年有登革热传播风险的监测月数占比达64.52%(20/31),2021年7-8月甚至出现暴发风险(BI > 10),提示在蚊媒流行季节,武汉市媒介伊蚊密度历年均存在登革热传播风险,且风险程度有所上升。
综上,武汉市媒介伊蚊密度呈反弹趋势,武汉市面临的登革热传播风险不容忽视。在新冠肺炎疫情防控的同时,为克服室内阳性容器样本减少带来的幼蚊密度低估,可适当增加伊蚊监测方法,如诱蚊诱卵器法,以增强监测结果的代表性和可靠性。在蚊媒流行季节,尤其是6-9月,应加强家庭和社区参与媒介伊蚊控制措施,如可将防蚊灭蚊知识与新冠肺炎防控信息相结合,提醒居民注意个人卫生的同时关注环境卫生,及时清除家庭内部和周围的蚊虫孳生点;同时,还可探索将针对新冠病毒的洗手液与针对虫媒病毒病媒介的驱虫剂结合使用的防蚊策略。此外,对处于新冠肺炎疫情封控的区域,也应按照武汉市媒介伊蚊季节消长规律,适时采取媒介伊蚊的控制措施。
利益冲突 无
| [1] |
Lwande OW, Obanda V, Lindström A, et al. Globe-trotting Aedes aegypti and Ae. albopictus: Risk factors for arbovirus pandemics[J]. Vector Borne Zoonotic Dis, 2020, 20(2): 71-81. DOI:10.1089/vbz.2019.2486 |
| [2] |
Tsheten T, Gray DJ, Clements ACA, et al. Epidemiology and challenges of dengue surveillance in the WHO south-east Asia region[J]. Trans R Soc Trop Med Hyg, 2021, 115(6): 583-599. DOI:10.1093/trstmh/traa158 |
| [3] |
Messina JP, Brady OJ, Golding N, et al. The current and future global distribution and population at risk of dengue[J]. Nat Microbiol, 2019, 4(9): 1508-1515. DOI:10.1038/s41564-019-0476-8 |
| [4] |
戴本南, 王芬, 潘洁, 等. 湖北省首起输入性登革热引起本地暴发流行的特征及处置效果分析[J]. 公共卫生与预防医学, 2020, 31(4): 62-65. Dai BN, Wang F, Pan J, et al. Epidemic characteristics and treatment effect of the first dengue fever outbreak in Hubei province[J]. J Public Health Prev Med, 2020, 31(4): 62-65. DOI:10.3969/j.issn.1006-2483.2020.04.015 |
| [5] |
罗超, 陈琼, 谭仕碧, 等. 重庆市万州区2019年登革热暴发疫情流行特征及相关因素[J]. 中国热带医学, 2021, 21(7): 654-657, 662. Luo C, Chen Q, Tan SB, et al. Epidemic characteristics and influential factors of dengue fever in Wanzhou, Chongqing, 2019[J]. China Trop Med, 2021, 21(7): 654-657, 662. DOI:10.13604/j.cnki.46-1064/r.2021.07.08 |
| [6] |
刘牧文, 孙昼, 考庆君, 等. 2017-2019年浙江省杭州市登革热流行特征和时空聚集性分析[J]. 疾病监测, 2022, 37(4): 481-486. Liu MW, Sun Z, Kao QJ, et al. Spatiotemporal distribution of dengue fever in Hangzhou, Zhejiang, 2017-2019[J]. Dis Surveill, 2022, 37(4): 481-486. DOI:10.3784/jbjc.202106300379 |
| [7] |
刘小波, 岳玉娟, 贾清臣, 等. 2020-2021年我国12省份媒介伊蚊生态学调查[J]. 中国媒介生物学及控制杂志, 2022, 33(1): 8-15. Liu XB, Yue YJ, Jia QC, et al. Ecological investigation of Aedes vector in 12 provinces of China in 2020-2021[J]. Chin J Vector Biol Control, 2022, 33(1): 8-15. DOI:10.11853/j.issn.1003.8280.2022.01.002 |
| [8] |
牟笛, 崔金朝, 殷文武, 等. 2015-2018年我国登革热暴发流行病学特征分析[J]. 中华流行病学杂志, 2020, 41(5): 685-689. Mu D, Cui JZ, Yin WW, et al. Epidemiological characteristics of dengue fever outbreaks in China, 2015-2018[J]. Chin J Epidemiol, 2020, 41(5): 685-689. DOI:10.3760/cma.j.cn112338-20190715-00523 |
| [9] |
刘起勇. 我国登革热流行新趋势、防控挑战及策略分析[J]. 中国媒介生物学及控制杂志, 2020, 31(1): 1-6. Liu QY. Dengue fever in China: New epidemical trend, challenges and strategies for prevention and control[J]. Chin J Vector Biol Control, 2020, 31(1): 1-6. DOI:10.11853/j.issn.1003.8280.2020.01.001 |
| [10] |
耿梦杰, 任翔, 彭质斌, 等. 2021年我国夏季重点传染病疫情形势分析[J]. 疾病监测, 2021, 36(8): 811-817. Geng MJ, Ren X, Peng ZB, et al. Incidence of key infectious diseases in summer of 2021, China[J]. Dis Surveill, 2021, 36(8): 811-817. DOI:10.3784/jbjc.202106170344 |
| [11] |
Fansiri T, Buddhari D, Pathawong N, et al. Entomological risk assessment for dengue virus transmission during 2016-2020 in Kamphaeng Phet, Thailand[J]. Pathogens, 2021, 10(10): 1234. DOI:10.3390/pathogens10101234 |
| [12] |
Ong SQ, Ahmad H, Ngesom AMM. Implications of the COVID-19 lockdown on dengue transmission in Malaysia[J]. Infect Dis Rep, 2021, 13(1): 148-160. DOI:10.3390/idr13010016 |
| [13] |
Harapan H, Ryan M, Yohan B, et al. Covid-19 and dengue: Double punches for dengue-endemic countries in Asia[J]. Rev Med Virol, 2021, 31(2): e2161. DOI:10.1002/rmv.2161 |
| [14] |
Chang FS, Tseng YT, Hsu PS, et al. Re-assess vector indices threshold as an early warning tool for predicting dengue epidemic in a dengue non-endemic country[J]. PLoS Negl Trop Dis, 2015, 9(9): e0004043. DOI:10.1371/journal.pntd.0004043 |
| [15] |
Fustec B, Phanitchat T, Aromseree S, et al. Serological biomarker for assessing human exposure to Aedes mosquito bites during a randomized vector control intervention trial in northeastern Thailand[J]. PLoS Negl Trop Dis, 2021, 15(5): e0009440. DOI:10.1371/journal.pntd.0009440 |
| [16] |
Bowman LR, Runge-Ranzinger S, McCall PJ. Assessing the relationship between vector indices and dengue transmission: A systematic review of the evidence[J]. PLoS Negl Trop Dis, 2014, 8(5): e2848. DOI:10.1371/journal.pntd.0002848 |
| [17] |
陈秋梅, 王热勤, 吴海霞, 等. 甘肃省天水市2017-2020年两种重要媒介蚊虫监测结果分析[J]. 中国媒介生物学及控制杂志, 2021, 32(4): 456-460. Chen QM, Wang RQ, Wu HX, et al. Surveillance results of two important vector mosquitoes in Tianshui, Gansu, China, 2017-2020[J]. Chin J Vector Biol Control, 2021, 32(4): 456-460. DOI:10.11853/j.issn.1003.8280.2021.04.014 |
| [18] |
魏超, 马海芳, 廖宁, 等. 广西壮族自治区2020-2021年登革热媒介伊蚊密度专项调查结果分析[J]. 中国媒介生物学及控制杂志, 2022, 33(1): 25-29. Wei C, Ma HF, Liao N, et al. An analysis of special investigation results of dengue vector Aedes density in Guangxi Zhuang Autonomous Region, China, 2020-2021[J]. Chin J Vector Biol Control, 2022, 33(1): 25-29. DOI:10.11853/j.issn.1003.8280.2022.01.005 |
 2023, Vol. 34
2023, Vol. 34


