俯冲带是地球表面和地球深部物质循环的重要场所[1],板块向下俯冲过程中,将水带入地球内部,形成不同类型的含水矿物[2]。随着板块的继续俯冲,一些含水矿物发生脱水,释放的大量流体会引起部分熔融、诱发地震以及导致地震波速异常和电导率异常[3-10]。在俯冲带的中源深度(30~300 km)存在双地震带, 其上层地震被认为与“湿”榴辉岩脱水有关,而下层地震则认为是由于叶蛇纹石的脱水造成的[11-12]。
蛇纹石是俯冲带重要的含水矿物之一,其化学式为Mg3Si2O5(OH)4,其平均含水量近13%。蛇纹石有3个种属:纤蛇纹石、利蛇纹石和叶蛇纹石,其中仅叶蛇纹石在300 ℃以上是稳定相[12]。前人采用不同的技术方法对叶蛇纹石脱水过程进行了研究,其中包括热重方法、XRD和红外光谱等方法[11, 13-15]。这些研究表明:叶蛇纹石脱水速率大于其黏性松弛速率,表明叶蛇纹石脱水会产生高孔隙压力,引起岩石的弱化和脆性破裂,从而诱发俯冲带双地震带的下层地震[11, 13, 15-16]。
叶蛇纹石脱水过程不是简单的一步反应,而是复杂的多步反应[11, 13-15, 17-18]。在常压下,叶蛇纹石在低温阶段脱水首先生成镁橄榄石,在800~1 000 ℃以后,才有顽火辉石相出现[17-19]。前人在研究叶蛇纹石脱水动力学过程时,往往将叶蛇纹石脱水生成镁橄榄石和顽火辉石的过程看作一步反应,但实际上这两种矿物的形成次序不同会导致其对动力学的影响不同,这可能掩盖了低温下仅出现镁橄榄石相过程中的脱水动力学信息,因此本研究尝试研究叶蛇纹石在低温下仅出现镁橄榄石相过程的脱水动力学。
本研究主要是通过同步辐射X射线粉末衍射技术在680、700、710和720 ℃下原位地测量叶蛇纹石脱水过程特征峰的变化,以及产生新相的特征峰。利用叶蛇纹石和其产物特征峰随时间的变化规律,研究叶蛇纹石脱水机制和反应生成的产物。同步辐射X射线具有高强度、高度准直、高度极化、高分辨率、信号强度大和采集时间短等特点,因此能够准确地表征叶蛇纹石脱水过程及其产物的生成过程。
1 实验样品叶蛇纹石样品采集于日本长崎变质带,挑选纯的叶蛇纹石单矿物作为实验样品。叶蛇纹石样品在合肥工业大学进行电子探针分析,其化学成分为Mg2.75Fe0.09Al0.06Si2.03O5(OH)4(详细见表 1)。实验前将叶蛇纹石粉碎并研磨成细粉末,再通过沉淀法将样品分成不同粒径:< 5、5~10、10~15、15~20、20~25和>25 μm。其中 < 5 μm粒径的叶蛇纹石粉末被筛选出来用于同步辐射X射线粉末衍射实验,实验前将样品置于150 ℃真空干燥箱内烘烤保持一周,以除去自由水。
|
|
表 1 叶蛇纹石成分电子探针分析结果 Table 1 Electron probe micro-analyzer results of antigorite composition |
X射线粉末衍射实验在上海光源同步辐射中心的BL14B1线站进行,光强采用18 keV能量,波长0.068 87 nm[20]。将样品放置在单晶Al2O3管内;Al2O3管两端用石英毛堵住;然后在单晶管外绕上电阻丝对样品加热;将K型热电偶伸入Al2O3单晶管中紧靠样品以精确测量样品温度[21-22]。首先以50 ℃/min升到600 ℃,然后以20 ℃/min分别升至目标温度(680,700,710和720 ℃),到达目标温度以后一直保温,直至观察不到明显相变为止,温控误差在±5 ℃。
3 实验结果图 1为700 ℃条件下,叶蛇纹石的脱水过程。叶蛇纹石(Atg)的特征主要分布在2θ为5.370 8、10.752 5和15.565 5位置;产物的特征峰主要分布在2θ为7.646 0、10.074 4、14.143 5、15.915 5、17.293 8和22.478 6位置。在700 ℃经历1 782 s后,叶蛇纹石特征峰逐渐消失,产物的峰逐渐增强。对产物进行图谱识别,表明产物为镁橄榄石(Fo),剩余物质以无定形态存在,无滑石或者顽火辉石生成。

|
Download:
|
| 图 1 在700 ℃条件下叶蛇纹石及其脱水产物峰随时间的变化 Fig. 1 Variations in the intensities of antigorite and reaction product with time at 700 ℃ | |
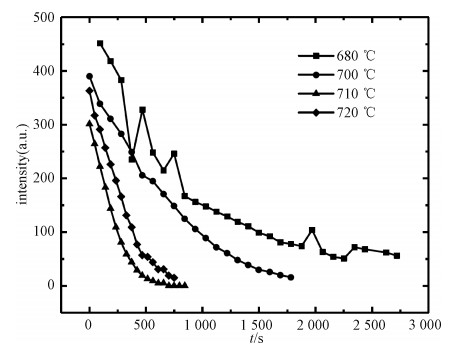
以2θ为5.370 8特征峰强度(高度,It)随时间变化表示反应进行程度,通过观察在680、700、710和720 ℃不同温度下特征峰随时间的变化(图 2),发现等温反应温度越高,叶蛇纹石脱水所需时间越短。在同一温度下,叶蛇纹石开始脱水反应快,脱水量大;剩余少量的水需要更长时间脱完。
|
Download:
|
| 图 2 叶蛇纹石在680、700、710和720 ℃条件下等温过程衍射峰强度随时间的变化 Fig. 2 Variation in the intensity of antigorite with time at 680, 700, 710, and 720 ℃ | |
叶蛇纹石在825 ℃以前脱水生成顽火辉石;在825 ℃以后,叶蛇纹石脱水才有顽火辉石生成[18],与本研究叶蛇纹在725 ℃以前脱水仅出现镁橄榄石相一致。同步辐射X射线粉末衍射图谱采集时间短[20],导致富硅区域没来得及成核生成顽火辉石。
叶蛇纹石脱水分为4个阶段[17],第1个阶段(脱水阶段),质子迁移到反应区域,Mg和Si反向迁移,O相对来说基本不发生改变,此时Mg:Si仍然为3:2,产物为无定形物质;第2个阶段(阳离子重组),阳离子局部分离进入富镁区域和富硅区域;第3个阶段(镁橄榄石结晶):阳离子和氧离子堆积形成镁橄榄石,阶段2和3可以在很大程度上同时进行;第4个阶段(顽火辉石结晶):富硅区域形成顽火辉石,但此阶段没有前面3个阶段稳定,反应容易停止在第3个阶段末,第4个阶段反应更加复杂。Brindley和Hayami[17]发现叶蛇纹石常压条件下,1 000 ℃以前主要进行前3步反应,没有顽火辉石形成。最近的研究表明,叶蛇纹石脱水过程中,顽火辉石重结晶发生在820 ℃以后,低于800 ℃主要是镁橄榄石的重结晶[14, 18-19]。本研究实验温度低于800 ℃,只有镁橄榄石生成,与前人研究结果一致[14, 17-19]。
对于等温反应,可以定义归一化的反应进程α=1-It/I0, 其中It表示t时刻某角度特征峰的强度(高度), I0表示刚到目标温度时特征峰的强度。采用经典的成核与生长的Avrami方程来分析叶蛇纹石脱水动力学,Avrami方程[23]表示为
| $ \alpha = 1 - \exp \left( { - k{t^n}} \right), $ | (1) |
其中:α为归一化的反应进程,k为反应速率常数,t为反应时间,n为反应级数。利用Avrami方程,可以得到在不同温度下叶蛇纹石的动力学参数n值和反应速率常数k(见表 2)。反应级数n与成核机制有关的参数,n为1、2和3分别代表晶界成核、晶棱成核和晶角成核[24]。Chollet等[11]研究表明在4.5 GPa、567~681 ℃条件下叶蛇纹石脱水速率为10-4 s-1,叶蛇纹石脱水分为两个阶段,第1阶段反应生成镁橄榄石和含水中间相时n=2,表明脱水受晶棱成核控制;第2阶段反应生成橄榄石和顽火辉石,此阶段反应级数为4,无对应的成核和生长机理[16]。在常压高温条件下,Gualtieri等[19]采用X射线粉末衍射实验计算叶蛇纹石脱水反应级数n为0.8,与本研究反应级数(n=1.1~1.3)基本一致,表明在常压高温条件下叶蛇纹石脱水受晶界成核控制。
|
|
表 2 叶蛇纹石脱水过程中的动力学参数 Table 2 Kinetic parameters for the dehydration reaction of antigorite |
反应速率常数k可以由Arrhenius方程决定:
| $ k = A\exp \left( { - E/\left( {{\rm{RT}}} \right)} \right), $ | (2) |
其中:k是反应速率常数,A是指前因子,E是活化能,R是理想气体常数,T是开氏温度。利用表 2中数据采用最小二乘拟合(如图 3所示),获得叶蛇纹石脱水活化能为105.97 kJ/mol。

|
Download:
|
| 图 3 反应常数lnk随温度的变化关系 Fig. 3 Relationship between reaction constant lnk and temperature | |
Viti[14]通过粒径为10~20 μm的叶蛇纹X射线粉末衍射实验获得叶蛇纹石在560~1 000 ℃脱水,生成镁橄榄石、顽火辉石和流体,所需活化能为255 kJ/mol, 其反应完成了叶蛇纹石脱水的4个阶段。而本研究中叶蛇纹石脱水在较低温度(≤ 720 ℃)下进行,没有顽火辉石生成,只完成了叶蛇纹石脱水的前3个阶段,叶蛇纹石脱水仅形成顽火辉石所需的活化能为105.97 kJ/mol,与方解石和石英岩的晶界扩散活化能相一致(~100 kJ/mol)[13]。纤蛇纹石脱水生成的顽火辉石来源于两个部分,一部分来自于MgSi3O7在770~800 ℃分解为顽火辉石和二氧化硅,另一部分来自于二氧化硅与镁橄榄石反应生成顽火辉石,顽火辉石的形成与蛇纹石中离子跨晶棱或者晶面迁移和重排有关,这些过程比晶界需要更高的能量[25]。Balucan等[18]采用二维相边界反应机制得到叶蛇纹石脱水活化能119~122 kJ/mol,略高于本研究结果,可能由于富硅区域无定形物质结晶形成少量顽火辉石导致。本研究采用~5 μm粒径的叶蛇纹石样品进行实验,低于Balucan等[18]的样品粒径长度75 μm。Criado和Ortega[26]用热分析技术研究粒径对CaCO3热分解的影响时,发现CaCO3分解活化能随粒径的减少而减少,Wang等[27]发现滑石粒径越小,反应越快,因此叶蛇纹石的粒径不同也会导致其反应活化能不同。
5 结论本文通过同步辐射原位X射线粉末衍射技术对叶蛇纹石脱水过程特征峰进行分析,发现叶蛇纹石在加热时间较短,不高于720 ℃时,脱水形成镁橄榄石和水,并没有顽火辉石或者滑石生成,而是以无定形物质状态存在。采用Avrami方程处理叶蛇纹石特征峰2θ (5.370 8)的数据发现,叶蛇纹石脱水反应级数n为1.1~1.3,表明叶蛇纹石脱水遵循晶界成核控制。通过拟合Arrhenius方程,表明叶蛇纹石脱水仅形成镁橄榄石所需活化能为105.97 kJ/mol,指前因子为333.62 s-1。
日本Ikuo Katayama教授提供了叶蛇纹石样品,上海光源同步辐射中心BL14B1线站的文闻老师在实验过程中提供了指导和帮助, 中国地震局地震预测研究所的张瑞鑫提供了实验帮助,作者在此一并表示感谢。| [1] |
Tatsumi Y, Kogiso T. The subduction factory:its role in the evolution of the Earth's crust and mantle[J]. Geological Society, London, Special Publications, 2003, 219(1): 55-80. Doi:10.1144/GSL.SP.2003.219.01.03 |
| [2] |
Marschall H, Foster G. Boron isotopes:the fifth element[M]. Springer International Publishing, 2018:217-247.
|
| [3] |
Pommier A. Geophysical assessment of migration and storage conditions of fluids in subduction zones[J]. Earth, Planets and Space, 2014, 66: 38. Doi:10.1186/1880-5981-66-38 |
| [4] |
Ferrand T P, Hilairet N, Incel S, et al. Dehydration-driven stress transfer triggers intermediate-depth earthquakes[J]. Nature Communications, 2017, 8(15247): 1-11. |
| [5] |
Jung H, Green Ii H W, Dobrzhinetskaya L F. Intermediate-depth earthquake faulting by dehydration embrittlement with negative volume change[J]. Nature, 2004, 428: 545-549. Doi:10.1038/nature02412 |
| [6] |
Manthilake G, Bolfan-Casanova N, Novella D, et al. Dehydration of chlorite explains anomalously high electrical conductivity in the mantle wedges[J]. Science Advances, 2016, 2(5): 1-5. |
| [7] |
Manthilake G, Mookherjee M, Bolfan-Casanova N, et al. Electrical conductivity of lawsonite and dehydrating fluids at high pressures and temperatures[J]. Geophysical Research Letters, 2015, 42(18): 7398-7405. Doi:10.1002/2015GL064804 |
| [8] |
Wang D, Liu X, Liu T, et al. Constraints from the dehydration of antigorite on high-conductivity anomalies in subduction zones[J]. Scientific Reports, 2017, 7(16893): 1-9. |
| [9] |
Wang D, Guo Y, Yu Y, et al. Electrical conductivity of amphibole-bearing rocks:influence of dehydration[J]. Contributions to Mineralogy and Petrology, 2012, 164(1): 17-25. Doi:10.1007/s00410-012-0722-z |
| [10] |
Hu H, Dai L, Li H, et al. Influence of dehydration on the electrical conductivity of epidote and implications for high-conductivity anomalies in subduction zones[J]. Journal of Geophysical Research:Solid Earth, 2017, 122(4): 2751-2762. Doi:10.1002/2016JB013767 |
| [11] |
Chollet M, Daniel I, Koga K T, et al. Kinetics and mechanism of antigorite dehydration:implications for subduction zone seismicity[J]. Journal of Geophysical Research:Solid Earth, 2011, 116(B04203): 1-9. |
| [12] |
Peacock S M. Are the lower planes of double seismic zones caused by serpentine dehydration in abducting oceanic mantle?[J]. Geology, 2001, 29(4): 299-302. Doi:10.1130/0091-7613(2001)029<0299:ATLPOD>2.0.CO;2 |
| [13] |
Sawai M, Katayama I, Hamada A, et al. Dehydration kinetics of antigorite using in situ high-temperature infrared microspectroscopy[J]. Physics and Chemistry of Minerals, 2013, 40(4): 319-330. Doi:10.1007/s00269-013-0573-9 |
| [14] |
Viti C. Serpentine minerals discrimination by thermal analysis[J]. American Mineralogist, 2010, 95(4): 631-638. Doi:10.2138/am.2010.3366 |
| [15] |
Liu T, Wang D, Shen K, et al. Kinetics of antigorite dehydration:rapid dehydration as a trigger for lower-plane seismicity in subduction zones[J]. American Mineralogist, 2019, 104(2): 282-290. |
| [16] |
Perrillat J-P, Daniel I, Koga K T, et al. Kinetics of antigorite dehydration:a real-time X-ray diffraction study[J]. Earth and Planetary Science Letters, 2005, 236(3): 899-913. |
| [17] |
Brindley G W, Hayami R. Kinetics and mechanisms of dehydration and recrystallization of serpentine*-I[J]. Clays and Clay Minerals, 1963, 12(1): 35-47. Doi:10.1346/CCMN.1963.0120107 |
| [18] |
Balucan R D, Kennedy E M, Mackie J F, et al. Optimization of antigorite heat pre-treatment via kinetic modeling of the dehydroxylation reaction for CO2 mineralization[J]. Greenhouse Gases:Science and Technology, 2011, 1(4): 294-304. Doi:10.1002/ghg.33 |
| [19] |
Gualtieri A F, Giacobbe C, Viti C. The dehydroxylation of serpentine group minerals[J]. American Mineralogist, 2012, 97(4): 666-680. Doi:10.2138/am.2012.3952 |
| [20] |
Yang T, Wen W, Guang-Zhi Y, et al. Introduction of the X-ray diffraction beeline of SSRF*[J]. Nuclear Science and Techniques, 2015, 26(020101): 1-5. |
| [21] |
Liu C, Zhang R, Shen K, et al. An in situ kinetic study of the dehydration of brucite using synchrotron X-ray powder diffraction[J]. The Canadian Mineralogist, 2018, 56(1): 101-108. |
| [22] |
张瑞鑫, 易丽, 刘红, 等. 铁含量对滑石脱水动力学的影响及其地质意义[J]. 地质通报, 2017, 36(6): 1051-1055. |
| [23] |
Avrami M. Granulation, phase change, and microstructure kinetics of phase change. Ⅲ[J]. The Journal of Chemical Physics, 1941, 9(2): 177-184. Doi:10.1063/1.1750872 |
| [24] |
Cahn J W. The kinetics of grain boundary nucleated reactions[J]. Acta Metallurgica, 1956, 4(5): 449-459. Doi:10.1016/0001-6160(56)90041-4 |
| [25] |
Dlugogorski B Z, Balucan R D. Dehydroxylation of serpentine minerals:implications for mineral carbonation[J]. Renewable and Sustainable Energy Reviews, 2014, 31: 353-367. Doi:10.1016/j.rser.2013.11.002 |
| [26] |
Criado J M, Ortega A. A study of the influence of particle size on the thermal decomposition of CaCO3 by means of constant rate thermal analysis[J]. Thermochimica Acta, 1992, 195: 163-167. Doi:10.1016/0040-6031(92)80059-6 |
| [27] |
Wang D, Wang Y, Yi L, et al. Dehydration kinetics of natural talc[J]. The Canadian Mineralogist, 2015, 53(4): 643-651. Doi:10.3749/canmin.1400089 |
 2020, Vol. 37
2020, Vol. 37 


