2. 北京石油化工学院化学工程学院, 北京 102617
2. School of Chemical Engineering, Beijing Institute of Petrochemical Technology, Beijing 102617, China
纳米二氧化钛(TiO2)由于尺寸的细微化,表现出独特的物理和化学特性,其在新能源(各类电池材料、氢能等)制备、环境保护(空气、水体与土壤的污染控制)、化工、医药、航空和军事等领域有着广阔的应用前景[1-7]。纳米TiO2具有高的光催化活性,在污水处理与抗菌等领域具有重要应用价值。TiO2有板钛矿、锐钛矿和金红石3种常见的晶型,其中锐钛矿TiO2在光催化等方面表现出优异的性能[8-9]。由于纳米TiO2大的比表面积与高的表面能,使小颗粒极易团聚形成带有若干弱连接界面的尺寸较大的团聚体,很难稳定分散在液体介质中,从而降低了TiO2分散液的稳定性与光催化活性,影响其实际应用[10-12]。因此,纳米TiO2的均匀分散是充分发挥其性能的前提,也是制备纳米材料的关键所在。
在实际应用中,将纳米TiO2光催化分散液喷涂在基底上形成薄膜,利用TiO2良好的光催化活性,使基底具有自清洁、抗菌、净化空气等能力。例如,将纳米TiO2分散液喷涂在建筑外墙上,形成透明的光催化膜层。当太阳光照射时,纳米TiO2形成光生电子-空穴对,与吸附在表面的H2O、O2等反应形成OH·、O2-·等具有强氧化性的活性基团[13]。这些基团可有效降解有机污染物,使基底具有自清洁的能力。因此,研制分散均匀、稳定性好的纳米TiO2水性分散液,对促进其降解污染物、自清洁表面产业的发展具有重要意义。
目前,主要通过在纳米TiO2表面进行无机/有机包覆,或加表面活性剂等手段来提高TiO2分散液的均匀性与稳定性[10-15]。无机或有机物的加入,削弱了纳米TiO2的光催化活性;同时增加了材料、过程与环保成本。因此,不加稳定剂制备均匀稳定的纳米TiO2分散液是该方向的难点。本工作采用沉淀-溶剂热联用的方法,制备粒径均匀的锐钛矿型纳米TiO2材料。在无修饰的情况下,通过超声得到分散均匀、稳定性好的锐钛矿型纳米TiO2水性分散液。该分散在室温静置180 d后,仍保持澄清透明,对有机污染物罗丹明B的降解仍旧表现出优异的光催化活性。喷涂该分散液的铝板也表现出良好的亲水性与自清洁能力。
1 实验部分 1.1 实验试剂和仪器四氯化钛(TiCl4),氨水(NH3·H2O,25%~28%,西陇化工股份有限公司),无水乙醇(C2H5OH,北京市化学试剂厂),双氧水(H2O2,30%,北京化学试剂厂)。所用试剂均为分析纯,实验用水为去离子水。
D8 Focus型X射线粉末衍射仪(XRD,德国布鲁克公司),Cu Kα辐射源,λ=0.154 06 nm;S-4800扫描电子显微镜(SEM,日本日立公司),扫描电压5 kV,T20透射电子显微镜(TEM,美国FEI公司),加速电压200 kV,Renishaw拉曼光谱分析仪(Renishaw,英国雷尼绍公司),激发波长514 nm;U-3900型UV-Vis漫反射光谱(DRS,Hitachi U-3900),积分球测试;Escalab 250Xi X射线光电子能谱仪(XPS,美国赛默飞公司)。
1.2 分散液的制备 1.2.1 纳米二氧化钛的制备在冰水浴中配制浓度为0.2 mol/L的酸性TiCl4水溶液,将该溶液缓慢滴加至50 mL 0.5 mol/L的氨水溶液中,至体系pH为8.0,整个过程均需搅拌,滴加完毕后,继续搅拌30 min,得到白色乳状液,静置3 h。离心分离得到白色沉淀,用去离子水将其洗涤3次,超声分散在200 mL无水乙醇中,分为4等份,分别置于100 mL聚四氟乙烯内衬不锈钢高压反应釜中。将反应釜放置在鼓风干燥箱中150 ℃反应8 h。反应结束后冷却至室温,产物分别用去离子水和乙醇洗涤数次,-65 ℃下冷冻干燥得到白色粉末。
1.2.2 纳米二氧化钛分散液的制备准确称量不同重量的纳米TiO2白色粉末,加到1 L去离子水中,超声20 min。在搅拌下,往上述体系中缓慢滴加微量的双氧水,至体系的pH为7.0,继续搅拌30 min,得到一定浓度的淡蓝色半透明的纳米TiO2分散液。
1.3 光催化降解实验通过在紫外光照下罗丹明B溶液的降解反应,评价纳米TiO2分散液的光催化活性与稳定性。将0.5 mL 200 mg/L的罗丹明B水溶液加入到100 mL纳米TiO2分散液中,于暗处搅拌1 h以达到吸脱附平衡。之后进行紫外光(365 nm)照射。每隔15 min取样,8 000 r/min离心5 min后,取上层澄清溶液,以紫外分光光度计分析罗丹明B溶液浓度(对应于553 nm处的吸光度)。
1.4 稳定性实验将制备的纳米TiO2分散液置于室温环境中,每隔一段时间对分散进行拍照,观察纳米TiO2颗粒的沉降情况。同时,取分散液进行光催化降解实验,考察其活性稳定性。
1.5 涂膜实验将制备的纳米TiO2分散液喷涂在表面清洁的铝板上,经紫外光照射后,通过测试铝板表面接触角的变化,考察其表面的亲水性。喷涂装置为日常化妆用的小喷壶。单层膜制备:喷涂一次分散液,置于烘箱中80 ℃干燥20 min,自然冷却后,测试接触角;5层与10层膜制备:单层膜烘干,自然冷却后,喷涂第2层,然后重复喷涂至需要的层数。取1 mL浓度为25 mg/L的罗丹明B溶液滴加到喷涂有分散液与空白的铝板基底上,紫外光照下,考察铝板的自清洁能力。
2 结果与讨论 2.1 纳米TiO2的表征 2.1.1 晶体结构图 1(a)为纳米TiO2经冷冻干燥后的XRD图谱。由图可见,该样品的结晶性良好,所有衍射峰与锐钛矿TiO2的PDF卡片(JPCDS Card No. 21-1272)一致,表明其为锐钛矿相[16]。该样品的拉曼图谱见图 1(b),位于144、399、515与639 cm-1的拉曼峰,分别归属于锐钛矿相TiO2的Eg、B1 g、A1 g与Eg峰。因此,拉曼结果进一步证实,分散液用纳米TiO2为纯的锐钛矿相。

|
Download:
|
| 图 1 纳米TiO2的XRD (a)与拉曼图谱(b) Fig. 1 XRD patterns (a) and Raman spectra (b) of TiO2 sample | |
将分散液直接滴到电镜硅片或铜网上,自然晾干后,采用扫描电镜与透射电镜对分散液用纳米TiO2的形貌进行表征,测试结果见图 2。明显看出,所制备纳米TiO2粒度均匀,分散良好。从TEM图统计得到,纳米TiO2的粒径约为(29±2) nm,粒径相对标准偏差小于8%,样品粒度的均一性良好。图 2(c)为单个纳米TiO2颗粒的高分辨图,晶面间距0.35 nm归属于锐钛矿相TiO2的(101)晶面,表明所制备纳米TiO2为锐钛矿相的单晶颗粒。

|
Download:
|
| 图 2 纳米TiO2的SEM(a)与TEM(b, c)图片 Fig. 2 SEM (a) and TEM (b, c) images of the TiO2 nanoparticles | |
所制备纳米TiO2的红外光谱结果见图 3。位于3 410 cm-1与1 628 cm-1处的振动峰分别归属于样品表面吸附的水分子中O—H的伸缩振动与弯曲振动。2 918 cm-1与2 857 cm-1处极弱的振动峰分别为C—H的非对称与对称伸缩振动峰,1 385 cm-1处为C—H的弯曲振动峰。可见,C—H的红外特征峰很弱。纳米TiO2在制备与后处理过程中,只有无水乙醇含有C—H键。因此,纳米TiO2表面残留的微量有机物为乙醇。

|
Download:
|
| 图 3 纳米TiO2的红外图谱 Fig. 3 FT-IR spectra of the TiO2 nanoparticles | |
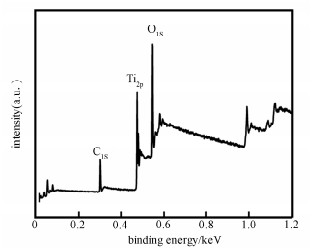
纳米TiO2的XPS图谱如图 4所示。可看出,样品含有Ti、O、C这3种元素。其中C元素主要来自XPS测试时,环境中的污染C源,很少一部分为样品表面的微量乙醇。因此,结合红外结果可知,所制备的纳米TiO2表面处理较干净,纯度高,利于得到高催化活性的纳米TiO2分散液。
|
Download:
|
| 图 4 纳米TiO2的XPS图谱 Fig. 4 XPS full survey spectra of the TiO2 nanoparticles | |
选取浓度分别为0.03、0.05与0.08 g/L的纳米TiO2分散液,加H2O2调节体系的pH为7.0,将其用于光催化降解罗丹明B,考察其催化活性。
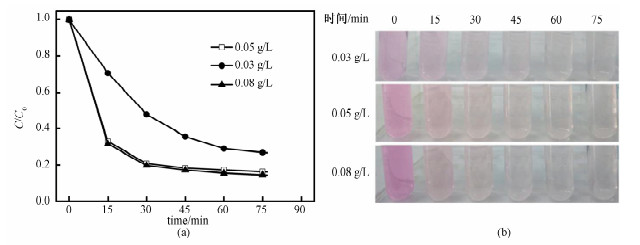
图 5为不同浓度的纳米TiO2分散液紫外光降解罗丹明B的曲线与照片。从图 5(a)可看出,浓度为0.05与0.08 g/L的分散液对罗丹明B的降解在30 min之后即接近完成,表明二者具有很高的催化活性,且降解速率基本一致。0.03 g/L的分散液降解效率和速率稍弱。由图 5(b)可知,3个浓度的分散液,在15 min时,罗丹明B明显褪色,30 min时,体系已由粉色变为无色,表明该纳米TiO2分散液具有高的光催化活性。上述结果表明,纳米TiO2的浓度对分散液的光催化活性有影响,浓度过低难以将罗丹明B降解完全。
|
Download:
|
| 图 5 不同浓度的纳米TiO2分散液紫外光降解罗丹明B曲线(a)与照片(b) Fig. 5 Degradation curves (a) and photographs (b) of photocatalytic degradation of RhB in TiO2 dispersion solution with different concentrations | |
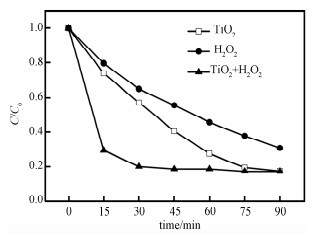
为考察H2O2对该分散液光催化活性的影响,将与0.05 g/L分散液相同浓度的TiO2与H2O2分别作为催化剂在紫外光条件下降解相同浓度的罗丹明B溶液,实验结果如图 6所示。可看出,TiO2与H2O2单独作为催化剂时,均可有效降解罗丹明B。当加入H2O2后,分散液的光催化活性明显提高。这是因为H2O2在紫外光照射下可以直接产生具有氧化性的OH·,且H2O2具有氧化性,是一种很好的电子受体,在光催化反应过程中可以捕获TiO2表面的光生电子,抑制光生电子与空穴的复合[17],从而提高分散液的光催化活性。因此,该分散液具有高的光催化活性与以下两个因素有关:1)纳米颗粒的高度分散,使纳米TiO2的光催化活性完全表现出来;2)体系中加入的微量双氧水,使体系的氧化性增强,同时抑制光生载流子的复合。
|
Download:
|
| 图 6 不同催化剂紫外光降解罗丹明B曲线 Fig. 6 Degradation curves of RhB solution using different photocatalysts | |
选取浓度为0.05 g/L的分散液,考察纳米TiO2在分散液中的分散稳定性与活性稳定性。
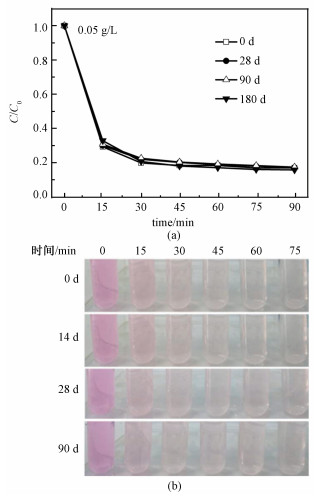
浓度为0.05 g/L的纳米TiO2分散液放置不同时间的照片如图 7所示。可看出,放置180 d后,该分散液仍呈半透明淡蓝色,且底部未见明显的TiO2沉淀,表明该分散液具有很好的分散稳定性。由于拍照时光线与角度未保持完全一致导致90 d时溶液颜色与0、28和180 d时溶液颜色稍有差别。该分散液的分散性与稳定性不受微量H2O2的影响。根据文献[18-19]报道,在TiO2的分散液中加入微量的H2O2,可以使体系变为黄色,因为H2O2与TiO2表面的羟基可以生成一种黄色的络合物,对TiO2起到敏化作用。在本分散液中加入微量H2O2后,分散液的颜色未发生变化,表明H2O2与TiO2表面的羟基形成了很少量的络合物。因此,H2O2对TiO2表面几乎没有修饰作用。图 8(a)与8(b)分别为0.05 g/L的纳米TiO2分散液放置不同时间,在紫外光照射下,降解罗丹明B的曲线与照片。可见,该分散液的催化活性在180 d内没有随时间的延长而降低,表明其具有很好的活性稳定性,同时也进一步证实材料的分散稳定性。

|
Download:
|
| 图 7 浓度为0.05 g/L的纳米TiO2分散液放置不同时间的照片 Fig. 7 Photographs of 0.05 g/L TiO2 dispersion solution aged for different days | |
|
Download:
|
| 图 8 纳米TiO2分散液放置不同时间后降解罗丹明B的曲线(a)与照片(b) Fig. 8 Degradation curves (a) and photographs (b) of photocatalytic degradation of RhB in TiO2 dispersion solution aged for different days | |
纳米TiO2在紫外光照射下,表现出超亲水性。将其喷涂在基底上成膜,可以提高基底的亲水性与自清洁能力。本文在铝板上喷涂不同层数的0.05 g/L的纳米TiO2分散液,测试基底表面接触角随时间的变化,考察其自清洁能力。
固体表面的亲水性与接触角呈负相关关系,即接触角越小,亲水性越强。如图 9所示,与光照前相比,光照5 h后,铝板的接触角大幅度减小,喷涂10层的样品更明显,接触角由84.1°减小到25.9°。当分散液喷涂层数较少时,铝板表面的纳米TiO2颗粒较少,未能将其表面紧密覆盖,光照后,接触角减小不明显。当喷涂层数较多时,纳米TiO2将铝板表面完全覆盖,光照后,接触角明显减小。

|
Download:
|
| 图 9 紫外光照前后喷涂分散液的铝板接触角的变化图 Fig. 9 Contact angles of aluminium plates sprayed with TiO2 dispersion solution before and after UV light irradiation | |
上述结果表明,喷涂分散液后,铝板表面由疏水转变为良好的亲水性。结合2.2节,该分散液具有很高的光催化活性,因此,经处理后的铝板具有良好的自清洁能力与光催化活性。
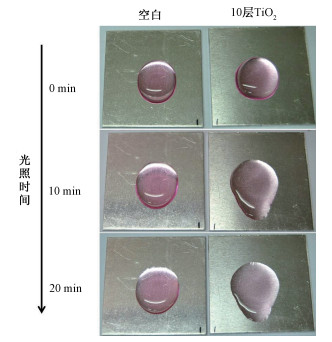
图 10为放置60 d后,喷涂10层纳米TiO2分散液的铝板与空白板在紫外光照下,降解相同浓度罗丹明B的对照图片。可看出,光照20 min后,经处理的铝板表面的罗丹明B几乎完全褪色,而空白板上无明显变化。结果表明,喷涂分散液后的铝板具有很强的自清洁能力。
|
Download:
|
| 图 10 喷涂分散液的铝板在紫外光照下降解罗丹明B的照片 Fig. 10 Photographs of photocatalytic degradation of RhB solution under UV light irradiation on aluminium plates before and after spraying TiO2 dispersion solution | |
本文采用沉淀-溶剂热联用的方法,合成粒度均匀的锐钛矿型纳米TiO2材料。无表面修饰与稳定剂,将该材料超声分散在去离子水中,即可获得分散均匀、稳定性好、光催化活性高的锐钛矿型纳米TiO2水性分散液,放置180 d后仍表现出良好的分散稳定性与活性稳定性。铝板基底上喷涂该分散液后,表现出良好的亲水性与自清洁能力。
| [1] |
Chen X B, Mao S S. Titanium dioxide nanomaterials:synthesis, properties, modifications, and applications[J]. Chemical Reviews, 2007, 107: 2891-2959. DOI:10.1021/cr0500535 |
| [2] |
Thompson T L, Yates J T. Surface science studies of the photoactivation of TiO2-New photochemical processes[J]. Chemical Reviews, 2006, 106: 4428-4453. DOI:10.1021/cr050172k |
| [3] |
Gordon T R, Cargnello M, Paik T, et al. Nonaqueous synthesis of TiO2 nanocrystals using TiF4 to engineer morphology, oxygen vacancy concentration, and photocatalytic activity[J]. Journal of the American Chemical Society, 2012, 134: 6751-6761. DOI:10.1021/ja300823a |
| [4] |
高濂, 郑珊, 张青红. 纳米氧化钛光催化材料及应用[M]. 北京: 化学工业出版社, 2002.
|
| [5] |
刘姗.纳米二氧化钛/水性聚氨酯复合材料的制备及其表征[D].合肥: 中国科学技术大学, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10358-1011284210.htm
|
| [6] |
Zhang W B, Fu J M, Xiao X M, et al. Treatment of organic pollutants in aqueous solution by homogenous and heterogeneous advanced oxidation processes[J]. Journal of the Graduate School of the Chinese Academy of Sciences, 2005, 22(1): 122-127. |
| [7] |
Feng X J, Jiang L. The synthesis and switchable surface wettability of one dimensional inorganic Nano-materials[J]. Journal of the Graduate School of the Chinese Academy of Sciences, 2007, 24(4): 537-542. |
| [8] |
Cheng X L, Hu M, Huang R, et al. HF-free synthesis of anatase TiO2 nanosheets with largely exposed and clean {001} facets and their enhanced rate performance as anodes of lithium-ion battery[J]. ACS Applied Materials & Interfaces, 2014, 6: 19176-19183. |
| [9] |
Wu Q, Wu Z J, Li Y L, et al. Controllable Synthesis and photocatalytic activity of anatase TiO2 single crystals with exposed {110} facets[J]. Chinese Journal of Catalysis, 2012, 33: 1743-1753. DOI:10.1016/S1872-2067(11)60448-8 |
| [10] |
Tarun K M, Chuen Y L. Synthesis, isolation, and redispersion of resorcinarene-capped anatase TiO2 nanopar-ticles in nonaqueous solvents[J]. Journal of Colloid and Interface Science, 2007, 310: 178-183. DOI:10.1016/j.jcis.2007.01.094 |
| [11] |
Saeed F. A review of polymeric dispersant stabilisation of titania pigment[J]. Advances in Colloid and Interface Science, 2009, 151: 24-32. DOI:10.1016/j.cis.2009.07.004 |
| [12] |
郝喜海, 李慧敏, 李菲, 等. 纳米二氧化钛的表面改性研究[J]. 无机盐工业, 2012, 44(1): 30-32, 42. DOI:10.3969/j.issn.1006-4990.2012.01.009 |
| [13] |
Bertrand F, German S A, Anwar A, et al. Dispersion and surface functionalization of oxide nanoparticles for transparent photocatalytic and UV-protecting coatings and sunscreens[J]. Science and Technology of Advanced Materials, 2013, 14: 023001. DOI:10.1088/1468-6996/14/2/023001 |
| [14] |
杨月锋, 任强, 李坚, 等. ARGET-ATRP合成双亲性嵌段共聚物及对二氧化钛分散效率的影响[J]. 化工学报, 2011, 62(6): 1756-1762. DOI:10.3969/j.issn.0438-1157.2011.06.042 |
| [15] |
张银芳, 熊祖江, 张秀芹, 等. 乳酸接枝纳米二氧化钛/聚乳酸复合物的制备[J]. 高分子材料科学与工程, 2016, 32(11): 145-149. |
| [16] |
Liu S W, Yu J G, Wang W G. Effects of annealing on the microstructures and photoactivity of fluorinated N-doped TiO2[J]. Physical Chemistry Chemical Physics, 2010, 12: 12308-12315. DOI:10.1039/c0cp00036a |
| [17] |
王有乐, 常德政, 袁金华. 双氧水助光催化降解直接大红染料废水的研究[J]. 兰州理工大学学报, 2007, 33(2): 70-72. DOI:10.3969/j.issn.1673-5196.2007.02.018 |
| [18] |
Li X Z, Chen C C, Zhao J C. Mechanism of photodecomposition of H2O2 on TiO2 surfaces under visible light irradiation[J]. Langmuir, 2001, 17: 4118-4122. DOI:10.1021/la010035s |
| [19] |
Liu T X, Li X M, Yuan X, et al. Enhanced visible-light photocatalytic activity of a TiO2 hydrosol assisted by H2O2:surface complexation and kinetic modeling[J]. Journal of Molecular Catalysis A:Chemical, 2016, 414: 122-129. DOI:10.1016/j.molcata.2016.01.011 |
 2018, Vol. 35
2018, Vol. 35 


