2. 南京大学医学院附属鼓楼医院感染管理办公室,江苏 南京 210008
2. Infection Management Office, Nanjing Drum Tower Hospital, The Affiliated Hospital of Nanjing University Medical School, Nanjing 210008, China
随着国民经济水平和医疗技术的飞速发展,内镜诊疗量急剧增加,内镜感染防控问题也接踵而至。内镜直接进入人体腔道,若清洗消毒不当,易导致严重的医院感染事件[1]。软式内镜材料精密、内部结构复杂,各种管道互相通联形成空腔和盲端,清洗消毒的难度较高,常采用化学消毒剂浸泡的方式进行消毒处理。内镜手工清洗消毒的操作流程包括预处理-测漏-清洗-漂洗-消毒-终末漂洗-干燥。《软式内镜清洗消毒技术规范》(WS 507—2016)[2]规定终末漂洗水应为纯化水或无菌水,并保证细菌总数≤10 CFU/100 mL。纯化水能降低生物总有机碳,减少细菌内毒素和微生物数量[3]。然而,纯化水过滤后缺乏余氯,无法抑制微生物生长,使管道内容易形成生物膜造成持续污染,而且制备工艺复杂,容易在生产、储存、运输过程中和使用终端等各个环节受到污染[4-9]。
纪学悦等[10]从天津市的终末漂洗水中分离出铜绿假单胞菌、蜡样芽孢杆菌、嗜水气单胞菌等,是造成内镜清洗消毒失败的重要原因之一,这些细菌大多是条件致病菌,容易通过内镜检查等方式造成交叉感染[11]。许多内镜感染的暴发和假暴发与受污染的终末漂洗水有关[12-15]。终末漂洗水合格可以提高内镜再处理的合格率(OR=4.078,95%CI:1.750~9.501)[8, 16]。因此,本研究旨在探讨晨间用水之前进行一定时长的排放能否提高内镜终末漂洗水的质量,以及合适的纯化水管路的消毒频率,为国内外规范的制定提供依据。
1 对象与方法 1.1 研究对象江苏省某三甲医院内镜中心的手工清洗工作站停止用水后末端管路残留的纯化水,终末漂洗水出水口见图 1。该内镜中心年工作量约10万例,每日工作量约450例,其管路使用年限为12年。
 |
| 图 1 终末漂洗水出水口和研究材料 Figure 1 Outlet of final rinse water and research materials |
无菌采样瓶,0.45 μm滤膜,营养琼脂培养基,见图 1。
1.3 研究方法第一阶段,晨间排放时间点的研究。管路消毒后每日早上6:00用75%乙醇消毒出水口,并将水龙头打开至最大(持续供水压力0.75 MPa),对内镜室两个终末漂洗水采样端口排放0、1、3、5、7 min后分别取水标本各100 mL进行微生物检测,根据5个时间组的平均菌落数找出最佳排放时间。每日两个端口共采样10份,连续监测35 d(5周),一共350份,每时间组70份。第二阶段,管路消毒频率的研究。根据第一阶段确定的晨间排放时间找出管路消毒的最佳频率。管路消毒后每日从两个采样口共采样2份,每周14份,连续监测5周,一共70份。
1.4 微生物检测方法微生物检测方法使用倾注琼脂法和滤膜法。使用漩涡混匀仪将装有终末漂洗水标本100 mL的无菌采样瓶充分振荡后,分别取水标本1.0 mL平行接种于两个平皿,置于(36±1)℃恒温箱培养48 h,计数菌落数。将剩余98 mL终末漂洗水标本在无菌操作下采用滤膜(0.45 μm)过滤浓缩,将滤膜接种在凝固的营养琼脂平皿上,置于(36±1)℃恒温箱培养48 h,计数菌落数。
1.5 观察指标和判断标准(1) 两个平行平皿和滤膜上的菌落数之和为水标本的菌落总数(CFU/100 mL)。
(2) 根据《软式内镜清洗消毒技术规范》(WS 507—2016)对清洗消毒室纯化水的要求,菌落总数≤10 CFU/100 mL为阴性,反之为阳性。倾注琼脂法和滤膜法微生物检测结果展示,如图 2。
 |
| 图 2 倾注琼脂法和滤膜法微生物检测结果展示 Figure 2 Microbial detection results by agar pouring method and filter membrane method |
对研究者、洗消员进行统一的标准化理论与操作培训,微生物采样和检测由一名固定研究者完成,每次微生物检测前对仪器进行标准化校正,确保实施及测量标准化。数据录入采用双人两次录入且进行一致性检验,保证录入数据的准确性。采样时由一人用秒表记时,发出“起、停”指令,另一人负责采集水标本。
1.7 统计分析应用SPSS 26.0对数据进行统计分析。正态分布的计量资料以均数±标准差(x±s)表示,偏态分布的计量资料以中位数及四分位数[M(P25,P75)]表示。服从正态分布时,组间比较采用单因素方差分析,组间比较前先进行方差齐性检验,方差齐时采用LSD法进行两两比较,方差不齐时采用Kruskal-Wallis秩和检验或Tamhane’s T2(M)。不服从正态分布时,组间比较采用Kruskal-Wallis秩和检验,两两比较采用Bonferroni校正。计数资料以绝对数或百分比表示。检验水准为双侧α=0.05,P≤0.05为差异有统计学意义。
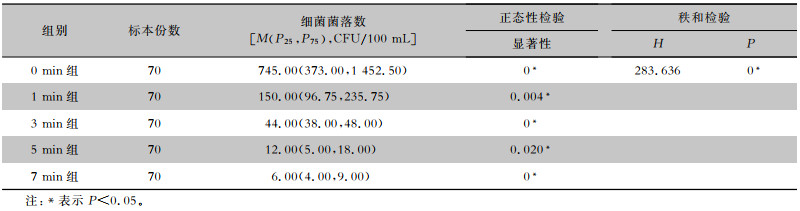
2 结果 2.1 终末漂洗水晨间排放时间研究终末漂洗水不同晨间排放时间点采样,监测结果显示,0 min、1 min、3 min、5 min组菌落中位数均>10 CFU/100 mL,7 min组菌落中位数<10 CFU/100 mL。5组菌落数合格率依次为2.86%、2.86%、2.86%、41.43%、85.71%。细菌菌落数数据不服从正态分布,5组数据相互独立,故采用多样本的Kruskal-Wallis H检验,结果显示,不同时间点采样终末漂洗水细菌菌落数比较,差异存在统计学意义(H=283.636,P<0.001),见表 1。5组终末漂洗水细菌数两两比较,Bonferroni多重比较结果显示,5 min组与7 min组之间差异无统计学意义(P=1.000),其他各组之间差异均有统计学意义(均P<0.05)。5组不同晨间排放时间终末漂洗水细菌数折线图,见图 3。根据结果,最佳晨间排水时间为7 min。
| 表 1 终末漂洗水不同排放时间点采样细菌监测结果及比较 Table 1 Comparison of bacterial monitoring results of final rinse water samples at different discharge time points |
|
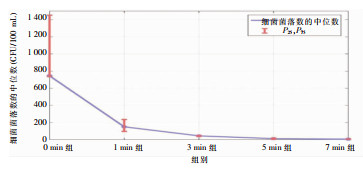 |
| 图 3 5组不同晨间排放时间终末漂洗水细菌菌落数折线图 Figure 3 Line chart of bacterial colony numbers in final rinse water from 5 time points of morning discharge |
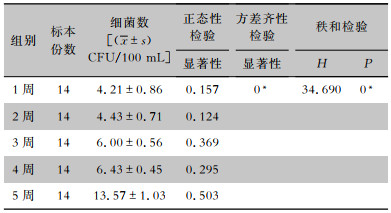
监测结果显示,管路消毒后不同时间点(消毒后1、2、3、4、5周)采样,终末漂洗水细菌菌落数平均值分别为4.21、4.43、6.00、6.43、13.57 CFU/100 mL,细菌菌落数合格率分别为100%、100%、100%、100%、28.57%。各组数据相互独立,均服从正态分布且方差不齐,故采用多样本的Kruskal-Wallis H检验,结果显示,纯化水管路消毒后不同时间点采样,终末漂洗水细菌菌落数比较,差异存在统计学意义(H=34.690,P<0.001),见表 2。两两比较采用Bonferroni多重比较,结果显示,纯化水管路消毒后1、2、3、4周与5周之间差异均有统计学意义(均P<0.05),1、2、3、4周之间差异均无统计学意义(均P>0.05)。根据结果,纯化水管路最佳消毒频率确定为每4周一次。
| 表 2 纯化水管路消毒后连续5周的终末漂洗水细菌监测结果 Table 2 Bacterial colony numbers in final rinse water for 5 consecutive weeks after purified water pipeline was disinfected |
|
终末漂洗作为内镜消毒后的最终漂洗环节,终末漂洗水的质量关系着整个消毒结果最终是否合格,以及后续发生医院感染的风险[17]。2020年上海市30所三级医疗机构的终末漂洗水合格率仅63.09%[17],2016—2020年天津市16个区的医疗机构终末漂洗水合格率仅50%[10],2012—2015年山东省不同级别医疗机构的内镜中心终末漂洗水有70.3%甚至超过了100 CFU/mL[18]。Willis[12]连续4个月监测20个内镜中心的终末漂洗水,发现超过60%的终末漂洗水不符合规范。以上文献均显示,内镜清洗消毒失败的原因与终末漂洗水合格率不足有关,保证终末漂洗用水质量是预防内镜感染的重要手段之一。
本次调查结果显示,内镜终末漂洗水排放0、1、3、5、7 min时的细菌中位数分别为745.00、150.00、44.00、12.00、6.00 CFU/100 mL,不同时间组终末漂洗水细菌菌落数折线图显示,0 min与1 min时的终末漂洗水细菌菌落数呈现断崖式转折,而且最初排放(即0 min时)的那一段甚为严重,残留在末端管路内的终末漂洗水存在一定程度的微生物污染。纯化水不含氯,长时间滞留在末端管路内,反而有利于微生物生长,如果再次用水前没有排放残水,直接用来漂洗消毒后的内镜,可能导致内镜的二次污染[19]。
3.2 内镜终末漂洗水需要晨间排放残水国内以往文献对于终末漂洗水晨间排放时间缺乏一致的结论,同时也缺乏具体的试验研究和数据支持用于指导临床。不同文献认为早上用水之前应排放终末漂洗水1~2 min[19]、10~15 min[6],采集水标本之前需要排放终末漂洗水1 min[5, 8, 20-22]、5 min[23]、10 min[19],但均未提供数据支持。《口腔综合治疗台水路清洗消毒技术规范》指出,口腔综合治疗台水标本宜在每日开诊前,连续放水30 s后采集。《血液净化标准操作规程》2021版指出,血液净化处理用水需放水至少60 s后采集。但口腔科和血液净化对于纯化水的要求均为菌落数≤100 CFU/mL(即10 000 CFU/100 mL),而内镜对于纯化水的要求为菌落数≤10 CFU/100 mL,远高于血液净化和口腔科对纯化水的要求,意味着内镜中心需要在终末漂洗水质量控制方面付出更多的努力。
本研究对排放0、1、3、5、7 min后的终末漂洗水细菌菌落数进行统计分析发现,5 min组与7 min组之间差异无统计学意义,其他各组之间差异均有统计学意义;然而排放5 min时细菌菌落的中位数仍>10 CFU/100 mL,但排放7 min时细菌菌落的中位数达到合格范围,因此确定内镜中心晨间排残水时间为7 min。
3.3 内镜纯化水管路需要定期消毒Pang等[14]研究发现,终末漂洗水标本中有54%培养出铜绿假单胞菌,并认为是供水管路的生物膜污染了终末漂洗水。王晓蕾等[24]对其医院纯化水细菌总数超标问题进行溯源,发现过滤器更换不及时和定期消毒维护不充分导致了污染,因此需要对纯化水及其管路定期监测和消毒。若纯化水管路长期未消毒,内镜内壁可形成以奥斯陆莫拉菌、嗜麦芽窄食单胞菌、铜绿假单胞菌、藤黄微球菌等水生类细菌为主的生物膜,对内镜的消毒和感染防控造成巨大挑战[25]。虽然纯化水管路保持不间断循环运行,但分支末端管路仍存在部分死腔。停止用水后,末端管路的水呈静止状态,一定时长后容易滋生微生物,若不进行有效干预,可能会导致内镜清洗消毒环节的二次污染[26],因此纯化水管路的消毒频率尤为重要。Marek等[27]通过反渗透系统,定期进行纯化水管路的消毒,2008—2013年连续5年未从内镜管腔中检出假单胞菌、环境分枝杆菌和军团菌,但目前国内外对于纯化水管路的消毒并未制定明确的规范指南和专家共识。
本研究结果显示,对纯化水管路消毒后1、2、3、4周终末漂洗水采样,细菌菌落数平均值均在合格范围,而第5周的终末漂洗水细菌菌落数为超标状态。多重比较结果显示,1、2、3、4周与5周之间差异均有统计学意义,1、2、3、4周之间差异均无统计学意义。因此,纯化水的管路消毒频率确定为每4周一次,与国内学者[23, 28]研究结果一致。纯化水过滤后因缺乏余氯,无法抑制微生物生长,如果连续使用而不进行消毒处理,管路内可能会不断滋生微生物,影响供水质量[28],因此确定消毒频率是关键。
该内镜中心纯化水的管路设计较久远,分支管路长度大约40 m,管外径20.00 mm,存在末端管路纯化水滞留的问题,有一定的微生物污染风险,需要在晨间用水之前进行排放。本次研究结果表明,残留在末端管路内的终末漂洗水存在一定程度的污染,建议晨间排放7 min后再开始用水,并每隔4周对纯化水管路进行消毒。本研究的创新点在于从终末漂洗水的晨间排放时间和管路消毒频率两个角度开展微生物检测,以提高纯化水用水质量。本研究仅代表单中心的管路设计和工作安排,未来需要更多中心的研究数据为内镜用水工作提供参考。由于各家医院纯化水管路的建筑设计不尽相同,但总有盲端的存在,因此需要关注末端水的排放问题。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
李阳, 姜亦虹. 医疗机构消化内镜清洗消毒历史和现状调查[J]. 中国感染控制杂志, 2017, 16(10): 960-962, 965. Li Y, Jiang YH. History and current situation of digestive endoscope cleaning and disinfection in domestic medical institutions[J]. Chinese Journal of Infection Control, 2017, 16(10): 960-962, 965. DOI:10.3969/j.issn.1671-9638.2017.10.015 |
| [2] |
中华人民共和国国家卫生和计划生育委员会. 软式内镜清洗消毒技术规范WS 507—2016[J]. 中国感染控制杂志, 2017, 16(6): 587-592. The National Health and Family Planning Commission of the People's Republic of China. Regulation for cleaning and disinfection technique of flexible endoscopes WS 507—2016[J]. Chinese Journal of Infection Control, 2017, 16(6): 587-592. |
| [3] |
吴丹丹. 纯化水终端管路改良及集中式管理在内镜中心消毒质量控制中的应用研究[D]. 合肥: 安徽医科大学, 2020. Wu DD. Application of terminal pipeline improvement and centralized management in disinfection quality control of endoscopy center[D]. Hefei: Anhui Medical University, 2020. |
| [4] |
朱炫瑞, 庄宜锦, 刘文龙, 等. 吉林省72所医疗机构软式内镜终末漂洗用水管理现状调查[J]. 中国感染控制杂志, 2022, 21(7): 642-650. Zhu XR, Zhuang YJ, Liu WL, et al. Management status of final rinsing water for flexible endoscopes in 72 medical institutions in Jilin Province[J]. Chinese Journal of Infection Control, 2022, 21(7): 642-650. |
| [5] |
曾其莉, 江永忠, 李艳伟, 等. 医疗机构内镜终末漂洗水微生物污染调查与风险分析[J]. 中国消毒学杂志, 2022, 39(3): 203-205, 210. Zeng QL, Jiang YZ, Li YW, et al. Investigation and risk analysis of microbial contamination of endoscopic final rinse water in medical institution[J]. Chinese Journal of Disinfection, 2022, 39(3): 203-205, 210. |
| [6] |
周晓红, 李晓君, 郭健芬, 等. 一起胃肠镜终末漂洗水微生物检测超标事件的干预处置报告[J]. 中国消毒学杂志, 2022, 39(3): 239-240. Zhou XH, Li XJ, Guo JF, et al. An report of exceeding the standard in microbiological detection of final rinsing water for gastrointestinal endoscopy[J]. Chinese Journal of Disinfection, 2022, 39(3): 239-240. |
| [7] |
张枭然, 阎颖, 千新玲, 等. 新建内镜中心验收时纯水系统染菌情况调查与处置[J]. 中国感染控制杂志, 2021, 20(12): 1114-1118. Zhang XR, Yan Y, Qian XL, et al. Investigation and disposal of bacterial contamination in pure water system during accep-tance of newly built endoscopy center[J]. Chinese Journal of Infection Control, 2021, 20(12): 1114-1118. DOI:10.12138/j.issn.1671-9638.20218313 |
| [8] |
纪学悦, 宁培勇, 费春楠, 等. 2016年—2020年天津市胃肠道内镜再处理评估效果的多因素分析[J]. 中国内镜杂志, 2021, 27(9): 1-7. Ji XY, Ning PY, Fei CN, et al. Multivariate analysis of the evaluation on gastrointestinal endoscopic reprocessing in Tianjin, China, 2016-2020[J]. China Journal of Endoscopy, 2021, 27(9): 1-7. |
| [9] |
Zhao L, Liu YW, Li N, et al. Response of bacterial regrowth, abundant and rare bacteria and potential pathogens to secondary chlorination in secondary water supply system[J]. Sci Total Environ, 2020, 719: 137499. DOI:10.1016/j.scitotenv.2020.137499 |
| [10] |
纪学悦, 费春楠, 刘军, 等. 天津市消化内镜使用情况调查及消毒灭菌的影响因素分析[J]. 中华医院感染学杂志, 2017, 27(14): 3354-3357. Ji XY, Fei CN, Liu J, et al. Situation of use of gastrointestinal endoscopes and influencing factors for disinfection and ste-rilization in Tianjin[J]. Chinese Journal of Nosocomiology, 2017, 27(14): 3354-3357. |
| [11] |
Gillespie TG, Hogg L, Budge E, et al. Mycobacterium chelonae isolated from rinse water within an endoscope washer-disinfector[J]. J Hosp Infect, 2000, 45(4): 332-334. |
| [12] |
Willis C. Bacteria-free endoscopy rinse water-a realistic aim?[J]. Epidemiol Infect, 2006, 134(2): 279-284. DOI:10.1017/S0950268805005066 |
| [13] |
Walker JT, Bak A, Marsden G, et al. Final rinse water quality for flexible endoscopy to minimize the risk of post-endosco-pic infection. Report from Healthcare Infection Society Working Party[J]. J Hosp Infect, 2022, 124: 79-96. DOI:10.1016/j.jhin.2022.02.022 |
| [14] |
Pang JL, Perry P, Ross A, et al. Bacteria-free rinse water for endoscope disinfection[J]. Gastrointest Endosc, 2002, 56(3): 402-406. DOI:10.1016/S0016-5107(02)70046-1 |
| [15] |
Muscarella LF. Application of environmental sampling to flexible endoscope reprocessing: the importance of monitoring the rinse water[J]. Infect Control Hosp Epidemiol, 2002, 23(5): 285-289. DOI:10.1086/502053 |
| [16] |
Ji XY, Ning PY, Fei CN, et al. The importance of sampling technique and rinse water for assessing flexible gastrointestinal endoscope reprocessing: a 3-year study covering 59 centers[J]. Am J Infect Control, 2020, 48(1): 19-25. DOI:10.1016/j.ajic.2019.07.008 |
| [17] |
史庆丰, 胡必杰, 崔扬文, 等. 上海市30所三级医疗机构软式内镜终末漂洗水现状调查[J]. 中华医院感染学杂志, 2020, 30(6): 923-926. Shi QF, Hu BJ, Cui YW, et al. Current status of final rinse water for flexible endoscopes in 30 tertiary medical institutions of Shanghai[J]. Chinese Journal of Nosocomiology, 2020, 30(6): 923-926. |
| [18] |
杨彬. 2013—2015年山东省医疗机构感染控制现状及其相关危险因素研究[D]. 济南: 山东大学, 2016. Yang B. Study on status of the infection control and related risk factors in medical institutions in Shandong Province during 2013-2015[D]. Jinan: Shandong University, 2016. |
| [19] |
朱彩霞, 李桂明, 劳婉仪. 内镜清洗用水的质量控制与管理[J]. 医疗装备, 2021, 34(18): 47-49. Zhu CX, Li GM, Lao WY. Quality control and management of endoscope cleaning water[J]. Medical Equipment, 2021, 34(18): 47-49. |
| [20] |
邓秀梅, 文清德, 蒋雪丽, 等. 内镜中心水处理系统异常情况分析与对策[J]. 中国消毒学杂志, 2022, 39(11): 879-880. Deng XM, Wen QD, Jiang XL, et al. Analysis and countermeasures of abnormal conditions in endoscopy central water treatment system[J]. Chinese Journal of Disinfection, 2022, 39(11): 879-880. |
| [21] |
纪学悦, 宁培勇, 费春楠, 等. 软式内镜再处理质量的评价方法研究[J]. 中国消毒学杂志, 2021, 38(7): 552-554. Ji XY, Ning PY, Fei CN, et al. Study on evaluation method of reprocessing quality of flexible endoscopy[J]. Chinese Journal of Disinfection, 2021, 38(7): 552-554. |
| [22] |
宁培勇, 纪学悦, 丁津华, 等. 不同检测方法对内镜消毒效果监测的应用性研究[J]. 中国内镜杂志, 2019, 25(6): 67-71. Ning PY, Ji XY, Ding JH, et al. Different test methods for detecting disinfection effect of endoscope[J]. China Journal of Endoscopy, 2019, 25(6): 67-71. |
| [23] |
吴丹丹, 赵梅, 佘婷婷, 等. 内镜中心改良的医用纯化水终端管路在纯化水质量管理中的应用研究[J]. 中华医院感染学杂志, 2020, 30(11): 1757-1760. Wu DD, Zhao M, She TT, et al. Application of improved medical purified water terminal pipeline in endoscopic center for purified water quality management[J]. Chinese Journal of Nosocomiology, 2020, 30(11): 1757-1760. |
| [24] |
王晓蕾, 范晶晶, 沈益鸣, 等. 某医院集中式纯水供应系统微生物污染情况和消毒效果调查[J]. 中国消毒学杂志, 2019, 36(12): 913-915. Wang XL, Fan JJ, Shen YM, et al. Investigation on microbial contamination and disinfection effect of centralized pure water supply system in a hospital[J]. Chinese Journal of Disinfection, 2019, 36(12): 913-915. |
| [25] |
王萍, 韩梦鸽, 沈国锋, 等. 持续性次氯酸消毒对内镜终末漂洗水的消毒效果[J]. 中国感染控制杂志, 2022, 21(7): 617-622. Wang P, Han MG, Shen GF, et al. Disinfection effect of persistent hypochlorous acid on final rinsing water for endoscope[J]. Chinese Journal of Infection Control, 2022, 21(7): 617-622. |
| [26] |
王伟民, 马久红. 消化内镜清洗消毒失败的相关原因及应对策略[J]. 中华医院感染学杂志, 2017, 27(17): 4077-4080. Wang WM, Ma JH. Reasons and countermeasures of disinfection failure of digestive endoscopy[J]. Chinese Journal of Noso-comiology, 2017, 27(17): 4077-4080. |
| [27] |
Marek A, Smith A, Peat M, et al. Endoscopy supply water and final rinse testing: five years of experience[J]. J Hosp Infect, 2014, 88(4): 207-212. |
| [28] |
付桂枝, 张晓秀. 消毒供应中心纯化水管路的消毒管理与监测[J]. 中国消毒学杂志, 2015, 32(10): 1036-1037. Fu GZ, Zhang XX. Disinfection management and monitoring of purified water pipes in disinfection supply center[J]. Chinese Journal of Disinfection, 2015, 32(10): 1036-1037. |



