空气污染严重影响人体健康。空气污染物主要包括SO2、NOX、CO、O3和大气颗粒物。可吸入颗粒物(大气颗粒物中空气动力学直径≤2.5 μm的细颗粒物,PM2.5)和人体健康密切相关,它可经过呼吸道进入支气管和肺部。大量流行病学调查研究表明,可吸入颗粒物与人类呼吸系统疾病的发病率和死亡率密切相关,可引起哮喘、肺功能下降、呼吸系统炎症,甚至累及心血管系统、神经系统、免疫系统,促进癌症发生[1-5]。随着环境破坏日益加重,空气污染尤其是PM2.5污染日益加重,引起世界普遍关注。本研究选用PM2.5空气污染物所致Wistar大鼠肺损伤模型,动态观察PM2.5空气污染物致炎症损伤过程中肺部炎症细胞因子的变化情况,旨在探索PM2.5空气污染物导致炎症损伤的致病机制。
1 材料与方法 1.1 主要仪器与试剂Hi-Vol PM2.5高通量(1.13 m3/min)粉尘采样器(美国Tisch Environmental Inc公司),硝化棉滤膜(美国GE公司),KQ-100DB型数控超声波清洗器(河南兄弟仪器设备有限公司),8050F液气类动式染毒控制装置(天津合普公司),PCR扩增仪(德国T3 thermocycle公司),ABI Prism 7500荧光实时定量PCR仪(美国Applied Biosystems公司),NanoDrop ND-2000分光光度计(美国Thermo Fisher Scientific公司)。TRIZOL Reagent、SYBR Select Master Mix(美国Thermo Fisher Scientific公司),大鼠酶联免疫法(ELISA)试剂盒(美国R & D公司)。
1.2 PM2.5空气污染物与有毒气体制备 1.2.1 PM2.5颗粒物采集选用日本120F型大流量粉尘采样器和上海恒生玻璃纤维滤纸, 采样流量1 000 L /min, 在沈阳市区交通要道每天连续采样24 h, 共采集2个月。采样后将滤纸剪成1 cm2小块, 置于蒸馏水中超声处理, 6层无菌纱布过滤,将滤液10 000 r/min离心20 min, 收集底层颗粒物,上清液继续收集颗粒物,最后将浓缩上清液及所有底层颗粒物真空冷冻干燥, -80 ℃保存。
1.2.2 有毒气体制备本研究所用SO2、NO2、CO混合气(低、中、高3种浓度)由具有国家标准物质资质认证的大连特种气体产业公司提供。染毒时混合气的动态浓度控制在国家空气质量标准的1、10及100倍。
1.3 分组与处理90只10~12周雄性Wistar大鼠,北京维通利华实验动物中心提供,许可证号:SCXK(京) 2007-0001,常规饲养于沈阳医学院实验动物研究中心的SPF(specific pathogen free)级动物室内,12 h光照,温度22~24 ℃,湿度(55±15)%。将90只大鼠随机分为12组:9个染尘染毒组(低、中、高剂量染尘染毒组分别染尘染毒1、7、30 d),每组8只,3个对照组(1、7、30 d),每组6只。(1) 染尘:大鼠乙醚麻醉,采用气管非暴露式注入染尘方法,经气管注入1 mL含PM2.5生理盐水混悬液(低、中、高剂量组分别含PM2.5 0.04、0.40、4.00 mg),对照组大鼠注入1 mL生理盐水。(2) 染毒:染尘后第2天各组大鼠动式染毒,采用液气类动式染毒控制装置,在3个体积为0.3 m3的有机玻璃染毒柜中分别放入低、中、高剂量染毒组大鼠,CO、SO2、NO2气体的浓度分别为低剂量组4、0.15、0.12 mg/m3,中剂量组40、1.50、1.20 mg/m3,高剂量组400、15.00、12.00 mg/m3,每天染毒4 h,对照组大鼠吸入正常空气。分别于染毒结束后第2天将大鼠处死。常规乙醚麻醉,用3 mL生理盐水灌洗支气管肺泡,共3次,合并肺泡灌洗液(bronchoalveolar lavage fluid, BALF),离心,上清液-80 ℃冻存。肺组织置于无RNA酶的EP管中,-80 ℃冻存。
1.4 指标与方法 1.4.1 BALF中炎症细胞因子含量检测采用ELISA法,检测BALF中白细胞介素-4(interleukin-4,IL-4)、IL-6、γ干扰素(interferon gamma,IFN-γ)、肿瘤坏死因子-α(tumor necrosis factor alpha,TNF-α)含量。分别设标准品孔,待测样品孔,每孔分别加标准品或待测样品100 μL,混匀,37 ℃孵育120 min;洗板机吸干液体,每孔加入100 μL生物素标记的抗体工作液(IL-4、IL-6、IFN-γ、TNF-α均1: 10 000),37 ℃孵育1 h;每孔加200 μL洗液,洗板3次;每孔加入100 μL辣根过氧化物酶标记的亲和素工作液,37 ℃孵育1 h;每孔加200 μL洗液,洗板5次;每孔加90 μL底物工作液,37 ℃避光显色30 min后每孔加50 μL终止液。反应终止后5 min内酶标仪检测吸光度(A)值,检测波长为450 nm。
1.4.2 肺组织中炎症细胞因子mRNA表达检测采用qPCR法检测肺组织中IL-4、IL-6、IFN-γ、TNF-α mRNA表达量。按照试剂盒说明书提取大鼠肺组织总RNA,进行mRNA反转录、real-time PCR反应。基因引物由上海生工生物工程技术服务有限公司合成。基因引物序列如下:IL-4:上游5′CGAGCTCACTCTCTGTGGTG3′,下游5′GAACGAGGTCACAGGAGAA3′;IL-6:上游5′GCTGGAGTCACAGAAGGAG3′,下游5′GGCATAACGCACTAGGTTT3′;IFN-γ:上游5′GCGTCATTGAATCACACCTG3′,下游5′GAGCTCATTGAATGCTTGGC3′;TNF-α:上游5′GCCAGCCGATGGGTTGTA3′,下游5′GGTTGACTTTCTCCTGGTATG3′;磷酸甘油醛脱氢酶(reduced glyceraldehyde-phosphate dehydrogenase,GAPDH):上游5′CTCATGACCACAGTCCATGC3′, 下游5′TTCA-GCTCTGGGATGACCTT3′。PCR反应条件:95 ℃ 1 min,95 ℃10 s,60 ℃30 s,共40个循环。
1.5 统计分析计量资料以x±s表示,应用SPSS 18.0软件对数据进行统计分析,组间比较采用单因素方差分析后进行多重比较,以P<0.05为差异有统计学意义。
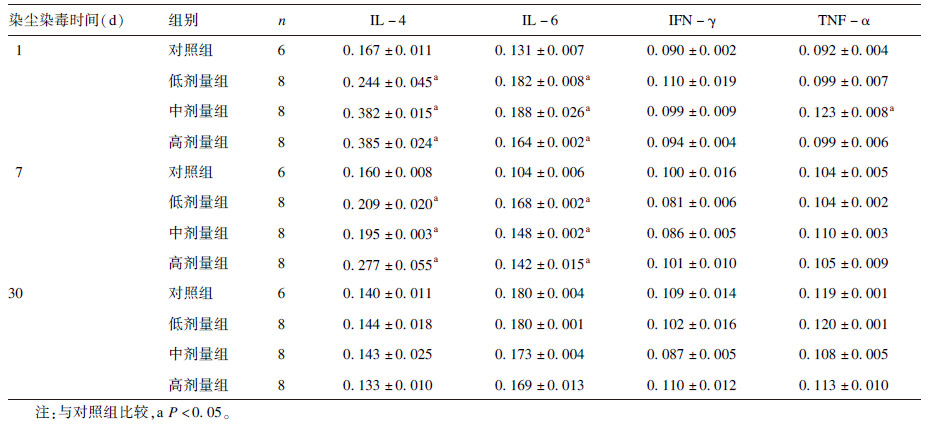
2 结果 2.1 染尘染毒对大鼠BALF中炎症细胞因子含量影响(表 1)| 表 1 染尘染毒对大鼠BALF中炎症细胞因子表达影响(x±s) |
染尘染毒1、7 d时,与对照组比较,各剂量染尘染毒组大鼠BALF中IL-4、IL-6含量均升高,差异有统计学意义(P<0.05);染尘染毒1 d时,中剂量染尘染毒组大鼠BALF中TNF-α含量高于对照组,差异有统计学意义(P<0.05);染尘染毒30 d时,与对照组比较,各剂量染尘染毒组大鼠BALF中各细胞因子含量无明显差异。
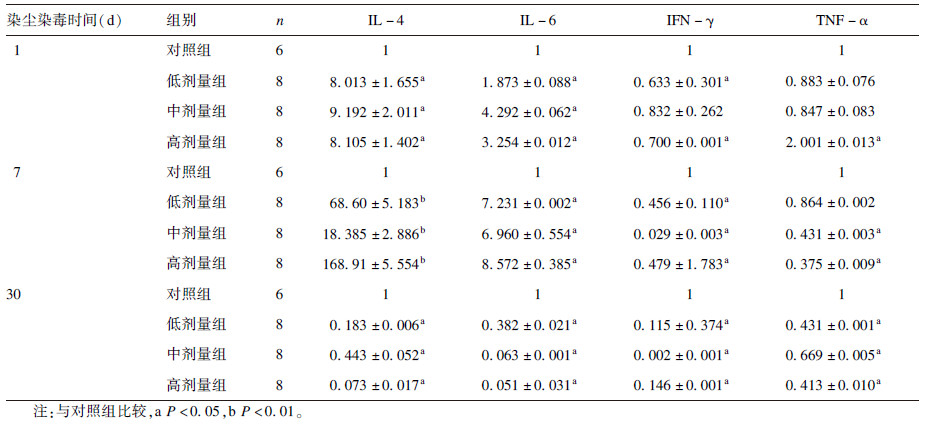
2.2 染尘染毒对大鼠肺组织中炎症细胞因子mRNA表达影响(表 2)| 表 2 染尘染毒对大鼠肺组织中炎症细胞因子mRNA表达影响(x±s) |
染尘染毒1 d时,与对照组比较,各剂量染尘染毒组大鼠肺组织中IL-4、IL-6 mRNA表达均升高,低、高剂量染尘染毒组大鼠肺组织中IFN-γ mRNA表达下降,高剂量染尘染毒组大鼠肺组织中TNF-α mRNA表达升高,差异均有统计学意义(P<0.05);染尘染毒7 d时,与对照组比较,各剂量染尘染毒组大鼠肺组织中IL-4、IL-6 mRNA表达明显升高,IFN-γ mRNA表达下降,中、高剂量染尘染毒组大鼠肺组织中TNF-α mRNA表达下降,差异有统计学意义(P<0.05);染尘染毒30 d时,各剂量染尘染毒组大鼠肺组织中各种炎症细胞因子mRNA表达均明显下降,差异有统计学意义(P<0.05)。
3 讨论空气污染物是由多种污染物组成的成分复杂的混合物,空气污染物主要通过呼吸道进入人体,气态污染物和颗粒污染物均能引起呼吸系统的病理生理变化[6]。粒径≤2.5 μm的细颗粒物(PM2.5)对空气质量和能见度均有重要影响,对人体健康影响更大。中国已于2012年将PM2.5列入环境空气质量检测指标。流行病学研究表明,长期暴露于空气污染物中的人群,其死亡率与空气污染物的浓度呈正相关。
目前认为,Th1/Th2(T helper type 1/ T helper type 2) 功能平衡在机体抗感染中至关重要[7]。Th1细胞主要分泌IL-2、IFN-γ,诱发巨噬细胞活化,从而增强其吞噬能力。Th2细胞主要分泌IL-4、IL-5、IL-6等,不利于抗原物质的清除。Th1和Th2细胞因子可促进本亚群、抑制另一亚群的生长分化。TNF-α主要由单核-巨噬细胞产生,在局部炎症反应中起重要作用;同时,TNF-α还具有活化巨噬细胞功能[8]。在鼠和人类细胞中,IFN-γ是通过上调的主要组织相容性复合体表达来活化巨噬细胞,产生一氧化氮及后继细胞因子[9]。而且IFN-γ可作为前炎症性细胞因子,诱导IL-12分泌,促进Th0细胞向Th1细胞分化,活化更多的效应细胞和细胞毒性细胞。IL-4、IL-6则起相反作用,可抑制巨噬细胞活化,阻断大多数IFN-γ活化巨噬细胞后的效应,并增加嗜酸性粒细胞趋化因子的表达,加重气道炎症反应[10]。本研究结果显示,染尘染毒1、7、30 d时,与对照组比较,大鼠BALF中IL-4、IL-6、TNF-α含量均表现为先升高后下降趋势,而IFN-γ水平变化不明显。提示,在PM2.5大气混合污染物致大鼠呼吸系统炎症损伤过程中,体液免疫应答占主导地位,而细胞免疫应答受到抑制,Th1/Th2平衡失调,不能刺激Th1保护性免疫反应;巨噬细胞清除PM2.5大气混合污染物动力不足。
| [1] | Ding PH, Wang GS, Guo YL, et al. Urban air pollution and meteorological factors affect emergency department visits of elderly patients with chronic obstructive pulmonary disease in Taiwan[J]. Environ Pollut, 2017, S0269-7491(16): 30887–30889. |
| [2] | Roberts S, Martin MA. Methods for bias reduction in time-series studies of particulate matter air pollution and mortality[J]. J Toxicol Envkon Health A, 2007, 70(8): 665–675. DOI:10.1080/15287390600974668 |
| [3] | Ostro B, Broadwin R, Green S, et al. Fine particulate air pollution and mortality in nine Califomia counties:results from CALFINE[J]. Environ Health Perspect, 2006, 114(1): 29–33. DOI:10.1289/ehp.8335 |
| [4] | Weber SA, Insaf TZ, Hall ES, et al. Assessing the impact of fine particulate matter (PM2.5) on respiratory-cardiovascular chronic diseases in the New York City Metropolitan area using hierarchical Bayesian model estimates[J]. Environ Res, 2016, 151: 399–409. DOI:10.1016/j.envres.2016.07.012 |
| [5] | Takizawa H. Impacts of particulate air pollution on asthma:current understanding and future perspectives[J]. Recent Pat Inflamm Allergy Drug Discov, 2015, 9(2): 128–135. |
| [6] | Ma M, Li S, Jin H, et al. Characteristics and oxidative stress on rats and traffic policemen of ambient fine particulate matter from Shenyang[J]. Science of the Total Environment, 2015, 526: 110–115. DOI:10.1016/j.scitotenv.2015.04.075 |
| [7] | 许淑云, 刘晓晴. 细胞因子和急性肺损伤[J]. 国外医学:呼吸系统分册, 2001, 21(4): 197–199. |
| [8] | 刘红菊, 李元桂, 毕爱华, 等. 肿瘤坏死因子在急性肺损伤发病机制中的作用[J]. 国外医学:免疫学分册, 1996(5): 229–231. |
| [9] | Chiu BL, Li CH, Chang CC. Selective modulation of MHC class Ⅱ chaperons by a novel IFN-γ-inducible class Ⅱ transactivator variant in lung adenocarcinoma A549 cells[J]. Biochem Biophys Res Commun, 2013, 440(1): 190–195. DOI:10.1016/j.bbrc.2013.09.066 |
| [10] | 肖纯凌, 席淑华, 王任群, 等. 大气污染对大鼠细胞因子的影响[J]. 中国公共卫生, 2003, 19(7): 839–840. DOI:10.11847/zgggws2003-19-07-47 |
 2017, Vol. 33
2017, Vol. 33