2. 广西医科大学实验动物中心
锰是人体必需微量元素之一,但锰过量摄入会毒害中枢神经系统〔1〕。有研究表明,锰还可以引起空间学习记忆障碍等大脑边缘系统损害症状,而海马是边缘系统的主要组成部位〔2〕。目前有关锰对边缘系统神经毒性作用研究较少,安全可靠的治疗药物尚未被发现;牛磺酸是条件必需氨基酸,近年来,越来越多的研究证明牛磺酸在对抗外源性毒物、保护神经功能方面有良好效果〔3, 4〕。本研究通过观察牛磺酸对锰所致体外培养海马神经元损伤的干预作用,拟为锰对大脑边缘系统的损伤研究及其治疗药物的发现提供科学依据。
1 材料与方法 1.1 主要试剂与仪器Dulbecco minimum essential media (DMEM)(美国Hyclone公司);胎牛血清、牛磺酸(美国Sigma 公司);氯化锰(天津市博迪化工有限公司);乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒(南京建成生物工程研究所);AnnexinV-FITC/PI双染细胞凋亡检测试剂盒(上海起福生物科技有限公司);其余试剂均为国产分析纯。HF safe 1200安全柜(香港热力发展有限公司);CO2培养箱(上海 Galaxys公司);CK40倒置相差显微镜(日本OLYMPUS公司);6010紫外-可见分光光度计(上海惠普有限公司);EPICS XL分析型流式细胞仪(美国Beckman公司);HITACHI H- 7650透射电子显微镜(日本日立公司)。
1.2 实验动物SPF级新生24h内的Wistar大鼠(广西医科大学医学实验动物中心,许可证号:SCXK桂2009-0002),体重15~30g。
1.3 方 法 1.3.1 神经元培养及鉴定新生Wistar大鼠于无菌条件下断头取脑,分离出双侧海马,制备成均匀细胞悬液,调整细胞密度至5 × 105个/mL,接种到培养板,37℃、5% CO2培养箱内培养。2 d后全量换液,第5 d时加入阿糖胞苷,培养8~ 12 d后用于实验研究。
1.3.2 染毒及干预锰组:只添加氯化锰对细胞进行染毒; 牛磺酸+锰组:同时添加氯化锰和牛磺酸;空白组:不添加任何干预物;牛磺酸组:只添加牛磺酸。参考郭松超等〔5〕的实验结果并结合本研究预实验结果,低、中、高剂量锰组的终剂量分别为0.2、0.8和1.2 mmol/L;牛磺酸终剂量为5 mmol/L。 各组处理24 h后测定各指标。
1.3.3 LDH测定收集各组培养液上清,参照试剂盒说明书进行测定,每组测定6个复孔。
1.3.4 流式细胞仪AnnexinV-PI双染法收集培养细胞,参照试剂盒说明书采用AnnexinV-FITC对细胞进行染色,染色后,1h内细胞悬液上流式细胞仪测定。每组测定3个复孔。
1.3.5 透射电镜标本制作收集培养细胞,1 500 g离心5~ 10 min后弃上清液;加入约1mL胎牛血清重悬细胞,以同等转速离心3~5 min后弃上清;加入2.5%的戊二醛固定至少2 h;常规透射电镜包埋处理。
1.4 统计分析应用SPSS 16.0软件进行F检验和t检验。
2 结 果 2.1 培养神经元的生长动态及鉴定(图 1)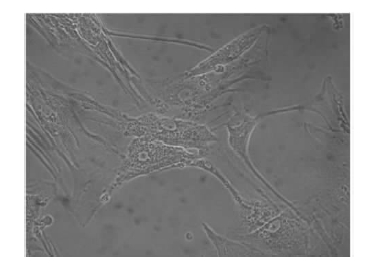 | 图 1 正常培养9 d 的海马神经元( 40 × 10) |
细胞接种24 h 后基本贴壁,2~3 d长出突起的细胞增多,4~5 d胞体进一步铺展,6~7 d胞浆出现丰富而明显的尼氏体,细胞间生长密集,加入阿糖胞苷后细胞背景渐清晰,存活细胞胞体饱满,呈三角形或多边形,胞核圆、大,核仁清晰可见,突起较粗,呈双极、三极或多极,细胞间突起相互交织。8~12 d达高峰,2~3 周后逐渐衰退。尼氏染色可见神经细胞胞浆富含蓝色颗粒,胞核及核仁被染成蓝紫色,突起被染成淡蓝色;胶质细胞则无丰富的胞浆颗粒及清晰深染的核仁。
2.2 各组神经元LDH活力及凋亡情况(表 1)| 表 1 各组神经元LDH 活力、凋亡率比较 |
低、中、高剂量锰组的LDH活力均比空白组明显增高(F=31.802,P< 0.001),高剂量锰组比低剂量锰组明显增高(t=5.587,P< 0.001);牛磺酸组LDH活力与空白组比较差异无统计学意义 (t=1.315,P=0.218);牛磺酸+低剂量锰组LDH活力比低剂量锰组明显降低(t=2.871,P=0.017)。流式细胞仪定量测定的神经元凋亡率结果表明,中、高剂量锰组凋亡率均比空白组明显增高(F=159.05,P< 0.001),且随着染锰剂量的增加凋亡率上升,呈剂量-反应关系;牛磺酸+中剂量锰组明显低于中剂量锰组(t=3.813,P=0.019),牛磺酸+高剂量锰组明显低于高剂量锰组(t=3.709,P=0.021);牛磺酸+中剂量锰组、牛磺酸+高剂量锰组与空白组比较差异均无统计学意义。
2.3 海马神经元超微结构变化(图 2~4)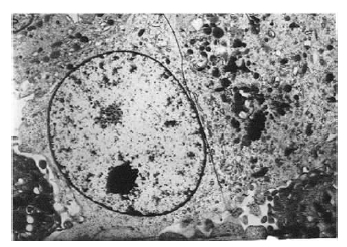 | 图 2 空白组海马神经元超微结构( 2 800 × ) |
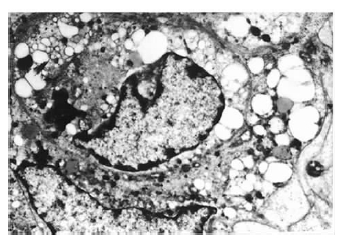 | 图 3 锰组海马神经元超微结构( 3 800 × ) |
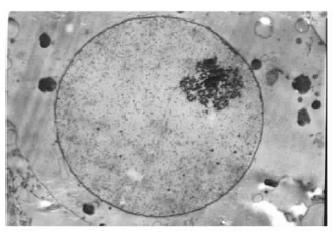 | 图 4 牛磺酸+锰组海马神经元超微结构( 3 800 × ) |
透射电镜下观察可见,空白组神经元核膜完整,核形正常,染色质均匀分布,以常染色质为主,胞浆内各种细胞器均匀分布于核周;牛磺酸组神经元形态学表现与空白组相近;锰组神经元胞体浓缩、胞浆有大量空泡形成,胞核变形、皱缩,核内染色质浓缩、边集,部分神经元胞膜破裂,胞浆内容物释放;牛磺酸+锰组多数胞核形态正常,染色质浓集、核固缩等现象减少,胞浆空泡化程度也比锰组有所降低。
3 讨 论凋亡是由遗传控制、受基因调控的程序性细胞死亡过程〔6〕。本研究通过电镜观察证实了染锰海马神经元凋亡的发生。FCM定量结果表明,神经元凋亡率随染锰剂量的增加呈上升趋势,呈剂量-反应关系,而低剂量锰组与空白组比较差异无统计学意义,推测是染锰剂量较低,尚未达到诱导细胞凋亡的水平。
坏死是非遗传控制的意外细胞死亡。当强烈刺激因素作用于细胞并超过其承受能力时,坏死发生,此时胞膜破裂,胞浆内容物释放,LDH外溢,通过测定LDH活力可反映细胞坏死情况〔6〕。本研究中锰组LDH活力比空白组均明显增高,提示锰可直接引起培养的海马神经元发生坏死,且染锰剂量越高,对神经元的促坏死作用越大。本研究中牛磺酸对锰神经毒性的干预作用主要体现在拮抗凋亡和减轻坏死二个方面: FCM结果表明,牛磺酸+锰组的凋亡率均比同剂量锰组有所下降。电镜观察结果也证实牛磺酸+锰组神经元超微结构有所改善,表明牛磺酸对锰致海马神经元凋亡有一定拮抗作用,在体外实验中也得到证实〔7〕。牛磺酸对神经元坏死的拮抗作用随着染锰剂量增加而减弱:牛磺酸+低剂量锰组LDH活力比低剂量锰组明显降低,而牛磺酸+中、高剂量锰组与中、 高剂量锰组比较,差异均无统计学意义,表明随着染锰剂量增加,神经元受损程度加重,破裂坏死的细胞增多,牛磺酸无法进入神经元胞体而失去干预作用。牛磺酸对神经元的产生保护作用的机制并不十分清楚,且对不同的神经元作用机制似乎也不同〔8〕。
| 〔1〕 | Burton NC,Guilarte,TR.Manganese neurotoxicity:lessons learned from longitudinal studies in nonhuman primates[J].Environmental Health Perspectives,2009,117(3):325-332. |
| 〔2〕 | 肖忠新,牛丕业,李慧,等.锰对大鼠空间学习记忆影响[J].中国公共卫生,2010,26(3):381-382. |
| 〔3〕 | Ma N,asoh M,Kawanishi S,et al.Protection effect of taurine on nitrosative stress in the mice brain with chronic exposure to arsenic[J].Journal of Biomedical Science,2010,17(Suppl 1):S1-S7. |
| 〔4〕 | Pan C,Gupta A,Prentice H,et al.Protection of taurine and granulocyte colony stimulating factor against excitotoxicity induced by glutamate in primary cortical neurons[J].Journal of Biomedical Science,2010,17(Suppl 1):S1-S18. |
| 〔5〕 | 郭松超,陆彩玲,陈维平,等.牛磺酸拮抗锰诱导体外培养的皮层神经细胞凋亡[J].营养学报,2008,30(1):82-91. |
| 〔6〕 | 司徒镇强,吴军正.细胞培养[M].修订版.西安:世界图书出版公司,2006:276. |
| 〔7〕 | 黄世文,郭松超,陆彩玲.牛磺酸对染锰大鼠海马神经毒性的影响[J].中国职业医学,2008,35(5):374-377. |
| 〔8〕 | Taranukhin AG,Taranukhina EY,Saransaari P,et al.Neuroprotection by taurine in ethanol-induced apoptosis in the developing cerebellum[J].Journal of Biomedical Science,2010,17(Suppl 1):S1-S12. |
 2011, Vol. 27
2011, Vol. 27