2. 华中科技大学同济医学院公共卫生学院职业与环境卫生学教研室
苯并(a)芘[Benzo (a) Pyrene, B(a)P]在体内主要由肝脏代谢, 经酶代谢活化可生成终致癌物, 引起DNA损伤, 启动致突变、致癌过程〔1〕。牛磺酸(taurine)是体内含量最丰富的氨基酸, 研究发现牛磺酸可通过减轻脂质过氧化, 而拮抗某些毒物、药物的肝毒性, 并有拮抗人胚肝细胞(L-02细胞) DNA损伤的作用〔2, 3〕。鉴于人胚肝细胞有较完整的代谢酶系, 本课题通过微核实验观察B(a)P致人胚肝细胞的微核率和核分裂指数, 研究染色体的损伤及牛磺酸对其的保护作用。
1 材料与方法 1.1 材料人胚肝细胞(武汉大学中国典型培养物保藏中心); B(a)P、二甲基亚砜(DMSO)、牛磺酸、细胞松弛素B (美国Sigma公司); DMEM培养基和新生小牛血清(美国Gibco公司); 胰蛋白酶(美国Amresco公司); 其他试剂皆为国产分析纯。
1.2 细胞培养L-02细胞在含10%新生小牛血清的DMEM培养基中, 于37℃、5% CO2的培养箱中培养。L-02细胞生长状态良好, 处于对数生长期时可用于实验。
1.3 胞质分裂阻滞法微核实验(CBMNT)将L-02细胞按5×105接种于100 ml细胞培养瓶中, 加10%新生小牛血清, 再加DMEM培养基至5 ml。于37℃、5% CO2的培养箱中培养24 h后, 当细胞密度为50%~60%时开始实验。牛磺酸设1.0, 2.0, 4.0 mmol/L 3个浓度, B(a)P设12.5, 25, 50 μmol/L 3个剂量。实验按完全随机设计分成5组:(1)空白对照组; (2)溶剂对照组:加入DMSO; (3) B(a)P染毒组; (4)牛磺酸组:各个浓度加入培养体系后继续培养24 h; (5)牛磺酸预防组:L-02细胞先以3个不同浓度的牛磺酸预处理24 h, 再加入25 μmol/L的B(a)P培养24 h。5个组每种物质、每种浓度均设3个平行样。染毒结束后更换培养基, 加入10 μl细胞松弛素B (3 μg/ml), 培养24 h。收获细胞时, 通过胰蛋白酶消化细胞, 收集细胞离心后用KCl低渗处理细胞, 再次同样条件和时间离心后加入固定液(乙酸和甲醇按3:1比例配制), 离心, 重复固定2次后滴片, 以10%的Giemsa染色13 min, 用清水冲洗风干后用树胶封片保存。每个样本在光学显微镜400×10倍镜下记数单核、双核、三核及四核细胞, 总数记达500个以上。计算核分裂指数(NDⅠ)=(MⅠ+2MⅡ+3MⅢ+4MⅣ)/总细胞数, 其中MⅠ至MⅣ分别代表单核细胞到四核细胞的细胞数。同时计数1000个双核细胞中的微核(MN)数〔4〕。
1.4 统计分析所有数据采用SPSS 10.0统计软件进行统计处理, 计量资料进行单因素方差分析, 各实验组与对照组间比较用Dunnett-t检验。
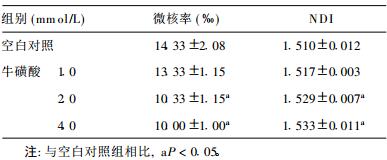
2 结果 2.1 牛磺酸对L-02细胞单独作用时微核的影响(表 1)| 表 1 牛磺酸对L-02细胞单独作用的微核率和核分裂指数(x±s) |
表 1可见, 与空白对照组比较, 2.0和4.0 mmol/L牛磺酸作用于L-02细胞诱导的微核率明显降低, 差异有统计学意义(P < 0.05)。而1.0 mmol/L牛磺酸作用于L-02与空白对照组微核率比较, 差异无统计学意义, 核分裂指数与其相一致。
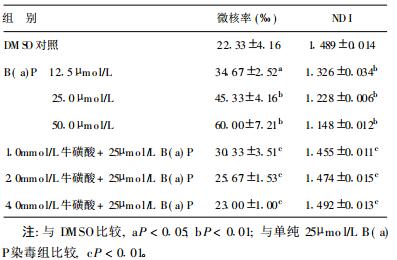
2.2 B(a)P对L-02细胞单独染毒时微核的影响(表 2)| 表 2 B(a)P单独染毒及牛磺酸预处理再染毒B(a)P致L-02细胞的微核率和核分裂指数(x±s) |
用B(a)P对L-02细胞单独染毒时, 可见随着B(a)P浓度的升高, 其诱导的微核率与溶剂对照组(DMSO)相比, 呈剂量依赖性显著升高, 差异有统计学意义(P < 0.05或P < 0.01)。B(a)P所有染毒浓度所产生的NDI与DMSO对照组相比均有显著下降, 差异有统计学意义(P < 0.01)。
2.3 牛磺酸预处理对B(a)P致L-02细胞毒性的保护作用(表 2)牛磺酸预处理L-02细胞后再加B(a)P染毒, 可观察到与单纯25 μmol/L B(a)P相比, 其诱导的微核率有随牛磺酸浓度增加而减少的趋势, 差异有统计学意义(P < 0.01)。1.0 mmol/L牛磺酸预处理组所诱导的微核比DMSO对照组高, 差异有统计学意义(P < 0.05);而2.0和4.0 mmol/L牛磺酸预处理组g与DMSO对照组比较差异无统计学意义。与单纯25 μmol/L B(a)P染毒比较, 牛磺酸预处理组使NDI明显升高, 呈剂量依赖性地显著升高, 差异有统计学意义(P < 0.01)。
3 讨论实验结果显示, B(a)P在12.5, 25, 50μmol/L的剂量条件下, 诱导的微核率明显增多, 核分裂指数明显降低, 且存在明显的剂量-反应关系。而1.0, 2.0, 4.0 mmol/L的牛磺酸预处理对25 μmol/LB(a)P引起的染色体损伤则具有明显的拮抗作用。
B(a)P在体内肝细胞线粒体P-450酶系的催化下, 可生成环氧化物并与DNA结合, 形成环氧化加合物引起DNA损伤, 从而启动致突变、致癌过程〔5〕。Garry S等发现, B(a)P 0.75 mg单独给予大鼠后, 用彗星实验检测其可引起肝细胞的DNA损伤〔6〕。本研究结果也表明, B(a)P对人胚肝细胞有染色体损伤的毒性作用, 随着B(a)P剂量的升高, 其毒性也增大。
牛磺酸为机体条件必需氨基酸, 可由食物供给或肝脏合成, 在人类一次性最高给予剂量达5 g时仍未观察到任何毒副作用。本研究显示, 不同浓度牛磺酸单独作用于L-02细胞时, 均未引起染色体损伤, 且中高剂量的牛磺酸诱导的微核率比空白对照组还低。Erman F等发现, 牛磺酸可以预防用乙醇与CCl4诱导的大鼠肝纤维化及脂质过氧化损伤〔7〕。宋樱〔8〕等研究发现, 牛磺酸对CCl4诱导的大鼠肝细胞损伤有保护作用。本实验结果显示, 经牛磺酸预处理的L-02细胞再染毒B(a)P, 所诱导的微核率与核分裂指数与单纯B(a)P染毒组相比, 染色体损伤随牛磺酸浓度增加逐渐减轻, 差异有统计学意义。表明牛磺酸对B(a)P致L-02细胞的染色体损伤具有保护作用, 且牛磺酸浓度越高, 保护作用越强。
综上所述, 牛磺酸对B(a)P诱导的肝细胞染色体具有良好的保护作用, 且牛磺酸可通过食物摄取, 无毒副作用, 表明牛磺酸可用于肝损伤及肝癌预防和治疗。
| [1] | Nesnow S, Davis C, Nelson GB, et al. Comparison of the genotoxic activities of the K-region dihydrodiol of benzo[J]. Mutat Res, 2002, 521 : 91–102. DOI:10.1016/S1383-5718(02)00218-8 |
| [2] | Miyazaki T, Karube M, Matsuzaki Y, et al. Taurine inhibits oxidative damage and prevents fibrosis in carbon tetrachloride-induced hepatic fibrosis[J]. J Heptol, 2005, 43(1) : 117–125. DOI:10.1016/j.jhep.2005.01.033 |
| [3] | 鲁力, 秦秋兰, 肖德强, 等. 牛磺酸对苯并(a)芘致人胚肝细胞损伤拮抗作用[J]. 中国公共卫生, 2007, 23(9) : 1131–1133. |
| [4] | Fenech M. The in vitro micronucleus technique[J]. Mutation Research, 2000, 455(1-2) : 81–95. DOI:10.1016/S0027-5107(00)00065-8 |
| [5] | 张桥. 毒理学基础[M].4版. 北京: 人民卫生出版社, 2003: 8-47. |
| [6] | Garry S, Nesslany F, Aliouat E, et al. Hematite (Fe2O3) enhances benzo[a]pyrene genotoxicity in endotracheally treated rat, as determined by Comet Assay[J]. Mutat Res, 2003, 538(1-2) : 19–29. DOI:10.1016/S1383-5718(03)00082-2 |
| [7] | Erman F, Balkan J, Cevikbas U, et al. Betaine or taurine administration prevents fibrosis and lipid peroxidation induced by rat liver by ethanol plus carbon tetrachloride intoxication[J]. Amino acids, 2004, 27(2) : 193–204. DOI:10.1007/s00726-004-0107-3 |
| [8] | 宋樱, 张敏, 王冬, 等. 牛磺酸和支链氨基酸对大鼠肝细胞氧化损伤的保护作用[J]. 青岛大学医学院学报, 2004, 40((1) : 20–24. |
 2009, Vol. 25
2009, Vol. 25

 , 林辉2, 鲁文清2, 肖德强1, 李习艺1, 曾高峰1
, 林辉2, 鲁文清2, 肖德强1, 李习艺1, 曾高峰1