2. 广西疾病预防控制中心;
3. 华中科技大学同济医学院公共卫生学院
牛磺酸(taurine)是一种具有多种生物学功能的氨基酸,如调节细胞钙稳态、稳定细胞膜、抗氧化、抑制肿瘤细胞增殖及胶原形成、对外源化合物的解毒作用等。研究表明,牛磺酸通过抗氧化作用可拮抗许多毒物对肝细胞的损害[1, 2]。苯并(a)芘[B(a)P]是一种公认的环境和食品污染物,世界卫生组织确定其为食物中强致癌物质之一,对人胚肝细胞DNA有明显的损伤作用[3]。本研究采用单细胞凝胶电泳技术(SCGE)检测牛磺酸对苯并(a)芘致人胚肝细胞DNA损伤的保护作用,同时测定氧化损伤相关指标及肝细胞损伤漏出酶含的变化,分析牛磺酸对苯并(a)芘肝细胞毒性的保护作用机制,为寻找有效的抗毒保肝营养因子提供科学依据。
1 材料与方法 1.1 主要仪器CO2培养箱,电泳仪、电泳槽,冷冻离心机,紫外可见分光光度计检测仪(日本SHIMADZU公司);荧光显微镜和荧光数码显微成像系统(日本OLYMPUS公司)。
1.2 主要试剂胎牛血清培养基(DMEM,美国Gibco公司);小牛血清(新西兰PerBio Science company公司);胰蛋白酶(武汉中键科技开发公司);正常熔点琼脂糖(德国Merck Darmstadt公司);低熔点琼脂糖(上海YITO BIO-INSTRUMENT公司);TritonX-100(美国Sino-American Biotec公司);二甲基亚砜(DMSO)、牛磺酸和苯并(a)芘(美国Sigma公司)。丙二醛(MDA)、还原型谷胱甘肽(GSH)、天门冬酸氨基转移酶(AST)、谷氨酸氨基转移酶(ALT)检测试剂盒(南京建成生物工程研究所)。
1.3 细胞株选用人胚肝细胞(L-02细胞)、(由武汉大学中国典型培养物保藏中心提供),华中科技大学环境与职业卫生学教研室传代保存。取生长状况良好并达一定密度的人胚肝细胞40l,与0.4%台盼蓝按1:1混合,镜下观察细胞存活率应不低于95%。按每孔细胞数约1105个,将其接种到16和24孔培养板,置CO2培养箱培养12h使细胞贴壁,12h更换新鲜培养基用于以下试验。
1.4 分组处理将人胚肝细胞随机分为5个组:(1) 空白对照组:不加任何试剂;(2) 溶剂对照组:加入浓度为10ml/L的DMSO;(3) 苯并(a)芘组:25mol/L苯并(a)芘,加入细胞培养体系后培养2h;(4) 牛磺酸组:设0.5,1.0,2.0和4.0mmol/L 4个浓度,加入培养体系后培养24h:(5) 牛磺酸预防组:细胞先以不同浓度的牛磺酸预处理24h,再加入25mol/L苯并(a)芘培养2h。试验中每种物质、每种浓度设3个复孔,培养体系中小牛血清浓度均为10%。
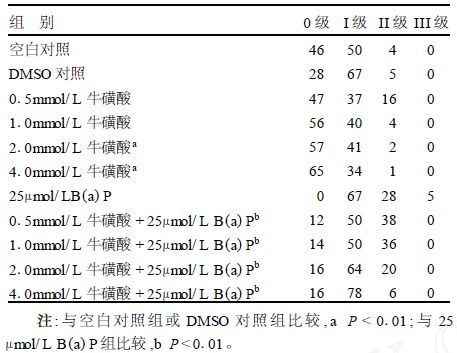
1.5 肝细胞DNA损伤测定培养结束后参照Singh方法对细胞进行单细胞凝胶电泳技术(SCGE)分析[4],操作步骤包括制片、裂解、解旋、电泳、中和和染色,然后每片在荧光显微镜下随机观察计数100个细胞核并拍照,用IMI彗星分析软件计算细胞平均Oliver尾矩值(彗星尾长与彗尾DNA含量之积,能灵敏反映细胞DNA断裂损伤)及标准差,根据彗星尾中DNA含量占彗星DNA总量的百分比将细胞损伤进行分级与计数[5](0级:<5%,表示无损伤;I级:5%~20%,表示轻度损伤;II级:20%~40%,表示中度损伤;III级:40%~95%,表示重度损伤;Ⅳ级:95%,表示完全损伤)。
1.6 氧化损伤及肝功能酶学指标测定培养结束后用分光光度法对上清液进行MDA、GSH、AST和ALT含量测定。
1.7 统计分析所有指标重复测3次取均值,采用SPSS11.0统计软件处理。计量资料各组间的显著性检验用方差分析,各实验组与对照组间比较用Games-Howell检验;计数资料用秩和检验;采用一元线性相关分析各指标间的相关性。
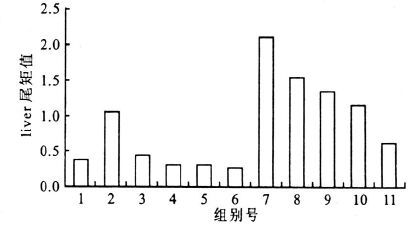
2 结果 2.1 牛磺酸和苯并(a)芘对肝细胞DNA损伤的作用(图 1,2表 1)由图 1可见,25mol/L的苯并(a)芘能引起人胚肝细胞明显的DNA损伤其Oliver尾矩值牛磺酸处理,可明显减轻苯并(a)芘对细胞DNA的损伤,其Oliver尾矩值与苯并(a)芘组比较,差异有统计学意义(P<0.01) ,呈剂量-效应关系。苯并(a)芘对人胚肝细胞DNA损伤及牛磺酸保护作用的彗星图像见图 2。
|
注:1 :空白对照组;2 :DMSO 对照组;3 :015 mmol/ L 牛磺酸组; 4 :110 mmol/ L 牛磺酸组;5 :210 mmol/ L 牛磺酸组; 6 :410 mmol/ L 牛磺酸组;7 :25μmollLB(a) P 组; 8 :015 mm01/ L 牛磺酸+ 25μmol/ LB(a) P 组; 9 :110 mmol/ L 牛磺酸+ 25μmol/ LB(a) P 组; 10 :210 mmol/ L 牛磺酸+ 25μmol/ LB(a) P 组; 11 :410 mmol/ L 牛磺酸+ 25μmol/ LB(a) P 组 图 1 牛磺酸和苯并( a) 芘对肝细胞DNA 损伤作用的Oliver 尾矩值图 |

|
图 2 牛磺酸和苯并( a) 芘对肝细胞DNA 损伤作用的彗星图像( ×400) |
| 表 1 牛磺酸和苯并(a)芘对肝细胞DNA损伤作用的分级 |
从表 1可见,苯并(a)芘肝细胞DNA损伤严重程度影响较大。2.0~4.0mmol/L牛磺酸有显著减轻细胞DNA损伤作用,若先用牛磺酸处理肝细胞,则可明显减轻苯并(a)芘所致细胞DNA损伤等级,并呈剂量-效应关系。
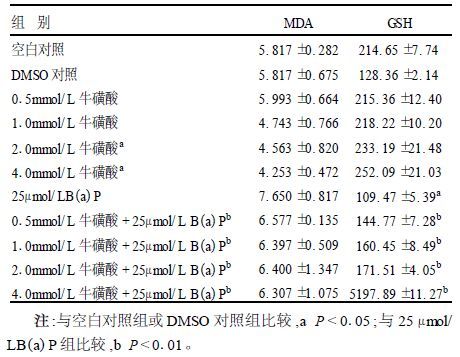
2.2 牛磺酸和苯并(a)芘对肝细胞氧化损伤的影响(表 2)| 表 2 牛磺酸和苯并(a)芘对肝细胞氧化损伤的影响( x ±s) |
苯并(a)芘能引起人胚肝细胞培养液中MDA含量增加和GSH含量降低,牛磺酸组的结果则正好相反;牛磺酸预防组中MDA含量变化不大,但GSH含量明显上升,与苯并(a)芘组比较,差异有统计学意义(P<0.01) 。
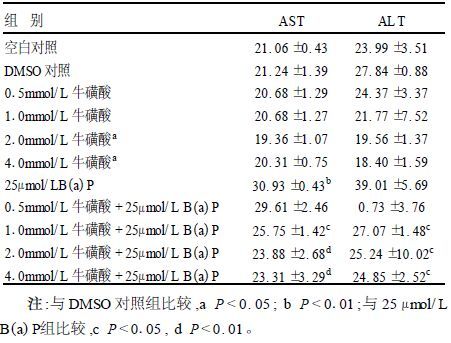
2.3 牛磺酸和苯并(a)芘对肝细胞转氨酶的影响(表 3)| 表 3 牛磺酸和苯并(a)芘对肝细胞转氨酶的影响( x ±s) |
苯并(a)芘可致人胚肝细胞培养液中AST和ALT含量升高,牛磺酸组与空白组比较,差异无统计学意义,而牛磺酸预防组却可使培养液中AST和ALT含量显著降低,与苯并(a)芘组比较,差异有统计学意义(P<0.01) 。
2.4 肝细胞DNA损伤与其他指标相关性分析将苯并(a)芘组和牛磺酸预防组对人胚肝细胞DNA损伤的Oliver尾矩值与培养液中氧化损伤及肝功能酶学指标做直线相关分析发现,Olive尾矩值与MDA含量呈明显正相关(r=0.852,P<0.01) ,与GSH含量呈明显负相关(r=-0.929,P<0.01) ,与AST、ALT含量呈明显正相关(r=0.930和0.927,P<0.01) 。
3 讨论本研究结果显示,不同浓度纯牛磺酸对人胚肝细胞能反映DNA损伤的Oliver尾矩值无影响,而牛磺酸预处理后能明显减轻苯并(a)芘引起的肝细胞DNA损伤,并呈一定的剂量-效应关系,表明牛磺酸有良好的拮抗苯并(a)芘致人胚肝细胞DNA损伤效果。本研究对细胞培养液中MDA及GSH含量测定结果表明,MDA含量随着牛磺酸浓度增加而降低,牛磺酸预防组MDA含量虽然与苯并(a)芘组比较,差异无统计学意义,但加入牛磺酸可使MDA含量降低。牛磺酸组GSH含量变化不大,但有随牛磺浓度高而增加的趋势;牛磺酸预防组GSH含量与苯并(a)芘比较显著增高,呈剂量-效应关系。提示牛磺酸具有拮抗苯并(a)芘引起的人胚肝细胞MDA含量升高及GSH下降作用。相关性分析表明,肝细胞DNA损伤的Olive尾矩值与MDA含量呈明显正相关,与GSH含量呈明显负相关,显示氧化损伤在苯并(a)芘致人胚肝细胞损伤机制中起重要作用,MDA升高和GSH降低可在一定程度上反映肝细胞DNA损伤情况。对细胞培养液中AST、ALT测定结果显示,牛磺酸组与空白对照组比较差异无统计学意义,牛磺酸预防组可显著抑制苯并(a)芘引起的转氨酶升高,表明牛磺酸具有拮抗苯并(a)芘引起人胚肝细胞AST、ALT含量升高,表明牛磺酸具有拮抗苯并(a)芘引人胚肝细胞AST、ALT含量升高的作用。从相关性上看,肝细胞DNA损伤的Olive尾矩值与AST、ALT含量呈明显正相关,表明转氨酶含量升高也可在一定程度上反映肝细胞DNA损伤情况。
综上所述,牛磺酸对人胚肝细胞无毒副作用,并可拮抗苯并(a)芘引起的肝细胞DNA损伤和毒性,抗细胞氧化损伤是其主要作用机制之一,表明牛磺酸为一种良好的具有抗化学性肝损伤的营养因子。
| [1] | Waters Eoin, Jiang Huai Wang, Redmond H Paul, et al. Role of tau2 rine in preventing acetaminophen-induced hepatic injury in the rat[J]. American Journal of Physiology, 2001, 280(6) : 1274–1279. |
| [2] | Hagar, Hanan H. The protective effect of taurine against cy2 closporine A-induced oxidative stress and hepatotoxicity in rats[J]. Toxicology Letters, 2004, 151(2) : 335–343. DOI:10.1016/j.toxlet.2004.03.002 |
| [3] | 秦秋兰, 鲁力, 肖德强, 等. 苯并(a) 芘对健康人肝细胞DNA 损伤作用的研究[J]. 广西医学, 2005, 28(4) : 489–492. |
| [4] | Singh NP, Mccopy MT, Tice RR, et al. A single technique for quan2 tification of low levels of DNA damage in indivedual cells[J]. Exp Cell Res, 1988, 175(1) : 184–191. DOI:10.1016/0014-4827(88)90265-0 |
| [5] | Anderon,D,Yu TW,Phillips BJ,et al.The effect of various antoxi2 dants and other modifying agents on oxygen-radical-gegerated DNA damage in human lymphocytes in the comet assay[J].Mul Res,1994,307:261-271. |
 2007, Vol. 23
2007, Vol. 23