实现“三精”放疗,是当今放疗时代的主旋律,其中,精确放射治疗是重中之重。目前肿瘤放射治疗已经广泛采用调强放疗(intensity modulated radiationtherapy, IMRT)、容积调强放疗(volume of rotating Intensity modulated radiotherapy, VMAT)等技术,这些技术要求摆位的精度更高[1],图像引导放疗(imaging guided radiationtherapy, IGRT)可以在治疗前追踪并纠正分次间的肿瘤位置误差[2],但是对于一些需要呼吸管理干预的肿瘤治疗,IGRT并不能够很好地纠正治疗分次内肿瘤位置误差。乳腺癌患者的靶区在胸部,在自由呼吸状下放疗的一部分剂量效应会以心脏毒性显现[3-4]。由于系统误差、自主呼吸运动、几何变形等因素的存在,使得靶区剂量照射准确性下降而正常组织受到不必要的照射,为了保证处方剂量覆盖足够的肿瘤靶区,需要在临床靶区(clinical target volume, CTV)周围外扩合适的边界得到计划靶区(planning target volume, PTV),边界过大会增加正常组织受照剂量,边界过小又不能保证足够的靶区覆盖。结合采用IGRT和OSMS技术不仅可以减少乳腺癌患者的摆位误差,还能在治疗过程中监控患者呼吸幅度及屏气情况,最大程度地减少CTV到PTV的外放边界。
1 资料与方法 1.1 入组标准回顾性分析选取2020年7月—2022年3月南方医科大学南方医院放疗科乳腺组左侧乳腺癌根治术后拟行放疗的28~65岁女性患者36名,治疗前无内乳和锁骨上淋巴结转移、无远处转移、无基础心脏病史,对全部患者进行CT定位前的呼吸训练宣教,经呼吸训练后须熟练掌握DIBH要点,熟悉胸式呼吸,屏气前后体表起伏腹背方向相差 > 0.8 cm,屏气时间 > 35 s,并可连续重复上述动作7次以上,经过此筛选方可入组DIBH组,其余24例患者平均分配到FB1组、FB2组,入组患者总数为36例。患者一般资料如 表1,入组患者能够很好地了解深吸气屏气的重要性,以及很好地配合放疗摆位。
|
|
表 1 患者一般资料 Table 1 General patient information |
对所有入组患者采用发泡胶进行塑形固定身体如图1所示。对于DIBH组患者,结合实时定位监测装置(real-time position management,RPM),让患者进行3次最大吸气,观察屏幕信标起伏状况,取最大吸气量平均值的80%,在患者身上勾画自由呼吸体表标记(FB)和深吸气屏气(DIBH)体表标记并在DIBH标记中心贴上铅点,分别在FB、DIBH下进行CT扫描;FB1、FB2组患者的原点标记中心铅点均贴在发泡胶上。所有患者扫描条件:120 kV,150 mAs,层厚5 mm。

|
图 1 左侧乳腺癌根治术后DIBH的CT定位体表标记 Figure 1 Body surface markers for CT localization under DIBH after radical mastectomy for left breast cancer |
将定位CT图像传至靶区勾画系统Pvmed V1.0勾画危及器官及计划靶区PTV,给予处方剂量:50 Gy/2 Gy/25 f,95%以上的处方剂量至少覆盖95%靶区体积,常规放疗完后根据术前影像资料后期电子线补量。主管医生勾画完靶区后再传至计划系统Eclipse 15.1,DIBH组的靶区勾画和计划设计均在DIBH的CT图像上进行,FB1、FB2组患者均只需在FB的CT图像上进行。统一采用IMRT治疗技术,6 MV,500 MU/min。物理师导出3个文件到DICOM,1个治疗计划RT plan,2个CT体表外轮廓(FB和DIBH的Body结构)RT structure,见图2。

|
图 2 基于OSMS引导的左侧乳腺癌治疗流程 Figure 2 OSMS-based treatment flow for left breast cancer |
其中,对于FB体表,当患者屏气腹背方向VRT值在中间值时进行捕获;DIBH体表也要VRT值在±0.05时进行捕获,如图3。
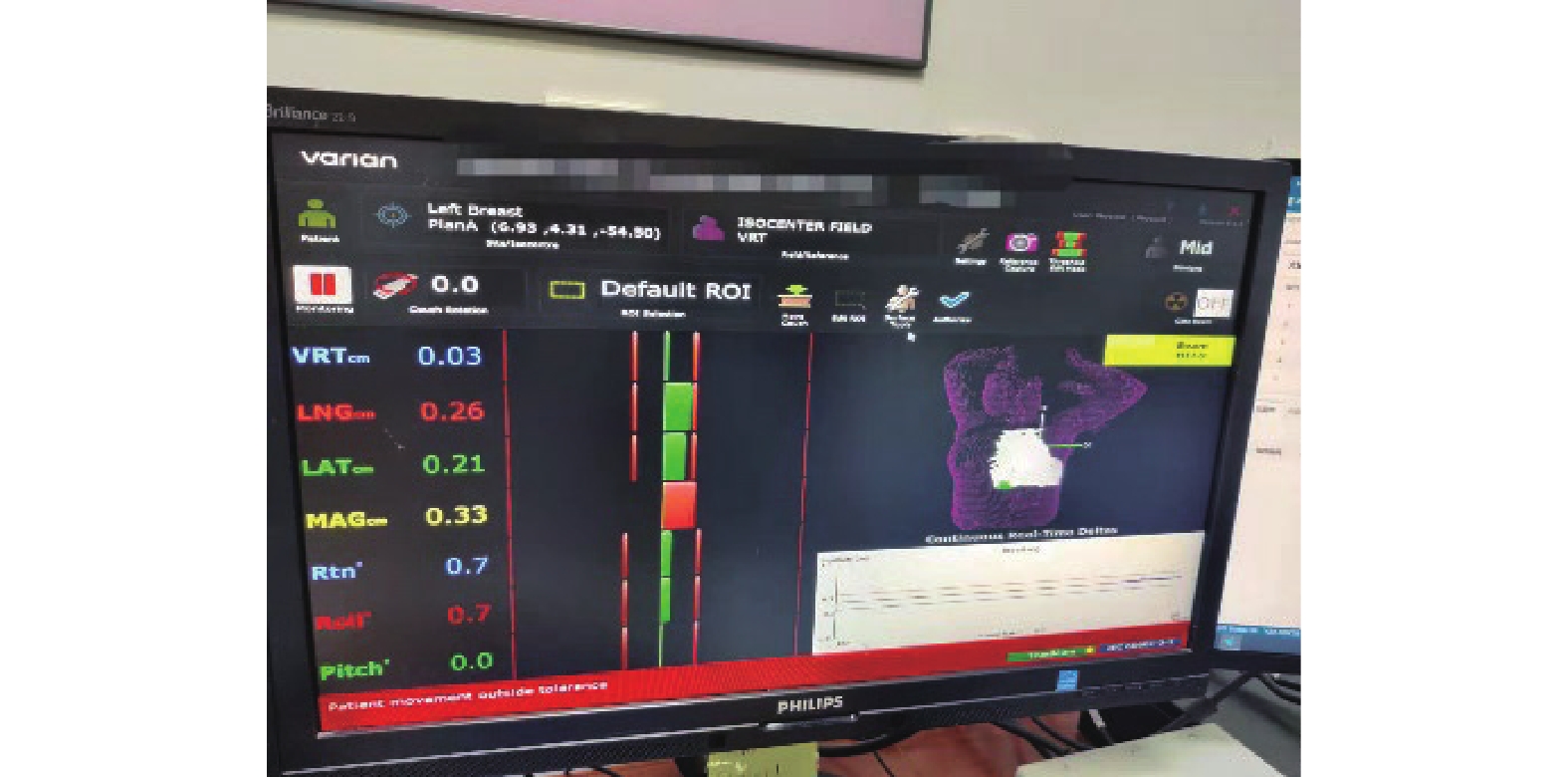
|
图 3 捕获DIBH体表 Figure 3 Captured DIBH body surface |
DIBH组患者经过OSMS引导在FB和DIBH 2种状态下相继进行六维自动摆位后进行治疗前CBCT验证,FB1组经过OSMS引导下进行FB状态下六维自动摆位后进行治疗前CBCT验证,FB2组不经过OSMS引导,通过激光灯摆位后进行治疗前CBCT验证。CBCT扫描参数:Head模式,半挡蝶形滤线器,机架自178°~340°,以防机架与体位固定装置相碰撞和体表投影被影像接收板遮挡。第一周治疗前3次采集每例患者CBCT图像,整个疗程总共采集6次CBCT图像,并进行在线配准。对于DIBH组患者,主要匹配CT图像与CBCT的胸椎、胸骨、PTV,FB1、FB2组患者主要匹配胸椎、胸骨位置。软件采用骨和软组织自动配准模式(线性 + 旋转)并结合手动微调,分别记录左右、头脚、腹背方向上的的绝对位移误差值,并计算平均值(m)和标准差(SD)。根据Stroom和Heijmen[5]的概念,系统误差用分次治疗最大误差的平均值(m)表示,随机误差用分次误差的标准差(SD)表示。群体系统误差和群体随机误差分别用Σ和σ表示。根据van Herk等[6]推导的计划靶区外扩边界的公式MPTV = 2.5Σ + 0.7σ分别计算左右、头脚、腹背方向上的MPTV。
1.5 统计学方法采用SPSS 25.0软件对各方向的摆位误差进行计算,数据经正态性检验符合正态分布采用m±SD表示[7]。DIBH组、FB1组、FB2组3组患者的靶区位移误差数据的相互比较采用t检验,检验水准α = 0.05。
2 结 果 2.1 摆位误差统计结果DIBH组、FB1组、FB2组的摆位误差用m±SD(cm)表示,见表2、表3。DIBH组与FB1组在腹背方向、RTN、ROLL方向统计结果有统计学意义(P < 0.05),FB1组与FB2组在腹背方向统计结果有统计学意义( P < 0.05)。因为FB2组没有经过OSMS引导进行六维自动摆位,所以FB2组没有采集到旋转位移误差值。
|
|
表 2 左乳癌根治术后DIBH、FB1、FB2 3组的线性摆位误差比较 Table 2 Comparison of linear setup errors among the DIBH, FB1, and FB2 groups after radical mastectomy for left breast cancer |
|
|
表 3 左乳癌根治术后DIBH、FB1、FB2 3组的旋转摆位误差比较 Table 3 Comparison of rotational setup errors among the DIBH, FB1, and FB2 groups after radical mastectomy for left breast cancer |
DIBH组与FB1组的旋转位移误差散点图分别是如图4、图5,DIBH组RTN、PITCH、ROLL方向旋转误差绝对值 ≤ 1°占比分别为70.09%、61.68%、64.49%,FB1组RTN、PITCH、ROLL方向旋转误差绝对值 ≤ 1°占比分别为66.67%、74.24%、78.78%。

|
图 4 DIBH组RTN、PITCH、ROLL方向旋转误差分布散点图 Figure 4 Scatter diagram of rotational error distribution in RTN, PITCH, and ROLL directions in the DIBH group |
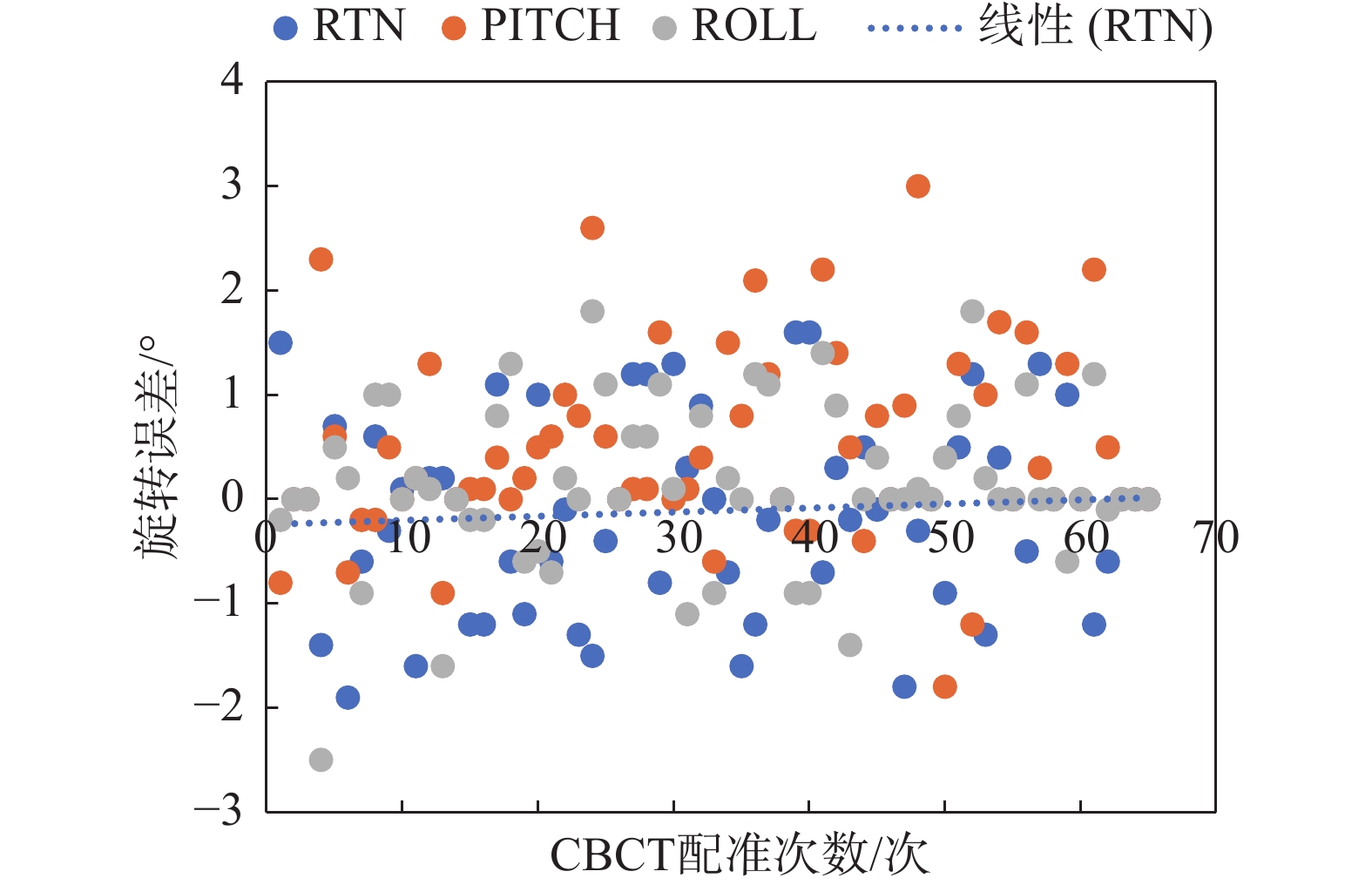
|
图 5 FB1组RTN、PITCH、ROLL方向旋转误差分布散点图 Figure 5 Scatter diagram of rotational error distribution in RTN, PITCH, and ROLL directions in the FB1 group |
根据靶区边界外扩公式MPTV = 2.5Σ + 0.7σ(Σ:组系统误差,σ:组随机误差)计算出个各方向上靶区边界的外放值,如表4。从表4可以看出,3组的计划靶区外扩边界MPTV值大小关系是在腹背、头脚方向上是DIBH < FB1 < FB2,在左右方向上是FB1 < DIBH < FB2。
|
|
表 4 DIBH、FB1、FB2三组的MPTV Table 4 MPTV values of the DIBH, FB1, and FB2 groups |
由查阅文献[8]可知,胸部肿瘤的摆位误差与头颈部肿瘤相比,前者更大,除了系统误差,患者的呼吸运动以及心脏搏动、不自主咳嗽等因素使患者的靶区位置在放疗过程中增加了很大的不确定性。放疗患者在治疗过程中的摆位误差是实现高质量放疗的关键因素,摆位误差的大小决定了临床靶区至计划靶区的外扩距离,如果外扩范围过大,周围正常组织会受到过量照射,外扩范围过小,肿瘤的受照剂量会不足,两者都会使治疗增益比下降,所以合适的MPTV值很重要。计算靶区外扩的方法和原理很多,其中Van Herk提出的靶区边界外放计算公式MPTV = 2.5Σ + 0.7σ得到了最广泛的认可。
体表引导放疗(surface guided radiation therapy,SGRT)本身具有自动摆位功能,精度高,速度快等特点[9-11]。Hamming等[12]报道通过 SGRT,左侧乳腺癌 DIBH 能够实现 5 mm 以内的位置误差,Laaksomaa 等[13]研究结果显示残差 3 mm 以内,光学体表引导的左侧乳腺癌 DIBH 可以大幅降低 IGRT次数[14-15]。本研究通过以OSMS引导DIBH、FB以及不使用OSMS引导、仅通过激光灯摆位3种状态下的摆位误差,计算得到3组的MPTV值。由于样本量太少,每组仅12例左侧乳腺癌根治术后患者,DIBH组与FB1组只有在平移腹背方向、旋转RTN、ROLL方向差异有统计学意义(P < 0.01),FB1组与FB2组只有在平移腹背方向有统计学意义,其余方向差异均无统计学差异( P > 0.05)。FB2组中没有旋转方向的数据,是因为根据体表标记线摆位时是3个维度,即腹背、头脚、左右等线性方向,不是每一次治疗前拍摄CBCT,而DIBH组与FB1组都有使用OSMS引导的六维自动移床摆位功能。
在统计学角度上DIBH组、FB1组和FB2组腹背方向的摆位误差和MPTV的大小关系是DIBH < FB1 < FB2。FB2组的体表标记线由于摩擦、出汗等重新补画会增大随机误差,并且影响了患者对自身的审美。在使用OSMS引导的过程中,没有电离辐射,只要患者有在治疗前拍摄CBCT,都会重新拍摄新体表(DIBH或FB),从 图4、图5可以看出,DIBH和FB的线性RTN值都有逐渐趋向于0的趋势,说明OSMS在整个疗程里减少患者旋转RTN方向的趋势里扮演着不可或缺的角色。DIBH技术的实施的关键因素之一是对患者的筛选宁缺毋滥,通过视频引导以及问卷的调查,对入组患者进行呼吸训练宣教,让患者在胸式呼吸状态下进行反复的自主屏气训练,以达到提高屏气时间,减少治疗时的屏气次数,增加患者屏气稳定性和重复性[16]的目的,减少放疗后不良反应的发生。提高治疗时患者屏气程度与CT定位屏气程度的一致性也是DIBH技术实施的关键因素[17],在使用OSMS 引导的过程中,患者首次摆位时,重复确认患者屏气状态下与体表 DIBH 标记重合后采集新的监控体表以引导后续屏气,后续每次屏气均要求OSMS工作站上的Vertical方向误差在±0.05 cm以内以保证屏气重复性,OSMS监测到六维误差超过设定阈值(±3 mm;±3°)时,控制加速器立刻停止出束。
综上所述,使用OSMS引导患者DIBH放疗时能够减小摆位误差,提高摆位精度,给主管医生勾画靶区提供了个体化CTV-PTV外扩重要依据。
| [1] |
Zagar TM, Cardinale DM, Marks LB. Breast cancer therapy-associated cardiovascular disease[J]. Nat Rev Clin Oncol, 2016, 13(3): 172-184. DOI:10.1038/nrclinonc.2015.171 |
| [2] |
Hirose TA, Arimura H, Fukunaga JI, et al. Observer uncertainties of soft tissue-based patient positioning in IGRT[J]. J Appl Clin Med Phys, 2020, 21(2): 73-81. DOI:10.1002/acm2.12817 |
| [3] |
Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Adjuvant chemotherapy in oestrogen-receptor-poor breast cancer: patient-level meta-analysis of randomised trials[J]. Lancet, 2008, 371(9606): 29-40. DOI:10.1016/S0140-6736(08)60069-0 |
| [4] |
Paszat LF, Mackillop WJ, Groome PA, et al. Mortality from myocardial infarction following postlumpectomy radiotherapy for breast cancer: a population-based study in Ontario, Canada[J]. Int J Radiat Oncol Biol Phys, 1999, 43(4): 755-762. DOI:10.1016/s0360-3016(98)00412-x |
| [5] |
Stroom JC, Heijmen BJ. Geometrical uncertainties, radiotherapy planning margins, and the ICRU-62 report[J]. Radiother Oncol, 2002, 64(1): 76-83. DOI:10.1016/s0167-8140(02)00140-8 |
| [6] |
Van Herk M. Errors and margins in radiotherapy[J]. Semin Radiat Oncol, 2004, 14(1): 52-64. DOI:10.1053/j.semradonc.2003.10.003 |
| [7] |
李钰, 高岩, 刘世龙, 等. 宫颈癌患者的膀胱充盈度一致性对放疗摆位误差的影响[J]. 中国辐射卫生, 2020, 29(3): 305-308. Li Y, Gao Y, Liu SL, et al. Effect of consistency of bladder filling volume on set-up errors in radiotherapy for the patients with cervical cancer[J]. Chin J Radiol Health, 2020, 29(3): 305-308. DOI:10.13491/j.issn.1004-714X.2020.03.027 |
| [8] |
甘晓根, 徐子海, 廖福锡. 应用CTVision图像引导分析胸部肿瘤在放疗中的摆位误差[J]. 中国医疗设备, 2012, 27(7): 157-159. Gan XG, Xu ZH, Liao FX. Analysis of set-up errors with use of CTVision imaging guided thoracic tumor radiation[J]. China Med Devices, 2012, 27(7): 157-159. DOI:10.3969/j.issn.1674-1633.2012.07.058 |
| [9] |
Hoisak JDP, Pawlicki T. The role of optical surface imaging systems in radiation therapy[J]. Semin Radiat Oncol, 2018, 28(3): 185-193. DOI:10.1016/j.semradonc.2018.02.003 |
| [10] |
张光伟, 吴何苟, 刘剑锋, 等. 光学表面监测系统自动摆位功能对乳腺癌放疗患者治疗精度及摆位时间的影响[J]. 中国医学物理学杂志, 2021, 38(4): 411-415. Zhang GW, Wu HG, Liu JF, et al. Effects of automatic setup function of optical surface monitoring system on treatment accuracy and setup time of breast cancer patients undergoing radiotherapy[J]. Chin J Med Phys, 2021, 38(4): 411-415. DOI:10.3969/j.issn.1005-202X.2021.04.003 |
| [11] |
Bartlett FR, Colgan RM, Carr K, et al. The UK HeartSpare study: randomised evaluation of voluntary deep-inspiratory breath-hold in women undergoing breast radiotherapy[J]. Radiother Oncol, 2013, 108(2): 242-247. DOI:10.1016/j.radonc.2013.04.021 |
| [12] |
Hamming VC, Visser C, Batin E, et al. Evaluation of a 3D surface imaging system for deep inspiration breath-hold patient positioning and intra-fraction monitoring[J]. Radiat Oncol, 2019, 14(1): 125. DOI:10.1186/s13014-019-1329-6 |
| [13] |
Laaksomaa M, Sarudis S, Rossi M, et al. AlignRT® and catalyst™ in whole-breast radiotherapy with DIBH: is IGRT still needed?[J]. J Appl Clin Med Phys, 2019, 20(3): 97-104. DOI:10.1002/acm2.12553 |
| [14] |
叶程伟, 周继丹, 商强, 等. 基于光学表面成像与锥形束CT结合的综合引导模式在头颈部肿瘤精确放疗中的研究[J]. 中国辐射卫生, 2019, 28(3): 346-350. Ye CW, Zhou JD, Shang Q, et al. Comprehensive guidance model based on optical surface imaging combined with cone beam CT in head and neck tumors accurate radiation therapy[J]. Chin J Radiol Health, 2019, 28(3): 346-350. DOI:10.13491/j.issn.1004-714X.2019.03.034 |
| [15] |
Boda-Heggemann J, Knopf AC, Simeonova-Chergou A, et al. Deep inspiration breath hold-based radiation therapy: aclinical review[J]. Int J Radiat Oncol BiolPhys, 2016, 94(3): 478-492. DOI:10.1016/j.ijrobp.2015.11.049 |
| [16] |
Misra S, Mishra A, Lal P, et al. Cardiac dose reduction using deep inspiratory breath hold (DIBH) in radiation treatment of left sided breast cancer patients with breast conservation surgery and modified radical mastectomy[J]. J Med Imaging Radiat Sci, 2021, 52(1): 57-67. DOI:10.1016/j.jmir.2020.12.004 |
| [17] |
Falco M, Masojć B, Macała A, et al. Deep inspiration breath hold reduces the mean heart dose in left breast cancer radiotherapy[J]. Radiol Oncol, 2021, 55(2): 212-220. DOI:10.2478/raon-2021-0008 |




