肾脏为放射敏感性组织, 所以在盆腔、腹部及脊柱的放疗时, 都有可能对肾脏造成损伤。随着射波刀、伽马刀的推广应用, 大剂量、低分割照射技术能够获得显著疗效。本实验从形态、功能方面观察大鼠肾脏单次照射后的改变, 探讨不同剂量电子线单次照射大鼠肾产生的放射生物学效应, 为腹部放疗的临床应用提供基础参数。
1 材料与方法 1.1 实验材料SPF级雄性SD大鼠120只, 体重280~300g。北京华阜生物提供(SCXK京2009- 2004)。自然光照、室温下给予标准饲料及水, 笼养。大鼠随机分为8、10、12和15 Gy双肾照射组、对照组, 每组24只。
1.2 照射方法大鼠腹腔10%水合氯醛(0.3 ml/ 100 g)麻醉, 俯卧于特制大鼠照射模具, 固定四肢。置于模拟机下定位确定照射范围, 探及两侧肾脏位置, 体表标记照射野, 限光筒限定照射野大小为2.5 cm × 2.5 cm的椭圆形。将定位好的大鼠置于Siemens Primus M直线加速器下采用5MeV的电子线照射双侧肾脏, 照射剂量分别为8、10、12、15 Gy, 方式为双肾照射。剂量率为300 cGy/min, 源皮距为100cm。对照组麻醉后佯装照射。
1.3 检测指标及方法 1.3.1 UP、UC检测照射后第1、3、6、9月, 各组随机取6只大鼠, 分别单独置于大鼠代谢笼, 禁食不禁水以排除食物对生化指标的影响, 收集24 h尿液, 送生化实验室分别测定UP、UC。
1.3.2 Scr及BUN检测照射后的1、3、6、9月, 各组随机取6只大鼠, 内眦静脉取血5ml, 处死大鼠并留取肾脏标本。静脉血送检验实验室分别测定CysC、及BUN。
1.3.3 形态学观察照射后第1、3、6、9月, 测量大鼠及双肾重量:受测大鼠给予24h禁食禁水处理, 安静状态下称重记录, 腹腔麻醉, 打开腹腔剥离双肾, 分析天平进行称重, 记录双肾重量。计算肾脏系数:肾脏系数=(双肾重量和/体重量)× 100%。将肾脏沿冠状面切成两半, 肾组织经10%甲醛固定, 常规石蜡包埋, 连续切片, HE染色, 光镜下观察肾小球、肾小管间质以及血管损伤程度的形态学变化。肾小球基于肾小球簇的硬化区域平均百分比分级:-:没有硬化; ±:硬化区域 < 5%;+:硬化区域5%~25%;+ +:硬化区域25%~50%;+++:硬化区域> 50%。肾小管间质损伤评级如下:-:没有损伤; ±:损伤 < 5%;+:损伤为5%~25%;++:损伤为25%~ 50%。血管病理改变评级通过血管壁增厚和管腔狭窄程度:-:没有增厚; +:轻度增厚; ++:中度增厚; +++:重度增厚。
1.4 统计学处理采用SPSS18.0统计软件进行分析, 所有数据均以x± s表示, 以单因素ANOVA进行检验, 组间两两比较采用LSD检验, P < 0.05为差异有统计学意义。
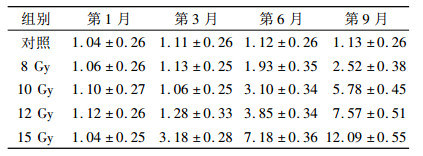
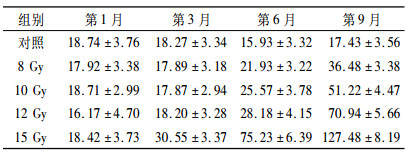
2 结果 2.1 UP/UC(即尿蛋白排泄率, 其增加是早期肾病诊断指标之一)与对照组相比, 各组均于照射后6个月升高(P < 0.01), 且照射后9个月的数值与第6个月相比, 升高明显(P < 0.01);不同照射剂量之间, 剂量较高组与较低组相比, 分别于不同时间点呈现显著差异(P < 0.01), 即照射后UP/UC改变具时间剂量依赖性, 见表 1。
|
|
表 1 照射后9个月不同时间UP/UC统计(g/g·100%) |
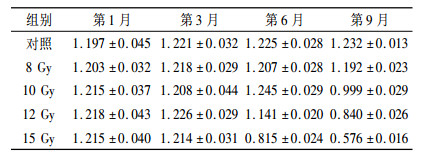
各组不同时间肾脏系数的比较与对照组相比, 照射后9个月各组肾脏系数均呈现下降趋势, 8 Gy照射后9个月变化均不明显, 10、12 Gy组于第9个月出现明显降低(P < 0.01), 而15 Gy组于照射后6个月出现明显下降, 且之后的每个时间点变化均比上一个月显著(P < 0.01);不同剂量之间, 照射后6个月起同一时间点不同剂量差异显著(P < 0.01), 即肾脏系数的变化于照射后9个月存在时间剂量依赖性, 见表 2。
|
|
表 2 各组不同时间肾脏系数的比较(x /%,x ± s) |
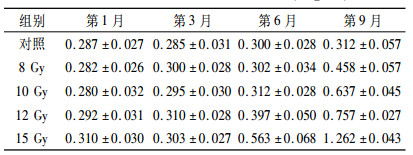
与对照组相比, 各组Scr均呈现升高趋势, 10Gy及以下照射组于照射后9个月升高显著(P < 0.01), 12 Gy及以上照射组显著改变出现于照射后第6个月, 之后改变均显著(P < 0.01);高剂量组与相对较低剂量组比较, 6个月后依次呈现显著差异(P < 0.01), 照射后9个月Scr改变存在时间剂量依赖性, 见表 3。
|
|
表 3 各组不同时间Scr的比较(mg /dl) |
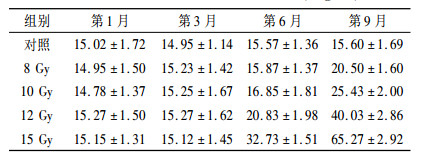
与对照组相比, 各组Scr均呈现升高趋势, 10 Gy及以下照射组与照射后9个月BUN升高显著(P < 0.01), 12 Gy及以上照射组显著改变出现于照射后第6个月, 之后改变均显著(P < 0.01);高剂量组与相对较低剂量组比较, 6个月后依次呈现显著差异(P < 0.01), 照射后9个月BUN改变存在时间剂量依赖性, 见表 4。
|
|
表 4 各组不同时间BUN的比较(mg /dl) |
与对照组相比, 各组CysC存在上升趋势, 10Gy及以上组照射后6个月起显著升高(P < 0.01), 8Gy组于9个月显著升高(P < 0.01);且剂量较高组别于照射后3个月起与较低组相比CysC数值较高, 差异具统计学意义(P < 0.01), 见表 5。
|
|
表 5 各组不同时间CysC的比较(ng /ml) |
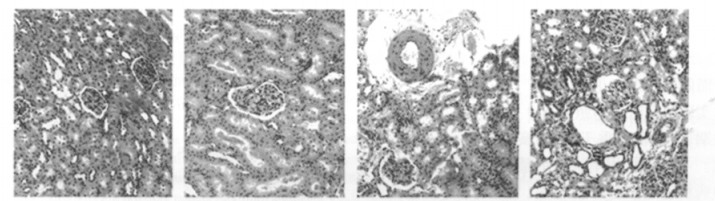
改变光镜下观察可见, 空白对照组肾脏结构清晰, 皮质、髓质结构正常, 肾小球、肾小管及间质均无异常改变。各照射组均观察到不同程度肾脏体积缩小, 皮质比例减小, 系膜细胞溶解, 后期呈现硬化趋势。其中15 Gy组硬化趋势最为明显。系膜基质与上皮细胞粘连, 肾小球毛细血管袢增厚, 血管腔扩大, 肾小管上皮细胞间隙增大, 部分上皮细胞肿胀、溶解、坏死。细胞基膜明显增厚(图 1d)。8 Gy组9月病理变化较轻微, 以系膜增生为主(图 1b)。15 Gy组3月开始12 Gy组6月开始可观察到肾小管间质纤维化改变, 但基本无炎性细胞浸润。9月均可观察到不同程度的血栓形成, 随剂量升高程度递增。见表 6, 图 1。
|
图 1 不同剂量照射后9个月光镜下结果 a:对照组,在每个时间节点均未发现明显异常; b:8Gy组,照射后9个月,显示系膜增生; c:12Gy组,照射后9个月,显示系膜增生,血管增厚,间质轻度纤维化; d:15Gy组,照射后9个月,显示肾小球硬化,肾小管扩张伴基底膜增厚,肾小管间质纤维化(HE×100) |
|
|
表 6 各照射剂量不同时间点HE染色统计结果 |
放疗是肿瘤治疗的重要手段之一, 但在治疗同时也会对正常组织器官产生一定影响。肾脏是放射敏感性器官, 在放疗过程中功能易受到损伤, 形成放射性肾病, 即肾经电离辐射, 可导致进展性的肾功能减退并伴有肾小球硬化和(或)肾小管间质纤维化。其损伤程度主要取决于照射总量、照射次数、照射体积和照射时期[1]。本实验采用不同剂量电子线照射大鼠肾脏, 在9个月的观察过程中, 成功构建了大鼠放射性肾损伤模型, 通过观察不同剂量照射后及不同时间点肾脏形态学、功能的变化, 探讨低分割照射后肾脏的放射生物学效应。
前期文献多以X射线进行照射, 本实验采用电子线取代X射线照射, 这是由大鼠肾脏解剖位置决定。高能电子束由于具有有限的射程, 可以有效的避免对靶区后深部组织的照射, 这是其最重要的剂量学特点。而高能X射线表面剂量比较低, 随着深度的增加, 深度剂量逐渐增加, 直至达到最大剂量点后呈指数递减[2]。大鼠体表至射野后界厚度约为1.7 cm左右, 故选用5 MeV电子线, 较大限度的保护了肾脏后面的肠壁组织, 减少肠道并发症的发生, 从而减小对实验效应的影响。已有研究证实, X射线照射大鼠剂量低于7.8 Gy时在一定时期内(< 26周)不会出现明显的肾损伤, 而高于13.3 Gy则会因产生急性肠道并发症致死[3, 4]。而本研究15 Gy照射组采用15 Gy电子线将大鼠肠道损伤有效控制, 并未出现因肠道坏死而致死的样本。且根据预实验结果, 高于15 Gy的放射线可因其肠道并发症等原因使存活率较低, 无法进行后续实验。Liu等[5, 6]曾经报道, 肾脏经过X射线单次照射(7~25 Gy)呈现剂量依赖性, 照射方法为单肾剖腹照射。通过对前期文献的参考, 本实验选取8 ~15 Gy分梯度进行照射以探讨不同剂量产生的生物学效应。
CysC是一种低分子量碱性蛋白质, 能够自由通过肾小球滤过膜, 并在近曲小管中几乎完全被重吸收和降解, 不再重新回到循环中, 同时肾小管不分泌CysC。且有实验证实CysC监测与传统的GFR检测方法相比更具有优越性, 特别是对GFR仅轻度升高的肾损害意义更大[7]。Scr和BUN比较容易受到肌肉组织质量、饮食蛋白摄入、肾小管分泌和肾外代谢等因素的影响, 故本研究选取CysC、Scr、BUN综合评价肾小球功能变化。本实验中, CysC、Scr、BUN均随时间推移呈现不断增高趋势, 具有时间与剂量依赖性。各照射组相比, 15 Gy照射组上述三个指标均明显升高(P < 0.05), 且升高时间最早, 12 Gy、10 Gy照射组次之, 8 Gy照射组变化最不明显, 说明肾功能损伤程度呈剂量依赖性, 即单次剂量大者损伤也加重。同一剂量组内比较, 肾脏功能损伤程度改变随着时间呈进行性加重, 呈现时间依赖性。这可能与肾组织更新缓慢, 肾实质细胞破坏后再生力低有关。
本研究光镜下观察病理显示, 各剂量组照射后, 大鼠肾小球、肾小管及肾间质均可产生一定的损伤, 但各个部位和各种细胞对射线的敏感性差异化明显。内皮细胞, 尤其是毛细血管的内皮细胞是对放射最敏感的细胞, 为肾脏放射损伤的靶点[8]。内皮细胞的损伤是可以修复的, 而基底膜的损伤往往是进行性的, 最终导致肾小球硬化[9]。肾小球的损伤是弥漫性的, 先于肾小管的改变。且病理改变具有时间剂量依赖性, 随时间延长各组病理损伤加重, 同一时间照射剂量越大损伤越明显。生化指标改变与病理变化大体相一致。本实验发现, 各照射组在照射后6月~9月生化指标均有显著升高, 提示照射后该时期损伤进展较快。而同期病理变化也印证了这点。
本实验研究时长为照射后9个月, 尚处于放射损伤急性期, 损伤程度重于修复, 实验结果也同样证实这一点。本研究采用单次大剂量照射大鼠双肾, 在9个月的病程进展中肾脏各组织(肾小球、肾小管及血管)均呈现渐进性病理改变, 未能反应常规分割照射中肾脏组织的修复问题。肾作为放射敏感器官, 对于分割剂量的变化比较敏感, 本实验组下一步研究将延长观察时间, 并对不同剂量分割照射造成的损伤及修复机制进行探索。
本研究表明, 大鼠单次双肾不同剂量电子线体外照射可引起不同程度肾脏形态及功能损伤, 且损伤程度与损伤出现时间同照射剂量相关, 即一定范围内(8 ~15 Gy)照射剂量越小所造成的肾脏损伤程度越轻, 出现时间越晚。经上述实验推测, 单次放射性治疗剂量越小, 造成肾脏损伤越小, 肾脏耐受性越强。因此降低单次分割剂量, 可以提高肾脏对放射的耐受性。
| [1] |
Robbins ME, Bonsib SM. Radiation nephropathy:a review[J]. Scanning Microsc, 1995, 9(2): 535-560. |
| [2] |
殷蔚伯, 余子豪, 徐国镇, 等. 肿瘤放射治疗学[M]. 北京: 中国协和医科大学出版社, 2008.
|
| [3] |
Moulder JE, Cohen EP, Fish BL. Captopril and losartan for mitigation of renal injury caused by single-dose total-body irradiation[J]. Radiat Res, 2011, 175(1): 29-36. DOI:10.1667/RR2400.1 |
| [4] |
Moulder JE, Fish BL. Late toxicity of total body irradiation with bone marrow transplantation in a rat model[J]. Int J Radiat Oncol Biol Phys, 1989, 16(6): 1501-1509. DOI:10.1016/0360-3016(89)90987-5 |
| [5] |
Delanian S, Baillet F, Huart J, et al. Successful treatment of radiation-induced fibrosis using liposomal Cu/Zn superoxide dismutase:clinical trial[J]. Radiother Oncol, 1994, 32(1): 12-20. DOI:10.1016/0167-8140(94)90444-8 |
| [6] |
Liu D, Razzaque MS, Nazneen A, et al. Role of heat shock protein 47 on tubulointerstitium in experimental radiation nephropathy[J]. Pathol Int, 2002, 52(5-6): 340-347. DOI:10.1046/j.1440-1827.2002.01362.x |
| [7] |
Ozer BA, Dursun B, Baykal A, et al. Can cystatin C be a better marker for the early detection of renal damage in primary hypertensive patients?[J]. Ren Fail, 2005, 27(3): 247-253. DOI:10.1081/JDI-56635 |
| [8] |
Schneider U, Besserer J, Mack A. Hypofractionated radiotherapy has the potential for second cancer reduction[J]. Theor Biol Med Model, 2010, 7: 4. DOI:10.1186/1742-4682-7-4 |
| [9] |
Jansen EP, Saunders MP, Boot H, et al. Prospective study on late renal toxicity following postoperative chemoradiotherapy in gastric cancer[J]. Int J Radiat Oncol Biol Phys, 2007, 67(3): 781-785. DOI:10.1016/j.ijrobp.2006.09.012 |