在核战争、核恐怖和核事故的情况下, 放射性核素通过呼吸道、消化道、皮肤和粘膜等进入机体导致放射性核素内污染, 使人体受到持续性照射, 特别是关键器官、组织、细胞受到持续性照射将诱发严重的辐射生物效应。在弄清污染的核素类型之后, 使用合适的促排剂, 可大大减少核素对人员的内照射危害。但是, 在放射突发事件的初期, 由于情况复杂, 很难快速确定造成污染的放射性核素类型; 而如果在鉴定出明确的核素种类后, 再使用相应的促排药, 此时往往已错过了用药的最佳时间, 促排效果大大下降; 同时, 在恐怖袭击的情况下, 可能会有多种放射性核素污染同时存在。因此, 如能研制对多种核素有效的广谱促排药, 在事件发生后快速给予, 可显著提高促排的效果。甲壳素(chitin, 简称CT)是由N-乙酰-2-氨基-2-脱氧-D-葡萄糖以β-1, 4糖苷键连接而形成的天然多糖, 而壳聚糖(chitosan, 简称CTS)是甲壳素经脱乙酰化处理后即N-脱乙酰化的产物, 是自然界中唯一的碱性多糖[1]。壳聚糖有很多功能特性, 例如亲水性、生物相容性、可降解性[2], 而且由于壳聚糖分子链上含有大量的-NH2和-OH可以分别作为配位点与静电反应位点而成为一种出色的金属螯合物[3], 此外, 壳聚糖的抗氧化特性同时也可以在体内发挥抗辐射的作用; 而乙二胺四乙酸含有氨羧基, 是经典的金属螯合剂, 但是EDTA有明显的副作用, 对肾脏、肝脏的损伤严重, 而且EDTA不能进入细胞, 因而不能将沉积于细胞内的放射性核素螯合出来, 而将EDTA与CTS接枝之后形成的复合物可利用氨基进一步制备形成纳米粒, 从而进入细胞, 将细胞内的放射性金属螯合出来。笔者通过酰化反应合成CTS-EDTA, 使产物既有伯氨基、羟基, 又有氨羧基, 形成两性离子型螯合物, 促进体内的放射性核素的排出, 同时也可发挥壳聚糖的辐射抗性, 切实解决军事及工业中的放射性核素体内污染问题。锶元素是混合裂变主要产物之一, 可经不同方式造成环境污染, 直接吸入或通过各种食物链进入人体内引起不同程度的内污染或损失效应。笔者以稳定锶元素为研究对象, 初步研究并比较了CTS与CTS-EDTA螯合锶元素的能力。
1 材料与方法 1.1 仪器恒温磁力搅拌器(DF-Ⅱ, 江苏省金坛市医疗仪器厂)、原子吸收光谱仪(SpectrAA 110/220, 美国Varian公司)、电子天平(FA1004, 上海天平仪器厂)、傅立叶变换红外光谱仪(MagnaIR, 美国Nicolet公司)、超导核磁共振仪(UNITY INOVA400, 美国Varian公司)、冷冻干燥机(FreeZone6 Liter Benchtop, 美国Labconco公司)、离心沉淀机(LXJ-Ⅱ, 上海医用分析仪器厂)、微型旋涡混合仪(XW-80A, 上海沪西分析仪器厂有限公司)、数字式酸度计(PHS-3TC, 上海天达仪器有限公司)、红外快速干燥箱(WS70-1, 巩义市英峪予华仪器厂)
1.2 试剂壳聚糖(Mw=185万DaDD=96.65%青岛海普生物技术有限公司, 经由本实验室提高脱乙酰度)、EDAC (上海共价化学科技有限公司)、乙二胺四乙酸(EDTA, AR上海化学试剂总厂所属上海试剂一厂)、盐酸(AR)、氢氧化钠(AR)、乙酸(AR)乙酸钠(AR)、氨水(AR)、SrCl2· 6H2O (AR)均购自国药集团化学试剂有限公司、D2O (GR北京崇熙科技孵化器有限公司)、CF3COOD (GR上海浩素化学技术有限公司)。
1.3 实验方法 1.3.1 壳聚糖的纯化将2.5g壳聚糖溶解于200mL1%醋酸溶液中, 加热至30℃并持续搅拌2h使壳聚糖充分解, 经4号砂芯漏斗抽滤之后, 用NH3· H2O将滤液pH值调至9, 然后反复离心洗涤, 经真空冷冻干燥备用。
1.3.2 CTS-EDTA的合成参考文献[4, 5]的报道, 称取0.1 gCTS, 加入10mL0.1mol/LHCl溶液, 在30℃, 持续磁力搅拌使CTS充分溶解, 再加入3.63gEDTA, 然后用5mol/LNaOH溶液调pH值至7, 再加入EDAC至最终浓度达0.1mol/L作缩合催化剂, 室温搅拌反应12h, 最后用去离子水、0.05mol/LNaOH溶液反复透析纯化, 经真空冷冻干燥之后即得产物。
1.3.3 CTS与CTS-EDTA的红外光谱扫描池窗材料:KBr; 红外光谱能量:40mW; 波数范围:400~4 000cm-1
1.3.4 CTS与CTS-EDTA核磁共振氢谱检测频率: 400MHz; 溶剂:D2O/CF3COOD (V/V=4:1);扫描范围:0~ 13ppm
1.3.5 CTS与CTS-EDTA体外螯合锶离子的对比实验首先用SrCl2· 6H2O配备10-4mol/L (即8.762mg/L) Sr2+溶液, 分设10min、30min、60min、90min共4个时间点, 每个时间点设Control组、CTS组与CTS-EDTA组, 每组同时设3个平行样。在各组试管中加入10mL10-4mol/L (即8.762mg/L) Sr2+溶液, 在微型旋涡混合仪上震荡混匀, 然后分别在10min、30min、60min、90min后以3 000rpm离心10min, 用原子吸收光谱法测定上清液中Sr2+浓度。
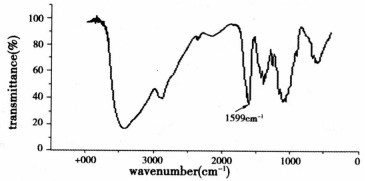
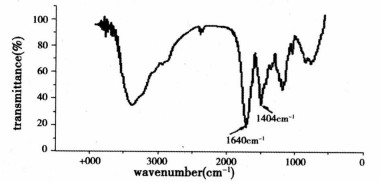
2 结果与讨论 2.1 红外光谱分析将合成前的CTS与合成后CTS-EDTA经充分干燥后, 与KBr压片进行红外扫描, 见图 1图 2。在CTS红外光谱(图 1)上, 1 599cm-1为壳聚糖上游离-NH2变形振动特征峰[6], EDTA通过缩合反应连接在该基团上; 在CTSEDTA红外光谱(图 2)上, 1 640cm1为EDTA与CTS连接的酰胺键的特征峰[6], 而1 404cm-1为CTS-EDTA钠盐中-COO-的特征峰[7], 都表明EDTA成功地连接到了CTS上。
|
图 1 壳聚糖红外光谱图 |
|
图 2 CTS-EDTA红外光谱图 |
将合成前的CTS与合成后CTSEDTA经充分干燥后, 用氘代试剂D2O/CF3COOD (V:V=4:1)作为溶剂溶解后, 扫描其核磁共振氢谱, 见图书室3, 图 4。
|
图 4 CTS-EDTA核磁共振氢谱图 |
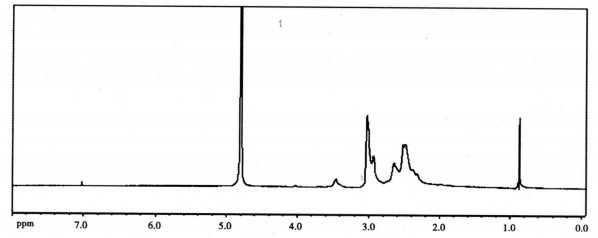
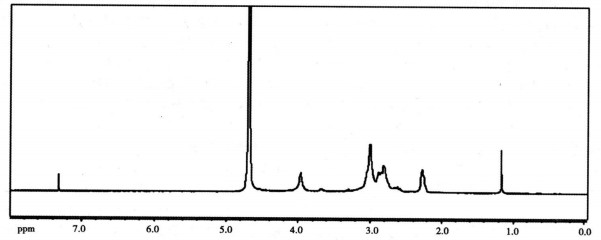
在CTS氢谱(图 3)上, δ4.878与δ1.3处的氢峰为溶剂峰, δ4.152处的氢峰归属于壳聚糖上的H-1, δ2.8-3.4处的氢峰归属于壳聚糖吡喃糖环上的H-3、H-4、H-5与亚甲基上的H-6, 而δ2.467处的氢峰归属于壳聚糖上的H-2[8, 9]; 在CTS-EDTA氢谱(图 4)上, 对比CTS氢谱出现了新的氢峰位移, 与CTS有部分氢峰重叠, δ4.996与δ1.1处的氢峰为溶剂峰, 由于复合物中亚甲基的增多, CTS-EDTA连接物CTS上的H-1信号峰移向了低场, 由δ4.878移至δ3.630, 而δ2.9-3.3归属于CTS上的H-3、H-4、H-5与H-6, δ2.8-2.2则主要为EDTA亚甲基中的氢峰位移, 与CTS上的H-2重叠; 由此, 我们推断EDTA被成功接枝到CTS上。
|
图 3 CTS核磁共振氢谱图 |
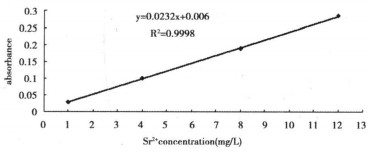
用标准值为1 000ug/mL的锶元素标准溶液配备浓度分别为1mg/L、4mg/L、8mg/L与12mg/L的锶元素溶液, 在原子吸收光谱仪上测定其平均吸光度, 作出锶元素浓度与吸光度之间的标准曲线图, 见图 5。
|
图 5 Sr2+浓度及其吸光度之间的标准曲线 |
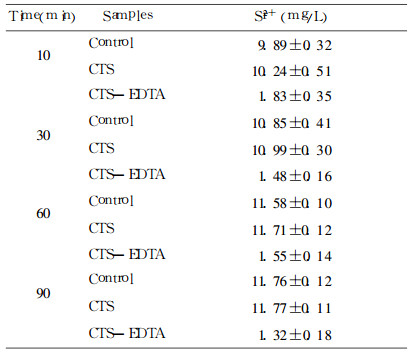
从图 5可见, 所作的标准曲线图的线性相关系数R2= 0.9998, 线性相关度良好, 说明Sr2+浓度在1mg/L~12mg/L的范围内, 所测溶液中Sr2+浓度与吸光度之间有良好的线性关系。可用作标准曲线图, 由测得的锶元素吸光度经所示公式y =0.0232x+0.006推算出相应的浓度。分别测定时间点10min、30min、60min与90min时各组溶液中Sr2+的浓度, 结果如表 1所示:
|
|
表 1 CTS与CTS-EDTA对Sr2+的体外螯合结果(x±s, n=6) |
由于用原子吸收光谱火焰法测量溶液中Sr2+的浓度变化时, 仪器会有累积效应, 所以按顺序从10min组、30min组、60min组至90min组地测量时, 导致Control组与CTS组的测得值均有轻微的上升趋势。尽管存在难以避免的仪器累积效应, CTS-EDTA组的测得值也是比Control组明显降低的。经统计学分析, 表 1中Control与CTS相比较, P>0.05, 无统计学意义, 说明CTS螯合Sr2+的能力极低; Control与CTS-EDTA相比较, P<0.0001, 有统计学意义, 说明连接了EDTA之后, CTS -EDTA螯合Sr2+的能力极大地提高。
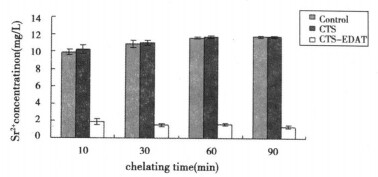
从各时间点Sr2+浓度与螯合时间之间的关系图(图 6)可以看到, 10min之后, CTS-EDTA组与Control组相比, 溶液中的Sr2+浓度急剧下降, 减少了约80%。经统计学分析, CTSEDTA组各时间点的Sr2+浓度的差异无显著性, 即表明随着时间的延长, Sr2+浓度的下降趋势不明显, 也可以说明螯合已接近平衡。
|
图 6 Sr2+浓度与螯合时间的关系图 |
通过缩合反应合成CTS-EDTA, 并通过红外图谱与核磁氢谱对合成的CTS-EDTA作了表征, 初步推断EDTA被成功接枝到CTS上; 而且CTS-EDTA螯合锶离子的能力在10min内可达到80%以上。这为进一步作体内螯合放射性锶元素或其他放射性元素的实验研究提供了实验依据。但是, 高分子量壳聚糖由于氢键作用, 结构紧密, 使得壳聚糖分子中活性官能团与自由基的作用机率降低, 抗辐射作用较低, 而低分子壳聚糖由于活性官能团的充分暴露, 易与自由基作用, 清除自由基, 发挥抗辐射的作用[10]。因此, 我们将在下一步实验中, 通过电离辐射降解和高温强碱洗脱法, 研制低分子量、高脱乙酰度的壳聚糖(要求黏均分子量为8 000Da, 脱乙酰度达95%以上), 合成的低分子量CTS-EDTA可以综合CTS的抗辐射特性与EDTA络合放射性金属离子的螯合性能, 发挥双重作用, 而且可以利用CTS-EDTA上富余的氨基进一步交联制备成纳米粒, 有望成为一种既能抗辐射又能将放射性金属离子从体内、甚至细胞内螯合出来的新型纳米型促排剂。
| [1] |
Jac-Young Je, Se-Kwon Kim. Reactive oxygen species scavenging activity of aminoderivatized chitosan with different degree of deacetylation[J]. Bioorganic & Medicinal Chemisty, 2006(14): 5989-5994. |
| [2] |
Bassi R, Prasher S O, Simpson B K. Removal of selected metal ions from aqueous solutions using chitosan flakes[J]. Separation Sciense and Technology, 2000(35): 547-560. |
| [3] |
FENG-CHIN WU, RU-LING TSENG, RUEY-SHIN JUANG. Kinetic modeling of liquid-phase adsorption of reactive dyes and metal ions on chitosan[J]. Wat.Res, 2001, 35(3): 613-618. |
| [4] |
Andreas Bernkop-Schnǜrch, Martina E.Krajicek. Mucoadhesive polymers as platforms for peroral peptide delivery and absorption:synthesis and evaluation of different chitosan-EDTA conjugates[J]. Journal of Controlled Release, 1998(50): 215-213. |
| [5] |
WU Zheng-hong, PING Qi-neng, LI Jian-ying, et al. Effect of Liposome Double-Coated with Chitosan and Chitosan EDTA Conjugates on Oral Absorption of Insulin[J]. Journal of Chinese Pharmaceutical Science, 2006, 15(3): 139-146. |
| [6] |
冯金城. 有机化合物结构分析与鉴定[M]. 北京: 国防工业出版社, 2003: 5.
|
| [7] |
王征, 刘万顺, 韩宝芹, 等. 低分子量壳聚糖及其衍生物的制备与溶菌酶对其降解的实验研究[J]. 海洋科学, 2007, 31(10): 36-40. DOI:10.3969/j.issn.1000-3096.2007.10.012 |
| [8] |
徐海娥, 闫翠娥. 叶酸和聚乙二醇接枝作基因载体用壳聚糖的合成与表征[J]. 化学研究与应用, 2007, 19(1): 60-63. DOI:10.3969/j.issn.1004-1656.2007.01.013 |
| [9] |
覃彩芹.壳低聚糖结构表征与分子量及其生物活性功能研究[C].武汉大学博士学位论文, 2002.
|
| [10] |
刑荣娥, 刘松, 于华华, 等. 不同分子量壳聚糖和壳聚糖硫酸酯的抗氧化活性[J]. 应用化学, 2005, 22(9): 958-961. DOI:10.3969/j.issn.1000-0518.2005.09.008 |