近年来, 肿瘤内直接注入放射性药物, 已成为治疗肿瘤的一种新方法〔1, 2〕。使用的核素源有90Y和32P-β源, 具有短半衰期、短射程、高能量、低穿透力等特点。90Y玻璃微球和32P瓷球, 在治疗肝脏恶性肿瘤时, 一般有两种方法:一, 药物经肝动脉由导管注入, 由于是全肝给药, 药量难以控制, 对正常肝组织会造成损伤, 而病灶部位的剂量不够。二, 将放射性药物直接注入病灶部位, 使肿瘤受到足够照射后坏死, 而周围的正常组织又不受损伤。直接注射时药物主要集中在注射点附近, 瘤体的大小和注射的位置对治疗效果有直接影响。因而, 临床上需要一种肿瘤等效材料, 模拟瘤体的大小和注射位置, 直接测定肿瘤内的剂量分布, 根据肿瘤大小, 制定出合理的用药剂量和最佳注射位置。
用热释光方法实测32P在肝肿瘤等效材料中的剂量分布, 了解其杀伤范围, 对临床介入治疗有科学的指导意义。
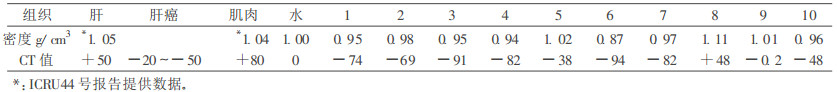
1 肝和肝癌等效材料的研制由ICRU44号报告提供的肝密度ρ: 1.053g/cm3, 肌肉密度ρ: 1.04g/cm3, 肌肉等效材料(RW-2), 密度ρ: 1.110g/cm3, 其物理性质为白色固体, 硬度和轫性较好, 可进行不同形状的加工。
由于肝和肌肉的密度较接近, 以肌肉等效材料为基准, 探索肝和肝癌等效材料的配方物质, 实验发现醋酸乙烯共聚物(EVA)和聚乙烯, 经高温熔化后, 按不同比例加入石蜡, 氧化钛, 氧化镁, 碳酸钙等物质充分熔化混匀, 冷却成型。选出密度接近1g/cm3的等效材料, 再进行CT扫描(机器型号: Shimadzu SCT-4500T, 工作条件: 120kV, 100mA, 280mA/s, L/2mm), 选出最接近人体正常肝和肝癌CT值的等效材料作为肝和肝癌等效材料。如表 1所示, 1~ 10 #等效材料的密度均接近1g/cm3, 但CT值的差异较大, 这种差异除了材料的配方物质不同外, 材料内部的均匀性也是原因之一。
|
|
表 1 比较肝和肝癌与等效材料的CT值 |
表 1中所有等效材料除配方物质不同外, 制作工艺完全一样。以肝和肝癌CT值为标准, 分别选出8#和10 #等效材料为肝和肝癌等效材料。这两种等效材料的区别是在醋酸乙烯共聚物(EVA/40 ~ 50)中, 加入其它配方物质的含量不同。将冷却成型的等效材料, 加工成5.5 ×3.1 ×2.5(cm3)小方块, 目的是检查材料内部是否有气泡, 同时也便于作摸拟实验时使用。
2 条件及方法监测剂量探测器:采用防化研究院生产的LiF(Mg.Cu.P)热释光方片, 尺寸为3.2×3.2×0.2(mm3)。它具有能响好, 灵敏度高和组织等效好等优点。每片的重复性误差5 %(10次), 10片测读分散性8%。用该剂量探测器测量β粒子的射程和剂量分布均优于粉末和管状剂量探测器。
测量仪:国产FJ-377热释光读出仪。
32P球源:将中国原子能研究院生产的32P瓷球粉末加入碘油后, 用振荡器使其悬浮液充分混匀后, 用微型注射器将150μL, 含4.4 ×105Bq的32P源, 注入直径为7.3mm的塑料小球内成为32P球源〔3, 4〕, 小球壁厚0.2mm。32P的平均E =0.695MeV, T1/2 =14d, 平均射程2.9mm。
用肝癌等效材料摸拟实体瘤, 取10片LiF(Mg.Cu.p)剂量探测器, 测量其剂量分布〔5, 6〕。任意取两块肝癌等效材料, 在第一块肝癌等效材料中心挖一小方孔5×5 ×2.3(mm3)。热释光剂量探测器按顺序编号1 ~ 10#排列放入小方孔内, 片与片之间必须整齐重叠, 剂量探测器与等效材料之间的空隙处必须用等效材料填满。在第二块肝癌等效材料中心, 用直径7.5mm的钻头钻一个深度为2.5cm圆孔, 要求圆孔底部为圆弧形, 弧度与32P球源的弧度基本相同, 圆孔底部圆弧的切点位置处钻透一直径约1.0mm小孔。实验时将放有剂量探测器的第一块肝癌等效材料与第二块肝癌等效材料完全重叠, 要求剂量探测器的中心对准小孔后, 再将32P球源放入圆孔内进行照射。这样β射线就可从1.0mm小孔射出, 近似为窄束β射线。从而保证每次实验时, 32P源的位置, 活度和体积不变。如图 1所示:

|
图 1 32P源在肝癌等效材料中的照射位置 |
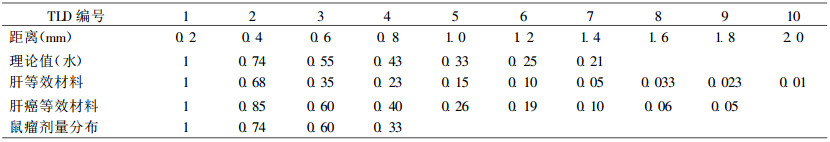
肝等效材料的实验步骤与肝癌等效材料相同, 照射时间、实验次数、照射位置和剂量探测器排列顺序及重叠位置完全一样, 以减少系统误差, 保证实验数据的可靠性, 结果列表 2。
|
|
表 2 32P源在肝、肝癌等效材料和鼠瘤中的剂量分布 |
为了验证和比较上述实验, 实测了32P源在鼠瘤内剂量分布。实验步骤如下:在昆明鼠腋下注入瘤细胞1 ×107/mL, 接种后8d, 长成1.5 ×1.4 ×1.0(cm3)至2.2 ×1.5 ×1.4 (cm3)实体瘤〔7〕, 杀死小鼠取出瘤块迅速冷冻, 等瘤块冻实后, 取出将瘤体切开分成两半块, 在其中半块瘤体上戳一小坑正好能注入32P源15 μL(1.1 ×105Bq), 盖上厚度为0.15mm的塑料薄膜, 将编有序号的热释光片重叠放在32P源上, 再盖上塑料薄膜。在另半块瘤体上戳一剂量探测器大小的方孔后, 再盖在剂量探测器上, 照射10min, 取出剂量探测器进行测量。结果列在表 2。
3 实验结果表 1中, 肝和肝癌等效材料的密度和CT值分别接近人体正常肝和肝癌的密度和CT值。表 2中肝和肝癌等效材料的剂量分布的变化趋势较一致。由表 1可知, 肝等效材料的密度和CT值均比肝癌等效材料高。所以肝等效材料对β射线的吸收比肝癌等效材料快, 如表 2所示。物质的密度越大, 对β射线的吸收越快。
表 2中10片剂量探测器的实测值结果是距32P球源0.2 ~ 2.0mm, 表中两种等效材料结果是同一实验条件下, 3次实验的平均值, 用0.2mm处均值归一后获得。在距源1.2mm处β射线剂量已减少80 %以上, 在距源2.0mm处已减少95 %以上。
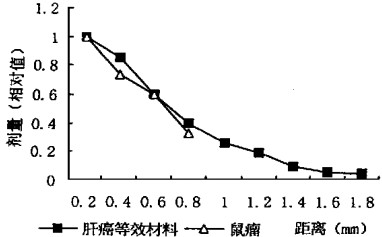
图 2比较了32P源在肝癌等效材料和鼠瘤中的剂量分布曲线。从曲线看, 32P源在肝癌等效材料中的剂量分布与鼠瘤中的剂量分布较一致, 在鼠瘤中距源0.8mm处约65 %以上剂量被吸收。在肝癌等效材料中距源0.8mm处60 %剂量被吸收。从肝癌等效材料的密度, CT值及对β射线的吸收与肿瘤基本一致。所以, 肝癌等效材料可以用于临床, 对肝癌大小, 注射位置, 注射点数及用药量进行模拟, 采用热释光方法实测肝癌剂量分布, 制定最佳的治疗方案, 对提高疗效, 减少病人痛苦和费用有非常重要的意义。
|
图 2 32P源在肝癌等效材料和鼠瘤中的剂量分布曲线 |
由于实验条件限制, 每片剂量探测器的厚度不一致在0.20 ~ 0.295mm之间, 10片总厚度2.58mm, 平均厚度误差12 %, 在表 2中每片剂量探测器所用厚度是0.20mm。若加上球源的壁厚0.2mm, 第一片剂量探测器距32P源应大于0.4mm。第10片热释光剂量探测器距32P球源应为2.78mm。
由于此实验是模拟核医学治疗中的瘤内直接注射法, 32P源在肿瘤内为理想的球源分布[8]。对不规则分布(如:点, 柱, 面源和任意型状源), 在此不进行讨论。
表 2和图 2的结果告诉我们, 肝等效材料对β射线的吸收比肝癌等效材料快, 在治疗中确定注射位置和注射点数时, 应考虑远离正常肝组织和其他正常器官, 以防受其损伤, 提高治疗质量。为临床开展肿瘤内照射治疗提供剂量学参考。
| [1] |
Order S. E., et al. A new method for delivering radioactive cyto-toxic agents in solid cancer[J]. Int. J. Radiot. Oncol. Biol. Phys, 1994, 30: 715-720. DOI:10.1016/0360-3016(92)90960-P |
| [2] |
Richard B., et al. Treatment of cancer with intratumoral infusion of radioisotopes[J]. Int. J. Radion. Oncol. Bsol. Phys, 1994, 30(3): 737-739. DOI:10.1016/0360-3016(92)90965-K |
| [3] |
Bochkarev V. V., et al. Distribution of absorbed energy from a point beta -source in a tissue -equivalent medium[J]. Interna-tional Journal of Applied Radialion and Isotopes, 1972, 23: 493-504. DOI:10.1016/0020-708X(72)90131-7 |
| [4] |
Werner Barry L., Kwork Cheuk S., Das Indea J. Dose distribu-tion in regions containing beta sources : large spherical source re-gions in a homogeneous medium[J]. Medical physics, 1988, 15(3): 358-365. DOI:10.1118/1.596231 |
| [5] |
Griffith Max H., et al. Direct dose confirmation of quantitative autoradiography with micro-TLD measurements for radioim-munotherap[J]. The Journal of Nuclear Medicine, 1988, 29(11). |
| [6] |
Wessels Barry W., Griffith M. Howard. Miniature thermolu-minescent dosimeter absorbed dose measurements in tumor phantom models[J]. The Joumal of Nuclear Medicine, 1986, 27: 1308-1314. |
| [7] |
Howell Roger., Narra Venkat R., Rao Dandamudi V. Ab-sorbed dose calculations for rapidly growing tumors[J]. The Journal of nuclear, 1992, 33(2). |
| [8] |
Howell Roger W., Rao Dandamudi V. Macroscopic dosimetry for radioimmunotherapy nonuniform activity distributions in solid tumors[J]. Med. Phys, 1989, 16(1). |