2. 陕西步长制药有限公司, 陕西 西安 710075;
3. 陕西国际商贸学院, 陕西 咸阳 712046;
4. 陕西省中药绿色制造技术协同创新中心, 陕西 西安 710075;
5. 青海省中医院, 青海 西宁 810000
2. Shaanxi Buchang Pharmaceutical Limited Company, Xi'an 710075, China;
3. Shaanxi Institute of International Trade & Commerce, Xianyang 712046, China;
4. Collaborative Innovation Center of Green Manufacturing Technology for Traditional Chinese Medicine in Shaanxi Province, Xi'an 710075, China;
5. Qinghai Hospital of Traditional Chinese Medicine, Xining 810000, China
冠心舒通胶囊是由君药广枣、臣药丹参、佐药丁香和冰片、使药天竺黄五味构成, 用于胸痹心血瘀阻证, 临床用于治疗冠心病、心绞痛出现的胸痛、胸闷、心慌、气短等症[1]。目前, 关于冠心舒通胶囊的临床疗效与作用机制相关研究较多, 质量控制研究较少。2020版中国药典冠心舒通胶囊的含量测定方法分为气相色谱法与高效液相色谱法[2], 气相色谱法以龙脑、异龙脑、丁香酚为指标成分, 高效液相色谱法以丹参酮ⅡA、丹酚酸B为指标成分, 质量控制较为全面, 但存在以下3个问题: ①色谱条件较多(气相色谱法1个检测条件, 高效液相色谱法2个检测条件), 为含量测定带来不便; ②君药广枣具有行气活血, 养心, 安神的功效[3], 临床主要用于气滞血瘀, 胸痹作痛, 心悸气短, 心神不定等症, 对冠心舒通胶囊发挥疗效至关重要, 且广枣的量(480 g) 占整个处方量(840 g) 约57%, 所占比重较大, 但含量测定未纳入君药广枣的指标成分; ③含量测定部分共包含5个对照品, 成本较高。
一测多评法(quantitative analysis of multi-components by single marker, QAMS) 作为一种可实现多个成分同步含量测定的多指标质量控制分析方法, 已应用于各国药典, 在多种中药材、饮片及中药制剂的多成分含量测定中得到广泛应用[4, 5], 如丹参、重楼、保心宁片、脑心清片等。冠心舒通胶囊未见一测多评方面的研究报道, 因此本文以原儿茶酸为内标物, 建立一测多评法同时测定冠心舒通胶囊中没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA 10种成分含量, 拟解决上述提到的色谱条件多、含量测定无君药广枣药效成分、成本高等问题。
材料与方法仪器与试剂 Agilent 1260型高效液相色谱仪(美国安捷伦公司); Waters 2695型高效液相色谱仪(美国Waters公司); 电子分析天平(型号BP211D, d = 0.01 mg, 德国赛多利斯天平有限公司); 超声波清洗器(型号: KQ-250DE型, 昆山市超声仪器有限公司); Agilent ZORBAX Extend-C18色谱柱(250 mm × 4.6 mm, 5 μm), Kromasil C18色谱柱(250 mm × 4.6 mm, 5 μm)、Diamonsil C18色谱柱(250 mm × 4.6 mm, 5 μm)。对照品丹参素钠(批号: 110855-201311, 纯度98.1%)、没食子酸(批号: 110831-200302, 纯度99.1%)、原儿茶醛(批号: 110810-201007, 纯度98.2%)、原儿茶酸(批号: 110809-201205, 纯度99.9%)、迷迭香酸(批号: 111871-201203, 纯度98.8%)、香草醛(批号: 100491-200901, 纯度100%, 供UV法测定)、丹参酮IIA (批号: 110766-200416, 纯度 > 99.8%)、丹酚酸B (批号: 111562-201313, 纯度97%)、丁香酚(批号: 110725-201213, 纯度99.7%)、隐丹参酮(批号: 110852-200806, 纯度 > 98%), 均购自中国食品药品检定研究院; 甲醇为色谱纯(美国Fisher试剂公司), 水为纯净水, 其他试剂均为分析纯。
实验材料 20批冠心舒通胶囊由陕西步长制药有限公司生产, 样品批号分别为120101 (S1)、120103 (S2)、120201 (S3)、120203 (S4)、120205 (S5)、120207 (S6)、120208 (S7)、120304 (S8)、120305 (S9)、120311 (S10)、120805 (S11)、120806 (S12)、120903 (S13)、120403 (S14)、120503 (S15)、130816 (S16)、131105 (S17)、131106 (S18)、131107 (S19)、131108 (S20)。
色谱条件 采用Agilent C18 (ZORBAX Extend RP C18, 250 mm × 4.6 mm, 5 µm) 色谱柱, 以甲醇(A)-0.4%甲酸水溶液(B) 为流动相, 梯度洗脱程序为0~15 min, 3%~28% A; 15~17 min, 28%~36% A; 17~40 min, 36%~38% A; 40~60 min, 38%~57% A; 60~80 min, 57%~75% A; 80~90 min, 75%~90% A; 90~100 min, 90%~100% A。流速1.0 mL·min-1, 检测波长280 nm, 柱温35 ℃, 进样量5 µL。
混合对照品溶液制备 精密称取没食子酸等10种对照品适量, 加甲醇溶液制成每1 mL分别含没食子酸7.575 μg、丹参素钠89.000 μg、原儿茶酸17.400 μg、原儿茶醛2.900 μg、香草醛2.178 μg、迷迭香酸73.814 μg、丹酚酸B 1.096 mg、丁香酚333.000 μg、隐丹参酮21.400 μg、丹参酮ⅡA 115.000 μg的溶液作为混合对照品溶液。
供试品溶液制备 精密称定冠心舒通胶囊内容物0.5 g, 置具塞锥形瓶中, 精密加入甲醇10 mL, 密塞, 称定重量, 超声(功率250 W, 频率40 kHz) 30 min, 放冷, 再称定重量, 用甲醇补足减失的重量, 摇匀, 滤过, 取续滤液, 即得。
专属性 取空白溶液、混合对照品溶液、供试品溶液分别进行测定, 比较色谱图。
线性关系 将混合对照品溶液分别进样2、4、6、8、10和12 μL, 以没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮、丹参酮IIA进样量(x, μg·mL-1) 与峰面积(Y) 作标准曲线, 计算回归方程。
精密度 精密吸取同一混合对照品溶液, 按色谱条件测定6次, 测定峰面积, 计算10种成分含量的RSD。
稳定性 取同一批供试品溶液, 于0、2、4、6、8、12和24 h按色谱条件进行测定, 记录峰面积, 计算10种成分含量的RSD。
重复性 取同一批供试品溶液, 按“供试品溶液制备”方法平行制备6份供试品溶液, 按色谱条件进行测定, 记录峰面积, 计算10种成分的含量RSD。
加样回收率 取6份冠心舒通胶囊内容物约0.25 g, 精密称定, 以1∶1的比例加入适量对照品溶液, 置具塞锥形瓶中, 精密加入甲醇10 mL, 密塞, 称定重量, 超声处理(功率250 W, 频率40 kHz) 30 min, 放冷, 再称定重量, 用甲醇补足减失的重量, 摇匀, 滤过, 取续滤液, 按色谱条件进行测定, 计算回收率。
相对校正因子的测定 相对校正因子(f) 计算公式为f = (As/Cs) / (Ai/Ci), 其中As、Cs分别为内参物对照品的峰面积和浓度; Ai、Ci分别为待测成分对照品的峰面积和浓度。分别进样4、6、8和10 μL, 按色谱条件项下测定各成分色谱峰峰面积, 以原儿茶酸为内参物, 计算不同进样量下其他9种成分的相对校正因子的平均值, 比较RSD值。
不同仪器、色谱柱对相对校正因子的影响 分别考察不同型号仪器(Agilent 1260型、Waters 2695型高效液相色谱仪) 和色谱柱(Agilent ZORBAX Extend-C18、Kromasil C18、Diamonsil C18, 规格为250 mm × 4.6 mm, 5 μm) 对相对校正因子的影响, 计算相对校正因子的平均值, 比较RSD值。
不同柱温对相对校正因子的影响 考察不同柱温(33、34、35、36和37 ℃) 对相对校正因子的影响, 计算相对校正因子的平均值, 比较RSD值。
不同流速对相对校正因子的影响 考察不同流速(0.8、0.9、1.0、1.1和1.2 mL·min-1) 对相对校正因子的影响, 计算相对校正因子的平均值, 比较RSD值。
待测组分色谱峰的定位 取混合对照品溶液, 按色谱条件分别测定不同型号仪器(Agilent 1260型、Waters 2695型高效液相色谱仪) 和色谱柱(Agilent ZORBAX Extend-C18、Kromasil C18、Diamonsil C18, 规格为250 mm × 4.6 mm, 5 μm) 各待测色谱峰的保留时间, 以原儿茶酸色谱峰保留时间为基准, 采用相对保留时间值对色谱峰进行定位, 并计算RSD值。
样品含量测定 取20批冠心舒通胶囊样品适量, 按供试品溶液制备方法制备样品溶液, 按色谱条件进行测定, 分别采用一测多评法和外标法(external standard method, ESM) 计算冠心舒通胶囊中没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的含量, 并用相对误差(RE) 进行评价。
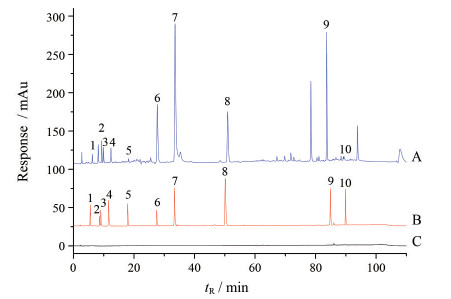
结果 1 方法学考察 1.1 系统适应性10个成分与相邻色谱峰分离度均大于1.5, 色谱图见图 1, 专属性良好。
|
Figure 1 High performance liquid chromatograms of Guanxinshutong capsule (A), mixed references (B) and blank solvent (C). 1: Gallic acid (GA); 2: Sodium danshensu (SDSS); 3: Protocatechuic acid (PCA); 4: Protocatechuic aldehyde (PCAE); 5: Vanillin (VL); 6: Rosmarinic acid (RA); 7: Salvianolic acid B (SAB); 8: Eugenol (EG); 9: Cryptotanshinone (CTS); 10: Tanshinone IIA (TST) |
各成分在各自范围内线性关系良好, 具体结果见表 1。
| Table 1 Linear relationships of ten components |
没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的RSD分别为0.266%、1.694%、1.354%、1.659%、1.333%、1.455%、1.580%、1.351%、1.807%和1.034%, 表明仪器精密度良好。
1.4 重复性没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的RSD分别为2.877%、2.650%、2.727%、2.144%、1.199%、2.377%、1.906%、1.188%、2.805%和2.852%, 表明该方法重复性良好。
1.5 稳定性没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的RSD分别为0.655%、0.924%、0.695%、0.749%、0.719%、1.601%、0.473%、0.492%、0.086%和0.998%, 表明溶液在24 h内稳定性良好。
1.6 加样回收率没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的加样回收率分别为100.601%、99.149%、103.474%、103.362%、101.162%、98.609%、98.204%、101.981%、100.423%和102.083%, RSD分别为2.474%、2.463%、1.871%、1.845%、1.702%、1.763%、2.836%、1.253%、2.162%和2.823%, 表明方法准确度高。
2 一测多评法 2.1 相对校正因子的测定以原儿茶酸为内参物, 没食子酸、丹参素钠、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的相对校正因子分别为0.759、3.630、0.185、0.532、4.240、3.245、1.729、0.691和0.702, RSD值均小于3%。
2.2 不同仪器、色谱柱对相对校正因子影响不同高效色谱仪及色谱柱条件下, 计算各成分的相对校正因子如表 2所示, RSD值均小于2.5%, 表明不同的高效液相色谱仪和色谱柱对相对校正因子没有显著影响, 方法稳定性好。
| Table 2 The relative correction factor (f) of different instruments and chromatographic columns (n = 3). C1: Kromasil C18; C2: Diamonsil C18; C3: Agilent ZORBAX Extend-C18 |
不同柱温下计算相对校正因子, RSD值分别为1.311%、0.401%、2.184%、1.728%、0.931%、1.063%、1.252%、1.899%和2.416%, 表明各化合物相对校正因子在33~37 ℃的稳定性良好。
2.4 不同流速对相对校正因子的影响不同流速下计算相对校正因子, RSD值分别为2.267%、1.426%、2.431%、2.006%、0.368%、0.664%、1.917%、1.503%和2.344%, 表明各成分相对校正因子在0.8~1.2 mL·min-1流速内稳定性良好。
2.5 待测组分色谱峰的定位采用相对保留时间(tR) 法确定各待测组分的出峰时间[6, 7], 结果见表 3, RSD小于3%, 差异较小, 表明采用相对保留时间法对冠心舒通胶囊中10种有效成分进行峰定位具有可行性。
| Table 3 Relative retention time determined by different instruments and columns (n = 3) |
通过外标法测定冠心舒通胶囊中没食子酸、丹参素钠、原儿茶酸、原儿茶醛、香草醛、迷迭香酸、丹酚酸B、丁香酚、隐丹参酮和丹参酮ⅡA的平均含量分别为227.381、3.283、0.457、0.150、65.213、1.035、18.204、9.265、1.449和1.939 mg·g-1。采用一测多评法分别以原儿茶酸为内参物计算待测成分的含量, 与外标法测得的含量进行比较, 结果见表 4, 表明10种有效成分均能在20批样品中检测出来, 两种方法测得RE值在-3%~3%, 表明一测多评法可行, 结果准确度较高。
| Table 4 Content (mg·g-1) of ten components determined by quantitative analysis of multi-components by single marker method (QAMS) and external standard method (ESM). n = 3. RE (%) = (QAMS - ESM) / ESM × 100 |
本研究选择了活性明确、含量较高的代表成分作为冠心舒通胶囊质量控制的指标性成分进行一测多评法的含量测定, 主要包括了酚酸类没食子酸、原儿茶酸、迷迭香酸、丹酚酸B, 酚类丹参素钠、原儿茶醛、香草醛、丁香酚, 丹参酮类隐丹参酮和丹参酮ⅡA。其中没食子酸、丹参素钠、原儿茶酸、原儿茶醛、迷迭香酸和丹酚酸B具有改善心肌缺血、抑制动脉粥样硬化、抗血小板凝聚、缓解脑缺血再灌注、改善微小循环功能的药效作用[8-10], 香草醛可以通过血脑屏障, 通过减少体内和体外的氧化应激损伤而发挥神经保护作用[11], 丁香酚可通过调节下丘脑-垂体-肾上腺皮质和脑内单胺系统发挥抗应激作用在神经保护过程中发挥重要作用[12, 13], 隐丹参酮和丹参酮ⅡA是治疗心血管疾病的有效药物, 具有抗动脉粥样硬化、清除氧自由基、改善血流动力学、保护心肌及抑制心肌凋亡等作用[14]。因此, 所选指标成分均具有与冠心舒通胶囊中医理论、药理作用和主治功能相符的药理特性。
比较乙酸乙酯、50%甲醇、无水甲醇、50%乙醇、95%乙醇、无水乙醇和水等不同溶剂作为供试品提取溶剂时的峰面积的个数、峰面积的大小, 选择甲醇为最佳提取溶剂; 比较加热回流提取法与超声提取法用于供试品制备时的色谱图, 峰面积与个数差异不大, 考虑操作便捷选择超声提取法, 并对超声时间进行考察, 选择30 min; 先后考察了乙腈、甲醇为有机相, 磷酸、醋酸、甲酸水溶液为水相的洗脱结果, 甲醇-0.4%甲酸水溶液色谱峰能被较好的分离出来。
通过全波长扫描, 10种成分最大吸收在280 nm处较多, 其余吸收都在280 nm附近, 且色谱基线平稳、基线分离良好、灵敏度均较好, 可以满足定量分析要求, 因此选择280 nm作为检测波长。
一测多评法仅需1个价廉易得的有效成分, 即可实现多成分的同步测定[15]。原儿茶酸价廉易得, 是君药广枣发挥药理活性的重要物质基础[16]。2020版中国药典中使用原儿茶酸对照品的共9处, 其中北沙参药材、狗脊饮片、棕榈饮片、天王补心丸、急支糖浆、脑心清片、柿叶提取物以原儿茶酸为对照品进行薄层色谱鉴别, 狗脊饮片、刺五加浸膏以原儿茶酸为质量控制成分进行含量测定, 且为很多企业制剂、院内制剂的质控指标成分, 因此可采用原儿茶酸为内参物, 控制冠心舒通胶囊质量的同时, 也可用于其余药材、饮片、提取物、制剂的质量控制, 兼顾标品共享、节省成本的原则。
本课题组采用该测定方法, 构建心肌细胞缺氧/复氧(H/R) 模型, 测定10种成分对H/R心肌损伤作用, 结果表明除香草醛、没食子酸和原儿茶醛无保护作用, 其余均有明显的保护作用, 为冠心舒通胶囊治疗冠心病筛选出7种活性成分[17]。由于冠心舒通胶囊中佐药丁香和冰片均含有挥发油, 且龙脑、异龙脑是药典的质控成分, 因此下一步拟建立气相一测多评方法, 完善冠心舒通胶囊的质量控制体系。
作者贡献: 龙凯花进行了一测多评方法的建立、实验数据处理、撰写文章; 杜霞和刘洋进行了实验设计及文章修改等; 王春柳和杨东花对本文的方法建立提供帮助; 刘峰、张红、李晔从选题与设计、方法建立及文章修改提供了指导。
利益冲突: 无利益冲突。
| [1] |
Huang ZZ, Nie XZ, Chen YB, et al. Effect of Guanxinshutong capsule on Ca2+-CaM-CaMPKⅡδ in cardiomyocytes influence of signal system[J]. Chin Tradit Pat Med (中成药), 2017, 39: 1701-1705. |
| [2] |
Chinese Pharmacopeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[M]. Beijing: China Medical Science Press, 2020: 1416.
|
| [3] |
Huang YJ, Tong HY, Huang XJ, et al. Research progress and molecular docking research on pharmacological activities of Choerospondias axillaris in the treatment of cardiovascular diseases[J]. Asia-Pac Tradit Med (亚太传统医药), 2021, 17: 170-176. |
| [4] |
Wang ZM, Qian ZZ, Zhang QW, et al. Technical guidelines established by the quantitative analysis of multi-components by single marker method[J]. China J Chin Mater Med (中国中药杂志), 2011, 36: 657-658. |
| [5] |
Hu RX, Liang YH, Xu WL, et al. Application and research progress of QAMS in traditional Chinese medicine[J]. China J Pharm Anal (药物分析杂志), 2019, 39: 1968-1979. |
| [6] |
Liang XY, Zhou XG, He B, et al. Simultaneous determination of 7 constituents in Xiao'er Jinqiao granules by QAMS[J]. J China Pharm (中国药房), 2020, 31: 1179-1184. |
| [7] |
Wang Y, Ju ZC, Zhang T, et al. Determination of six effective ingredients in Imperatae Rhizoma concentrated granules by ultra-performance liquid chromatography using two internal references[J]. Acta Pharm Sin (药学学报), 2022, 57: 467-473. |
| [8] |
Liu M, Huang HG, Yu NC, et al. Simultaneous determination of five water soluble components of Salvia miltiorrhiza in Yangshen Kangshuai mixture by high performance liquid chromatography[J]. Chin J Hosp Pharm (中国医院药学杂志), 2021, 41: 2447-2450. |
| [9] |
Zhao YX, Chen YQ. Rosmarinic acid attenuates hypoxic-ischemic encephalopathy in neonatal rats through AMPK/mTOR pathway[J]. Tradit Herb Drugs (中草药), 2021, 52: 6897-6903. |
| [10] |
Lu ML, Qin JP, Luo YD, et al. Establishment of HPLC fingerprints of Bawei Longzuan Granules and determination of seven constituents[J]. Chin Tradit Pat Med (中成药), 2019, 41: 1232-1236. |
| [11] |
Tang LP, Yan J, Fan F, et al. The Neuroprotective effect of vanillin on hypoxic-ischemic brain injury in neonatal rats[J]. Prog Mod Biomed (现代生物医学进展), 2021, 21: 3833-3840, 3855. |
| [12] |
Li SS, Li F, Li F, et al. Research progress in chemical constituents and pharmacodynamics of Eugenia caryophyllata[J]. Northwest Pharm J (西北药学杂志), 2021, 36: 863-868. |
| [13] |
Garabadu D, Sharma M. Eugenol attenuates scopolamineinduced hippocampal cholinergic, glutamatergic, and mitochondrial toxicity in experimentalrats[J]. Neurotox Res, 2019, 35: 848-859. DOI:10.1007/s12640-019-0008-6 |
| [14] |
Liu L, Zhang LJ, Min Y, et al. Research progress on pharmacological action of tanshinone ⅡA[J]. J Jilin Med Univ (吉林医药学院学报), 2020, 41: 212-214. |
| [15] |
Zhu JJ, Wang ZM, Gao HM, et al. Advances on quality evaluation of Chinese materia medica by QAMS[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2016, 22: 220-228. |
| [16] |
Xang P, Ma XQ, Ma CM, et al. Simultaneous determination of five active components in Choerospondiatis Fructus by RP-HPLC[J]. Pharmacol Clin Chin Mater Clin Med (中药新药与临床药理), 2018, 29: 189-193. |
| [17] |
Zhang RR, Huang ZZ, Long KH, et al. Preliminary screening of active components in Guanxin Shutong capsules based on myocardial cell protection[J]. Northwest Pharm J (西北药学杂志), 2020, 35: 57-61. |
 2022, Vol. 57
2022, Vol. 57


