血瘀证是指人体内血行不畅、壅阻血脉或血溢脉外、停积为瘀的证候[1]。血瘀证涉及多种疾病, 如冠心病心绞痛、糖尿病、肝硬化、痛经等[2, 3]。《灵枢·痈疽》云: “血泣则脉不通”, “邪与气血两凝, 结聚络脉”, 表明血瘀证主要体现在血液流动性、凝滞性与黏度的变化。而气血运行不畅所致瘀血阻滞经脉, 血不循经, 引发机体异常出血, 反复不止, 即凝血系统异常[4]。现代医学研究表明, 血瘀证的治疗策略包括改善血流动力学、改善血液流变学、调节微循环障碍、调节炎症反应、抗血栓、改善血管内皮功能等作用[5]。《神农本草经》始记大黄(Rhei Radix et Rhizoma)“下瘀血, 血闭, 破瘴瘕积聚”。现代研究表明大黄活血祛瘀功效的药理作用基础是改善微循环、改善血液流变性、抗血栓等[6]。这与现代医学对血瘀证的认识不谋而合。然而, 由于血瘀证病理机制比较复杂, 目前大黄治疗血瘀证的作用机制尚未完全阐明。前期的工作中, 本课题组基于大黄成分的积累特征进行研究[7], 并对大黄-桃仁药对治疗寒凝血瘀模型的血液流变学和凝血四项作用进行研究[8]。已有的研究也报道了大黄及其单体的活血化瘀作用, 尤其在大黄活性成分含量方面进行了总结。研究结果证实, 大黄蒽醌类化合物的母核结构引入氨基、取代氨基、烃基和阳离子成盐后的水溶性明显提高, 活血作用增强[9, 10]。当游离蒽醌衍生物中的8位羟基被葡萄糖基取代时, 大黄结合型蒽醌糖苷的水溶性增大, 同时对于血小板的亲和力增强[11]。上述内容为本研究的深入开展提供了依据。
代谢组学是机体受外源及内源性刺激后, 对动态应答产生的小分子代谢物的定量测定, 已被广泛用于探究疾病的分子机制[12]。Sheng等[13]利用代谢组学探索复方二仙汤调节双侧去卵巢大鼠脂质代谢紊乱特征。Gao等[14]借助代谢组学发现逍遥散抗抑郁与其调节能量代谢和神经递质有关。Xu等[15]采用代谢组学研究了瓜蒌-薤白药对可干预动脉粥样硬化小鼠肝脏甘油磷脂及鞘脂的代谢紊乱从而抑制动脉粥样硬化疾病。因此, 采用代谢组学定性定量检测血浆中的小分子代谢物, 并挖掘相应的差异代谢物和代谢通路对阐释大黄治疗血瘀证的代谢作用机制有重要意义。
本研究以大黄为研究对象, 通过检测大鼠血液流变学及凝血功能指标, 采用UHPLC-Q/TOF-MS对空白组、血瘀证组和给药组大鼠血浆中的内源性代谢物进行分析鉴定。采用多元统计分析方法进行代谢特征综合分析, 归纳并总结大黄调节血瘀证过程中的关键差异代谢物和差异代谢通路, 为深入探讨该药及其相关复方的治疗作用和血瘀证相关疾病的药效作用机制奠定基础。
材料与方法仪器与试剂 QTOF/MS-6545质谱仪、1290 Infinity LC超高效液相色谱仪(美国Aglient公司); 涡旋混合器MIX-200 (上海净信实业发展有限公司); 离心机5427R (德国艾本德公司); 甲醇(德国Merck公司)、乙腈(德国Merck公司)、甲酸(美国Thermo Fisher公司)、2-氯苯丙氨酸(美国Thermo Fisher公司) 均为分析纯; 大黄采于陕西省镇巴县, 经陕西中医药大学中药鉴定教研室胡本祥教授鉴定为药用大黄Rheum officinale Baill.的根及根茎; 盐酸肾上腺素注射液(批号H42021700) 购自中国武汉市大药业有限公司; 3.2%柠檬酸钠抗凝管(批号20200607)、肝素钠抗凝管(批号20190905) 购自于利医疗器械有限公司; 凝血酶原时间试剂盒(批号20190214)、活化部分凝血活酶时间试剂盒(批号20190214)、凝血酶时间试剂盒(批号20190114) 和血浆纤维蛋白原试剂盒(批号20192012) 购自中国泰州中勤世帝生物技术有限公司; 实验中使用的水通过使用Milli-Q水净化系统(美国Millipore公司) 进行净化。
实验动物 雌性健康SD (Sprague-Dawley) 大鼠(200 ± 20 g), 购自西安交通大学医学部实验动物中心, 动物许可证号: SCXK (陕) 2018-001。所有程序均按照中华人民共和国国家科学技术委员会颁布的《实验动物管理条例》进行。本研究已获得陕西中医药大学实验动物伦理委员会批准(批准号: SUCMDL20210309002)。
样品制备 称取3份大黄, 每份500 g。均用8倍量的水进行热回流提取1 h。自然冷却后, 倾出水煎液, 加入6倍量的水进行再次热回流提取1 h, 滤过, 倾出水煎液。自然冷却后, 合并水煎液进行70 ℃水浴浓缩至相当于生药1 g·mL-1, 冷藏备用。
动物分组、造模与给药 将48只雌性SD大鼠随机分为6组(每组8只), 即为空白对照组(control, C)、模型组(model, M)、大黄低剂量组(extracts of rhubarb with low doses, RRR-L)、大黄中剂量组(extracts of rhubarb with middle doses, RRR-M)、大黄高剂量组(extracts of rhubarb with high doses, RRR-H)、复方丹参滴丸阳性对照组(compound Danshen dripping pills, CDDP)。RRR-L组给药剂量为1.8 g·kg-1, 相当于临床等效剂量的2倍; RRR-M组给药剂量为3.6 g·kg-1, 相当于临床等效剂量的4倍; RRR-H组给药剂量为7.2 g·kg-1, 相当于临床等效剂量的8倍; CDDP组给药剂量为0.073 g·kg-1; 空白组、模型组给予相应容积的纯净水。大鼠均统一按体重灌胃给药, 每日1次, 连续给药7天, 药物剂量换算公式如下: 人每日剂量× 0.018 / 200 × 1 000 ×临床等效剂量。于第8天除空白组外其余各组大鼠皮下注射给予盐酸肾上腺素注射液0.8 mg·kg-1, 共2次, 间隔时间为4 h, 第1次给予盐酸肾上腺素2 h后将大鼠置于0~2 ℃冰水中游泳10 min, 造成大鼠急性血瘀模型[16]。第2次给予盐酸肾上腺素后, 禁食不禁水。于末次给药后12 h用异戊巴比妥腹腔注射麻醉, 腹主动脉取血。置于离心管(内含20 μL肝素钠溶液) 中, 静置30 min后, 3 500 r·min-1离心5 min, 取上清液, 即得血浆, -80 ℃保存。
样本前处理 取样本100 μL加入到对应的已编号的1.5 mL离心管中, 加入300 μL纯甲醇(含1 μg·mL-1的2-氯苯丙氨酸) 除去血浆中的蛋白。涡旋2 min, 放入-20 ℃冰箱孵育0.5 h。在4 ℃、12 000 r·min-1条件下离心10 min; 取200 μL上清液转移至新的1.5 mL离心管中, -20 ℃静置0.5 h。再将上清液在12 000 r·min-1、4 ℃条件下离心15 min。取上清液于进样瓶中, 等量吸取每个血浆样品20 μL合并, 将其混合均匀后作为血浆质控样本。
色谱条件 色谱柱: Waters ACQUITY UHPLC HSS T3 C18 (1.8 µm, 2.1 mm × 100 mm); 溶剂体系: 0.04%乙酸/水(A) 和0.04%乙酸/乙腈(B) 为流动相; 梯度程序: 0~3 min, 5%~21% B; 3~5 min, 21%~50% B; 5~9 min, 50%~70% B; 9~10 min, 70%~95% B; 10~14 min, 95%~5% B。柱温: 35 ℃; 流速: 0.3 mL·min-1; 进样量: 1 μL。
质谱条件 采用电喷雾离子源, 型号: Agilent 6410A; 正负离子模式质谱参数: 干燥器流速: 8 L·min-1; 雾化器压力: 40 psi (1 psi ≈ 6.9 kPa); 雾化器温度: 325 ℃; 碎裂电压: 135 V。
数据分析和模式识别分析 首先, 通过Proteo Wizard软件转换为mzML格式。峰提取、对准和保留时间校正由XCMS程序执行。支持向量回归模型用于校正峰面积。每组样品中的缺失率>50%的峰均应过滤。之后, 通过搜索实验室的自建数据库并整合公共数据库和metDNA, 可以获得代谢识别信息。最后, 通过R程序进行统计分析。统计分析包括单变量分析和多变量分析。单变量统计分析包括t检验和方差多重分析。多元统计分析包括主成分分析(principal component analysis, PCA)、偏最小二乘判别分析(partial least squares discrimination analysis, PLS-DA) 和正交偏最小二乘判别分析(orthogonal projection to latent structure discrimination analysis, OPLS-DA)。
统计学分析 使用IBM SPSS Statistics 21.0统计软件进行数据统计分析, 组间数据采用单因素方差分析(one-way ANOVA), 两组样本分析采用独立样本t检验, 分析数据以P<0.05为差异有统计学意义。
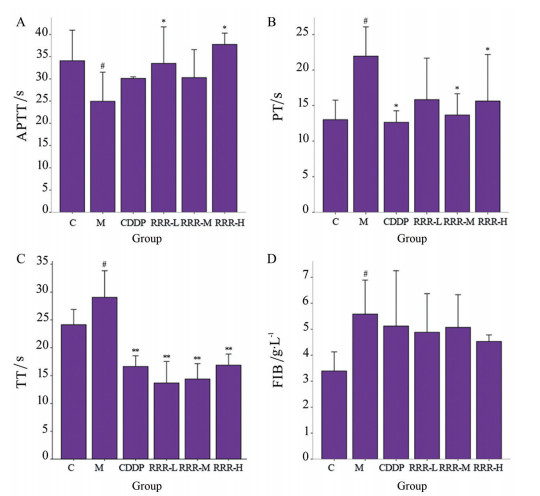
结果 1 各组大鼠凝血功能与血液流变学指标的变化结果如图 1所示, 与空白组相比, 模型组的全血黏度(whole blood viscosity, WBV) 和血浆黏度(plasma viscosity, PV) 显著升高(P<0.05), 表示造模成功。与模型组相比, RRR-L、RRR-M、RRR-H和CDDP组对WBV (1 s-1)、WBV (5 s-1)、WBV (50 s-1)、WBV (100 s-1)、WBV (200 s-1) 均有显著改善作用(P<0.01), CDDP组和RRR-L组对PV均有改善作用(P<0.05), 表明大黄具有调节血液流变学的作用。如图 2所示, 与空白组相比, 模型组的凝血酶时间(thrombin time, TT)、凝血酶原时间(prothrombin time, PT) 和活化部分凝血活酶时间(activated partial thromboplastin time, APTT) 水平显著降低(P<0.05), 血浆纤维蛋白原(plasma fibrinogen, FIB) 水平显著升高(P<0.05)。与模型组相比, 大黄组的TT、PT、APTT和FIB水平有不同程度的回调。特别是大黄治疗可以显著回调模型组的APTT (P<0.05); RRR-L组显著回调PT和APTT的异常(P<0.05); RRR-M组显著回调APTT的异常(P<0.01); RRR-H组显著回调TT和APTT (P<0.05或P<0.01) 的异常。CDDP组显著回调APTT和PT的异常(P<0.05或P<0.01)。上述结果表明大黄具有调节凝血功能的作用。

|
Figure 1 The effect of rhubarb on the hemorheology function of rats with blood stasis syndrome (n = 6, |
|
Figure 2 The effect of rhubarb on blood coagulation function in rats with blood stasis syndrome (n = 6, |
PCA3D结果显示, 在负(图 3A) 正(图 3B) 离子下空白组、模型组和给药组富集趋势均有所区别。OPLS-DA结果显示空白组与模型组分离明显, 负离子模式(图 4A) R2X = 0.369, R2Y = 0.995, Q2 = 0.837, 正离子模式(图 4B) R2X = 0.451, R2Y = 0.989, Q2 = 0.876, 证明模型的可靠程度较高。模型组与给药组分离明显, 负离子模式(图 4C) R2X = 0.387, R2Y = 0.992, Q2 = 0.868, 正离子模式(图 4D) R2X = 0.32, R2Y = 0.997, Q2 = 0.835。对模型进行200次随机排列组合实验, 验证了数据多元分析模型的有效性(图 4E、F)。结果表明各组之间代谢轮廓存在明显差异, 即各组之间血浆代谢物发生了变化。

|
Figure 3 PCA chart of rat plasma metabolites. A: Negative ion mode; B: Positive ion mode |

|
Figure 4 OPLS-DA diagram of rat plasma metabolites. A: Control group and model group in negative ion mode; B: Control group and model group in positive ion mode; C: Model group and Rhubarb with high-doses group in negative ion mode; D: Model group and rhubarb with high-doses group in positive ion mode; E: Random permutation and combination experiment in negative ion mode; F: Random permutation and combination experiment in positive ion mode |
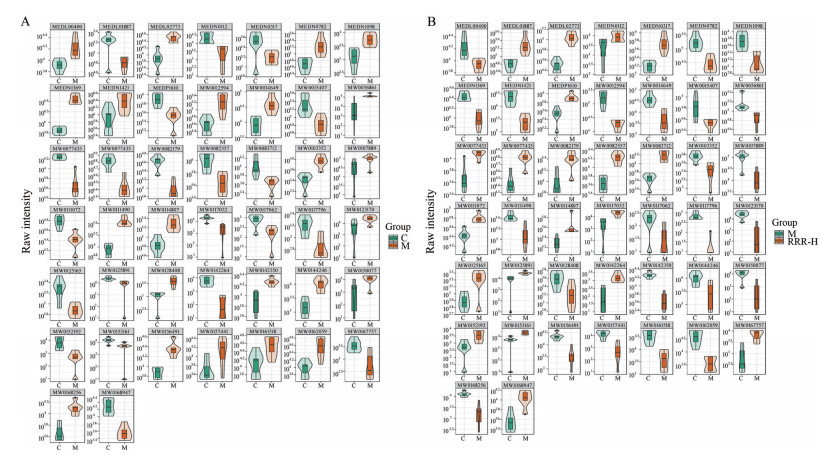
根据VIP ≥ 1, P<0.05, 差异倍数≥ 2或差异倍数≤ 0.5为标准筛选大黄调节血瘀证大鼠的血浆差异代谢物。在正负离子模式下, 分别鉴定正常组和模型组、模型组和RRR-H组的差异代谢物。与空白组相比, 模型组中共有226个代谢物发生显著性变化, 与模型组相比, RRR-H组共有155个代谢物发生显著性变化。44个差异代谢物在三组中均发生显著变化(图 5), 其中39个差异代谢物在空白组与模型组、模型组与RRR-H组中的变化趋势相反。即(±)8-HETE、牛磺脱氧胆酸、γ-鼠胆酸、2-甲酰氨基苯甲醛、四氢蝶酰二谷氨酸、视黄酸和乙酰氧基-8-姜酚等21个显著上调的差异代谢物转为下调。PC(15∶0/20∶2(11Z, 14Z))、PC(18∶1(9Z)/18∶1(9Z))、水杨醛、乙醇酸、马尿酸、水苏碱、柠檬酸、甲硫氧嘧啶和去甲哌啶等18个显著上调的差异代谢物转为下调。差异代谢物按化学类别分可分为氨基酸、脂肪酸、糖类、有机酸类、酚类、苯丙酸类等物质, 按代谢过程可分为脂质代谢类、花生四烯酸代谢类、氨基酸代谢类等。结果表明, 大黄可以通过调节PC(15∶0/20∶2(11Z, 14Z))、PC(18∶1(9Z)/18∶1(9Z))、(±)8-HETE、牛磺脱氧胆酸、γ-鼠胆酸等差异代谢物治疗血瘀证。
|
Figure 5 Violin diagram of differential metabolite expression levels. A: Differential metabolite in control group and model group; B: Differential metabolite in model group and rhubarb with high-doses group |
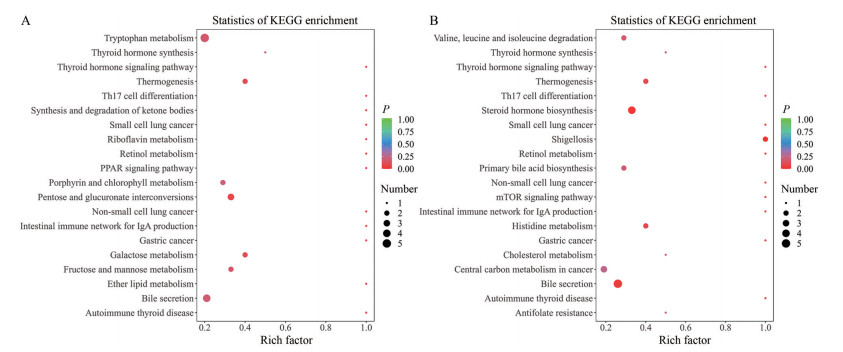
为了获得上述代谢物的表达信息, 作者进行了代谢途径富集分析。在空白组和模型组中共发现97条差异代谢途径, 在模型组和RRR-H组共发现74条代谢途径, 此处选择了具有统计学意义的(P<0.05) 前20条代谢途径。图 6A为正负离子下空白组和模型组的差异代谢途径, 图 6B为正负离子下模型组和RRR-H组的差异代谢途径, 其显著富集于脂质代谢、炎症因子和免疫和类固醇激素合成等。脂质代谢途径包括亚油酸代谢和不饱和脂肪酸等。炎症因子和免疫途径包括花生四烯酸代谢。类固醇激素合成途径包括类固醇激素生物合成。氨基酸代谢途径包括苯丙氨酸代谢和色氨酸代谢等。结果表明大黄可通过脂质代谢途径、炎症因子、免疫途径和类固醇激素合成途径治疗血瘀证。
|
Figure 6 Analysis of differential metabolic pathways in rats with blood stasis syndrome. A: Differential metabolic pathways in control group and model group; B: Differential metabolic pathways in model group and rhubarb with high-doses group |
本研究采用冰水暴露模拟大鼠的气滞状态, 导致血瘀证的发生。利用UHPLC-QTOF/MS技术和多元统计分析方法分别比较了对照组与模型组、模型组与给药组大鼠血浆中的代谢物, 发现了大黄影响血瘀证的44个差异代谢物, 97条差异代谢通路。主要结果包括: ①磷脂酰胆碱通过调节亚油酸代谢、花生四烯酸代谢、不饱和脂肪酸的生物合成途径调节脂质代谢功能。②花生四烯酸及其代谢产物(类花生酸) 可以促进促炎细胞因子的表达和炎症反应。③通过调节牛磺脱氧胆酸、γ-鼠胆酸改善类固醇激素的生物合成途径。
脂质代谢途径包括亚油酸代谢、α-亚麻酸代谢、花生四烯酸代谢、不饱和脂肪酸的生物合成等。在本研究中, 与空白组相比, 模型组中的PC(15∶0/20∶2(11Z, 14Z)) 和PC(18∶1(9Z)/18∶1(9Z)) 水平下调。与模型组相比, RRR-H组中的PC(15∶0/20∶2(11Z, 14Z)) 和PC(18∶1(9Z)/18∶1(9Z)) 水平上调。这与之前的研究一致[17-19], 磷脂酰胆碱是细胞膜结构中的主要磷脂, 参与氧化应激作用[20], 磷脂酰胆碱调节血小板合成途径, 调节血栓形成和炎症作用[21], 说明磷脂酰胆碱的代谢异常可能与血瘀证的发生和发展有关。
花生四烯酸代谢途径涉及前列腺素、血栓烷素和白细胞三烯等二十碳衍生物的直接前体的合成, 类二十碳烷酸对血液流变学、血管弹性、和血小板激活等具有重要的调节作用。在本研究中, 与空白组相比, 模型组大鼠体内的(±)8-HETE的水平高于健康大鼠, 9, 10-二羟基-12Z-十八碳烯酸的水平低于健康大鼠。大黄可以改善血瘀证大鼠体内(±)8-HETE和9, 10-二羟基-12Z-十八碳烯酸的异常水平。研究表明, 血瘀证的发病机制与炎症因子和免疫途径有关[22]。花生四烯酸及其代谢产物可以促进促炎细胞因子的表达和炎症反应[23]。花生四烯酸主要通过环氧合酶和脂肪加氧酶进行合成, 可以激活在血管平滑肌细胞上表达的G蛋白偶联受体, 从而引起炎症反应[24]。因此, 推测血瘀证的发生与花生四烯酸代谢紊乱引起的炎症有关。此外, 大黄可预防血瘀证的发生并抑制血瘀证的炎症状态。
类固醇激素的生物合成代谢途径主要包括雄激素和雌激素的产生。在本研究中, 与正常组对照相比, 模型组大鼠体内的牛磺脱氧胆酸、γ-鼠胆酸代谢物水平升高, 而大黄可明显改善其异常水平, 表明类固醇激素可能参与了血瘀证的发展。花生四烯酸环氧合酶产物促进类固醇生成急性调节基因表达, 生成类固醇激素[25]。一项研究表明, 肝硬化失代偿期患者的促肾上腺皮质激素、糖皮质激素水平与血瘀证有一定的相关性[26]。糖皮质激素能刺激骨髓造血功能使红细胞和血红蛋白含量增加。大剂量可使血小板和纤维蛋白原增加, 缩短凝血酶原时间, 刺激骨髓中的中性粒细胞释放入血而使中性粒细胞数增多的同时也使白细胞总数增加[27]。此外, 伴有血瘀证的原发性痛经与类固醇激素合成途径有关[28]。
本文基于UHPLC-QTOF/MS和多元统计分析研究大黄调节血瘀证的代谢机制, 初步证实了大黄通过调节脂质代谢途径、炎症因子和免疫反应途径及类固醇激素途径调节血瘀证, 为大黄的临床用药提供了参考, 同时也为其他多功效中药的代谢机制研究提供了新的思路和方法。
作者贡献: 沈霞和颜永刚负责整体设计及文章修改, 王艳霞负责实验操作、数据处理及文章撰写, 彭亮和杨冰月协助指导实验, 平凡、朱琳和佘鑫华协助完成动物实验。
利益冲突: 所有作者均不存在任何利益冲突。
| [1] |
Wang ZY, Li L, Liu JX, et al. Research progress of change of platelet in blood stasis syndrome and effect of traditional Chinese medicine[J]. China J Chin Mater Med (中国中药杂志), 2021, 46: 5201-5209. |
| [2] |
Vilchinsky V, Ginzburg K, Fait K, et al. Cardiac-disease-induced PTSD (CDI-PTSD): a systematic review[J]. Clin Psychol Rev, 2017, 55: 92-106. DOI:10.1016/j.cpr.2017.04.009 |
| [3] |
Pan XL, Hao EW, Xie JL, et al. Molecular mechanism of blood-activating and stasis- removing Chinese medicine in regulating blood stasis syndrome[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2018, 24: 227-234. |
| [4] |
Yang YZ, Deng Y, Yang XJ, et al. Effects of different compatibility of angelica sinensis on hemorheology, coagulation function and pathology of heart and lung in acute blood stasis rats[J]. Pharmacol Clin Chin Mater Clin Med (中药药理与临床), 2018, 34: 125-129. |
| [5] |
Zhang Q, Li YL. Discussion on the application of activating blood and resolving stasis in heart diseases[J]. J Liaoning Univ Tradit Chin Med (辽宁中医药大学学报), 2020, 22: 111-115. |
| [6] |
Lu L, Li HQ, Fu DL, et al. Rhubarb root and rhizome-based Chinese herbal prescriptions for acute ischemic stroke: a systematic review and meta-analysis[J]. Complement Ther Med, 2014, 22: 1060-1070. DOI:10.1016/j.ctim.2014.10.002 |
| [7] |
Li H, Hei XB, Li YM, et al. Characterization of accumulation profile of 10 constituents in various parts of Rheum officinale at different years old stage[J]. Chin Tradit Herb Drugs (中草药), 2019, 50: 1690-1697. |
| [8] |
Wang HY, Yan YG, Wang YL, et al. Ancient literature data mining on the best ratio of Taoren-Dahuang to promoting blood circulation and removing blood stasis and its effects analysis on rat model of cold congelation and blood stasis[J]. Chin J Tradit Chin Med Pharm (中华中医药杂志), 2018, 33: 2563-2567. |
| [9] |
Liu J, Wu F, Chen C. Design and synthesis of aloe-emodin derivatives as potent anti-tyrosinase, antibacterial and anti-inflammatory agents[J]. Bioorg Med Chem Lett, 2015, 25: 5142-5146. DOI:10.1016/j.bmcl.2015.10.004 |
| [10] |
Tan P, Zhang HZ, Li Y, et al. Preliminary study on antiplatelet aggregation of 10 anthraquinones in Rhei Radix et Rhizoma based on bioassay[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 859-865. |
| [11] |
Zhang HZ, Tan P, Liu ZD, et al. Activating blood biological potency assay and chemical fingerprint chromatogram applied to quality evaluation of rhubarb[J]. Acta Pharm Sin (药学学报), 2017, 52: 436-442. |
| [12] |
Nam M, Kim MS, Hwang G. Optimization and validation of capillary electrophoresis- and gas chromatography-tandem mass spectrometry methods for the analysis of intermediate metabolites in glycolysis and pentose phosphate pathways within biological samples[J]. J Chromatogr A, 2021, 1656: 462-531. |
| [13] |
Sheng N, Wang CH, Jia ZX, et al. The mechanism of Er-xian decoction in regulating lipid metabolism disorders on bilateral ovariectomized rats based on metabolomics study[J]. Acta Pharm Sin (药学学报), 2021, 56: 2403-2409. |
| [14] |
Gao Y, Wang P, Xu T, et al. Comprehensive analysis of antidepressant metabolic characteristics of Xiaoyao San and its mechanism of regulating energy metabolism and neurotransmitter[J]. Chin Tradit Herb Drugs (中草药), 2021, 52: 1360-1368. |
| [15] |
Xu PB, Ding LD, Chou JW, et al. Study on effect of "trichosanthis fructus-allii macrostemonis bulbus" on atherosclerosis in ApoE-/- mice based on liver metabonomics[J]. China J Chin Mater Med (中国中药杂志), 2021, 46: 5320-5329. |
| [16] |
Li SJ, Li WX, Tang YP, et al. Comparative analysis of the promoting blood effects of the combination of different proportions of Danggui and Honghua by the principal component analysis and multi-attribute comprehensive index methods[J]. Acta Pharm Sin (药学学报), 2014, 49: 1304-1309. |
| [17] |
Tan J, Wang C, Zhu H, et al. Comprehensive metabolomics analysis of Xueshuan Xinmaining tablet in blood stasis model rats using UPLC-Q/TOF-MS[J]. Molecules, 2018, 23: 1650. DOI:10.3390/molecules23071650 |
| [18] |
Yuan ZW, Zhong LJ, Ji P, et al. Plasma metabolomics of angelica intervene in blood stasis syndrome rats[J]. Nat Prod Res Dev (天然产物研究与开发), 2018, 30: 559-567. |
| [19] |
Cao D, Xu C, Xue Y, et al. The therapeutic effect of Ilex pubescens extract on blood stasis model rats according to serum metabolomics[J]. J Ethnopharmacol, 2018, 227: 18-28. DOI:10.1016/j.jep.2018.08.026 |
| [20] |
Stamenkovic A, O'hara kimberley A, Nelson DC, et al. Oxidized phosphatidylcholines trigger ferroptosis in cardiomyocytes during ischemia-reperfusion injury[J]. Am J Physiol Heart Circ Physiol, 2021, 320: H1170-H1184. DOI:10.1152/ajpheart.00237.2020 |
| [21] |
Li L, Yao DN, Lu Y, et al. Metabonomics study on serum characteristic metabolites of psoriasis vulgaris patients with blood-stasis syndrome[J]. Front Pharmacol, 2020, 11: 558731. DOI:10.3389/fphar.2020.558731 |
| [22] |
Ma CY, Liu JH, Liu JX, et al. Relationship between two blood stasis syndromes and inflammatory factors in patients with acute coronary syndrome[J]. Chin J Integr Med, 2017, 23: 845-849. DOI:10.1007/s11655-016-2746-0 |
| [23] |
Sandre P, Da SC, De VP, et al. Chronic nutritional restriction of omega-3 fatty acids induces a pro-inflammatory profile during the development of the rat visual system[J]. Brain Res Bull, 2021, 174: 366-378. DOI:10.1016/j.brainresbull.2021.07.001 |
| [24] |
Edwards JM, Mccarthy CG, Wenceslau CF. The obligatory role of the acetylcholine-induced endothelium-dependent contraction in hypertension: can arachidonic acid resolve this inflammation?[J]. Curr Pharm Des, 2020, 26: 3723-3732. DOI:10.2174/1381612826666200417150121 |
| [25] |
Shao J, Wang HX, Yuan GL, et al. Involvement of the arachidonic acid cytochrome P450 epoxygenase pathway in the proliferation and invasion of human multiple myeloma cells[J]. Peer J, 2016, 4: e1925. DOI:10.7717/peerj.1925 |
| [26] |
Zhao FR, Zhao LH, Wang TF, et al. ACTH and GC levels in patients with hepatitis cirrhosis at two stages and their correlation with TCM pattern elements[J]. J Beijing Univ Tradit Chin Med, 2015, 38: 351-355. |
| [27] |
Huang LQ, Zhao CQ. Research progress of glucocorticoid in obstetrics and gynecology[J]. J China Pharm (中国药房), 2012, 23: 4214-4216. |
| [28] |
He Y, Wang LJ, Liu TT, et al. Analysis of therapeutic mechanism of siwutang in primary dysmenorrhea syndrome based on metabolomics technique[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2017, 23: 82-89. |
 2022, Vol. 57
2022, Vol. 57


