桂花(Osmanthus fragrans), 别称岩桂、木犀, 为木犀科(Oleaceae) 木犀属(Osmanthus) 植物, 广泛分布在我国长江流域及其以南地区, 资源十分丰富。桂花作为我国传统十大名花之一, 具有良好的观赏价值。除此之外, 由于其花香浓郁, 也常被作为天然香料用于制作食品与化妆品。桂花在自然选择和人工选择的双重作用下, 形成了众多品种。以花色和开花季节作为划分的依据, 桂花被分为金桂、银桂、丹桂和四季桂四大品种群[1]。桂花具有良好的药用价值。《本草纲目》中记载: 桂花生津、避臭、化痰、治疗风火牙痛。现代研究发现, 桂花中含有木脂素类、三萜类、苯乙醇类、环烯醚萜类等类型的化学成分[2-4], 其中桂花乙醇提取物具有抗炎、抗氧化、降血糖等生物活性[5-7]。
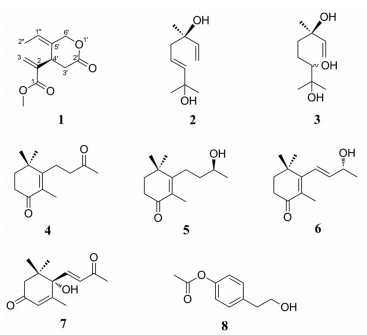
金桂(Osmanthus fragrans var. thunbergii) 为金桂品种群的代表品种, 是桂花的一个变种, 其花的颜色为金黄色, 浓至柠檬黄。本课题组前期对不同品种的桂花进行了比较系统的化学成分研究以及药理活性测定, 发现了一些具有良好生物活性的化合物[8-10]。鉴于金桂具有丰富的资源, 为了进一步了解其化学成分, 并为其开发利用奠定基础, 本课题组对金桂开展了较为系统的化学成分研究。结果从金桂干花95%乙醇提取物中分离得到8个化合物, 经1D、2D-NMR、HR-ESI-MS、IR、UV等波谱技术结合其理化性质分别鉴定为: (R, E)-2-(5-亚乙基-2-氧代四氢-2H-吡喃-4-基) 丙烯酸甲酯[methyl (R, E)-2-(5-ethylidene-2-oxotetrahydro-2H-pyran-4-yl) acrylate, 1]、(R, E)-2, 6-二甲基-辛-3, 7-二烯-2, 6-二醇(2)、(6R)-2, 6-二甲基-辛-7-烯-2, 3, 6-三醇(3)、2, 4, 4-三甲基-3-(3-氧代丁基)-环己-2-烯-1-酮(4)、(S)-2, 4, 4-三甲基-3-(3-羟基丁基)-环己-2-烯-1-酮(5)、(R, E)-2, 4, 4-三甲基-3-(3-羟基丁基-1-烯-1-基)-环己-2-烯-1-酮(6)、(S, E)-3, 5, 5-三甲基-4-羟基-4-(3-氧代丁-1-烯-1-基)-环己-2-烯-1-酮(7) 和对乙酰氧基苯乙醇(8)。其中化合物1为新化合物, 其余化合物均为首次从金桂植物中分离得到(图 1)。
|
Figure 1 The structures of compounds 1-8 |
化合物1: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热不显色; 薄层喷以碱性高锰酸钾, 显黄色;
1的1H NMR谱(400 MHz, CDCl3) 数据显示了14组氢信号。其中δH 6.30 (1H, s)、5.68 (1H, s) 和5.75 (1H, dd, J = 8.2, 7.0 Hz) 为烯氢信号; δH 3.78 (3H, s) 为甲氧基氢信号, δH 1.54 (3H, d, J = 7.0 Hz) 为与次甲基相连的甲基信号; δH 2.73 (1H, dd, J = 15.3, 6.7 Hz) 和2.83 (1H, dd, J = 15.3, 6.7 Hz) 为同碳偶合的脂肪亚甲基氢信号; δH 4.63 (1H, d, J = 12.8 Hz) 和4.86 (1H, d, J = 12.8 Hz) 为与吸电子基团相连的同碳偶合的脂肪亚甲基氢信号, δH 3.94 (1H, t, J = 6.7 Hz) 为脂肪次甲基氢信号。
1的13C NMR谱(DEPT谱) 显示了11个碳信号, 其中δC 172.2 (C) 和166.4 (C) 为2个酯羰基碳信号, 提示1中有2个酯基; δC 140.3 (C)、131.5 (C)、127.0 (CH) 和126.5 (CH) 为4个烯碳信号, 提示1中有2个双键; δC 52.3 (CH3) 为1个甲氧基碳信号, δC 72.7 (CH2) 为与吸电子基团相连的亚甲基信号, δC 35.9 (CH2) 为1个脂肪亚甲基信号, δC 36.1 (CH) 为1个脂肪次甲基碳信号和δC 14.1 (CH3) 为1个脂肪甲基碳信号。以上信息并结合1的不饱和度, 推测1可能为含有1个单环的单萜类化合物。
1的HSQC谱显示, δH 6.30 (1H, s) 和5.68 (1H, s) 均与δC 127.0 (CH) 相关, 提示δH 6.30和5.68为烯碳δC 127.0上的两个末端烯氢; δH 2.73 (1H, dd, J = 15.3, 6.7 Hz) 和2.83 (1H, dd, J = 15.3, 6.7 Hz) 与δC 35.9 (CH2) 相关, 证实δH 2.73和2.83为脂肪亚甲基δC 35.9上两个氢原子; δH 4.63 (1H, d, J = 12.8 Hz) 和4.86 (1H, d, J = 12.8 Hz) 与δC 72.7 (CH2) 相关, 证实δH 4.63和4.86为与吸电子基相连的脂肪亚甲基δC 72.7上两个氢原子。
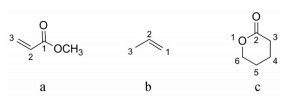
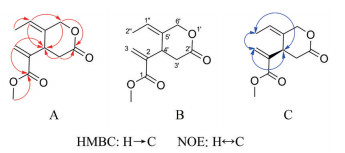
1的HMBC谱(图 2A) 显示, 末端烯氢信号δH 6.30 (1H, s) 和5.68 (1H, s), 以及甲氧基氢信号δH 3.78 (3H, s), 均与酯羰基δC 166.4存在远程相关, 提示1的结构中存在一个丙烯酸甲酯片段(a片段); 脂肪甲基氢信号δH 1.54 (3H, d, J = 7.0 Hz) 与δC 131.5 (C) 和126.5 (CH) 存在远程相关, 且与烯氢δH 5.75 (1H, dd, J = 8.2, 7.0 Hz) 相互偶合, 提示1结构中存在一个丙烯基片段(b片段); δH 2.73 (1H, dd, J = 15.3, 6.7 Hz) 和2.83 (1H, dd, J = 15.3, 6.7 Hz) 以及δH 4.63 (1H, d, J = 12.8 Hz) 和4.86 (1H, d, J = 12.8 Hz) 均与δC 172.2 (C)、131.5 (C) 和36.1 (CH) 存在远程相关; δH 3.94 (1H, t, J = 6.7 Hz) 与δC 172.2 (C)、131.5 (C)、72.7 (CH2) 和35.9 (CH2) 存在远程相关, 提示1结构中存在一个氧代四氢吡喃环片段(c片段)。
|
|
Figure 2 The key HMBC correlations (A), the planar construction (B) and the key NOE correlations (C) of 1 |
a片段的H-3 [δH 6.30, 5.68 (1H each, s)] 与c片段的C-4 (δC 36.1) 存在远程相关, c片段的H-4 (δH 3.94) 与a片段的C-2 (δC 140.3) 和C-3 (δC 127.0) 存在远程相关, c片段的H-3 (δH 2.73和2.83) 与a片段的C-2 (δC 140.3) 存在远程相关, 证明a片段(丙烯酸甲酯) 的C-2与c片段的C-4相连; b片段H-2 (δH 5.75) 与b片段的C-1 (δC 131.5), c片段的C-4 (δC 36.1) 和C-6 (δC 72.7) 存在远程相关, 同时, 结合1的分子式, 证明b片段的C-1和c片段的C-5为同一原子; b片段H-3 (δH 1.54) 与c片段的C-5 (δC 131.5) (即b片段C-1) 存在远程相关, 进一步证明b片段和c片段共有一个碳原子。至此, 1的平面结构确定为2-(5-乙烯基-2-氧代四氢-2H-吡喃-4-基) 丙烯酸甲酯[methyl-2-(5-ethylidene-2-oxotetrahydro-2H-pyran-4-yl) acrylate] (图 2B)。
1的NOEDS谱1显示, 当照射H-2'' (δH 1.54) 时, H-4' (δH 3.94) 和H-3 (δH 5.68, 6.30) 信号分别产生了增益, 说明H-2''与H-4'和H-3之间存在NOE相关关系, 即证明甲基与C-4'和Δ3处于同侧, 故确定双键Δ5'(1'')为顺式(E) 构型; 1的NOEDS谱2显示, 当照射H-4' (δH 3.94) 时, H-3 (δH 5.68) 信号产生了增益, 即H-4'与H-3之间存在NOE相关关系, 加之, NOEDS谱1中也显示了H-2''和H-3信号之间存在NOE相关关系, 证明a片段(丙烯酸甲酯) 应取代在c片段(氧代四氢吡喃环) 的环上方, 即C-4'的绝对构型为R-构型。
综上所述, 最终确定1为methyl (R, E)-2-(5-ethylidene-2-oxotetrahydro-2H-pyran-4-yl) acrylate (图 2C), 为一新化合物, 并命名为金桂素(osthunin)。根据1的1H、13C NMR、HSQC以及HMBC谱, 将1的1H和13C信号全部进行了归属(表 1)。
| Table 1 1H (400 MHz) and 13C NMR (100 MHz) data of 1 in CDCl3 |
Bruker AV-400核磁共振仪(Varian Corporation, USA); 静电场轨道阱质谱(Thermo Fisher Scientific, USA); Nicolet 6700红外分光光度计(Thermo Electron Co., USA); UV-3600紫外分光光度计(Shimadzu, Kyoto, Japan); GL-3000制备高效液相色谱仪(Gelai Precision Instruments Co., Ltd., Chengdu China); 薄层色谱硅胶GF254、柱色谱用硅胶G (青岛海洋化工有限公司, 300~400目、200~100目); 柱色谱聚酰胺(江苏长丰化工有限公司); MCI CHP-20P (75~150 μm, 日本Mitsubishi公司); 其余试剂为分析纯; 金桂干燥花朵, 2019年8月采自四川省成都市都江堰市, 经四川大学华西药学院天然药物学系黄静教授鉴定为金桂Osmanthus fragrans var. thunbergii, 凭证标本(GH20190901) 保存于四川大学华西药学院天然药物学系(药学科教大楼808室)。
1 提取与分离金桂干燥花朵19 kg, 用95%乙醇(40 L) 连续回流2 h, 提取2次, 过滤, 滤液减压回收乙醇, 得到约为原体积1/6的浓缩液(7 L)。浓缩液中加入等体积的水, 搅拌均匀后静置, 过滤, 得到滤液和沉淀(940 g), 滤液进一步浓缩得到棕黑色浸膏(397.6 g)。浸膏(397.6 g) 经硅胶(200~300目) 柱色谱分离, 二氯甲烷-甲醇(20∶1~0∶1) 梯度洗脱, 得到5个部分(Frs.1~5)。Fr.1 (64 g) 经硅胶柱色谱, 石油醚-乙酸乙酯(10∶1~0∶1) 梯度洗脱, 得到6个部分(Frs.1-1~1-6)。将Fr.1-2 (10 g) 经聚酰胺柱色谱分离, 水、10%~90%乙醇梯度洗脱, 得到4个部分(Frs.1-2-1~1-2-4)。Fr.1-2-1 (1.5 g) 经硅胶柱色谱、反相制备高效液相色谱分离得到化合物1 (47 mg)、2 (52 mg)、4 (20 mg) 和6 (7 mg)。Fr.1-2-2 (310 mg) 经反复硅胶柱色谱分离得到化合物8 (144 mg)。Fr.1-3 (6.3 g) 经聚酰胺色谱分离, 水、10%~50%乙醇梯度洗脱, 得到4个部分(Frs.1-3-1~1-3-4)。Fr.1-3-1 (1.4 g) 经反复硅胶柱色谱、反相制备高效液相色谱分离得到化合物5 (150 mg) 和7 (19 mg)。Fr.1-5 (7 g) 经聚酰胺色谱分离, 水、10%~50%乙醇梯度洗脱, 得到3个部分(Frs.1-5-1~1-5-3)。Fr.1-5-1 (1.2 g) 经反复硅胶柱色谱分离得到化合物3 (49 mg)。
2 结构鉴定化合物1: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热不显色; 薄层喷以碱性高锰酸钾, 显黄色;
化合物2 [(R, E)-2, 6-二甲基-辛-3, 7-二烯-2, 6-二醇]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显褐色。EI-MS: m/z 171 [M+H]+。1H NMR (400 MHz, CDCl3): δH 5.91 (1H, dd, J = 17.3, 10.7 Hz, 7-H), 5.70 (1H, d, J = 15.7 Hz, 3-H), 5.61 (1H, dt, J = 15.7, 7.0 Hz, 4-H), 5.20 (1H, d, J = 17.3 Hz, 8α-H), 5.05 (1H, d, J = 10.7 Hz, 8β-H), 2.25 (2H, m, 5-H), 1.31 (6H, s, 1-, 1'-H), 1.27 (3H, s, 1''-H); 13C NMR (100 MHz, CDCl3): δC 144.8 (C-7), 142.7 (C-3), 121.8 (C-4), 112.2 (C-8), 72.9 (C-6), 70.9 (C-2), 45.1 (C-5), 30.0 (C-1), 29.9 (C-1'), 27.5 (C-1'')。
化合物3 [(6R)-2, 6-二甲基-辛-7-烯-2, 3, 6-三醇]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显褐色。EI-MS: m/z 189 [M+H]+。1H NMR (400 MHz, CDCl3): δH 5.90 (1H, m, 7-H), 5.23 (1H, d, J = 17.4 Hz, 8α-H), 5.04 (1H, d, J = 10.4 Hz, 8β-H), 3.35 (1H, m, 3-H), 1.82 (1H, dt, J = 14.2, 7.4 Hz, 5α-H), 1.68 (1H, dt, J = 14.2, 7.4 Hz, 5β-H), 1.56 (1H, m, 4α-H), 1.41 (1H, m, 4β-H), 1.31 (3H, s, 1''-H), 1.20 (3H, s, 1-H), 1.15 (3H, s, 1'-H); 13C NMR (100 MHz, CDCl3): δC 144.9 (C-7), 112.4 (C-8), 79.3 (C-3), 73.3 (C-2), 73.3 (C-6), 39.5 (C-5), 29.0 (C-1''), 26.6 (C-1'), 26.0 (C-4), 23.4 (C-1)。
化合物4 [2, 4, 4-三甲基-3-(3-氧代丁基)-环己-2-烯-1-酮]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显黄色。ESI-MS: m/z 209.2 [M+H]+。1H NMR (400 MHz, CDCl3): δH 2.56 (2H, m, 2''-H), 2.46 (4H, m, 6-, 1''-H), 2.17 (3H, s, 4''-H), 1.79 (2H, t, J = 6.8 Hz, 5-H), 1.72 (3H, s, 1'-H), 1.14 (6H, s, 1'''-, 2'''-H); 13C NMR (100 MHz, CDCl3): δC 207.1 (C-3''), 198.8 (C-1), 163.5 (C-3), 131.4 (C-2), 42.4 (C-2''), 37.4 (C-5), 36.6 (C-4), 34.3 (C-6), 29.9 (C-4''), 26.8 (C-1'''), 26.8 (C-2'''), 24.2 (C-1''), 11.6 (C-1')。
化合物5 [(S)-2, 4, 4-三甲基-3-(3-羟基丁基)-环己-2-烯-1-酮]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显黄色。ESI-MS: m/z 211.1 [M+H]+。1H NMR (400 MHz, CDCl3): δH 3.85 (1H, m, 3''-H), 2.44 (2H, dd, J = 7.5, 6.3 Hz, 6-H), 2.39 (1H, m, 5β-H), 2.19 (1H, m, 5α-H), 1.78 (2H, dd, J = 7.5, 6.3 Hz, 1''-H), 1.75 (3H, s, 1'-H), 1.56 (2H, m, 2''-H), 1.23 (3H, d, J = 6.1 Hz, 4''-H), 1.15 (3H, s, 2'''-H), 1.15 (3H, s, 1'''-H); 13C NMR (100 MHz, CDCl3): δC 199.2 (C-1), 165.0 (C-3), 130.9 (C-2), 68.5 (C-3''), 38.0 (C-2''), 37.5 (C-1''), 36.5 (C-4), 34.3 (C-6), 27.0 (C-2'''), 27.0 (C-1'''), 27.0 (C-5), 23.6 (C-4''), 11.6 (C-1')。
化合物6 [(R, E)-2, 4, 4-三甲基-3-(3-羟基丁基-1-烯-1-基)-环己-2-烯-1-酮]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显浅黄色。ESI-MS: m/z 209.2 [M+H]+。1H NMR (400 MHz, CDCl3): δH 6.21 (1H, dt, J = 16.5, 1.2 Hz, 1''-H), 5.69 (1H, dd, J = 16.2, 5.7 Hz, 2''-H), 4.45 (1H, m, 3''-H), 2.50 (2H, dd, J = 7.5, 6.2 Hz, 6-H), 1.83 (2H, dd, J = 7.5, 6.2 Hz, 5-H), 1.79 (3H, d, J = 1.1 Hz, 1'-H), 1.35 (3H, d, J = 6.4 Hz, 4''-H), 1.14 (3H, s, 1'''-H), 1.14 (3H, s, 2'''-H); 13C NMR (100 MHz, CDCl3): δC 199.6 (C-1), 160.8 (C-3), 140.6 (C-2''), 130.1 (C-2), 125.3 (C-1''), 68.8 (C-3''), 37.4 (C-6), 35.6 (C-4), 34.4 (C-5), 27.4 (C-1'''), 27.4 (C-2'''), 23.7 (C-4''), 13.5 (C-1')。
化合物7 [(S, E)-3, 5, 5-三甲基-4-羟基-4-(3-氧代丁-1-烯-1-基)-环己-2-烯-1-酮]: 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显黄色。ESI-MS: m/z 223.2 [M+H]+。1H NMR (400 MHz, CDCl3): δH 6.83 (1H, d, J = 15.7 Hz, 1''-H), 6.45 (1H, d, J = 15.7 Hz, 2''-H), 5.94 (1H, s, 2-H), 2.48 (1H, d, J = 17.2 Hz, 6α-H), 2.31 (1H, d, J = 17.2 Hz, 6β-H), 2.29 (3H, s, 4''-H), 1.87 (3H, d, J = 1.5 Hz, 1'-H), 1.09 (3H, s, 1'''-H), 1.01 (3H, s, 2'''-H); 13C NMR (100 MHz, CDCl3): δC 197.8 (C-1), 197.4 (C-3''), 161.0 (C-3), 145.4 (C-1''), 130.5 (C-2''), 127.8 (C-2), 79.3 (C-4), 49.7 (C-6), 41.6 (C-5), 28.4 (C-4''), 24.5 (C-2'''), 23.1 (C-1'''), 18.9 (C-1')。
化合物8 (对乙酰氧基苯乙醇): 无色油状液体, 薄层喷以10%硫酸乙醇溶液, 加热显浅黄色, EI-MS: m/z 179 [M-H]-。1H NMR (400 MHz, CDCl3): δH 7.06 (2H, d, J = 8.5 Hz, 2-, 6-H), 6.78 (2H, d, J = 8.5 Hz, 3-, 5-H), 4.24 (2H, t, J = 7.1 Hz, 8-H), 2.86 (2H, t, J = 7.1 Hz, 7-H), 2.05 (3H, s, 2'-H); 13C NMR (100 MHz, CDCl3): δC 171.8 (C-1'), 154.7 (C-4), 130.1 (C-2), 130.1 (C-6), 129.6 (C-1), 115.5 (C-3), 115.5 (C-5), 65.6 (C-8), 34.3 (C-7), 21.1 (C-2')。
化合物2~8: 分别与文献对比, 最终分别确定为(R, E)-2, 6-二甲基-辛-3, 7-二烯-2, 6-二醇(2)[11]、(6R)-2, 6-二甲基-辛-7-烯-2, 3, 6-三醇(3)[12]、2, 4, 4-三甲基-3-(3-氧代丁基)-环己-2-烯-1-酮(4)[13]、(S)-2, 4, 4-三甲基-3-(3-羟基丁基)-环己-2-烯-1-酮(5)[14]、(R, E)-2, 4, 4-三甲基-3-(3-羟基丁基-1-烯-1-基)-环己-2-烯-1-酮(6)[15]、(S, E)-3, 5, 5-三甲基-4-羟基-4-(3-氧代丁基-1-烯-1-基)-环己-2-烯-1-酮(7)[16]和对乙酰氧基苯乙醇(8)[17]。
作者贡献: 俞雅芮负责实验设计、实验实施以及文章的撰写, 刘梦影、黄娇参与数据分析, 黄静负责文章的审阅和提出论文写作的建议, 并最终定稿。
利益冲突: 作者声明无利益冲突。
| [1] |
Zang DK, Xiang QB, Liu YL, et al. The studying history and the application to international cultivar registration authority of sweet osmanthus[J]. J Plant Resour Environ (植物资源与环境学报), 2003, 12: 49-53. |
| [2] |
Liu J, Nakamura S, Xu B, et al. Chemical structures of consti-tuents from the flowers of Osmanthus fragrans var. aurantiacus[J]. J Nat Med, 2015, 69: 135-141. DOI:10.1007/s11418-014-0869-1 |
| [3] |
Machida K, Yamauchi M, Kurashina E, et al. Four new lignan glycosides from Osmanthus fragrans var. aurantiacus[J]. Helv Chim Acta, 2010, 93: 2164-2175. DOI:10.1002/hlca.201000074 |
| [4] |
Yin W, Song ZR, Liu JQ, et al. Chemical constituents of Osmanthus fragrans[J]. China J Chin Mater Med (中国中药杂志), 2015, 40: 679-685. |
| [5] |
Jeong DE, Shim SY, Lee M. Anti-inflammatory activity of phenyl-propyl triterpenoids from Osmanthus fragrans var. aurantiacus leaves[J]. Int Immunopharmacol, 2020, 86: 1-7. |
| [6] |
Xue TT, Zang HY, Li J, et al. Antioxidant activity of volatile oil from Osmanthus fragrans in vitro[J]. China Condiment (中国调味品), 2014, 39: 18-20. |
| [7] |
Yang JY, Park JH, Chung N, et al. Inhibitory potential of consti-tuents from Osmanthus fragrans and structural analogues against advanced glycation end products, α-amylase, α-glucosidase, and oxidative stress[J]. Sci Rep, 2017, 7: 45746. DOI:10.1038/srep45746 |
| [8] |
Huang M, Liu M, Xu HR, et al. Studies on the chemical components of the roots of Osmanthus fragrans 'Rixianggui' (Ⅱ)[J]. Chin J Synth Chem (合成化学), 2013, 21: 689-691. |
| [9] |
Jiang HY, Zhong SY, Wu LP, et al. A new sesquiterpene glycoside from Osmanthus fragrans var. aurantiacus[J]. Acta Pharm Sin (药学学报), 2019, 54: 2277-2281. |
| [10] |
Li SY, Bai XM, Zhou FJ, et al. Study on the analgesic and anti-inflammation effects of a new component from the roots of Osmanthus fragrans 'rixianggui'[J]. Pharmacol Clin Chin Mater Med (中药药理与临床), 2016, 32: 38-41. |
| [11] |
Tsankova E, Mustakerova E, Todorova M. Acyclic terpenoids from Achillea depressa Janka[J]. C R Acad Bulg Sci, 2003, 56: 51-54. |
| [12] |
Detlef M. Linalool and cineole type glucosides from Cunila spicata[J]. Phytochemistry, 1995, 39: 1115-1118. DOI:10.1016/0031-9422(95)00108-J |
| [13] |
Lucimar P, Anita JM. Microbial monooxygenases applied to fragrance compounds[J]. J Mol Catal B Enzym, 2007, 44: 78-86. DOI:10.1016/j.molcatb.2006.08.007 |
| [14] |
Francisco AM, Rodney L, Rosa MV, et al. Bioactive apocarotenoids from Tectona grandis[J]. Phytochemistry, 2008, 69: 2708-2715. DOI:10.1016/j.phytochem.2008.08.018 |
| [15] |
Takahiro M, Seikou N, Souichi N, et al. Neolignan and megastigmane glucosides from the aerial parts of Isodon japonicus with cell protective effects on BaP-induced cytotoxicity[J]. Phytochemistry, 2017, 137: 101-108. DOI:10.1016/j.phytochem.2017.02.007 |
| [16] |
Wanda K, Klaudia M, Edward S. Norisoprenoids from aerial parts of Cichorium pumilum[J]. Biochem System Ecol, 2004, 32: 343-346. DOI:10.1016/j.bse.2003.08.005 |
| [17] |
Deepika S, Raghubind K. A new phenolic compound from the flowers of Jasminum multiflorum[J]. Chem Nat Compounds, 2014, 50: 48-49. DOI:10.1007/s10600-014-0863-6 |
 2022, Vol. 57
2022, Vol. 57


