2. 江西中医药大学大型精密仪器共享服务中心, 江西 南昌 330004
2. Large Precision Instrument Sharing Service Center, Jiangxi University of Chinese Medicine, Nanchang 330004, China
咳嗽是上呼吸道感染、哮喘及肺癌等许多急、慢性呼吸道疾病的常见症状, 往往伴随咳痰。现有镇咳西药作用范围窄且不良反应大[1-5], 如: 此类药物对慢性咳嗽无明显疗效且不具有祛痰功能; 可引起严重的肠道综合征并易使人嗜睡成瘾或可抑制呼吸中枢神经系统并导致排痰困难。祛痰西药同样具有使人头晕、恶心、胃肠道出血及皮疹等严重不良反应[4, 5]。因此研究与开发新型镇咳祛痰药物已成为咳嗽排痰安全防治的迫切需求。桔梗为桔梗科植物桔梗Platycodon grandiflorum (Jacq.) A. DC.的干燥根, 具有宣肺、利咽、祛痰、排脓之功效, 其主要活性部位为桔梗总皂苷。课题前期基于桔梗总皂苷镇咳祛痰谱效关系研究结果阐明了桔梗总皂苷镇咳活性成分[6], 但其镇咳祛痰机制仍并不清楚。
代谢组学是系统生物学的一个分支, 旨在研究生物系统对遗传或外部刺激的整体代谢反应。借助色谱、质谱等技术, 并结合数理统计学方法对生物体液或组织中存在的小分子进行定性和定量分析。通过分析生物样品中内源性代谢物的变化, 可以识别出反映生物状态并解释人体病理状态的潜在生物标志物。目前代谢组学已被广泛用于中药领域, 包括疾病的诊断和机制研究、寻找药物作用靶点和生物标志物等研究[7, 8]。本研究应用代谢组学以阐明桔梗总皂苷镇咳祛痰作用机制, 以为其新药开发提供参考依据。
材料与方法实验材料与试剂 桔梗药材样本采集于内蒙古自治区赤峰市, 经江西中医药大学钟国跃研究员鉴定为桔梗科植物桔梗Platycodon grandiflours (Jacq.) A. DC.的干燥根。色谱级乙腈(德国Merck公司), 色谱级甲酸(美国Thermo Fisher Scientific公司), 苯酚红(批号: 20170901, 天津市大茂化学试剂厂); 枸橼酸喷托维林片(每片含枸橼酸喷托维林25 mg, 批号: 180104, 上海玉瑞生物科技安乡药业有限公司); 2-氯-L-苯丙氨(上海源叶生物科技有限公司); 分析纯正丁醇、浓氨水和氯化铵均为分析纯(西陇化工股份有限公司), 水为超纯水。
仪器 AB Sciex Triple TOF 5600+高分辨飞行时间质谱仪(美国AB SCIEX公司), 配备DuoSpray离子源及Shimadzu LC-30A超高效液相色谱仪(日本Shimadzu公司)。5430R型高速冷冻离心机(德国Eppendorf公司), R-210型旋转蒸发仪(瑞士Buchi公司), KQ-3200DE型数控超声波清洗器(昆山超声仪器有限公司), 402AI型超声雾化器(江苏鱼跃医疗设备股份有限公司), UV-1800型紫外分光光度计(日本Shimadzu公司), CP-214型电子天平(上海奥豪斯有限公司), QL-901型涡旋仪(海门市其林贝尔仪器制造有限公司)。
实验动物 SPF级雄性KM小鼠18~22 g, 购置于湖南斯莱克景达实验动物有限公司, 动物生产许可证号: SCKX (湘) 2019-0004。所有对动物的实验操作和处理均通过江西中医药大学实验动物伦理委员会的批准(批准号: JZLLSC-20190235)。
镇咳模型构建及血液采集 40只雄性KM小鼠, 随机均分成正常组(normal)、模型组(model)、镇咳阳性药枸橼酸喷托维林组(pentoxyverine, Pen)、桔梗总皂苷给药组(Platycodon total saponins, PTS)。桔梗总皂苷给药剂量为3.2 g·kg-1·d-1 (按生药计), 镇咳阳性药枸橼酸喷托维林组给药剂量为100 mg·kg-1·d-1, 正常组和模型组灌胃等量(15 mL·kg-1·d-1) 生理盐水。给药7 d, 于末次给药1 h后, 正常组小鼠摘眼球取血, 其余组小鼠依次置于透明玻璃罩内, 浓氨水定量恒压喷雾, 5 s后立即取出, 记录小鼠从接受喷雾开始到出现咳嗽的潜伏期, 以及2 min内的咳嗽次数(咳嗽标准: 表现为小鼠腹肌收缩, 同时张大嘴, 有时可有咳嗽声音)。采集完咳嗽相关数据后, 立即摘眼球取血。
祛痰模型构建及血液采集 40只雄性KM小鼠, 随机均分成正常组(normal)、模型组(model)、祛痰阳性药氯化氨组(ammonium chloride, AmCh)、桔梗总皂苷给药组(PTS)。桔梗总皂苷给药剂量为3.2 g·kg-1·d -1 (按生药计), 祛痰阳性药氯化铵组给药剂量为10 mg·kg-1·d-1, 正常组和模型组灌胃等量(15 mL·kg-1·d-1) 生理盐水。给药7 d, 于末次给药30 min后, 正常组小鼠摘眼球取血, 其余组小鼠腹腔注射0.5% 酚红生理盐水溶液20 mL·kg-1, 30 min后摘眼球取血。取血后暴露气管, 剥去气管周围组织, 剪下自甲状软骨下至支气管分支处的一段气管, 放入2 mL生理盐水的试管中, 旋涡振荡器振荡5 min后超声振荡洗涤20 min, 加入50 g·L-1 NaHCO3 1 mL, 1 500 r·min-1离心10 min, 取上清液, 546 nm处测吸光值, 与酚红标准曲线比较, 折算出酚红排泄量。
血清样本制备方法 镇咳和祛痰实验所得血液样品在室温下静置约1 h, 然后以4 000 r·min-1离心10 min以获得血清。血清样本置于-80 ℃保存, 使用时置于4 ℃解冻。将250 μL血清与50 μL 2-氯-L-苯丙氨酸(1 mg·mL-1) 和650 μL乙腈混合。将混合物在4 ℃放置15 min, 并在4 ℃以12 000 r·min-1离心20 min。从每种溶液中小心地取出450 μL上清液, 并用N2气流干燥。然后将获得的残余物溶于200 μL 10%乙腈水溶液中。将溶液涡旋混合50 s, 并在4 ℃下以12 000 r·min-1离心15 min, 以获得用于UHPLC-Q-TOF/MS分析的最终样品。质量控制(QC) 样品用于控制样品收集和制备方法的稳定性。从每组中收集15 μL血清样品并混合以获得QC样品, 在整个分析过程中每10个样品进行分析。
代谢组学样品分析方法 质谱正离子模式参数如下: 离子源温度(TEM), 500 ℃; 气帘气(CUR), 40 psi; 辅助气1 (GS1) 和辅助气2 (GS2), 50 psi; 离子喷雾电压(ISVF), 5.5 kV; 碰撞能量(CE), 35 V; 碰撞能量补充(CES), 15 V; 去簇电压(DP), 100 V。负离子模式参数如下: TEM, 550 ℃; CUR, 40 psi; GS1和GS2, 50 psi; ISVF, -4.5 kV; CE, 35 V; CES, 15 V; DP, -100 V。m/z范围为100~1 250 Da。数据通过Analyst TF工作站(1.6版本) 获取。色谱柱为Agilent ZORBAX Eclipse plus C18 (100 mm × 2.1 mm, 1.8 μm) 色谱柱。流动相为0.1%甲酸水(A) 和乙腈(B)。流速为0.3 mL·min-1。洗脱梯度: 0~3 min, 10%~58% B; 3~10 min, 58%~58% B; 10~23 min, 58%~95% B; 23~25min, 95% B; 25~25.1 min, 95%~10% B; 25.1~30 min, 10% B。进样量2 μL, 柱温箱40 ℃。
数据处理 药效数据采用SPPS数据统计分析软件对各组数据进行单因素方差分析, 并进行组间比较, P < 0.05为有统计学差异。代谢组学中, Q-TOF/MS质谱获取的原始数据由MarkerView 1.2软件处理。经过包括峰匹配, 对齐, 过滤和归一化总面积在内的预处理程序后, 获得了一个包含样品信息的三维数据集, 其中包括峰强度、保留时间(RT) 和质荷比(m/z)。RT和m/z数据用作每个离子的标识符。此外, 去除了超过80%样品中缺少值的峰。然后, 将所得数据矩阵导入软件SIMCA 14.1软件中, 以通过OPLS-DA分析代谢物谱并可视化正常组和模型组之间的代谢差异。OPLS-DA中变量投影重要性值(variable importance in projectin, VIP) 大于1且t检验的P值小于0.05 (P < 0.05) 的内源代谢物被视为与镇咳祛痰作用有关的差异性代谢物。通过与METLIN和HMDB等数据库相结合比对, 鉴定差异性代谢物。代谢通路分析在MetaboAnalyst 4.0平台完成。
结果 1 UHPLC-Q-TOF/MS的稳定性和重复性QC样品的叠加总离子流(TIC) 色谱图表明, 在对所有样品进行大规模分析时, 其变化均在实验可接受范围内。同时, 选择质控样品中提取的离子色谱图(EIC) 以评估系统的稳定性和重复性。以正离子模式分析的QC样品为例, 计算出提取的7个色谱峰的保留时间的RSD为0.05%~0.42%, 峰面积的RSD为2.06%~13.78%, 分子量实测值的RSD为4.65×10-5%~2.48×10-3%。结果表明, UHPLC-Q-TOF/MS分析具有良好的稳定性和可重复性。
2 镇咳、祛痰药效浓氨水诱导的小鼠咳嗽模型以及小鼠气管酚红排泄法分别是研究中草药等天然产物的镇咳与祛痰活性的经典模型。本研究采用浓氨水喷雾法与气管酚红排泄法分别评价了桔梗总皂苷的镇咳与祛痰药效活性, 结果见图 1。图 1A显示了总皂苷对浓氨水引咳模型中小鼠咳嗽潜伏期的影响, 结果表明, 与模型组相比, 桔梗总皂苷(PTS) 能够极显著增加小鼠咳嗽潜伏期(P < 0.01), 对潜伏期的延长效果甚至优于阳性药枸橼酸喷托维林。同时桔梗总皂苷也能够极显著降低该咳嗽模型中小鼠咳嗽次数(P < 0.01), 如图 1B所示。在祛痰药效实验中, 桔梗总皂苷组也能够显著增加酚红排泄模型中小鼠的酚红排泄量(P < 0.01), 这也提示桔梗总皂苷有较好的祛痰能力, 如图 1C所示。

|
Figure 1 The results of antitussive and expectorant effects. A: Incubation period; B: Number of coughs; C: Phenol red excretion. n = 10, x ± s. **P < 0.01 vs model group. Pen: Pentoxyverine group; AmCh: Ammonium chloride group; PTS: Platycodon total saponins group |
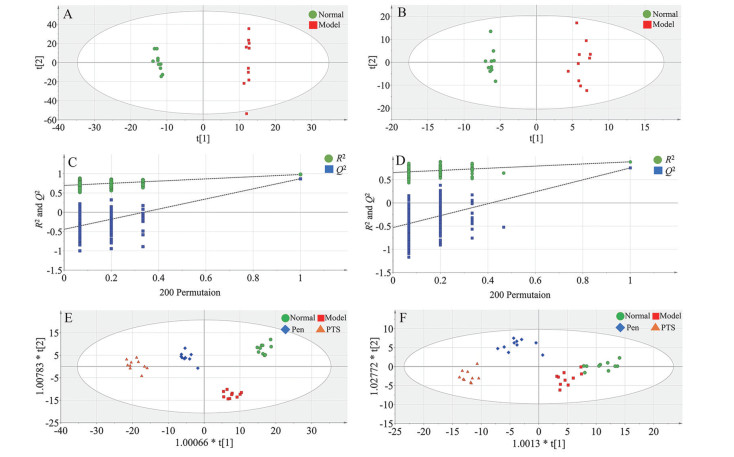
UHPLC-Q-TOF/MS在高质量分离度、质量准确度和可重现的响应强度方面具有优势, 使它能够在一次运行中鉴定和定量生物样品中的数百种代谢物[9]。PCA能够较为直观地获取不同组别之间代谢轮廓的差别和聚类结果, 它常被用来观察不同组别之间是否有分类趋势以及是否有离群的数点[10]。PCA结果如图 2所示。从图 2A和2B中可以看出, 正常组和模型组的血清样品在正离子和负离子模式下均具有良好的分化, 表明正常组和模型组的代谢物是不同的。
|
Figure 2 PCA results in normal group vs model group: positive ion mode (A) and negative ion mode (B); Permutation test results in normal group vs model group (n = 200): positive ion mode (C) and negative ion mode (D); OPLS-DA results: positive ion mode (E) and negative ion mode (F) |
为了最大程度地分离样本, 建立了偏最小二乘判别分析(PLS-DA) 和正交偏最小二乘判别分析(OPLS-DA) 的监督模式识别方法。通过PLS-DA模型的随机排列检验(n = 200), 结果如图 2C和2D所示。因此, 正离子和负离子模式下解释率R2和预测能力Q2的结果分别为0.526和-0.506、0.701和-0.534。这些结果表明该模型具有良好的稳定性和预测能力, 并且没有过度拟合。
作为一种有监督的化学计量学方法, OPLS-DA专注于寻找区分组的变量, 这是区分和识别潜在生物标志物的可靠工具。因此, UPLC-Q-TOF/MS与OPLS-DA结合用于代谢物鉴定和代谢组学分析。OPLS-DA得分图的结果如图 2所示。正离子模式的R2X、R2Y和Q2值分别为0.595、0.997和0.854 (图 2E), 负离子模式的R2X、R2Y和Q2值分别为0.55、0.988和0.833 (图 2F), 表明拟合的良好预测能力。由于在正离子模式和负离子模式中同一组中的样品紧密聚集, 因此观察到了不同组之间的明显分离。这些分布模式表明氨水致咳影响了小鼠血清中的内源性代谢产物谱, 这与文献报道结果一致[11]。
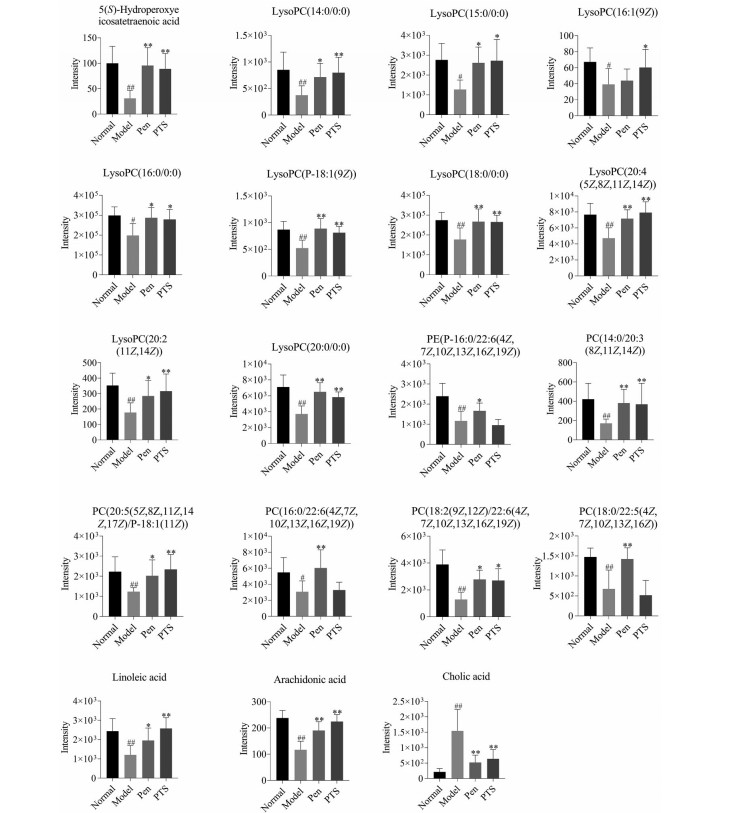
3.2 镇咳差异性代谢物鉴定使用前文所述的方法筛选鉴定出了区分正常组和模型组的19种差异性代谢物。这些差异性代谢物即潜在的生物标志物, 桔梗总皂苷能够调控其中的16种趋于正常水平。这些代谢物的信息见表 1。图 3集中显示了不同组中这些差异性代谢物的变化趋势。
| Table 1 Differential metabolites of normal group vs model group |
|
Figure 3 Change trend of 19 different metabolites in antitussive model. n = 10, x ± s. #P < 0.05, ##P < 0.01 vs normal group; *P < 0.05, **P < 0.01 vs model group |
将桔梗总皂苷参与调控的差异性代谢物数据导入MetaboAnalyst 4.0平台, 以探索受桔梗总皂苷治疗影响可能的代谢途径。影响值高于0.10的途径被认为是潜在的靶途径[11], 并映射到KEGG上, 以反映机体对桔梗总皂苷治疗后的反应。结果如图 4所示。根据分析结果, 筛选出3个途径, 包括亚油酸代谢(影响值1.0)、花生四烯酸代谢(影响值0.4) 和甘油磷脂代谢(影响值0.2)。

|
Figure 4 Metabolic pathway analysis of antitussive model. 1: Linoleic acid metabolism; 2: Arachidonic acid metabolism; 3: Glycerophospholipid metabolism |
采用镇咳相同模型分析方法, 首先进行无监督的PCA, 结果如图 5所示。从图 5A和5B中可以看出, 正常组和模型组的血清样品在正离子分离效果较好, 说明二者代谢产物存在差异性。

|
Figure 5 PCA results in normal group vs model group: positive ion mode (A) and negative ion mode (B); Permutation test results in normal group vs model group (n = 200): positive ion mode (C) and negative ion mode (D); OPLS-DA results: positive ion mode (E) and negative ion mode (F) |
为了最大程度地分离样品, 建立了偏最小二乘判别分析(PLS-DA) 和正交偏最小二乘判别分析(OPLS-DA) 的监督模式识别方法。评估了PLS-DA模型的随机排列检验(n = 200) 和解释率(R2) 和预测能力(Q2), 结果如图 5C和5D所示。正离子和负离子模式下R2和Q2的结果分别为0.349和-0.231、0.953和-0.533。这些结果表明该模型具有良好的稳定性和预测能力, 并且没有过度拟合。
OPLS-DA得分图的结果如图 5所示。正离子模式的R2X、R2Y和Q2值分别为0.576、0.968和0.714 (图 5E), 负离子模式的R2X、R2Y和Q2值分别为0.719、0.981和0.685 (图 5F), 表明拟合的良好预测能力。由图可以看出, 正离子模式下阳性药物组与模型组重叠度较高, 但负离子模式下二者仍表现出一定的分离度。同理, 正常组、模型组、阳性药物组及桔梗总皂苷的分布情况说明酚红、阳性药及桔梗总皂苷均可影响正常组代谢产物谱。
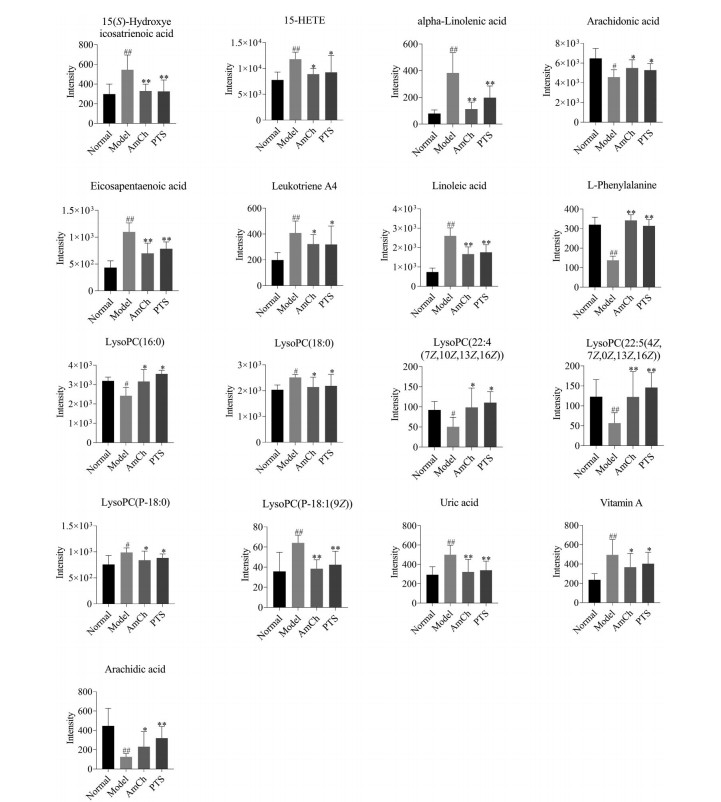
4.2 差异性代谢物鉴定根据OPLS-DA和t检验的结果, 发现了区分正常和模型组的17种差异性代谢物, 见表 2。桔梗总皂苷给药治疗后, 17种差异代谢物水平均已趋于正常水平。图 6集中显示了不同组中这些生物标志物的变化趋势。这一结果表明, 桔梗总皂苷可有效逆转酚红产生的差异性代谢产物水平, 发挥祛痰药效。
| Table 2 Differential metabolites of normal group vs model group |
|
Figure 6 Change trend of 17 different metabolites in expectorant model. n = 10, x ± s. #P < 0.05, ##P < 0.01 vs Normal; *P < 0.05, **P < 0.01 vs Model |
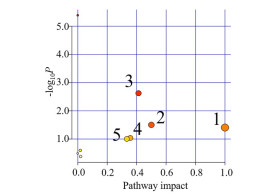
将桔梗总皂苷参与调控的差异性代谢物导入MetaboAnalyst 4.0平台, 以探索受桔梗总皂苷发挥祛痰药效可能的代谢途径。结果如图 7所示。根据分析结果, 筛选出3个途径, 包括亚油酸代谢(影响值1.0), 苯丙氨酸、酪氨酸和色氨酸的生物合成(影响值0.5), 花生四烯酸代谢(影响值0.4), 苯丙氨酸代谢(影响值0.3) 和α-亚麻酸代谢(影响值0.3)。
|
Figure 7 Metabolic pathway analysis of expectorant model. 1: Linoleic acid metabolism; 2: Phenylalanine, tyrosine and tryptophan biosynthesis; 3: Arachidonic acid metabolism; 4: Phenylalanine metabolism; 5: α-Linolenic acid metabolism |
咳嗽咳痰的机制极为复杂, 目前尚缺少特异性模型研究其机制。代谢组学研究药物或外界因素干预时机体内源性代谢物的变化, 可识别反映生物状态并解释人体病理状态的潜在生物标志物, 已被广泛用于中药领域, 包括疾病的诊断和机制研究。因此, 特别适合于中药镇咳祛痰机制研究。
本文药效学研究结果显示桔梗总皂苷能显著延长浓氨水引咳模型中小鼠的咳嗽潜伏期和咳嗽次数, 能显著增加酚红排泄模型中小鼠的酚红排泄量。代谢组学研究结果表明, 桔梗总皂苷可以通过亚油酸代谢、花生四烯酸代谢和甘油磷脂代谢发挥镇咳活性。可通过调控亚油酸代谢, 苯丙氨酸、酪氨酸和色氨酸的生物合成, 花生四烯酸代谢, 苯丙氨酸代谢和α-亚麻酸代谢发挥祛痰活性。
通过共同代谢通路功能分析可知, 亚油酸可以促进成纤维细胞分泌NO、TNF、IL-1β和IL-8等炎症介质。这些炎症介质不仅参与肺部炎症的发生[12], 而且对自身或其他细胞的增殖具有不同的调节作用[13]。花生四烯酸是一种多不饱和脂肪酸, 在生物体内分布广泛且含量高。花生四烯酸的主要代谢产物是前列腺素、血栓烷、白三烯和羟基脂肪酸。花生四烯酸在免疫调节、细胞信号转导、血管舒张, 尤其是炎症中起重要作用[14]。另一方面, 甘油磷脂类化合物, 例如磷脂酰胆碱(PCs) 和溶血磷脂酰胆碱(LysoPCs), 是细胞膜结构的重要组成部分, 同时也是一种重要的趋化介质, 可通过特定的G蛋白偶联受体改变免疫细胞的激活, 参与炎症过程。已有研究表明, Farfarae Flos可通过调控甘油磷脂代谢途径可产生镇咳作用[11]。
此外, 苯丙氨酸、酪氨酸和色氨酸的生物合成以及苯丙氨酸代谢均为氨基酸代谢的重要环节。苯丙氨酸在生物体内起到维持生长发育等功能, 酪氨酸和色氨酸能够合成神经递质以及激素。α-亚麻酸属于ω-3多不饱和脂肪酸类型, 它的代谢产物为细胞膜的组成成分, 此外α-亚麻酸能够抑制肿瘤坏死因子和IL-1β等炎症介质的生成。在机体内发挥抗炎和调节免疫的作用。但L-苯丙氨酸与α-亚麻酸水平在镇咳模型组与给药组中并没有产生显著性变化, 说明这一机制可能与桔梗总皂苷的镇咳机制相关性不大。
综上分析可知, 桔梗总皂苷既可通过相同的代谢通路同时发挥镇咳祛痰药效, 也可通过不同的代谢通路分别发挥镇咳祛痰药效。课题组前期研究表明, 桔梗总皂苷镇咳活性成分有12个, 祛痰活性成分有17个, 其中有4个成分兼具镇咳祛痰活性[6]。基于这一研究结果可在一定程度上推测不同的活性成分可能调控不同的代谢通路分别发挥镇咳祛痰药效, 而相同的成分可能共同调控同一通路同时发挥镇咳祛痰药效。但这一推测仍有待进一步验证, 相关实验正在进行之中。
作者贡献: 张迟和曾金祥构思并设计了实验, 王新红、张迟和周丽进行论文整体实验和数据分析, 任玲玲、毛竹、袁恩和周立分协助实验开展与数据分析, 王新红和张迟撰写并修改了论文。
利益冲突: 所有作者均声明不存在利益冲突。
| [1] |
Reynolds SM, Mackenzie AJ, Spina D, et al. The pharmacology of cough[J]. Trends Pharmacol Sci, 2004, 25: 569-576. DOI:10.1016/j.tips.2004.09.009 |
| [2] |
Paneliya AM, Patgiri BJ, Nariya MB, et al. Antitussive activity of Vasa Avaleha formulations on sulfur dioxide-induced coughing in mice[J]. Int J Green Pharm, 2015, 9: 180-183. DOI:10.4103/0973-8258.161236 |
| [3] |
Saraswathy GR, Sathiya R, Anbu J, et al. Antitussive medicinal herbs-an update review[J]. Int J Pharm Sci Drug Res, 2013, 6: 12-19. |
| [4] |
Rubin BK. Mucolytics, expectorants, and mucokinetic medications[J]. Respir Care, 2007, 52: 859-865. |
| [5] |
Zhang T, Zhou XD. Clinical application of expectorant therapy in chronic inflammatory airway diseases (Review)[J]. Exp Ther Med, 2014, 7: 763-767. DOI:10.3892/etm.2014.1494 |
| [6] |
Zhang C, Wang XH, Zeng JX, et al. Study on the active components of Platycodonis Radix in antitussive and expectorant effect based on specttrum effect relationship[J]. J Chin Med Mater (中药材), 2020, 43: 1920-1927. |
| [7] |
Chen CC, Yin QC, Tian JS, et al. The mechanism of the anti-depression effect of the Radix Bupleuri Radix Paeoniae Alba herb pair determined by liver metabolomics[J]. Acta Pharm Sin (药学学报), 2020, 55: 941-949. |
| [8] |
Qi YS, Li X, Qin XM, et al. Anti-cancer effect of the flavonoids of Astragalus combined with cisplatin on Lewis lung carcinoma-bearing mice[J]. Acta Pharm Sin (药学学报), 2020, 55: 930-940. |
| [9] |
Xu XB, Gao BB, Guan QJ, et al. Metabolomic profile for the early detection of coronary artery disease by using UPLC-QTOF/MS[J]. J Pharm Biomed Anal, 2016, 129: 34-42. DOI:10.1016/j.jpba.2016.06.040 |
| [10] |
Ke CF, Zhang T, Wu XY, et al. Statistical methods for metabolomics data analysis[J]. Chin J Health Stat (中国卫生统计), 2014, 31: 357-359. |
| [11] |
Li J, Zhang ZZ, Lei ZH, et al. NMR based metabolomic comparison of the antitussive and expectorant effect of Farfarae Flos collected at different stages[J]. J Pharm Biomed Anal, 2018, 150: 377-385. DOI:10.1016/j.jpba.2017.12.028 |
| [12] |
Cui L, Zheng DH, Lee YH, et al. Metabolomics investigation reveals metabolite mediators associated with acute lung injury and repair in a murine model of influenza pneumonia[J]. Sci Rep, 2016, 6: 26076. DOI:10.1038/srep26076 |
| [13] |
Xue ZY, Hua YL, Li JX, et al. Effect of diffrernt processed volatile oils from Angelica sinensis on urinary metabolomics rats[J]. China J Chin Mater Med (中国中药杂志), 2016, 41: 928-939. |
| [14] |
Wu D, Xu J, Song EB, et al. Acetyl salicylic acid protected against heat stress damage in chicken myocardial cells and may associate with induced Hsp27 expression[J]. Cell Stress Chaperones, 2015, 20: 687-696. DOI:10.1007/s12192-015-0596-x |
 2022, Vol. 57
2022, Vol. 57


