2. 河北省中药配方颗粒技术创新中心, 河北 石家庄 050091;
3. 河北省中药材品质评价与标准化工程研究中心, 河北 石家庄 050091;
4. 河北省高校中药配方颗粒应用技术研发中心, 河北 石家庄 050091
2. Hebei TCM Formula Granule Innovation Center, Shijiazhuang 050091, China;
3. Hebei TCM Quality Evaluation and Standardization Engineering Research Center, Shijiazhuang 050091, China;
4. TCM Formula Granule Research Center of Hebei Province University, Shijiazhuang 050091, China
橘红为芸香科植物橘(Citrus reticulata Blanco) 及其栽培变种的干燥外层果皮。秋末冬初果实成熟后采收, 用刀削下外果皮, 晒干或阴干, 具有理气宽中, 燥湿化痰的功效。用于咳嗽痰多, 食积伤酒, 呕恶痞闷等症状[1]。“橘红”之名, 始见宋·陈衍《宝庆本草折衷》陈皮项下[2], 历代医家多将橘红用于下气消痰。橘红近年来在中药应用中逐渐广泛, 如经典名方半夏白术天麻、养胃汤等。现代研究表明, 橘红主要含有黄酮类、挥发油、生物碱等化学成分[3, 4], 橘红中最常见的黄酮类化合物可分为黄酮苷类化合物(如橙皮苷、芸香柚皮苷等) 和多甲氧基黄酮类(如川陈皮素、橘皮素、5-羟基-6, 7, 8, 4'-四甲氧基黄酮等)[5, 6]。橙皮苷、川陈皮素等黄酮类化合物被认为是其主要生物活性成分, 具有抗氧化、抗炎、抗癌、调节心血管系统功能、保护神经系统等多种药理活性[7, 8]。
目前橘红的测定方法多为高效液相色谱法(HPLC), Yao等[9]和Zhang等[10]采用HPLC法测定了《中国药典》2020版中橘红项下橙皮苷的含量, 仅以橙皮苷作为质量评价指标, 含量测定指标单一, 不利于其质量控制; Shi等[11]虽然采用一测多评方法同时测定了橘红水煎液中12种化学成分, 但是其分析时间长, 过程繁琐, 且多个成分标准品短缺, 不能准确控制橘红药材的质量。
近年来LC-MS法已成为一种多成分微量分析的重要方法, 尤其是超高效液相色谱(UPLC) 分离技术的应用, 使得高通量分析成为可能[12]。本实验采用UPLC-MS/MS法同时对橘红中的6种黄酮类成分和1种有机酸类成分进行测定, 并将其应用于不同产地橘红的质量分析。该方法简便、快速、灵敏度高, 为全面控制橘红的质量提供参考。
材料与方法仪器 Shimadzu LC-30A型超高效液相色谱仪(日本岛津公司, 包括DGU-30A3型在线真空脱气机, LC-30AD型二元泵, SIL-30AC型自动进样器, CTO-30A型柱温箱); 4500 QTRAP三重四极杆线性离子阱质谱仪(美国AB公司, 配有ESI离子源); Analyst® TF 1.6.3数据采集软件(美国AB公司); BSA224S-CW、CPA225D型电子分析天平(赛多利斯科学仪器北京有限公司); YB-150型多功能粉碎机(永康市速锋工贸有限公司)。
试药、试剂与样品 绿原酸(批号MUST-16031610, 纯度99.39%)、芦丁(批号MUST-16031813, 纯度98.00%)、芸香柚皮苷(批号MUST-18101010, 纯度98.37%)、橙皮苷(批号MUST-17032502, 纯度98.76%)、甜橙黄酮(批号MUST-18041505, 纯度98.57%)、川陈皮素(批号MUST-18042205, 纯度98.86%)、橘皮素(批号MUST-18012910, 纯度99.73%) 均购自成都曼斯特生物技术有限公司; 乙腈、甲醇(色谱纯, 德国Merck公司)、甲酸(色谱纯, Dikma, USA), 其他试剂均为分析纯, 实验用水为屈臣氏蒸馏水; 15批橘红药材由神威药业集团有限公司提供, 经河北省药品检验院主任中药师孙宝惠鉴定为芸香科植物橘(Citrus reticulata Blanco) 及其栽培变种的干燥外层果皮。药材产地信息见表 1。
| Table 1 Origin information of Citri Exocarpium Rubrum medicinal materials |
色谱条件 色谱柱: Shim-pack GIST C18 (100 mm × 2.1 mm, 2 μm), 日本岛津公司, 流动相A为乙腈, B为0.1%甲酸水, 梯度洗脱(0~2 min, 10%~20% A; 2~8 min, 20%~50% A; 8~10 min, 50%~95% A; 10~12 min, 95% A; 12~15 min, 10% A), 每次进样前预平衡5 min, 再进行洗脱程序。柱温30 ℃, 流速为0.4 mL·min-1, 进样量1 μL。
质谱条件 采用多重反应监测(multiple reaction monitoring, MRM) 的扫描方式下正负离子同时监测, 离子源为电喷雾离子源(ESI源), 离子化电压(IS) 为5 500和-4 500 V, 离子源温度(TEM) 为550 ℃, 喷雾气(GS1, N2) 为380 kPa (55 psi), 辅助气(GS2, N2) 为380 kPa (55 psi), 接口持续加热, 全程通入氮气, 气帘气(CUR, N2) 为242 kPa (35 psi), 碰撞气(CAD) 压力为medium, 每个离子对的滞留时间(dwell time) 为100 ms。每个待测化合物的监测离子对、解簇电压(DP) 及碰撞能量(CE) 见表 2。
| Table 2 MS analysis of parameters of seven detected components in Citri Exocarpium Rubrum |
对照品溶液的配制 分别精密称取7个对照品适量, 加甲醇定容至刻度, 摇匀, 即得对照品储备液; 分别精密吸取各对照品储备液适量置同一量瓶中, 加80%甲醇溶液定容至刻度, 摇匀, 即得每1 mL含绿原酸0.055 μg、芦丁1.632 μg、芸香柚皮苷6.320 μg、橙皮苷35.280 μg、甜橙黄酮0.114 μg、川陈皮素1.354 μg、橘皮素0.602 μg的混合对照品储备液。
供试品溶液的制备 精密称取橘红粉末(过四号筛) 约0.1 g, 置于100 mL具塞锥形瓶中, 加入80%甲醇[5] 50 mL, 密塞, 精密称定质量, 超声处理(功率250 W, 频率40 kHz) 40 min, 取出放冷, 再称定, 用甲醇补足减失重量, 摇匀, 取上清液, 用0.22 μm微孔滤膜滤过, 将续滤液用80%甲醇稀释5倍, 即得供试品溶液。
专属性 分别精密吸取混合对照品溶液和供试品溶液各1 μL, 按上述液质联用条件进样分析, 比较混合对照品溶液和供试品溶液的色谱图。
线性关系 精密量取混合对照品储备液0.3、0.5、1、2、4和6 mL, 分别置10 mL量瓶中, 用80%甲醇溶液稀释至刻度, 摇匀, 得到7个成分的系列浓度混合对照品溶液。分别精密吸取上述储备液1 μL, 按上述液质联用条件进样分析。
精密度 精密量取混合对照品储备液适量加80%甲醇稀释5倍, 精密吸取稀释后混合对照品溶液1 μL, 按上述液质联用条件进样分析, 连续进样6次, 测定峰面积, 计算RSD值。
稳定性 取同一批次(S7) 橘红样品, 按“供试品溶液的制备”项下方法平行制备供试品溶液, 分别于0、4、8、12、16和24 h按上述液质联用条件进样分析, 测定峰面积, 计算RSD值。
重复性 取同一批次(S7) 橘红样品, 分别精密称取低(0.05 g)、中(0.1 g)、高(0.15 g) 三个水平样品量, 每个水平3份样品, 按“供试品溶液的制备”项下方法制备供试品溶液, 精密吸取各供试品溶液1 μL, 按上述液质联用条件进样分析, 测定峰面积, 计算含量和RSD值。
加样回收率 取同一批次(S7) 已知含量的橘红样品9份, 每份取约0.05 g, 精密称定, 按每3份为一组, 每组精密加入对照品绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素、橘皮素的量相当于橘红样品中各对照品含量的50%、100%、150%, 按“供试品溶液的制备”项下方法制备供试品溶液, 精密吸取各供试品溶液1 μL, 按上述液质联用条件进样分析, 测定峰面积, 计算7个成分的含量、平均加样回收率和RSD。
结果 1 方法学考察 1.1 专属性供试品溶液中被测定成分与7个对照品的保留时间相同。被测定成分分离效果良好, 无其他干扰, 比较各测定成分和对照品的MRM色谱图, 见图 1, 两者一致, 表明本法专属性良好。

|
Figure 1 The representative MRM chromatograms of the standard substances of seven components (A) and samples of Citri Exocarpium Rubrum (B). 1: Chlorogenic acid; 2: Rutin; 3: Narirutin; 4: Hesperidin; 5: Sinensetin; 6: Nobiletin; 7: Tangeretin |
以对照品浓度为横坐标(X), 以峰面积为纵坐标(Y), 绘制标准曲线, 计算得到各成分的回归方程和线性范围, 见表 3。结果表明, 7个成分在各自的范围内呈良好线性关系, 方法灵敏度较高。
| Table 3 Regressive equations, correlation coefficients and linear ranges |
绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素和橘皮素的峰面积RSD分别为2.99%、1.54%、1.27%、2.47%、2.18%、2.06%和1.66%, 表明仪器精密度良好。
1.4 稳定性绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素和橘皮素峰面积RSD分别为3.03%、2.03%、1.36%、0.75%、2.0%、2.0%和1.25% (n = 6)。结果表明供试品溶液在24 h内稳定性良好。
1.5 重复性绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素和橘皮素质量分数的RSD分别为3.78%、1.83%、4.30%、3.58%、2.57%、2.45%和2.3% (n = 9)。结果表明该方法重复性良好。
1.6 加样回收率绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素和橘皮素平均加样回收率分别为99.32%、106.75%、101.59%、103.91%、106.13%、105.21%和102.88% (n = 9)。RSD分别为3.06%、1.33%、3.94%、3.30%、1.85%、1.96%和2.04% (n = 9), 表明该方法准确度良好。
2 样品含量测定精密称取15批橘红样品, 按“供试品溶液的制备”项下方法制备供试品溶液, 精密吸取各供试品溶液1 μL, 按上述液质联用条件进样分析, 测定峰面积, 计算绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素、橘皮素的含量。15批样品测定结果见表 4。
| Table 4 The contents of seven components in fifteen batches of Citri Exocarpium Rubrum |
为了进一步分析研究不同产地橘红药材化学成分差异, 以15批样品中7种化学成分含量为变量, 使用SPSS 26.0软件进行聚类分析(HCA) 和主成分分析(PCA) 分析。
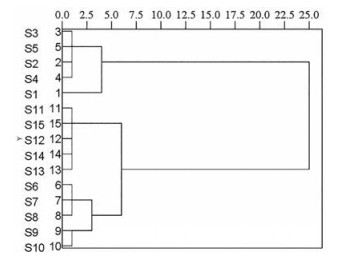
HCA分析是一种常见的无监督模式识别方法, 可将具有相似特点的样品归为一类, 可用于不同产地药材的区分与鉴别[13, 14]。以测定的6种黄酮类成分和1种有机酸类成分的含量为变量, 使用SPSS 26.0软件, 采用组间联接法, 以平方欧式距离为度量, 对不同产地橘红药材进行HCA分析, 聚类图见图 2。当5 < 阈值< 10时, 可将15批样品明显的分为2类, 其中第Ⅰ类为S1~S5, 产地为四川成都; 第Ⅱ类为S6~S10、S11~S15, 产地为湖北襄阳和浙江金华。通过HCA结果可以看出, 第Ⅰ类样品中7种成分的总含量相对较低, 单独聚为一类; 第Ⅱ类样品中7种成分的总含量接近, 聚为一类, 但是浙江金华产地的橘红7种成分总含量要高于湖北襄阳。7种成分中含量最高的为橙皮苷, 其次为芸香柚皮苷和川陈皮素。
|
Figure 2 Hierarchical cluster analysis of Citri Exocarpium Rubrum medicinal materials from different origins. S1-S5 Chengdu, Sichuan; S6-S10 Xiangyang, Hubei; S11-S15 Jinhua, Zhejiang |
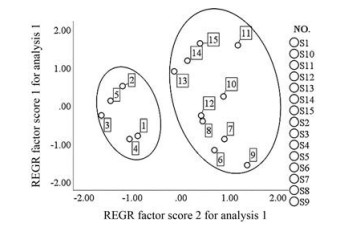
PCA分析是一种重要的多元统计分析方法, 其本质是以最大方差为原则进行分析, 将数据的多元变量抽取出少量主成分, 前几个主成分对于复杂的中药体系而言, 往往能够表征化学量测数据的整体情况, 该方法被广泛用于中药材比较与区分中[15, 16]。因此, 在HCA的基础上, 进一步采用PCA对橘红药材进行比较区分, PCA分析结果和HCA分析结果一致, 见图 3。综合聚类分析和主成分分析结果, 不同产地橘红可以分为两类, 所建立的分析方法可用于不同产地橘红药材的区分比较与质量控制。
|
Figure 3 Principal components analysis of Citri Exocarpium Rubrum medicinal materials from different origins. S1-S5 Chengdu, Sichuan; S6-S10 Xiangyang, Hubei; S11-S15 Jinhua, Zhejiang |
实验过程中考察了不同提取方式、提取时间、不同纯度提取溶剂的提取效果, 结果表明以80%甲醇作为提取溶剂时, 超声处理40 min、7种成分含量较高; 以乙腈和0.1%甲酸水为流动相, 采用梯度洗脱的方式进行分析, 缩短了分析时间, 各峰形对称, 基线分离, 且同分异构体不相互干扰, 可以得到满意的分离效果。
通过质谱针泵进样的方式对7个成分进行母离子、子离子的选择, 并且优化每个成分的DP和CE。川陈皮素、橘皮素和甜橙黄酮在正离子模式下响应较好, 绿原酸、芦丁、芸香柚皮苷、橙皮苷4个成分在负离子模式下响应较好, 因此采用MRM的扫描方式下正负离子同时监测, 实现一次进样完成多成分同时定量的需求。
首次采用UPLC-MS/MS分析方法同时测定橘红药材中绿原酸、芦丁、芸香柚皮苷、橙皮苷、甜橙黄酮、川陈皮素、橘皮素7个成分的含量, 并应用该方法检测15批橘红药材, 结合HCA和PCA分析, 对不同产地橘红药材进行了鉴别和区分, 浙江金华和湖北襄阳所产橘红药材含量高于四川成都, 可能与其不同地域的气候原因有关。结果表明, 本研究所建立的含量测定方法分析时间短、灵敏度高、专属性强、准确度高, 为橘红药材的质量控制和进一步复方制剂研发提供参考, 也为其他相似药材的开发指引提供可行性的研究方法和思路。
作者贡献: 范帅帅主要进行了本文的选题与设计、方法建立、实验数据处理、撰写文章及对编辑部修改意见进行核修等。任海波在制备橘红样品及配制溶液时提供帮助。杨梦婷对文章图片修改提供了宝贵的意见。王鑫国对本文选题与设计、实验思路提供了宝贵的意见。牛丽颖从选题的设计、实验思路、方法建立及文章修改提供了专业的指导。
利益冲突: 无任何利益冲突。
| [1] |
Chinese Pharmacopoeia Committee. The Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2015 Ed. Part Ⅰ. Beijing: China Medical Science Press, 2020: 76.
|
| [2] |
Chen Y. Baoqing Herbal Compromise (宝庆本草折衷)[M]. Beijing: People's Medical Publishing House, 1991: 159.
|
| [3] |
Yu X, Sun S, Guo YY, et al. Citri Reticulatae Pericarpium (Chenpi): botany, ethnopharmacology, phytochemistry, and pharmacology of a frequently used traditional Chinese medicine[J]. J Ethnopharmacol, 2018, 220: 265-282. DOI:10.1016/j.jep.2018.03.031 |
| [4] |
Xu SS, Xu J, Zhang XM, et al. Research progress on Citri Reticulatae Pericarpium, Aurantii Fructus Immaturus, and Aurantii Fructus and Q-marker predictive analysis[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 35-44. |
| [5] |
Liu EH, Zhao P, Duan L, et al. Simultaneous determination of six bioactive flavonoids in Citri Reticulatae Pericarpium by rapid resolution liquid chromatography coupled with triple quadrupole electrospray tandem mass spectrometry[J]. Food Chem, 2013, 141: 3977-3983. DOI:10.1016/j.foodchem.2013.06.077 |
| [6] |
Zhao LH, Zhao HZ, Zhao X, et al. Simultaneous quantification of seven bioactive flavonoids in Citri Reticulatae Pericarpium by ultra-fast liquid chromatography coupled with tandem mass spectrometry[J]. Phytochem Anal, 2016, 27: 168-173. DOI:10.1002/pca.2612 |
| [7] |
Zheng M, Lu S, Xing J. Enhanced antioxidant, anti-inflammatory and alpha-glucosidase inhibitory activities of citrus hesperidin by acid-catalyzed hydrolysis[J]. Food Chem, 2021, 336: 127539. DOI:10.1016/j.foodchem.2020.127539 |
| [8] |
Li RR, Zhao D, Li MM, et al. Study on the metabolites of Bulbus Fritillariae Thunbergii and Pericarpium Citri Reticulatae in rats based on HPLC-Q exactive-orbitrap high-resolution mass spectrometry[J]. Chin J Pharm Anal (药物分析杂志), 2020, 40: 1413-1424. |
| [9] |
Yao YJ, Zang FJ, Hao JJ, et al. Study on the quality standard of Citri Exocarpium Rubrum formula granules[J]. Guangzhou Chem Ind (广州化工), 2020, 48: 71-73. |
| [10] |
Zhang Q, Luo JY, Hu WJ, et al. Analysis on quality value transmitting of substance benchmark of Houpo Wenzhong Decoction[J]. China J Chin Mater Med (中国中药杂志), 2021, 46: 810-819. |
| [11] |
Shi LQ, Wang RJ, Liu TS, et al. A rapid protocol to distinguish between Citri Exocarpium Rubrum and Citri Reticulatae Pericarpium based on the characteristic fingerprint and UHPLC-Q-TOF MS methods[J]. Food Funct, 2020, 11: 3719-3729. DOI:10.1039/D0FO00082E |
| [12] |
Zhao QL, Zhang L, Bian XK, et al. Analysis of 8 triterpene acids in Poria from different habitats based on UPLC-QTRAP-MS[J]. Chin J Pharm Anal (药物分析杂志), 2020, 40: 1169-1177. |
| [13] |
Liu KH, Tang SY, Zhao LY, et al. Principal component and cluster comparative analysis of Ophiopogonis Radix from Zhejiang and Sichuan Provinces based on their morphological character[J]. Chin Tradit Herb Drugs (中草药), 2021, 52: 1765-1771. |
| [14] |
Zhen YQ, Tian W, Zhi YJ, et al. Correlation study on non-volatile ingredients of Menthae Haplocalycis Herba formula granules and traditional herbal pieces by UPLC-MS/MS[J]. China J Chin Mater Med (中国中药杂志), 2021, 46: 1134-1140. |
| [15] |
Lin L, Li HH, Xie H, et al. Quality study of Inulae Flos based on HPLC and chemometrics[J]. Chin Tradit Herb Drugs (中草药), 2021, 52: 1751-1758. |
| [16] |
Zhang B, Sun XL, Guo YL, et al. Chemical constituents of Ginseng Radix et Rhizoma with different growth years and different origins based on LC-MS[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2020, 26: 206-212. |
 2021, Vol. 56
2021, Vol. 56


