越南槐(Sophora tonkinensis) 为豆科(Leguminosae) 槐属(Sophora) 植物, 其干燥根茎为传统中药山豆根[1]。该药用植物主要分布于我国广西、云南和贵州交界地带, 在越南北部也有少量分布, 生于亚热带或温带的石山或石灰岩山地的灌木林中[2]。山豆根性苦寒, 有毒, 归肺、胃经, 具有清热解毒、消肿利咽的功效, 主要用于治疗火毒蕴结、齿龈肿痛、口舌生疮等[3]。现代研究表明, 喹诺里西啶类生物碱为山豆根的主要活性成分[4], 其抗炎、抗病毒和抗肿瘤等多种药理作用的研究一直深受关注[5]。虽然目前已有许多含山豆根的制剂, 如肝炎灵注射剂、复方山豆根口服液、桂林西瓜霜和阮氏上清丸等。但是山豆根的药用研究依然存在着药效物质基础不够明确, 药理研究不够深入等问题。另外, 近年来由于山豆根市场需求量不断加大和无节制采挖, 其野生资源逐渐枯竭, 急需开展山豆根可持续利用与资源保护研究。
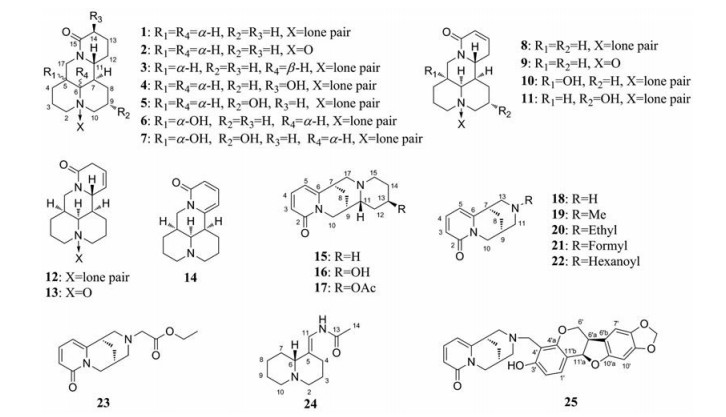
本实验从山豆根中分离得到25个喹诺里西啶类生物碱(图 1), 通过应用各种光谱和波谱技术, 分别鉴定为苦参碱(1)[6-9]、氧化苦参碱(2)[8-10]、allomatrine (3)[11]、14β-羟基苦参碱(4)[7]、9α-羟基苦参碱(5)[10, 12]、槐醇(6)[12, 13]、5α, 9α-二羟基苦参碱(7)[14]、槐果碱(8)[7, 8]、氧化槐果碱(9)[7, 8, 13]、5α-羟基槐果碱(10)[4, 15]、9α-羟基槐果碱(11)[16]、lehmannine (12)[17, 18]、lehmannine N-oxide (13)[19]、槐胺(14)[8, 9]、鹰爪豆碱(15)[20]、baptifoline (16)[21]、O-acetylbaptifoline (17)[22]、金雀花碱(18)[4, 23, 24]、N-甲基金雀花碱(19)[23-25]、N-乙基金雀花碱(20)[23, 26]、N-甲酰基金雀花碱(21)[24.26]、N-己酰基金雀花碱(22)[27]、12-(1-乙酰氧基乙基)-金雀花碱(23)、lusitanine (24)[28]和tonkinensine B (25)[29]。其中化合物23为新的金雀花碱型衍生物, 化合物13、16、17和24首次从越南槐根茎中分离得到。基于山豆根在抗炎方面的传统药用, 对分离鉴定的化合物进行了抑制LPS诱导小鼠巨噬细胞RAW 264.7释放NO能力评价, 发现化合物1、6、19、20有明显的抗炎活性。
|
Figure 1 Chemical structures of compounds 1-25 |
化合物23无色油状物。通过高分辨质谱HR-ESI-MS的分子离子峰m/z 299.136 7 [M+Na]+ (计算值299.136 6), 推导出其分子式为C15H20N2O3, 不饱和度为7。红外光谱吸收峰表明化合物中存在酯羰基(1 735 cm-1) 和酰胺羰基(1 648 cm-1)。1H NMR数据(表 1) 的烯氢质子信号说明化合物存在一个α吡啶环单元δH 6.43 (1H, dd, J = 9.0, 1.2 Hz, H-3)、7.26 (1H, dd, J = 9.0, 6.8 Hz, H-4)、5.97 (1H, dd, J = 6.8, 1.2 Hz, H-5)][6]。13C NMR (表 1) 和DEPT数据显示共有15个碳信号, 包括3个羰基信号: 151.4 (C-6)、163.8 (C-2)、170.4 (C-15); 5个次甲基信号: 28.1 (C-9)、35.5 (C-7)、104.8 (C-5)、116.8 (C-3)、139.8 (C-4); 6个亚甲基和1个甲基信号14.3 (C-17)。
| Table 1 1H and 13C NMR data of compound 23 (CDCl3, 600 MHz for 1H NMR, and 150 MHz for 13C NMR) |
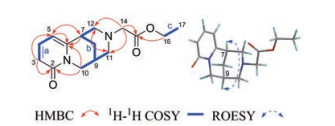
以上这些数据表明, 化合物23为金雀花碱型衍生物。将化合物23的1H NMR数据与12-cytisineacetate比较, 发现二者非常相似[30], 主要的不同在于少了12-cytisineacetate中的甲氧基信号δH 3.63 (3H, s, COOCH3), 多了一个甲基信号δH 1.19 (3H, t, J = 7.2 Hz) 和一个亚甲基信号δH 4.07 (2H, q, J = 7.2 Hz)。因此, 推测12-cytisineacetate中的甲基在化合物23中被乙基取代。这一推断通过H2-16/H3-17的1H-1H COSY相关(图 2), 以及H2-16 [δH 4.07 (2H, q, J = 7.2 Hz)] 和C-15 (δC 170.4) 的HMBC相关得到证实。因此, 化合物的平面结构得到确定。
|
Figure 2 Key 1H-1H COSY, HMBC and ROESY correlations of compound 23 |
化合物23的构型通过ROESY实验和与类似物的旋光值对比分析得到确定。在ROESY谱中, H-7/H-9的NOE相关表明H-7和H-9有着相同的取向。另外, 根据文献中报道的类似物的旋光值[N-methylcytisine ([α]D20-233 (c 0.43, EtOH)); N-ethylcytisine ([α]D27-216.7 (c 0.31, EtOH)); N-propionyl cytisine ([α]D20-241 (c 1, CHCl3)); N-acetyl cytisine ([α]D20-200 (c 1, CHCl3)); N-hexanoylcytisine ([α]D20-141 (c 0.07, MeOH))][26, 27, 31, 32], 说明化合物23 [[α]D24-89.9 (c 0.1, MeOH)] 与金雀花碱(cytisine, 18) 有着相同的绝对构型。综合上述所有数据, 化合物23的结构鉴定为12-(1-乙酰氧基乙基)-金雀花碱。
2 化合物活性检测采用Griess法考察了山豆根中分离到的25个生物碱抑制LPS诱导小鼠巨噬细胞RAW 264.7释放NO能力。结果表明, 化合物1、6、19、20具有明显的抗炎作用, IC50值分别为39.86 ± 0.65、23.66 ± 0.37、34.56 ±0.45和47.68 ± 0.58 μmol·L-1。其中化合物6的抑制作用与阳性对照L-NMMA的活性相当。同时, 化合物1、6、19、20对小鼠巨噬细胞RAW 264.7未表现出毒性作用(IC50 > 50 μmol·L-1) (表 2)。
| Table 2 Inhibitory effects of compounds 1, 6, 19, and 20 on LPS-induced NO production in macrophages. aL-NMMA was used as positive control; bIC50: 50% inhibitory concentration; cCC50: 50% cytotoxic concentration |
本文对山豆根中的生物碱类成分进行了系统的化学成分研究, 共分离鉴定了25个喹诺里西啶类生物碱, 其中化合物23为新化合物, 化合物13、16、17、24首次从山豆根中分离得到。喹诺里西啶类生物碱分布广泛, 存在于豆科20多个属的植物中。现代药理研究表明该类化合物具有抗炎、抗病毒和抗肿瘤等多种药理作用[5]。本研究发现化合物1、6、19、20有明显的抗炎活性。这一结果加深了对山豆根中生物碱类化学成分的认识。同时, 对中药山豆根传统抗炎功效与化学成分之间的关系也有了初步认识。
实验部分一维、二维核磁数据由Bruker Avance III HD 600型核磁共振仪(瑞士Bruker公司) 测定; Jasco DIP-370数字旋光仪(日本东京JASCO公司) 测定; ZF-1型紫外分析仪(海门市其林贝尔仪器制造有限公司); HR-ESI-MS数据使用API QStar-Pulsar LC-Q-TOF质谱仪获得; Bruker Tensor-27红外光谱仪; Hei-VAP Value G3型旋转蒸发仪(德国Heidolph公司); 3111型CO2恒温培养箱(Thermofisher公司); CKX41型倒置相差显微镜(OLYMPUS); Spectra Max M2多功能读板机(美国Moleccular Devices公司); 薄层色谱硅胶GF254、柱色谱硅胶购于青岛海洋化工; SephadexLH-20 (Amersham Biosciences公司); 碱性氧化铝(天津达茂化学试剂厂); ODS-C18 (75 μm) 反相填充材料(日本YMC公司); MTT、DMSO均为Solarbio公司生产; 胎牛血清(Hyclone公司); 胰蛋白酶(Roche公司); DMEM细胞培养基(Invitrogen公司); 中国科学院典型培养物保藏中心昆明细胞库的小鼠单核巨噬细胞RAW 264.7, 其编号为: KCB200603YJ。
药材样品于2019年6月采自云南省文山州西畴县, 经昆明理工大学生命科学与技术学院陈宣钦副教授鉴定为越南槐(Sophora tonkinensis) 的干燥根茎, 样品标本(编号: KUMST20190708) 保存于昆明理工大学植物化学重点实验室。
1 提取与分离越南槐干燥根茎40 kg粉碎, 用95%乙醇水溶液室温浸泡3次, 每次48 h, 将乙醇提取物减压浓缩至无醇味, 合并提取液得到总提取物。与水混悬的总提取物用0.1%盐酸溶液调节pH至2~3后用乙酸乙酯萃取3次, 萃取后的水相加入17%氨水溶液调节pH至9~10, 再用氯仿萃取3次, 得到氯仿相(总生物碱, 320 g)。
氯仿相(320 g) 首先经过碱性氧化铝柱色谱分离, 依次用石油醚-乙酸乙酯(9∶1~1∶1)、石油醚-丙酮(2∶1~1∶1) 和氯仿-甲醇(9∶1~0∶1) 作为流动相进行梯度洗脱, 根据TLC检测结果, 合并得到F0~F6七个组分, 其中组分F0为油状非生物碱成分。
组分F1段(22.1 g) 经正相硅胶柱色谱(石油醚-乙酸乙酯-二乙胺, 130∶5∶5~5∶5∶0.1) 分离, 通过TLC检测合并得到化合物1 (14.0 g) 和组分F1-1~F1-3三部分。组分F1-1 (170.0 mg) 经多次硅胶分离得到化合物8 (8.0 mg)、12 (4.0 mg)、13 (2.0 mg) 和14 (3.0 mg)。化合物3 (6.1 mg) 从组分F1-2 (110.0 mg) 中通过反复的硅胶柱色谱和Sphadex LH-20凝胶柱色谱(氯仿-甲醇, 1∶1) 分离得到。组分F2段(1.2 g) 经正相硅胶柱(乙酸乙酯-甲醇, 15∶1~1∶1) 洗脱得到化合物23 (11.8 mg)。组分F3段(8.4 g) 经正相硅胶柱(乙酸乙酯-甲醇, 20∶1~1∶1) 梯度洗脱得到F3-1~F3-5五个组分。组分F3-3 (3.9 g) 经过多次硅胶柱色谱和Sphadex LH-20凝胶柱色谱(氯仿-甲醇, 1∶1) 分离得到化合物10 (181.9 mg)、11 (16.4 mg)、15 (5.6 mg)、17 (192.9 mg)、20 (2.8 mg) 和22 (15.5 mg)。化合物5 (385.5 mg)、6 (148.8 mg) 和19 (102.3 mg) 从组分F3-4 (1.5 g) 中经过多次硅胶和Sphadex LH-20凝胶柱色谱(氯仿-甲醇, 1∶1) 分离得到。通过硅胶柱色谱(石油醚-丙酮-二乙胺, 80∶10∶0.9~5∶5∶0.1), 从组分F3-5 (209.5 mg) 中分离得到化合物24 (7.3 mg)。化合物4 (6.0 mg) 和21 (579.8 mg) 从组分F4段(2.4 g) 经过多次硅胶柱色谱和Sphadex LH-20凝胶柱色谱(氯仿-甲醇, 1∶1) 分离得到。组分F5 (200 g) 经过正相硅胶柱色谱(饱和氯仿-甲醇-水, 90∶10∶1~1∶1∶1) 洗脱得到化合物2 (180.0 g)、7 (11.1 mg)、18 (30.1 mg)、16 (12.5 mg) 和25 (7.0 mg)。化合物9 (47.6 mg) 从组分F6 (25.0 g) 中分离得到(正相硅胶柱, 洗脱剂饱和氯仿-甲醇-水, 90∶10∶1~1∶1∶1)。
2 结构鉴定化合物23 无色油状, HR-ESI-MS: m/z 299.136 7 [M+Na]+ (Calcd. for C15H20N2O3Na+, 299.136 6), 分子式为C15H20N2O3; [α]D20-89.9 (c 0.10, MeOH); UV λmax (MeOH) nm (log ε): 232 (3.5), 309 (3.5); IR (KBr) νmax: 2 918, 2 850, 1 735, 1 648, 1 547, 1 318, 1 261, 1 184, 1 028, 804 cm-1; ECD (c 6.16×10-4 M, MeOH), λmax (Δε) 203 (+5.46), 233 (+11.35), 314 (-10.06) nm; 1H NMR (CDCl3, 600 MHz) 和13CNMR (CDCl3, 150 MHz) 见表 1。
3 活性测定 3.1 MTT法测定细胞活力采用MTT法[33]检测化合物对RAW 264.7细胞的细胞活力。
3.2 抑制LPS诱导小鼠巨噬细胞RAW 264.7释放NO活性测定根据Griess反应, 测量培养基中积累的亚硝酸盐浓度作为产生NO的指标, 进行NO抑制实验[34]。将RAW264.7细胞接种于96孔板, 密度为每孔8×104个细胞, 设置三组实验, 分别为空白对照组(DMSO)、LPS刺激组(DMSO+LPS) 和化合物干预组(DMSO+LPS+不同浓度的化合物)。设置化合物浓度为3.125、6.25、12.5、25、50 μmol·L-1, LPS浓度为1 μg·mL-1, 每组设置3组复孔, 在恒温培养箱(37 ℃、5% CO2) 中共同培养24 h后, 使用Griess法检测吸光值(OD540), 计算NO含量, 实验平行三次, 结果为平均数±标准差, 通过MTT法检测化合物对细胞活力的影响。NO生成抑制率(%) = [(LPS刺激组OD-化合物干预组OD)/(LPS刺激组OD-空白组OD)]×100%。
作者贡献: 李蓉涛负责提出研究选题和设计研究方案; 张袁亚负责实施过程和采集整理数据; 张袁亚和叶瑞绒负责设计论文框架、起草论文和修订论文; 张治军和李蓉涛负责获取研究经费、技术或材料支持、指导性支持。
利益冲突: 本研究不存在研究者、伦理委员会成员、受试者监护人以及公开研究成果有关的利益冲突。
| [1] |
Li F, Li CP, Fu H, et al. Research progress of radix Sophorae tonkinensis and supplementary reports of assay method for toxic chemical composition[J]. Chin J Pharm Anal (药物分析杂志), 2013, 33: 1453-1463. |
| [2] |
Huang BY, Nong DX, Huang XY, et al. Resources investigation report on Chinese materia medica Sophora tonkinensis[J]. Mod Chin Med (中国现代中药), 2014, 16: 740-744. |
| [3] |
Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. Part 1. Beijing: China Medical Science Press, 2015: 27.
|
| [4] |
Zhang Y, Hu WZ, Chen XZ, et al. Bioactive quinolizidine alkaloids from Sophora tonkinensis[J]. China J Chin Mater Med (中国中药杂志), 2016, 41: 2261-2266. |
| [5] |
Cui Y. Research progress in chemical components, pharmacological effectiveness and toxicity of radix et rhizoma Sophorae tonkinensis[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2011, 17: 229-232. |
| [6] |
Xiao P, Li J, Kubo H, et al. ChemInform Abstract: (-)-14β-Hydroxymatrine, a new lupine alkaloid from the roots of Sophora tonkinensis[J]. ChemInform, 1996, 44: 1951-1953. |
| [7] |
Zhao DR, Xue Y, Chen XQ, et al. A study on the quinolizidine alkaloids of Sophora flavescens[J]. J Kunming Univ Sci Technol (Nat Sci) (昆明理工大学学报(自然科学版)), 2018, 43: 93-97. |
| [8] |
Lu B, Shi RB. Constituents in the alkaloid fraction of Kushen decoction[J]. China J Chin Mater Med (中国中药杂志), 2006, 31: 557-560. |
| [9] |
Tan CJ, Lu LN, Tang HM, et al. Alkaloids from Oxytropis ochrocephala Bunge[J]. Nat Prod Res Devel (天然产物研究与开发), 2015, 27: 1365-1367. |
| [10] |
Gao HY, Li GY, Wang HY, et al. Chemical constituents from the seeds of Sophora alopecuroides L.[J]. J Shihezi Univ (Nat Sci) (石河子大学学报(自然科学版)), 2011, 29: 75-78. |
| [11] |
Galasso V, Asaro F, Berti F, et al. On the molecular and electronic structure of matrine-type alkaloids[J]. Chem Phys, 2007, 330: 457-468. |
| [12] |
Negrete R, Cassels B, Eckhardt G. (+)-9α-Hydroxymatrine from Sophora macrocarpa[J]. Phytochemistry, 1983, 22: 2069-2072. DOI:10.1016/0031-9422(83)80047-8 |
| [13] |
Liu XJ, Cao MA, Li WH, et al. Alkaloids from Sophora flavescens Aition[J]. Fitoterapia, 2010, 81: 524-527. DOI:10.1016/j.fitote.2010.01.008 |
| [14] |
Ohmiya S, Higashiyama K, Otomasu H, et al. (+)-5α, 9α-Dihydroxymatrine, a new lupin alkaloid from Euchresta horsfeldii[J]. Phytochemistry, 1979, 18: 645-647. DOI:10.1016/S0031-9422(00)84277-6 |
| [15] |
Saito K, Arai N, Sekine T, et al. (-)-5α-Hydroxysophocarpine, a new lupin alkaloid from the seeds of Sophora flavescens var. angustifolia[J]. Plant Med, 1990, 56: 487-488. DOI:10.1055/s-2006-961018 |
| [16] |
Xiao P, Kubo H, Komiya H, et al. Lupin alkaloids from seeds of Sophora viciifolia[J]. Phytochemistry, 1999, 50: 189-193. DOI:10.1016/S0031-9422(98)00486-5 |
| [17] |
Ding PL, Liao ZX, Huang H, et al. (+)-12α-Hydroxysophocarpine, a new quinolizidine alkaloid and related anti-HBV alkaloids from Sophora flavescens[J]. Bioorg Med Chem Lett, 2006, 16: 1231-1235. DOI:10.1016/j.bmcl.2005.11.073 |
| [18] |
Lu B, Li JL, Yuan YJ. Isolation of alkaloids and structure elucidation of lehmannine from seed of Sophora alopecuroides[J]. Chin Tradit Herb Drugs (中草药), 2001, 32: 293-296. |
| [19] |
Ibragimov BT, Talipov SA, Kushmuradov YK, et al. Structure of lehmannine N-oxide[J]. Chem Nat Compounds, 1981, 17: 552-557. DOI:10.1007/BF00574375 |
| [20] |
Rycroft DS, Robins DJ, Sadler IH. Assignment of the 1H and 13C NMR spectra of the quinolizidine alkaloid anagyrine and determination of its conformation[J]. Magn Reson Chem, 1991, 29: 936-940. DOI:10.1002/mrc.1260290913 |
| [21] |
Kennelly EJ, Flynn TJ, Mmazzola EP, et al. Detecting potential teratogenic alkaloids from blue cohosh rhizomes using an in vitro rat embryo culture[J]. J Nat Prod, 1999, 62: 1385-1389. DOI:10.1021/np9901581 |
| [22] |
Saito K, Takamatsu S, Murakosh I, et al. Isolation of a new alkaloid (-)-O-acetylbaptifoline and the absolute stereochemical relationships of lupine alkaloids in Thermopsis chinensis[J]. J Nat Prod, 1989, 52: 1032-1035. DOI:10.1021/np50065a019 |
| [23] |
Przybył AK, Kubicki M. A comparative study of dynamic NMR spectroscopy in analysis of selected N-alkyl-, N-acyl-, and halogenated cytisine derivatives[J]. J Mol Struct, 2011, 985: 157-166. DOI:10.1016/j.molstruc.2010.10.036 |
| [24] |
Li X, Wang D, Cui Z. A new cytisine-type alkaloid from the stem bark of Maackia amurensis[J]. Nat Prod Res, 2010, 24: 1499-1502. DOI:10.1080/14786410903265561 |
| [25] |
Wang Z, Li S. Isolation and identification of alkaloids from Thesium chinense Turcz[J]. Chin J Med Chem (中国药物化学杂志), 2008, 16: 306-308. |
| [26] |
Murakoshi I, Watanab M, Haginiw J, et al. (-)-N-Ethylcytisine, a lupin alkaloid from the flowers of Echinosophora koreensis[J]. Phytochemistry, 1982, 21: 1470-1471. DOI:10.1016/0031-9422(82)80178-7 |
| [27] |
Ohmiya S, Murakoshi HO, Hagimiwa J. N-Formylcytisine: a new alkaloid from Thermopsis chinensis[J]. Phytochemistry, 1974, 13: 643-644. DOI:10.1016/S0031-9422(00)91367-0 |
| [28] |
Murakoshi I, Kidoguchi E, Haginiw J, et al. Isokuraramine and (-)-7, 11-dehydromatrine, lupin alkaloids from flowers of Sophora flavescens[J]. Phytochemistry, 1982, 21: 2379-2384. DOI:10.1016/0031-9422(82)85210-2 |
| [29] |
Li XN, Lu Z, Qin S, et al. Tonkinensines A and B, two novel alkaloids from Sophora tonkinensis[J]. Tetrahedron Lett, 2008, 49: 3797-3801. DOI:10.1016/j.tetlet.2008.04.003 |
| [30] |
Ohmiya S, Otomasu H, Hagimiwa J, et al. (-)-12-Cytisineacetic acid, a new lupin alkaloid in Euchresta japonica[J]. Phytochemistry, 1979, 18: 649-650. DOI:10.1016/S0031-9422(00)84278-8 |
| [31] |
Pan QM, Zhang GJ, Huang RZ, et al. Cytisine-type alkaloids and flavonoids from the rhizomes of Sophora tonkinensis[J]. J Asian Nat Prod Res, 2016, 18: 429-435. DOI:10.1080/10286020.2015.1131680 |
| [32] |
Rouden J, Ragot A, Gouaolt S, et al. Regio- and diastereoselective functionalization of (-)-cytisine: an unusual N-C acyl migration[J]. Tetrahedron: Asymmetry, 2002, 13: 1299-1305. DOI:10.1016/S0957-4166(02)00271-9 |
| [33] |
Chen TT, Huang TY, Li MY, et al. Correlation between bone protection of 1, 2, 3, 4, 6-pentyl-O-galloyl-beta-D-glucose and Nrf2/HO-1 signaling pathway[J]. Acta Pharm Sin (药学学报), 2020, 55: 907-914. |
| [34] |
Cao L, Li RT, Chen XQ, et al. Neougonin A inhibits lipopolysaccharide-induced inflammatory responses via downregulation of the NF-κB signaling pathway in RAW 264.7 macrophages[J]. Inflammation, 2016, 39: 1939-1948. DOI:10.1007/s10753-016-0429-9 |
 2021, Vol. 56
2021, Vol. 56


