2. 首都医科大学附属北京安贞医院, 北京 100029;
3. 首都医科大学附属北京天坛医院, 北京 100070;
4. 江苏康缘药业股份有限公司, 江苏 连云港 222067
2. Beijing Anzhen Hospital, Capital Medical University, Beijing 100029, China;
3. Beijing Tiantan Hospital, Capital Medical University, Beijing 100070, China;
4. Jiangsu Kanion Pharmaceutical Company, Lianyungang 222067, China
脑卒中是由于脑部血管突然破裂或因血管阻塞导致血液不能流入大脑而引起脑组织损伤的一种疾病, 每年我国约有196万人死于脑卒中[1]。缺血性脑血管病是脑卒中最常见的类型, 超早期静脉溶栓能显著改善急性缺血性卒中带来的神经功能缺损症状[2]。阿替普酶作为溶栓药物已在临床中使用, 但因其时间依赖性较强、给药过程较长及存在一定的出血风险, 极大限制了药物在临床中的广泛应用[3, 4]。研发更加安全有效、使用便捷的静脉溶栓药物是缺血性脑卒中救治领域的研究热点。溶栓新药研发离不开动物实验, 建立贴近临床实际应用的血栓溶栓药物药效评价方法则是静脉溶栓药物研发的关键步骤。
血流再灌注是判断急性缺血性脑卒中静脉溶栓药物疗效的关键指标[5]。临床中再灌程度评价主要基于CT血管造影术(CTA)、磁共振血管造影(MRA) 和数字减影血管造影(DSA) 进行评判, 其中DSA被视为金标准, DSA脑血管造影能够准确判断颅内血管闭塞部位、侧枝循环以及再灌注情况, 具有良好的时间和空间分辨率[6]。临床中评价再灌注情况最常用的方法是脑梗死溶栓血流分级(TICI) 系统[7], 该评分方法借鉴冠状动脉循环评分系统(TIMI) 制定, 用于量化脑血管再灌注程度, 该系统对于预测良好神经功能预后有较高的价值[8]。
在临床前溶栓药物药效学评价中, 尚无更贴近临床实际应用的评价体系。本文将临床TICI分级方法简化, 根据脑血流灌注程度, 提出了适用于比格犬脑血管闭塞药物药效评价的方法, 并通过阿替普酶溶解犬脑血管血栓实验验证该评价方法中的量化指标。
材料与方法实验动物 健康雄性比格犬(12 ± 3) kg, 12只, 由北京芳元缘养殖场提供, 许可证编号: SCXK (京) 2020-0001; No.110334201100036847, 动物实验通过了中国医学科学院药物研究所实验动物管理与动物福利委员会批准。实验动物分笼饲养, 食物与水充足, 12 h/12 h昼夜循环, 饲养温度维持在(25 ± 1) ℃, 湿度适中。
试剂和耗材 凝血酶(北京索莱保生物技术有限公司, T8021); 5F单弯导管(Cordis公司, 451-506P0); 导引导丝(Abbott公司, 1009664); 肝素钠(马鞍山丰原制药有限公司, 200619-2); 0.9%氯化钠(河北天成药业股份有限公司, C20052904); 舒泰(Virbac S.A公司, 83888104); 异氟烷(深圳市瑞沃得生物技术有限公司, R510-22-4); 丙泊酚乳状注射液(广东嘉博制药有限公司, 5A200301); 碘普罗胺注射液(拜耳医药保健有限公司, 316A)。
实验分组 将12只比格犬随机分为模型组和阿替普酶组(临床折算剂量1.68 mg·kg-1), 每组6只。
血栓制作 抽取比格犬静脉血20 mL, 常温下4 000 r·min-1离心10 min后, 取上层血浆l0 mL, 加入凝血酶1 000 μg混匀并注入尖端缩细的玻璃试管中。室温凝固2 h, 凝固后取出置入生理盐水中反复漂洗, 剪成长为5~8 mm的血栓条备用。
动物模型制作 采用介入手术建立比格犬急性血栓性脑血管闭塞动物模型, 分别于两侧腹股沟区备皮, 消毒铺巾, 穿刺右股动脉置入导管鞘, 置入导丝, 将5F单弯导管插至颈内动脉近端, 手推注显影剂确定血管走向, 正侧位造影判断血管走行情况。用1 mL注射器吸3~5条血栓条注入颈内动脉, 造影证实颈内动脉颅内段末端栓塞, 2 h后造影复查血管的灌注情况, 证实栓塞血管没有因血栓自溶复通, 之后30 min匀速静脉滴注阿替普酶。溶栓治疗后1 h, 脑血管造影, 判断血管复通情况, 进行评分。
评级标准与方法 为了方便实验数据后期统计分析, 比格犬脑梗死溶栓评分量表(DTICI) 按照评分分为0级、Ⅰ级、Ⅱa级、Ⅱb级和Ⅲ级共5个等级, 分别对应分数为0分、1分、2分、3分、4分、5分6个分数标准(表 1), 评分越低则脑闭塞程度越重, 评分采用双人背靠背盲评分方式, 两人结果一致则评分通过, 不同则进行第三人判评。
| Table 1 Dog thrombolysis in cerebral infarction scale (DTICI) |
统计学分析 采用SPSS 22.0统计分析软件进行统计分析及图表绘制。计量资料符合正态分布, 两组间比较采用独立样本t检验。P < 0.05为差异有统计学意义。
结果 1 比格犬脑血管闭塞模型建立对比格犬左脑血管进行造影, 观察脑血管分布。如图所示(图 1), 比格犬左侧颈内动脉是颈总动脉的一个分支, 管腔较细且走行迂回, 血栓容易停留, 下游管腔较为粗大的为大脑中动脉[9]。推注造影剂后, 动脉期、毛细血管期、静脉期依次显影。动脉期为颅内动脉血管成像, 血管较粗且颜色较深, 颅内动脉血管显影清晰正常; 动脉显影结束后, 毛细血管逐渐显影, 毛细血管期血流量最大, 整个左脑颜色加深全部显影; 静脉期, 血流经静脉窦流出脑室, 有明显静脉回流现象。以上结果表明, 通过DSA血管造影可以清晰观察颅内血流走行情况。

|
Figure 1 Normal intracranial angiogram in beagle dogs |
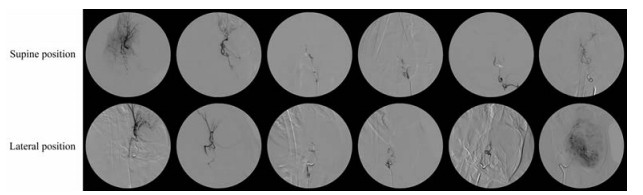
介入方式建立脑血管闭塞模型, 其后2 h进行造影观察血管闭塞程度, 结果可见(图 2), 模型组(n = 6) 比格犬左脑颅内因血栓置入, 颅内大脑中动脉正位、侧位均不显影, 且毛细血管期消失, 无静脉回流, 左脑大面积无血流通过, 以上结果表明, DSA血管造影可以清晰观察颅内血管闭塞情况。
|
Figure 2 DSA imaging of cerebral vessels in model group |
以上结果表明, 对比格犬脑部血管解剖结构DSA造影方法显影分辨率高, 脑血管闭塞模型建模方法稳定, 这对血管再灌程度评分方法的建立提供了重要的技术支持。
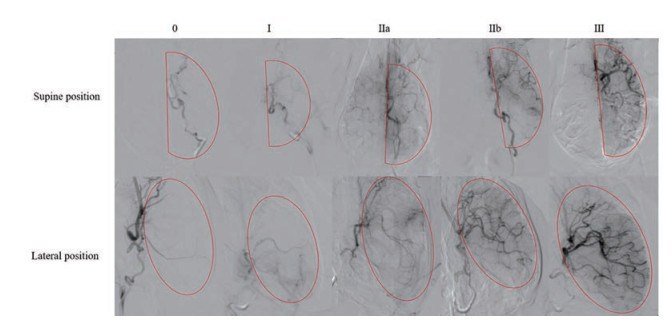
为了准确评价比格犬脑血管再通程度, 本研究建立了更加高效的新型溶栓药物药效评价方法(表 1)。根据血管再通程度, 0级为无灌注, 颈内动脉部分显影, 大脑中动脉无血流, 不显像, 无毛细血管期和动脉期; Ⅰ级主要表现为, 颅内颈内动脉显影, 且颅内动脉轻微显像, 但是无前向血流, 且毛细血管期、静脉期不显像; Ⅱa级为在Ⅰ级基础上, 颅内毛细血管部分显影, 显影面积小于左脑的二分之一; Ⅱb级为在Ⅱa基础上, 毛细血管显影大于二分之一; Ⅲ级为左脑血管完全显影, 血流顺畅流过, 三个时像清晰显像(图 3)。
|
Figure 3 Different grades of cerebral angiography, the red circle in the figure represents left brain area |
比格犬溶栓药效评价方法增加了评分方式, 将评级系统转化为具体分数, 更便于数据统计分析。
3 比格犬脑血管评分对阿替普酶溶栓作用评价上述实验提出了基于比格犬的新型脑部血管再灌程度评价方法。为了验证该标准的可行性, 以及是否能准确区分不同脑血管再通程度, 以溶栓阳性药阿替普酶验证新方法的量化指标。阿替普酶是被美国FDA批准使用的溶栓药物, 其溶栓效果被医学界认可[10], 因此本研究以阿替普酶作为验证药物。介入手术后2 h, 静脉滴注阿替普酶(1.68 mg·kg-1) 溶栓30 min。
溶栓前将比格犬(n = 6) 左脑血管血流按照评分标准进行评分, 66% (4只) 比格犬评分为1分, 血管闭塞比较严重, 图像显示左脑大面积无血流。溶栓后与溶栓前相比, 83% (5只) 动物评分达到3分及以上, 在图像(与评分对应) 中显示为颅内血管再通, 毛细血管期显影, 静脉回流恢复(图 4)。秩和检验分析结果表明, 给药前后血管再通评分具有显著差异(P = 0.01, P < 0.05)。

|
Figure 4 Alteplase promotes recanalization of occluded vessels. A: Score of DTICI in beagle dogs before and after alteplase administration; B: Rank sum test analysis of DTICI score before and after alteplase treatment (P < 0.05); C: DSA imaging results before and after alteplase treatment in beagle dogs |
本研究基于比格犬脑血管闭塞模型, 建立了新型犬急性血管闭塞药物溶栓再通评价方法, 并以阿替普酶作为溶栓药物, 对该实验方法以及评分系统进行验证。结果表明, 阿替普酶的血管再通药效明显, 且评分均达到3分及以上水平, 说明本评分系统可以较好地应用于比格犬颅内血管闭塞溶栓药物临床前药效评价, 为颅内血管闭塞性疾病溶栓药物临床前研究提供方法学支持。
目前, 缺血性脑卒中颅内血管血流灌注程度多采用数字减影技术(DSA)[11]、经颅多普勒(TCD)[12]、磁共振血管造影[13]等方法观测脑血流情况。本研究采用了血管显影金标准—血管造影技术DSA。与传统溶栓药效学评价方法相比, DSA不仅具有良好的空间分辨率, 能清晰观察颅内血管分布, 而且能客观反映颅内血管再通程度, 为准确分级可视化评价犬颅内血管闭塞程度奠定了技术基础。
脑梗死溶栓血流分级标准(TICI) 是目前临床公认的脑血管灌注水平评价系统, 可以准确评估脑梗患者颅内血流再灌程度, 指导临床治疗及用药。本评分方法基于临床TICI标准, 通过综合观察动脉期、毛细血管期、静脉期血流灌注情况, 将血流复灌程度分为5个等级, 以等级划分的方式评价了颅内血管灌注水平的变化。为了保障评分的客观性, 本研究采用背靠背式评分方法, 并对评分进行秩和检验分析, 比较给药前、后脑血管闭塞区血流灌注差异, 以此保证评价方法的准确性和客观性。
本实验模拟临床急性血栓性脑血管闭塞溶栓治疗, 如: 在给药时间窗选择中, 模拟脑卒中患者从发病到接受治疗时程, 采用脑血管闭塞后2 h进行阿替普酶溶栓治疗。另外, 本实验采用自体血栓制作动物模型, 更加贴切地模拟了脑卒中患者因血流淤滞引发的血栓性脑血管闭塞症状, 保证了临床症状与药效学评价方法的一致性。
本文通过借鉴临床脑梗死程度评级标准(TICI), 对颅内大血管闭塞药物溶栓效果的评价方法进行了优化。与临床当中相比, 本方法删除了TICI标准中显影剂清除速率对比的方法, 采用判断血流通过动脉期、毛细血管期血管显影程度进行颅内血管闭塞评分, 提高了对血管造影成像的评级效率, 同时降低使用难度, 使得评分过程在药效学评价中更加客观、高效。
本研究提出了基于大动物比格犬脑血管闭塞再通的评分方法, 之前有研究者通过计算溶栓前后比格犬颅内动脉期再通血管数量的方式进行溶栓药效学评价[14], 本评价方法与之相比, 不仅对动脉期血管再通程度进行评估, 还加入了对静脉期毛细血管再通的评级标准, 提高了药效评价方法的准确性。
以比格犬作为模型基础进行溶栓药物药效评价已经得到了认可[15], 与啮齿类动物相比, 比格犬脑血管直径变异不大且血管较粗, 血管走行情况更接近于人, 其实验结果可更好地向临床转化。比格犬可采用临床中公认的血管造影金标准DSA血管造影方法, 实现对颅内血管闭塞程度实时、可视化监测, 提供溶栓是否有效的直接证据。另外, 相比于小动物, 比格犬可采用介入方式建立模型, 最大限度地减少多余的操作损伤, 保证溶栓药效学评价的准确性和可靠性。
尽管本研究建立了比格犬急性血栓性脑血管闭塞模型以及评分标准, 但实验仍有不足之处。与临床患者数量相比, 新型评分标准采用的每组动物只数较少, 今后的实验会进一步加大样本量, 保障药效学评价方法准确性、客观性、可重复性, 为溶栓药物药效评价提供技术支持。
综上所述, 本文基于比格犬颅内大血管闭塞模型, 提出了新型溶栓药物评价方法, 并采用溶栓药阿替普酶验证了新方法的可行性, 为脑卒中治疗药物临床前溶栓药效评价提供了有力的理论依据和技术支持。
作者贡献: 张鹏主要完成了实验设计、文章起草、撰写与实验手术工作; 田毅为主要实验操作人员, 完成了实验动物手术任务; 马高亭提出比格犬颅内血管再通评价标准并进行了修改; 董超然和王明超完成了影像评级工作; 周建明和曹亮提供了实验药品; 朱海波指导整个实验进行, 包括实验设计、文章起草、新评价标准提出及修改。
利益冲突: 所有作者均声明没有利益冲突。
| [1] |
Wang LD, Liu JM, Yang Y, et al. The prevention and treatment of stroke still face huge challenges—brief report on stroke prevention and treatment in China, 2018[J]. Chin Circ J (中国循环杂志), 2019, 34: 105-119. |
| [2] |
Tomas P, Boris K, Ivana S, et al. Acute stroke therapy: a review[J]. Trends Cardiovas Med, 2017, 27: 59-66. DOI:10.1016/j.tcm.2016.06.009 |
| [3] |
William NW, Jonathan E, Kennedy RL, et al. Risk of intracerebral haemorrhage with alteplase after acute ischaemic stroke: a secondary analysis of an individual patient data meta-analysis[J]. Lancet Neurol, 2016, 15: 925-933. DOI:10.1016/S1474-4422(16)30076-X |
| [4] |
Kong LL, Ma YZ, Li L, et al. Advances in the study of mechanism of thrombolysis-induced hemorrhagic transformation and therapeutic drugs[J]. Acta Pharm Sin (药学学报), 2018, 53: 1467-1476. |
| [5] |
Grant M, Rudiger VK, Alessandro A, et al. Arterial obstruction on computed tomographic or magnetic resonance angiography and response to intravenous thrombolytics in ischemic stroke[J]. Stroke, 2017, 48: 353-360. DOI:10.1161/STROKEAHA.116.015164 |
| [6] |
Herzig R, Burval S, Krupka B, et al. Comparison of ultrasonography, CT angiography, and digital subtraction angiography in severe carotid stenoses[J]. Eur J Neurol, 2004, 11: 774-781. DOI:10.1111/j.1468-1331.2004.00878.x |
| [7] |
Kleine JF, Wunderlich S, Zimmer C, et al. Time to redefine success? TICI 3 versus TICI 2b recanalization in middle cerebral artery occlusion treated with thrombectomy[J]. J Neurointerv Surg, 2017, 9: 117-121. DOI:10.1136/neurintsurg-2015-012218 |
| [8] |
Radoslav R, Hanmidreza S, Jeffrey LS, et al. Impact of eloquent motor cortex-tissue reperfusion beyond the traditional thrombolysis in cerebral infarction (TICI) scoring after thrombectomy[J]. J Neurointerv Surg, 2020. DOI:10.1136/neurintsurg-2020-016834 |
| [9] |
Zhou XX, Zhang F, Yang YK, et al. Comparative study of basilar artery implanted with intracranial stent between beagle dogs and labrador dogs[J]. Chin J Exp Surg (中华实验外科杂志), 2017, 34: 2162-2164. |
| [10] |
Chen YX, Kong LL, Wang HG, et al. The role of pinocembrin in t-PA thrombolysis-induced hemorrhagic transformation[J]. Acta Pharm Sin (药学学报), 2019, 54: 448-453. |
| [11] |
Lee NJ, Chung SC, Jung HS, et al. Comparison of high-resolution MR imaging and digital subtraction angiography for the characterization and diagnosis of intracranial artery disease[J]. Am J Neuroradiol, 2016, 37: 2245-2250. DOI:10.3174/ajnr.A4950 |
| [12] |
Dixon Y, Digna C, Emmanuel N, et al. Cerebral hemodynaics in the elderly a transcranial doppler study in the Einstein aging study cohort[J]. J Ultras Med, 2016, 35: 1907-1914. DOI:10.7863/ultra.15.10040 |
| [13] |
Jiang L, Su HB, Zhang YD, et al. Collateral vessels on magnetic resonance angiography in endovascular-treated acute ischemic stroke patients associated with clinical outcomes[J]. Oncotarget, 2017, 8: 81529-81537. DOI:10.18632/oncotarget.21081 |
| [14] |
Liu S, Shi HB, Zhang P, et al. Dose-effective investigation of intraarterial r-Sak in canine model with acute cerebral infarctions[J]. J Intervent Radiol (介入放射学杂志), 2007, 16: 189-193. |
| [15] |
Zheng ZH, Zhu XX, Gan H, et al. Pharmacodynamics and pharmacokinetics of batroxobin in beagle dog[J]. Acta Pharm Sin (药学学报), 2013, 48: 1307-1311. |
 2021, Vol. 56
2021, Vol. 56


