2. 江苏康缘药业股份有限公司, 江苏 连云港 222001;
3. 中药制药过程新技术国家重点实验室, 江苏 连云港 222001
2. Jiangsu Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China;
3. State Key Laboratory of New-tech for Chinese Medicine Pharmaceutical Process, Lianyungang 222001, China
热毒宁注射液是一种中药复方注射液, 由栀子、金银花和青蒿3味中药精制而成, 有清热、疏风、解毒等功效[1], 临床上常用于治疗上呼吸道感染、急性支气管炎和肺炎。作为呼吸系统用药, 热毒宁注射液经雾化吸入替代注射方式治疗急性上呼吸道感染、慢性支气管炎症等疾病, 雾化吸入可有效提高药物在肺部的浓度, 起效迅速, 并能减少全身不良反应, 降低了静脉注射的致敏风险[2, 3]。临床前研究也发现, 空气压缩雾化器可有效递送热毒宁注射液到动物肺部, 发挥抗炎药效[4-7]。
目前临床药物雾化设备常采用超声和空气压缩雾化器, 但其体积较大、无内置电源需外部充电, 以及肺部给药效率低, 对非住院患者的治疗和雾化吸入培训均不利[8]。振动筛孔雾化器体积小、便于携带, 适用于非住院患者, 但振动筛孔雾化器的肺部给药效率也较低。有些辅助设备和技术, 例如可改善患者吸气同步性的定制储雾装置, 可通过改善患者吸入协同性而提高肺部递送效率, 但价格昂贵, 不易推广[9]。
储雾罐是定量吸入气雾剂(metered-dose inhaler, MDI) 使用过程中常用的辅助装置, 可使MDI与空气充分混合, 在一定程度上可提升气溶胶出雾和患者吸气同步性。筛孔雾化器加装定制的储雾罐后, 同样可显著提高装置的肺部递送效率[10]。但这种专门设计的储雾罐大大增加了患者的医疗费用, 且使用次数有限, 不易推广。本文以热毒宁注射液为对象, 考察不同雾化装置及加装常用的MDI储雾罐后能否提高雾化递送效率。
材料与方法实验仪器 实时喷雾粒度分析仪Spraytec (英国马尔文仪器有限公司); 新一代药用撞击器(next generation pharmaceutical impactor, NGI, 美国MSP公司); BRS 1100型呼吸模拟器、HCP5高容量真空泵(英国Copley Scientific有限公司); e2695高效液相色谱仪(美国Waters公司); TSI series4000实验室通用质量流量计(美国TSI有限公司)。雾化器和储雾罐见图 1, 包括PARI LC Sprint STAR型红芯压缩雾化器(A) (德国百瑞有限公司); Aerogen Solo雾化器(B)、Aerogen Ultra储雾罐(b) (德国爱尔真有限公司); Air Pro IV型雾化器(C) (深圳来福士雾化医学有限公司); NEB-001型雾化器(D) (青岛未来移动医疗科技有限公司); PARI储雾罐(a) (德国百瑞有限公司)。

|
Figure 1 Four different nebulizers and two spacers. A: Jet nebulizer; B, C, D: Mesh nebulizers; a: Metered-dose inhaler (MDI) spacer; b: Spacer matched with nebulizer B |
药材与试剂 热毒宁注射液(批号: 200320, 江苏康缘药业股份有限公司); 绿原酸对照品(批号: 110753-202018, 纯度为96.1%)、栀子苷对照品(批号: 110749-201919, 纯度为97.1%) (中国食品药品检定研究院); 乙腈-色谱级(美国Fisher公司); 磷酸-分析级(北京迈瑞达科技有限公司); 氯化钠注射液(0.9%, 四川科伦药业股份有限公司); 水为娃哈哈纯净水。
液相条件 OD-2 HYPERSIL C18色谱柱(250 mm × 4.6 mm, 5 μm); 柱温: 30 ℃; 流速: 1 mL·min-1; 流动相: 0.1%磷酸水溶液-乙腈(88∶12); 检测波长: 240 nm; 进样量: 10 μL[11]。
样品制备 精密称取绿原酸、栀子苷对照品适量, 加入50%甲醇-水溶解, 摇匀得绿原酸、栀子苷各500 μg·mL-1混合对照品溶液。精密吸取热毒宁注射液1 mL, 置于10 mL量瓶中, 加入生理盐水稀释至刻度, 摇匀后得到稀释10倍的热毒宁注射液稀释液。将绿原酸和栀子苷混合对照品溶液稀释得绿原酸和栀子苷各为100、200、500 ng·mL-1、1、2、5、10、20 μg·mL-1质量浓度的标准溶液, 按照其色谱条件进行高效液相色谱(HPLC) 测定, 以吸收峰面积对浓度进行线性回归。
气溶胶实时粒径分布的测定 除了《中华人民共和国药典》中规定的空气动力学粒径分布的测定, 气溶胶的实时粒径分布也是评价其体外吸入性能的重要指标。将流量计连接到马尔文实时喷雾粒度分析仪的人工喉管, 调节真空泵流速为15 mL·min-1, 取2 mL热毒宁注射液稀释液加入雾化器的药杯中, 将雾化器口含器咬嘴接口通过适配器直接接入人工喉管, 或将储雾罐加装在人工喉和雾化器之间, 打开软件, 矫正光路背景后启动雾化器开始测定, 待气溶胶透光率迅速上升时停止测试, 记录热毒宁注射液雾化后实时粒径随雾化时间的变化情况, 累计粒度分布百分数达到50%时对应的粒径Dx(50)也称中位粒径, 室温下重复测定3次, 结果取平均值。
空气动力学粒径分布的测定 按照《中华人民共和国药典》2020版操作, 将NGI放置在4 ℃冰箱中超过1.5 h后, 将已装好玻璃纤维滤纸的NGI按说明装配好, 连接好流量计后打开真空泵, 调节气流至15 mL·min-1, 取热毒宁注射液稀释液2 mL于雾化器药杯中, 将雾化器口含器咬嘴接口直接连接L型连接管, 或插入储雾罐连接环或接口, 通过适配器将储雾罐连接到L型连接管, 打开装置, 开始计时, 在预计时间内完成雾化, 关闭雾化器和真空泵。以10 mL 50%甲醇-水作为洗涤液, 洗涤NGI各级和雾化器中残留的热毒宁活性物质, 采用HPLC测定其中绿原酸和栀子苷的含量。将计算结果导入到CITDAS数据分析系统, 计算可得细微颗粒分数(fine particle fraction, FPF)、质量中值粒径(MMAD), 几何标准偏差(geometric standard deviation, GSD) 用以表征热毒宁注射液的空气动力学粒径分布。室温下重复测定3次, 结果取平均值。
递送速率和递送效率的测定 取2 mL热毒宁注射液稀释液于雾化器的药杯中, 将雾化器口含器咬嘴插口与呼吸模拟器的滤膜装置连接, 或将储雾罐加装在雾化器与滤膜装置之间, 将呼吸模拟器设定为成人模式: 潮气量500 mL、呼吸频率每分钟15循环、呼吸波形为正弦型、呼吸比为1∶1。加装滤膜后开启呼吸模拟器, 在雾化时间为1 min时停止雾化, 暂停呼吸模拟器, 取出滤膜, 置于装有10 mL 50%甲醇-水的离心管中, 涡旋30 s。在滤膜装置中再放入一张新的滤膜, 启动雾化器, 直至雾化器无气雾喷出, 雾化结束, 关闭雾化器, 5~10 s后停止呼吸模拟器, 使呼吸模拟器中的气体排尽。取出第2张滤膜, 以50 mL 50%甲醇-水洗涤滤膜上的热毒宁活性物质, 雾化器中残留的热毒宁药物以50 mL 50%甲醇-水洗涤, 摇匀后涡旋。采用HPLC测定其中的绿原酸和栀子苷含量, 室温下重复测定3次, 结果取平均值。第1张滤膜上吸附的药物含量与雾化时间之比即为递送速率, 第1张滤膜和第2张滤膜收集药物含量之和即为递送总量, 递送总量与雾化的2 mL热毒宁注射液稀释液中药物含量之比为递送效率。
统计学分析 实验数据采用平均值±标准差表示, 以GraphPad Prism 8软件进行独立样本t检验, P < 0.05表示差异有统计学意义。
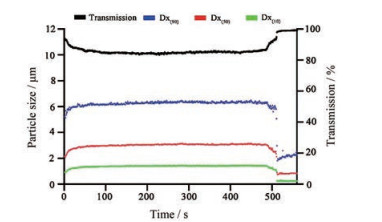
结果 1 热毒宁注射液雾化气溶胶实时粒径分布喷雾粒度分析仪用于实时测量雾化气溶胶粒径和透光率等参数, 透光率越高, 气溶胶浓度越低。Dx(10)、Dx(50)和Dx(90)分别为样品的累计粒度分布数达到10%、50%和90%时所对应的粒径。以雾化器D雾化热毒宁注射液, 在开始阶段, 气溶胶浓度逐渐升高, 透光率降低, Dx(10)、Dx(50)和Dx(90)升高; 平稳出雾后透光率和粒径值趋于稳定。雾化结束时, 雾滴减少, 透光率升高, 粒径降低(图 2)。中位粒径Dx(50)是评价气溶胶粒径分布最常用的参数, 未加储雾罐前4种雾化器的中位粒径平均值为2.98~3.74 μm, 使用储雾罐后变为2.05~5.22 μm, 储雾罐的应用使不同雾化器产生气溶胶的粒径发生差异。常规空气压缩雾化器A在使用储雾罐后中位粒径减小, 3种振动筛孔雾化器在使用储雾罐后, B和C的中位粒径增大, D的中位粒径减小, 且其中位粒径在使用储雾罐前后都小于B和C, 雾化器D产生的气溶胶粒子最小, 其雾化性能优于其他两种振动筛孔雾化器(表 1)。
|
Figure 2 Dynamic changes in droplet size and concentration over time following the nebulization of Re-Du-Ning injection via the mesh nebulizer D as measured with a Spraytec laser diffractometer. Dx(90), Dx(50) and Dx(10) are the corresponding particle sizes when the cumulative particle size distribution percentage of the sample reaches 90%, 50% and 10%, respectively |
| Table 1 The droplet size distribution of the nebulizer generated aerosols after nebulization of Re-Du-Ning injection via different nebulizers and spacers. n = 3, x±s. *P < 0.05, **P < 0.01 vs group without spacer |
微细粒子分数FPF为空气动力学粒径小于5 μm可沉积在肺部的粒子占总雾化输出粒子的百分比, 反映了气溶胶的可吸入粒子分数。质量平均空气动力学粒径MMAD反映了气溶胶的整体粒径水平, 影响其在呼吸道的沉积部位。FPF值越高, MMAD值越小, 气溶胶的可吸入粒子总量越多[12, 13]。
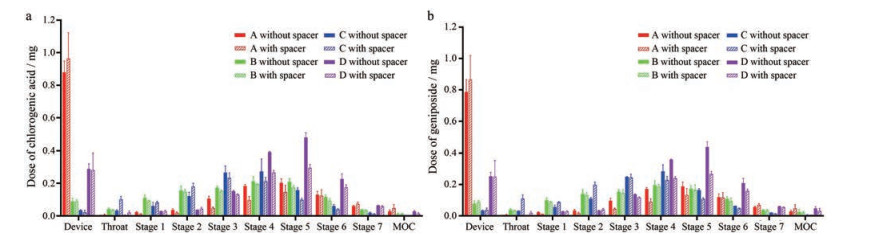
以绿原酸或栀子苷为指标成分分别测定的空气动力学特性没有显著差异, 证明二者的肺部分布行为一致(图 3)。当不加装储雾罐时, 雾化器A产生的热毒宁气溶胶MMAD为3.06~3.07 μm, 与文献[4, 5]报道的3.08 μm一致; 其他3种振动筛孔雾化器的雾化气溶胶MMAD在3.03~5.13 μm之间(表 2)。
|
Figure 3 Aerodynamic particle size distribution of nebulizer generated aerosols of Re-Du-Ning injection assessed by next generation pharmaceutical impactor (NGI) testing based on the determination of chlorogenic acid (a) and geniposide (b). n = 3, x±s. MOC: Micro-orifice collector |
| Table 2 NGI results of four different nebulizers. n = 3, x±s. FPF: Fine particle fraction; MMAD: Mass median aerodynamic diameter; GSD: Geometric standard deviation. *P < 0.05, **P < 0.01 vs group without spacer |
使用储雾罐对不同的雾化器产生的热毒宁雾化气溶胶空气动力学粒径分布产生的影响不尽相同。常规空气压缩雾化器A在使用储雾罐后FPF升高, MMAD减小, 有利于热毒宁粒子在肺部的沉积。振动筛孔雾化器B和D加罐与否对其MMAD影响不大(P > 0.05), 而C使用储雾罐后FPF降低, MMAD增加, 可吸入药物的总量减小, 不利于热毒宁粒子在肺内的沉积。
3 热毒宁注射液的递送速率和递送效率经HPLC测定, 2 mL热毒宁注射液稀释液中含绿原酸1.69 ± 0.14 mg、栀子苷1.58 ± 0.17 mg。以绿原酸和栀子苷为指标成分测定的热毒宁注射液的递送速率和递送效率如表 3。在4种不同的雾化器中, 相比于未加储雾罐, 常规的空气压缩雾化器A在加装储雾罐后, 递送速率和递送效率均有显著下降(P < 0.01), 加罐前后的雾化残留率也高于其他3种振动筛孔雾化器。相反, 加装储雾罐可将3种振动筛孔雾化器的递送效率从24%~35%增加到37%~68%。
| Table 3 Determination results of delivery rate and delivery efficiency of Re-Du-Ning injection. n = 3, x±s. *P < 0.05, **P < 0.01 vs group without spacer |
B是一个配置专门储雾辅助装置的雾化器。加装其自带的储雾罐后, B的递送速率和递送总量均有大幅增加(P < 0.01), 其中递送速率提高了约1倍, 而递送总量提高了约80%, 这一结果和文献[10]报道的数据基本一致。加装市售MDI储雾罐均可提高C和D两种雾化器的递送效率, 其中C的递送效率从28%增加到约35%, 而D则可从34%~35%提高到66%~68%。
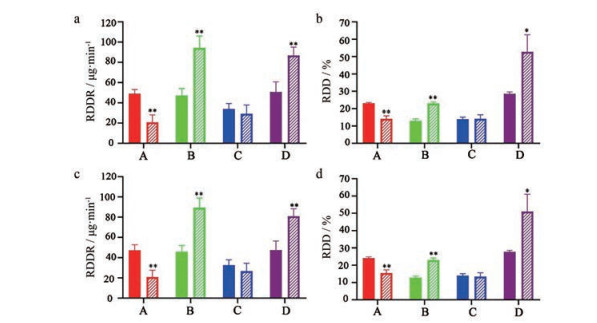
4 热毒宁注射液的可吸入递送速率和可吸入递送效率从递送药物到肺部效率的角度, 可吸入递送速率(respirable drug delivery rate, RDDR) 和可吸入递送效率(percentage of respirable delivered dose, RDD%) 是评价雾化器性能的两个重要指标。RDDR可通过可吸入粒子分数FPF×递送速率计算, 而RDD%可通过FPF×递送效率计算。空气压缩雾化器A的RDDR和RDD%分别为50 μg·min-1和23% (以绿原酸计), 而3种筛孔雾化器的RDDR和RDD%范围分别约为30~50 μg·min-1和12.9%~28.6% (以绿原酸计)。与空气压缩雾化器A相比, 筛孔雾化器并未能显著提高雾化性能(图 4)。
|
Figure 4 Results of respirable drug delivery rate (RDDR) and percentage of respirable delivered dose (RDD%). a: RDDR calculated by chlorogenic acid; b: RDD% calculated by chlorogenic acid; c: RDDR calculated by geniposide; d: RDD% calculated by geniposide. The bars filled with pure colors are groups without spacers while the bars filled with forward slash represent groups with spacers. n = 3, x±s. *P < 0.05, **P < 0.01 vs group without spacer |
但加装储物罐后, 常规空气压缩雾化器递送效率和可吸入递送效率大幅下降, 储雾罐的使用不利于常规空气压缩雾化器递送效率的提高, 原因可能是空气压缩气体流速过快, 导致雾滴沉积在储雾罐壁。B在设计上本身携带了储雾罐, 前期研究发现B的储雾罐可显著提高装置的递送效率[10]。本文同样发现B在加装该雾化器配套的定制储雾罐后MMAD和FPF变化不大, 递送效率和可吸入递送效率显著提高(P < 0.01)。C是一种雾化液滴分布较大的雾化器, 在加装储雾罐后MMAD增大, 虽然递送效率有小幅度的提高, 但可吸入递送效率并未有明显变化(P > 0.05)。D在使用储雾罐后, 其可吸入递送效率是未加罐的两倍, 超过了50%。与临床使用的空气压缩雾化器相比(以未加储雾罐的A为例), D加装储雾罐后, 其RDDR (85 μg·min-1) 和RDD% (52.7%以绿原酸计) 均有显著提升(P < 0.05), 可显著降低患者用药时间, 并适用于非住院患者。
讨论《中华人民共和国药典》2020版对雾化吸入溶液的体外吸入性能评价包括雾化液滴分布、空气动力学特性、递送速率和递送总量等参数。空气动力学粒径分布和实时液滴粒径分布的测定除可控制吸入溶液质量外, 还可预测药物粒子在肺部的沉积情况。递送速率和递送总量通过呼吸模拟器模拟与人体相仿的吸入和呼出模式, 可反映雾化过程中吸入药物的速度和总量[14]。本研究采用马尔文实时喷雾粒度分析仪、新一代药用撞击器和呼吸模拟器首次测定了振动筛孔雾化器递送中药复方的雾化性能, 并评价了加装市售MDI储雾罐对雾化气溶胶的影响。结果表明, 加装储雾罐对热毒宁雾化气溶胶的粒径分布和可吸入药物分数有一定影响, 但总体上可显著提升筛孔雾化器的递送效率。
MDI储雾罐作为一种市售辅助装置, 与较昂贵的雾化辅助装置相比, 具有价格优势; 储雾罐在临床上适用于无法自主呼吸的婴幼儿、老人以及手口配合不便的患者, 提高药物递送效率; 通过与振动筛孔雾化器联合使用, 不仅可方便携带, 还可实现雾化吸入的快速、高效递送, 在维持肺部药效的同时, 提高患者依从性。雾化吸入疗法为治疗呼吸系统疾病中药注射液的替代开辟了一条新的给药途径, 其可直接递送药物到达靶部位而提高药效、并减少静脉注射引起的不良反应。随着雾化技术的不断发展、雾化器和辅助装置的创新和推广, 替代中药注射液的雾化吸入给药将会更加高效和简便快捷, 具有广阔的发展前景和巨大的应用市场。
作者贡献: 廖永红负责论文选题、指导与审阅; 李超逸负责实验方案设计与实施、结果分析及文章撰写; 杨飞飞负责论文指导与修改; 刘春雨负责部分实验数据采集及实验监督。
利益冲突: 所有作者声明本文无任何利益冲突。
| [1] |
Ge W, Li HB, Yu Y, et al. Research on chemical constituents from Reduning injection (IV)[J]. Chin Tradit Herb Drugs (中草药), 2017, 48: 1597-1602. |
| [2] |
Wan Z, Xu ZF, Lin JM, et al. Investigation on clinical effects of the Reduning ultrasonic atomizing inhalation therapy on treating acute exacerbation of chronic bronchitis[J]. J Pract Tradit Chin Med (实用中医药杂志), 2014, 30: 298-299. |
| [3] |
Wang YD, Lao CF, Pan YF, et al. Clinical research on the treatment of fever caused by acute upper respiratory tract infection by ultrasonic atomizing inhalation of Reduning[J]. Hubei J Tradit Chin Med (湖北中医杂志), 2011, 33: 10-11. |
| [4] |
Luo G, Tao YH, Li C, et al. Correlation analysis of inhalation performance of Reduning inhalation solution[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2018, 24: 1-7. |
| [5] |
Zhang Y, Cheng BCY, Li C, et al. Characterization and comparison of Re-Du-Ning aerosol particles generated by different jet nebulizers[J]. RSC Adv, 2019, 9: 30292-30301. DOI:10.1039/C9RA06177K |
| [6] |
Zhang Y, Cheng BCY, Xie R, et al. Re-Du-Ning inhalation solution exerts suppressive effect on the secretion of inflammatory mediators via inhibiting IKKα/β/IκBα/NF-κB, MAPKs/AP-1, and TBK1/IRF3 signaling pathways in lipopolysaccharide stimulated RAW 264.7 macrophages[J]. RSC Adv, 2019, 9: 8912-8925. |
| [7] |
Sun J, Zhao RH, Shi YJ, et al. Study on pharmacological effects of Reduning inhalation solution on viral pneumonia in mice infected by influenza A/PR/8/H1N1[J]. Chin J Pharmacovig (中国药物警戒), 2021. https://kns.cnki.net/kcms/detail/11.5219.R.20210521.1659.031.html.
|
| [8] |
Tang Y, Zhu JB, Chen XJ, et al. A novel pulmonary delivery system — dry powder inhalers[J]. Acta Pharm Sin (药学学报), 2009, 44: 571-574. |
| [9] |
Longest W, Spence B, Hindle M. Devices for improved delivery of nebulized pharmaceutical aerosols to the lungs[J]. J Aerosol Med Pulm Drug Deliv, 2019, 32: 317-339. DOI:10.1089/jamp.2018.1508 |
| [10] |
Sarhan RM, Elberry AA, Abdelwahab NS, et al. Effect of a nebulizer holding chamber on aerosol delivery[J]. Respir Care, 2018, 63: 1125-1131. DOI:10.4187/respcare.06061 |
| [11] |
Liang JC, Huang YK, Cai Z, et al. Determination of chlorogenic acid and geniposide in Reduning injection by HPLC[J]. Chin J New Drugs (中国新药杂志), 2008, 17: 1522-1524. |
| [12] |
Li M, Wei NY, Zheng J, et al. In vitro nebulization characteristics of budesonide suspension for inhalation[J]. Acta Pharm Sin (药学学报), 2021. DOI:10.16438/j.0513-4870.2021-0309 |
| [13] |
Liang ZL, Wang XH, Ni R, et al. Preparation of budesonide sustained-release dry powder for inhalation and influence of lactose content[J]. Acta Pharm Sin (药学学报), 2015, 50: 1180-1185. |
| [14] |
Zhou Y, Wei NY, Lin L, et al. Compare the delivery rate and delivered amount of ambroxol hydrochloride nebules inhalation solution of two types of nebulizer by breathing simulator[J]. Chin J New Drugs (中国新药杂志), 2018, 27: 290-294. |
 2021, Vol. 56
2021, Vol. 56


