聚合物研究是头孢菌素类抗生素药品质量研究的重要内容[1], 对聚合物的精确测量和结构分析是聚合物研究的难点。目前, 已有聚合物结构研究报道的头孢菌素品种有头孢噻肟[2-4]、头孢拉定[5]、头孢他啶[6]、头孢地尼[7]、头孢克肟[8], 其中头孢噻肟二聚体结构已被《美国药典》收载并采用有关物质方法作为已知杂质进行限度控制。上述有聚合物结构报道的头孢菌素的结构有共同特点, 它们的7位侧链均含有活性基团氨基, 该基团是形成聚合物杂质的重要基团。此外, 7位侧链不含氨基的头孢菌素品种也有很多, 推测该类头孢菌素中聚合物含量和种类要少于上述品种, 而这类头孢菌素中聚合物的结构情况目前还未有报道, 因此有必要选择1个品种对该类头孢菌素中的聚合物结构和质控方法进行深入研究。本文采用柱切换液相色谱-高分辨质谱联用法(LC-MS/MS) 对聚合物的结构和位置进行分析。
头孢唑林钠为第一代头孢菌素, 主要用于治疗革兰阳性菌感染, 在临床上具有广泛应用。目前, 除《中国药典》 (2015年版) (简称ChP 2015) 外, 其他现行官方药典均未对头孢唑林钠中的聚合物杂质进行控制。ChP 2015采用葡聚糖凝胶色谱法(简称G10方法) 控制头孢唑林中的聚合物。G10凝胶色谱法曾是控制抗生素类药品中聚合物杂质的普遍方法, 但该法在聚合物检测的专属性和定量的准确性上暴露出问题[1], 后来逐渐被高效凝胶色谱法(固定相是TSK G2000SW, 简称TSK方法) 和反相高效液相色谱法(HPLC) 所取代。有文献[9, 10]报道了采用G10法和TSK法控制头孢唑林中的聚合物。因此, 也有必要针对头孢唑林钠中的聚合物情况选择最合理的聚合物质控方法。
材料与方法仪器 高效液相色谱仪: 岛津LC-20A型液相色谱系统(配二极管阵列检测器); 安捷伦1260 Infinity型液相色谱系统(配二极管阵列检测器); 戴安P680A二维液相色谱系统。柱切换-高分辨质谱系统由Thermo HPLC色谱系统(包括U3000四元低压梯度泵、自动进样器、柱温箱、切换阀和四波长检测器) 和Q Exactive Focus型MS/MS质谱仪(美国Thermo公司) 组成, 工作站为Xcalibur 1.0版。
样品 头孢唑林钠原料及制剂各1批, 由中国食品药品检定研究院提供。
对照品 头孢唑林对照品(批号: 130421-201204, 含量: 99.0%) 和头孢唑林杂质a (批号: 130708-201903W, 仅供系统适用性实验使用)、杂质f (批号: 130709-201401W, 含量: 99.4%)、杂质g (批号: 130710-201401W, 含量: 97.7%)、杂质h (批号: 130711-201903W, 仅供系统适用性实验使用)、杂质i (批号: 130712-201502W, 含量: 96.2%)、杂质j (批号: 130713-201502W, 含量: 87.7%)、杂质k (批号: 130714-201401W, 含量: 97.9%)、杂质m (批号: 130716-201903W, 仅供系统适用性实验使用)、杂质n (批号: 130714-201903W, 仅供系统适用性实验使用)对照品由中国食品药品检定研究院提供。
HPLC方法 色谱柱为资生堂Capcell Pak MG II (250 mm×4.6 mm, 5 μm), 流动相A为磷酸盐缓冲液(6.8 mg·mL-1的磷酸二氢钾溶液, 用10 mol·L-1的氢氧化钠溶液调节pH值至6.8), 流动相B为乙腈-磷酸盐溶液(6.8 mg·mL-1的磷酸二氢钾溶液) (1∶1), 流速为1.5 mL·min-1, 检测波长为254 nm, 柱温为30 ℃, 进样量为20 μL。梯度洗脱程序: 在0、7、15、35、45、50、55和65 min时, 流动相A的比例分别是98%、98%、85%、80%、50%、50%、98%和98%。
TSK方法 色谱柱为TSK gel G2000SWxl (日本TOSOH, 7.8 mm×300 mm, 5 μm), 流动相为磷酸盐缓冲液(pH 7.0) [0.005 mol·L-1磷酸氢二钠溶液-0.005 mol·L-1磷酸二氢钠溶液(61∶39)]-乙腈(95∶5), 流速为0.7 mL·min-1, 检测波长为254 nm, 柱温为30 ℃。
G10方法 色谱柱为Sephadex-G10凝胶色谱柱(大连依利特, 10.0 mm×300 mm), 流动相为磷酸盐缓冲液(pH 7.0) [0.1 mol·L-1磷酸氢二钠溶液-0.1 mol·L-1磷酸二氢钠溶液(61∶39)], 流速为1.5 mL·min-1, 检测波长为254 nm, 柱温为30 ℃。
二维液相色谱方法 用于将TSK方法或G10方法中的各色谱峰切入至HPLC色谱系统中。一维色谱条件: 同TSK方法或G10方法; 二维色谱条件: 同HPLC方法。定量环大小为200 μL。二维色谱工作流程: 通过十孔切换阀将第一维和第二维色谱系统进行联合, 用于目标化合物的二维色谱分析, 具体步骤如下[5]: 第一步, 首先将切换阀设为A位置, 采用右泵, 以TSK凝胶色谱系统(第一维色谱系统) 对供试品进行分离, 同时采用第二维色谱系统对HPLC色谱柱进行预平衡; 第二步, 当采用TSK凝胶色谱系统分离的目标杂质洗脱出峰后, 将切换阀设为B位置; 第三步, 采用第二维色谱系统将TSK柱后定量环中的目标杂质洗脱至第二根色谱柱中, 并采用第二维色谱系统进行分离分析。
柱切换液相色谱-高分辨质谱联用方法 液相条件: 一维液相方法同HPLC方法; 二维液相方法: 用于对目标杂质进行脱盐处理以及进行质谱分析。定量环大小为500 μL。流动相A为水-甲酸(100∶0.5), 流动相B为乙腈-甲酸(100∶0.5), 流速为0.7 mL·min-1, 柱温为30 ℃, 色谱柱为Zorbax SB-C18 (Agilent, 150 mm×4.6 mm, 5 μm), 梯度洗脱程序: 在0、tR、tR+5.0、tR+20.0、tR+25.0 min时, 流动相A的比例分别是100%、100%、100%、0、0, tR为待切换色谱峰在第一维色谱系统中的分析时间。质谱条件: 扫描电压(+) 3 kV, 毛细管温度(+) 350.0 ℃, 鞘气(+) 35 L·h-1, 辅助气(+) 10.00 L·h-1, 最大喷雾电流(+) 100.00, 探针加热器温度(+) 350.00 ℃, S-棱镜RF水平50.00, 离子源为HESI; 一级质谱方法: 正离子模式, 分辨率70 000, 扫描范围m/z 150~1 500; 二级质谱方法: 分辨率17 500, 分离窗口3.0 m/z, (N)CE 15 V。
溶液配制
供试品溶液 取本品适量, 加HPLC方法流动相A溶解并稀释制成每1 mL中含2.5 mg的溶液, 作为供试品溶液。
对照溶液 精密量取供试品溶液1 mL, 置100 mL量瓶中, 用HPLC方法流动相A稀释至刻度, 作为对照溶液。
系统适用性溶液 取杂质a、f、g、h、i、j、k、m、n对照品及头孢唑林对照品适量, 加HPLC方法流动相A溶解并稀释制成每1 mL中含各成分约为0.1 mg的混合溶液, 作为系统适用性溶液。
方法学验证
精密度 取系统适用性溶液, 连续进样6针, 计算主峰峰面积, 以相对标准偏差RSD%表示。
检测限与定量限 精密量取供试品溶液, 用HPLC方法流动相A进行稀释, 得到不同浓度的系列溶液, 以头孢唑林对照品为外标, 得到方法的最低定量限(LOQ) 和最低检测限(LOD)。
耐用性 考察在不同柱温、流速、流动相pH值和不同色谱柱条件下, 系统适用性溶液和供试品溶液中聚合物杂质的分离情况。
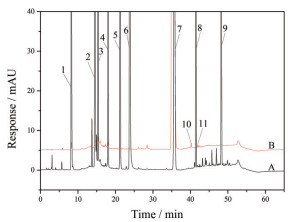
结果 1 HPLC法的分析结果采用HPLC色谱系统分析头孢唑林钠, 色谱图见图 1。头孢唑林各杂质的结构见图 2。
|
Figure 1 Chromatograms of cefazolin system suitability solution (A) and product (B). 1: Impurity f; 2: Impurity g; 3: Impurity h; 4: Impurity i; 5: Impurity j; 6: Impurity k; 7: Cefazolin; 8: Impurity m; 9: Impurity n; 10: Dimer 1; 11: Dimer 2 |

|
Figure 2 Chemical structures of cefazolin impurities. 1: Impurity a; 2: Impurity f; 3: Impurity g; 4: Impurity h; 5: Impurity i; 6: Impurity j; 7: Impurity k; 8: Impurity m; 9: Impurity n; 10: Dimer 1 |
由于HPLC系统含有不挥发的磷酸盐, 因此采用柱切换LC-MS/MS法分析主峰后的各色谱峰, 最终确认了图 1中的色谱峰10、11为聚合物, 其相对保留时间分别约为1.18、1.23, 命名为聚合物1、2; 其他色谱峰均不是聚合物。
根据聚合物的质谱碎裂信息, 对其可能结构和质谱裂解途径进行推测。聚合物1的质谱图见图 3A, 一级质谱图中存在m/z 795、m/z 833的准分子离子峰, 分别为[M+H]+和[M+K]+峰, 推测其相对分子质量为794; 根据相对分子质量, 为两分子头孢唑林减去3位侧链片段后的结构。二级质谱图中存在m/z 455的头孢唑林碎片和m/z 473的头孢唑林开环物碎片, 同时又具有头孢唑林的特征碎片(m/z 323、m/z 295、m/z 156), 进一步确定是头孢唑林二聚体, 推测聚合物1的结构可能有2个, 2个可能结构及质谱裂解途径见图 4。但从形成机制的角度看, 图 4A中的二聚体(成酯) 的可能性较小, 因此更倾向于认为是图 4B中的结构。

|
Figure 3 Mass spectrograms of the two cefazolin dimers. A: Dimer 1; B: Dimer 2 |

|
Figure 4 Two possible fragmentation pathways (A and B) of cefazolin dimer 1. a, b, c, d and e in each fragmentation pathway represent different fragmentation reactions |
聚合物2的质谱图见图 3B, 一级质谱图中存在m/z 795、m/z 833的准分子离子峰, 分别为[M+H]+和[M+K]+峰, 推测其相对分子质量为794; 根据相对分子质量, 可能是聚合物1的异构体, 聚合物2与聚合物1的二级质谱图略有不同, 聚合物2的二级质谱图不含有m/z 455的头孢唑林碎片, 仅存在特征性m/z 473的头孢唑林开环物碎片和头孢唑林的典型碎片峰m/z 323、m/z 295和m/z 156, 说明聚合物2也含有头孢唑林开环物碎片。此外, 从质谱图可知, 聚合物1加氢峰的精确m/z为795.090 63, 而聚合物2加氢峰的精确m/z为795.035 10, 聚合物1高分辨质谱结果和推测结构式的精确相对分子质量一致, 说明和聚合物1相比, 聚合物2中部分结构的元素组成发生改变。此外, 聚合物1和2的紫外光谱图显示, 聚合物1的紫外光谱图和头孢唑林相似, 而聚合物2的紫外光谱图和头孢唑林稍有不同, 进一步说明聚合物2的母核结构可能发生改变。但仅根据质谱结果, 很难得出确切的结构。
3 分析方法的验证 3.1 专属性采用中国药典有关物质方法中的系统适用性溶液对专属性进行考察。由图 1可见, 聚合物杂质峰与相邻色谱峰分离良好, 各聚合物杂质峰经质谱分析已经证明为所对应杂质, 同时聚合物杂质与各已知杂质均分离良好, 因此本法可有效分析头孢唑林聚合物, 专属性良好。
3.2 精密度方法的日内精密度为0.2%, 表明本实验方法的精密度良好。
3.3 检测限与定量限以头孢唑林钠计, 得到聚合物1和2的最低检测限分别为1×10-3 μg和3×10-3 μg; 聚合物1和2的最低定量限分别为3×10-3 μg和1×10-2 μg, 均满足实验要求。
3.4 耐用性考察在不同色谱条件下聚合物杂质的分离情况。流动相pH分别为6.7、6.8、6.9时, 均可有效分离头孢唑林聚合物; 柱温为28~30 ℃时, 可有效分离头孢唑林聚合物, 但柱温是32 ℃时, 聚合物2和其后相邻色谱峰分离变差; 流速为1.4~1.5 mL·min-1时, 可有效分离头孢唑林聚合物, 但流速为1.6 mL·min-1时, 聚合物2和其后相邻色谱峰共流出; 色谱柱分别为Capcell Pak MG II、YMC Pack Pro C18、Phenomenex Gemini C18、Ardesil Roband ODS (规格均为250 mm×4.6 mm, 5 μm) 时, 均可有效分离聚合物1, 但仅色谱柱Capcell Pak MG Ⅱ对聚合物2分离较好, 在其他色谱柱上聚合物2和其后相邻色谱峰共流出。由耐用性实验可知, 聚合物2的分离对柱温、流速、色谱柱类型较为敏感, 在实验过程中应注意控制这些参数。
上述方法学验证结果表明, 本研究采用的头孢唑林聚合物分析方法专属性良好、灵敏度高、耐用性良好, 适合作为头孢唑林钠原料和制剂中的聚合物分析方法。
4 实际样品测定采用主成分自身对照法, 以供试品溶液1%的自身稀释溶液作为对照溶液, 对1批头孢唑林制剂中的聚合物杂质进行测定。聚合物1和2的含量分别是0.06%和0.01%。由于聚合物2的含量较低, 建议根据更多其他批次产品中聚合物的检测结果, 以聚合物1作为指针性杂质, 对聚合物进行控制, 并设定合理的限度。
讨论目前已经有聚合物结构报道的头孢菌素的7位侧链均含有氨基。氨基作为活性基团, 可进攻另一分子3位侧链而形成二聚体[4-8]。本论文研究的头孢唑林7位侧链没有氨基, 其聚合物含量和种类均比7位侧链含有氨基的头孢类抗生素少。头孢唑林聚合物主要形成途径是2位侧链羧基进攻另一分子头孢唑林β-内酰胺环。
选择适宜的聚合物质控方法是聚合物研究的重点内容。本研究还对头孢唑林聚合物检测的G10方法和TSK方法进行了考察, 采用二维液相色谱系统, 将G10和TSK方法中的各色谱峰切入到HPLC色谱系统中, 结果显示, G10方法和TSK方法中的各色谱峰均可在HPLC系统中检测到, 而且在HPLC系统中均洗脱出不止1个色谱峰, 说明HPLC系统的分离效果和检测专属性优于G10法和TSK方法。
作者贡献: 张夏完成实验和论文撰写; 李进帮助解决实验疑难问题; 姚尚辰和尹利辉协助完成; 王晨和刘颖本文提供实验材料; 通讯作者许明哲为本文修改和指导; 通讯作者胡昌勤提出实验思路与理念并进行指导。
利益冲突: 无任何利益冲突。
| [1] |
Hu CQ. Impurity control strategy of β-lactam antibiotics polymer: the formation and development[J]. Chin J New Drug (中国新药杂志), 2020, 29: 1231-1244. |
| [2] |
Zhang Q, Yamamoto MB, Aki HM. Study on polymerization characteristics of cefotaxime[J]. Chin J Antibiot (中国抗生素杂志), 1992, 17: 428-434. |
| [3] |
Zhang Q, Yamamoto MB, Aki HM, et al. Polymerization of cephalosporins in aqueous solution[J]. Acta Pharm Sin (药学学报), 1996, 31: 306-312. |
| [4] |
Li J, Yao SC, Yin LH, et al. Analysis of polymer impurities in cefotaxime sodium raw materials[J]. Chin J Antibiot (中国抗生素杂志), 2020, 45: 883-892. |
| [5] |
Li J, Zhang PP, Yao SC, et al. Analysis of polymer impurities in cefradine raw materials and preparations[J]. Chin J Antibiot (中国抗生素杂志), 2019, 44: 362-369. |
| [6] |
Li J, Yao SC, Yin LH, et al. Analysis of polymer impurities in ceftazidime raw materials and preparations[J]. Acta Pharm Sin (药学学报), 2020, 55: 1889-1896. |
| [7] |
Li J, Yao SC, Yin LH, et al. Analysis of polymer impurities in cefdinir raw materials and preparations[J]. Chin J Antibiot (中国抗生素杂志), 2020, 45: 1005-1016. |
| [8] |
Li J, Yao SC, Yin LH, et al. Analysis of polymer impurities in cefixime raw materials and preparations[J]. Acta Pharm Sin (药学学报), 2020, 55: 2442-2448. |
| [9] |
Azezi M, Ma X. Determination of the polymer in cefazolin sodium by HPLC[J]. Chin J Antibiot (中国抗生素杂志), 2003, 28: 397-398, 437. |
| [10] |
Chen X. Determination of the polymer and related substances in cefazolin sodium for injection by TSKgel G2500PWXL column[J]. Strait Pharm J (海峡药学), 2010, 22: 39-41. |
 2021, Vol. 56
2021, Vol. 56


