2. 军事科学院军事医学研究院毒物药物研究所, 北京 100850;
3. 中国人民解放军 73101部队, 江苏 徐州 221000
2. China Institute of Pharmacology and Toxicology, Academy of Military Medical Sciences, Academy of Military Sciences, Beijing 100850, China;
3. 73101 Unit People's Liberation Army of China, Xuzhou 221000, China
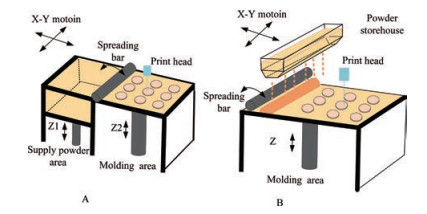
3D打印技术(3D printing technology) 是在20世纪80年代兴起的新型制造技术, 也被规范称为增材制造技术。3D打印的成型机制主要包括黏结剂喷射型、熔融丝沉积型和立体光固化成型等。近些年来主要应用于建筑工程、航天航空和生物医学等领域, 在药物制剂领域起步较晚[1]。2015年美国食品药品监督管理局(Food and Drug Administration, FDA) 批准上市了第一款3D打印药物左乙拉西坦速溶片上市, 用于治疗成人及儿童的急性癫痫发作, 该药物依靠自身疏松多孔的结构特点可在遇水几秒内迅速崩散[2-5], 于此正式拉开了3D打印在药物制剂领域研究的序幕。该上市药物采用了黏结剂喷射型3D打印成型机制。打印过程如图 1所示: 铺粉辊在粉床上铺设一层粉体, 打印头按照控制系统提供的模型切片信息在预定区域喷射黏结剂, 分层制造、层层叠加。国内黏结剂喷射型3D打印机主要分为下供粉式(图 1A) 和上供粉式(图 1B) 两种类型。上供粉式3D打印机在粉床后上方有一储粉仓, 铺粉时粉仓开闸粉料从粉仓落下, 铺粉辊将落下的粉料均匀铺设在粉床上, 通过调整粉仓开闸时间控制供粉量; 下供粉式3D打印机则在同一平面内分有两个区域, 供粉区和成型区。铺粉过程中, 供粉区平台上升一定高度, 铺粉辊将粉料铺送至成型区完成一次铺粉。通过调节供粉区Z轴上升的高度来调节供粉量。本研究中3D打印主要有两种黏结成型机制: ①处方中的粉末颗粒溶解于打印液, 在后续干燥过程中液体挥发, 粉末颗粒重新固化而连接成型; ②处方粉末含有固体黏合剂聚维酮, 可在吸收打印液后受激化将其周围的粉末颗粒黏结一起, 增加干燥后片剂的机械强度[6]。3D打印相比于传统制剂方式更能灵活可控, 可根据用药人群的精准需求实现个性化给药[7-10]。
|
Figure 1 Two types of drop-on-powder 3D printers. A: Lower feed powder; B: Upper feed powder |
氯氮平系二苯二氮杂卓类抗精神分裂药, 对精神病阳性及阴性症状均有较好的治疗效果, 适用于急性与慢性精神分裂症的各个亚型。其药理作用为对脑内5-羟色胺(5-HT2A) 受体和多巴胺(DA1) 受体有较强的阻滞作用而起到镇静催眠作用。并可用于一些传统抗精神病药治疗无效或疗效不好的患者[11], 是公认治疗该疾病的最佳药物。氯氮平浓度剂量比变异系数大[12, 13]、治疗窗窄和个体药代动力学差异大[14], 可借助3D打印的巨大优势, 实现个性化的药物剂量以满足不同年龄阶段及不同病况的患者需求[15]。本研究旨在利用全因子实验设计(design of experiment, DoE) 建立黏结剂喷射型3D打印的关键工艺参数设计空间, 实现打印机运行参数与药物处方的高度匹配, 发挥3D打印在个性化医疗中的显著优势。
材料与方法仪器与试剂 3D打印机(北京城市学院3D打印研究院, 型号: 3DHS); 电子分析天平(梅特勒, 型号: ME204); 鼓风干燥箱(上海精宏实验设备有限公司, 型号: DHG-9053A); 料斗混合机(中国浙江迦南科技股份有限公司, 型号: HSD); 硬度脆碎度检测仪(上海黄海药检, 型号: CJY-2C); 智能崩解仪(天津市鑫洲科技有限公司, 型号: ZB-ID); 氯氮平(武汉世吉药业有限公司, 批号: clo-20181220-06-A); 甘露醇50C (Roquette Freres, 批号: E983D); 乳糖140 (德国美剂乐集团, 批号: L101802218); 微晶纤维素PH101 (Asahi kasei公司, 批号: 1863); 聚维酮K30 (BSAF公司, 批号: G91897PT0); 草莓香精(芜湖市凯瑞香精有限公司, 批号: 20190411); 胶态二氧化硅(Evonik Degussa GmbH公司, 批号: 157062916); 无水乙醇(国药集团化学试剂有限公司, 批号: 20030498); 甘油(南昌白云药业有限公司, 批号: 20180108); 蒸馏水(屈臣氏公司)。
打印片剂的制备 粉体处方组成包括主药氯氮平, 填充剂甘露醇、乳糖和微晶纤维素, 矫味剂草莓香精, 助流剂胶态二氧化硅。原料药与辅料分别过120目筛, 并按处方比例用料斗混合机混匀; 液体处方组成包括基础溶剂: 50% (v/v) 乙醇溶液、增塑剂: 4% (m/v) 甘油、黏合剂: 0.3% (m/v) 聚维酮。打印步骤如图 2所示: ①利用计算机辅助软件(computer aided drafting, CAD) 建立立体光刻(stereo lithography, STL) 格式的三维立体模型, 将模型导入3D打印机控制系统; ②控制系统输出打印指令, 控制打印机打印片剂。首先供粉缸升高一定高度, 铺粉辊将粉铺送至成型缸, 铺粉完成后, 打印头按控制系统规定运行轨迹喷射打印液, 完成这一过程, 成型缸下降一层高度, 进行下一个铺粉打印过程, 逐层打印、层层叠加直至打印完成; ③完成片剂打印后, 取出片剂置于干燥箱中40 ℃干燥3 h。

|
Figure 2 Schematic representation of drop-on-powder three-dimensional printing |
关键工艺参数筛选与DoE 结合黏结剂喷射型3D打印技术的原理及特性, 通过初步的风险评估以及前期单因素实验选择了喷墨量(A)、层厚(B)、打印头X轴运行速度(C) 作为自变量, 以片剂硬度(Y1)、脆碎度(Y2)、分散均匀性(Y3)、打印耗时(Y4) 作为因变量。设计了三因素两水平三个中心点的全析因实验方案(表 1), 实验设计运行序列见表 2。前期的工艺参数摸索研究发现, 当层厚大于150 μm时, A等级设置为最大12时, 片剂依然无法实现充分的黏结, 故设定B低水平为100 μm, 高水平为150 μm。评估了与3D打印片剂特性相关的每个独立变量对因变量的影响及各变量之间的相互作用, P值小于0.05的变量被认为具有统计学意义。数据分析及绘图在Minitab软件上完成, 使用方差分析法对实验结果进行分析, 置信区间为95%。
| Table 1 23 Full factor design of experiment |
| Table 2 Design planning of 23 full factor experimental |
模型体积与含药量线性回归方程的建立 固定半径(r) 与模型高度(h) 的比值为1.25, 一定体积(V) 下会得出对应的r与h数值, 相应的换算公式如下所示。利用CAD画出个性化剂量模型如图 3所示。
| $ V=\pi r^{2} h $ | (1) |
| $ h=\frac{v}{\pi r^{2}} $ | (2) |
| $ r=1.25 \mathrm{~h} $ | (3) |
|
Figure 3 Schematic diagram of personalized dose model |
由公式(1)、(2) 和(3) 得
| $ h=\sqrt[3]{\frac{V}{1.25^{2} \pi}} $ | (4) |
片剂硬度脆碎度的测定 对各批次片剂进行硬度检测, 硬度结果取平均值(n = 6); 对片剂进行Y2检测, 测定前称定片剂总重为m1, 放入脆碎度检测仪圆筒中滚动100次再次称量片剂总重为m2, 按公式(5) 计算得出Y2。
| $ Y_{2}=\left(m_{1}-m_{2}\right) / m_{1} \times 100 \% $ | (5) |
片剂分散均匀性的测定 按照《中国药典》崩解时限检查法(通则0921) 检查, 使用升降式崩解仪, 将吊篮通过上端的不锈钢悬挂于金属支架上, 浸入1 L杯中, 杯内盛有温度为(15~25) ℃的水, 并调节吊篮位置使其下降时筛网距烧杯底部25 mm, 调节水位高度使吊篮上升时筛网在水面下15 mm处。不锈钢丝网的筛孔内径为710 μm, n = 6, 取最大值。
片剂的成型机制分析及评价 使用扫描电子显微镜(SEM) 分别在100和10 μm视野范围内扫描自制3D打印氯氮平分散片, 观察片剂的内部结构。
结果 1 全析因实验数据结果根据实验设计方案在不同参数下打印制剂, 并对制剂进行相应的质量检测, 结果见表 3。
| Table 3 Result of the 23 all-factors experimental design |
由图 4a、b可知, 自变量A和B是影响Y1的显著因素, 且B对片剂Y1影响更为显著。表 4对该模型进行了方差分析, 主效应P < 0.05, 显示模型是总体有效的。以未编码单位表示的回归方程为: Y1 = 22.08 + 6.082A - 0.310 1B。由图 4c、d的等值曲线图和曲面效应图看出, 随着A增大、B减小, 打印片剂Y1越大, 说明打印液的相对用量增大, 加强了黏结效果, 使成型片剂硬度加强。

|
Figure 4 Hardness full-factorial design result map. a: Pareto plot; b: Main effect plot; c: Contour plot; d: Surface plot |
| Table 4 Results of variance analysis of hardness mode. DF: Degree of freedom; Adj SS: Adjusted sum of squares deviations; Adj MS: Adjusted mean deviation sum of squares |
分析影响片剂Y2显著因素时, 剔除不显著影响因素对模型优化后, 由图 5a、b可知, 影响该片剂Y2的显著影响因素为B、A及A与B的交互作用, 表 5对该模型进行了方差分析, 主效应P < 0.05, 显示模型总体是有效的。以未编码单位表示的回归方程: Y2 = -34.0 + 2.605A + 0.393 1B - 0.030 05AB。在图 5c、d等值线图和曲面效应图中显示, A较低的情况下, B对Y2影响较大; A较高时, B对Y2影响相对较低。

|
Figure 5 Friability full-factorial design result map. a: Pareto plot; b: Main effect plot; c: Contour plot; d: Surface plot |
| Table 5 Results of variance analysis of friability |
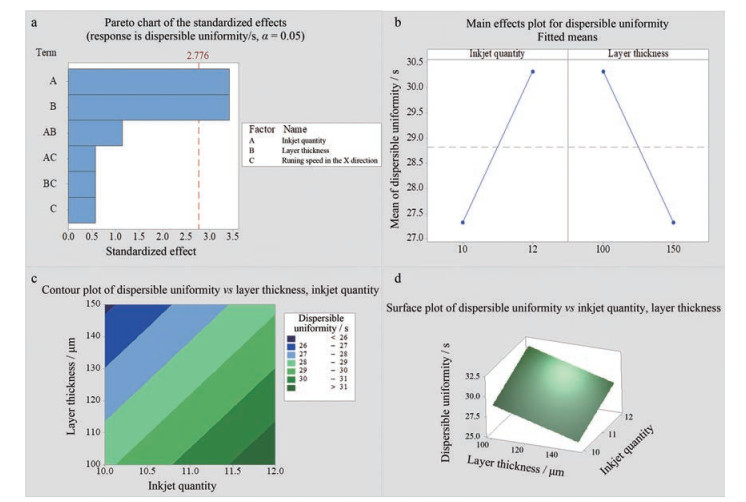
在图 6a、b的pareto和主效应交互图中, B和A是影响片剂Y3的显著因素, 表 6对该模型进行方差分析, 主效应P值为0.002 (P < 0.05), 显示模型总体有效。以未编码单位表示的回归方程: Y3 = 19.82 + 1.500A - 0.060 0B。图 6c、d的交互作用等值线图和曲面效应图中显示, A和B对片剂Y3均有显著影响。A越大, 片剂崩散全部通过筛网所用时间越长; B越大, 片剂崩散全部通过筛网所用时间越短。
|
Figure 6 Dispersible uniformity full-factorial design result map. a: Residual plot; b: Main effect plot; c: Contour plot; d: Surface plot |
| Table 6 Results of variance analysis of dispersible uniformity |
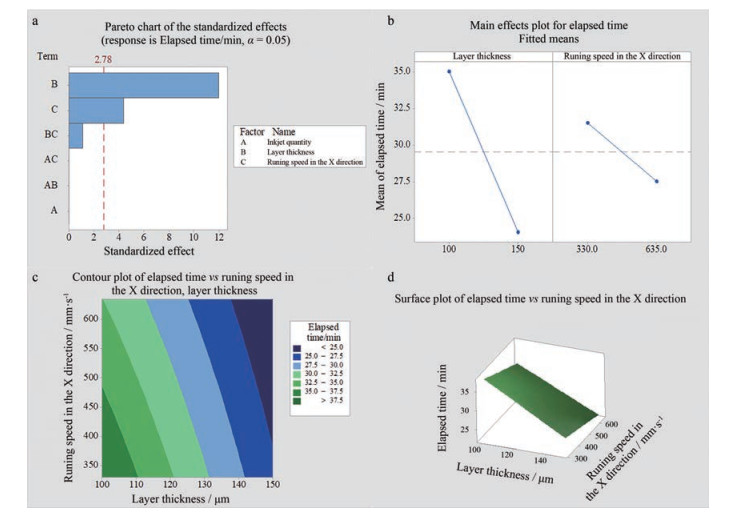
由7a、b pareto图及交互作用图可知, 影响片剂Y4的显著因素为B及C, 表 7对该模型进行方差分析, 主效应P值为0.000 (P < 0.05), 显示模型总体是有效。以未编码单位表示的回归方程: Y4 = 63.37 - 0.220 0B - 0.013 11C。图 7c、d的交互作用等值线图和曲面图显示, B及C对Y3有显著影响。B越大、C越快, 则Y3越短。
| Table 7 Results of variance analysis of elapsed time mode |
|
Figure 7 Elapsed time full-factorial design result map. a: Residual plot; b : Main effect plot; c: Contour plot; d: Surface plot |
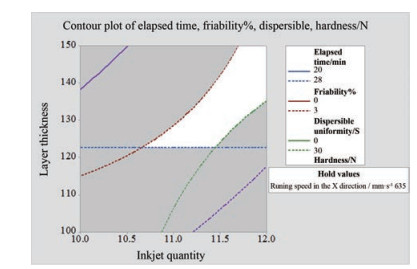
由以上结果显示, A和B是多个响应值的显著影响因素, A增加使打印片剂黏合更好, Y1升高、Y2降低、同时Y3变慢。B增加会降低成型片剂的机械强度, 使Y1下降、Y2升高。故A和B在影响输出响应时具有一定的交互作用。同时B增加会显著降低打印片剂的整体耗时, 提高打印效率。故结合以上影响因素, 确定各响应变量的目标范围建立了打印参数的设计空间, 如图 8白色区域所示。最终确定打印参数: A 12、B 150 μm和C 635 mm·s-1。
|
Figure 8 Design space of 3D printing clozapine process parameters |
固定模型r与h的比值为1.25, 按照公式(1~4) 计算不同模型体积为2 000、1 500、1 000、500、300和200 mm3下模型r和h, 打印出的片剂, 取平均片重计算规格含药量。结果见表 8。对结果进行拟合, 得出含药量(y) 与模型体积(x) 的回归方程: y = 0.062 x - 0.582 7 (R2 = 0.999 9)。
| Table 8 Table of radius (r) and height (h) corresponding to different model volumes |
由线性回归方程可计算出100 mg规格片剂模型体积为1 623.19 mm3, 12.5 mg规格片剂模型体积为211.90 mm3。模型验证结果如表 9所示。验证结果误差均在5%以内, 表明线性模性建立成功。12.5 mg小规格模型片剂Y2小于5%, 机械强度符合质量要求。结果表明, 优化后的工艺参数可以实现剂量模型的个性化灵活调控, 发挥3D打印的个性化优势。
| Table 9 Regression model verification results |
3D打印片剂外观及内部结构如图 9。由图 9a可以明显看出片剂逐层打印、层层黏结的痕迹; 图 9b是50倍视野范围内打印片剂内部结构的SEM图, 可以观察到有原辅料黏结痕迹, 黏结机制主要有两种, 一种为随着液滴的渗入粉末中的黏结剂被溶解而产生的物理黏结; 另一种为粉末中水溶性辅料溶解于水, 在随后的干燥过程中重新析出固化而产生的化学黏结[16]; 图 9c是在300倍视野范围SEM图, 可以看出打印片剂内部的众多细微孔道, 这些毛细孔道有利于片剂干燥的同时也有利于水分的进入, 实现片剂遇水快速崩散。

|
Figure 9 Scanning electron microscope (SEM) characterization of 3D printing tablets. a: Tablet appearance; b: SEM with magnification of 50; c: SEM with magnification of 300 |
3D打印与传统制剂相比, 具有极高可控性和灵活性。可控性具体表现在对复杂空间结构和精密制备过程的掌控; 灵活性则表现在剂量灵活、需求灵活和结构灵活等。本研究中用的黏结剂喷射型3D打印利用其成品高孔隙率的特点实现了难溶性药物口服吸收的问题。
基于黏结剂喷射型3D打印机的打印原理, 可调节的运行参数较多, 如打印头的运行速度、喷液量、打印头距粉床的高度、粉末铺层厚度。每个运行参数都会对产品质量、打印可行性、打印稳定性产生或多或少的影响, 这些参数之间的交互影响使用单因素考察并不能得到可靠结论。故本研究采用了DoE来对运行参数空间进行优化。DoE以数理统计和概率论为基础能够合理安排实验、高效且经济地获取数据、缩小误差从而得出正确的结论[17, 18]。在确定粉体与液体处方的基础上、通过对运行参数的优化实现打印机与粉体、液体处方高度匹配。并通过打印成品的质量研究反馈评价参数的设计空间, 确定了关键工艺参数为喷墨量、打印层厚及打印头X轴运行速度。从以上结果可以看出喷墨量和层厚对多个响应都有显著影响, 同时喷墨量与层厚还存在一定的交互作用。喷墨量过大、片剂硬度增大、分散变慢和因渗透过饱和而出现外观不平整。层厚过大, 打印液无法实现充分黏结而表现为片剂机械强度不足。故往往在参数调整时二者是相互协调的, 最终确定喷墨量等级为12。同时打印层厚还显著影响打印耗时, 层厚越大, 打印耗时越短, 故确定了打印层厚为150 μm (在前期单因素考察时, 当层厚超过150 μm时无法实现有效黏结)。打印头在X轴方向上的运行速度体现在打印头的喷射频率上, 速度越大频率越高。通过对低、中、高三个因素水平的考察, 确定不同速度下打印液体喷射的流畅性。结果表明不同X轴运行速度并不是影响片剂质量的显著因素, 但却显著影响打印的总耗时, 故最终确定了高水平635 mm·s-1的运行速度以确保不影响片剂理化性质的前提下提高打印效率。
通过对三维模型大小的调整建立了模型体积与含药量的线性回归方程。可准确、灵活地制备不同规格的药物, 本研究确定的药品最大规格为100 mg、最小规格为12.5 mg。在对线性模型验证过程中对两种规格进行了打印。重现性良好且最小规格成型片剂的外观、脆碎度(< 5%) 均符合质量要求, 也验证了粉体、液体处方和打印参数的高匹配度, 可实现剂量由低到高打印的稳定性, 为实现个性化医疗提供了一种技术支持。
同时, 3D打印也面临着许多制约和挑战, 其中最大的制约因素就是打印头工作的稳定性, 本研究用的打印头为爱普生4720喷头, 主要应用于二维打印, 且对墨水质量及性能要求极高。自制墨水对喷头寿命损耗较为严重, 损耗严重的喷头打印精密度下降, 直接导致成型片剂脆碎度的升高, 体现了设备装置的完善对3D打印制剂发展同样具有至关重要的意义。
作者贡献: 陈如心具体完成撰写任务; 韩晓璐、刘伯石、刘原兵和刘婷完成文献检索和筛选; 王增明、刘中成和郑爱萍确定文章方向及内容组成, 并对文章撰写质量进行把关和审校。
利益冲突: 文章内容不涉及相关利益冲突, 未涉及任何厂家及相关经济组织直接或间接的经济或利益的赞助。
| [1] |
Chen RX, Wang ZM, Han XL, et al. The principle of drop-on-powder 3D printing and its application and challenge in solid preparation[J]. Acta Pharm Sin (药学学报), 2020, 55: 2862-2868. |
| [2] |
Norman J, Madurawe RD, Moore CM, et al. A new chapter in pharmaceutical manufacturing: 3D-printed drug products[J]. Adv Drug Deliv Rev, 2017, 108: 39-50. DOI:10.1016/j.addr.2016.03.001 |
| [3] |
Wang X, Zhang C, Ping QN. Advances of 3D printing technology in advanced pharmaceutical preparations[J]. J Chin Pharm Univ(中国药科大学学报), 2016, 47: 140-147. |
| [4] |
Lee VC. Medical applications for 3D printing: current and projected uses[J]. Pharm Therapeut, 2014, 39: 704-711. |
| [5] |
Zheng Q. From the approving of 3D printing tablet to the innovation of drug delivery systems[J]. Acta Pharm Sin (药学学报), 2016, 51: 1655-1658. |
| [6] |
Yu DG, Yang XL, Xu HB, et al. Application of three-dimensional printing in pharmaceutics[J]. Chin J New Drugs (中国新药杂志), 2005, 14: 843-848. |
| [7] |
Lin MM, Chen PH, Tian P, et al. Optimization and evaluation of the structural design of clozapine orally disintegrating tablets by three dimensional printing[J]. Chin J New Drugs (中国新药杂志), 2019, 28: 739-744. |
| [8] |
Shi J, Wang ZM, Zheng AP. Applications and challenges of 3D printing technique in manufacturing pharmaceutical preparations[J]. Prog in Pharml Sci (药学进展), 2019, 43: 164-173. |
| [9] |
Liu Z, Sun PJ. The first 3D print antiepileptic drugs—spritam[J]. J Pharm Res (药学研究), 2015, 34: 556-558. |
| [10] |
Prakash K, Baishakhi D, Assaleh FH, et al. Top-down and bottom-upapproaches in 3D printing technologies for drug delivery challenges[J]. Crit Rev Ther Drug Carrier Syst, 2015, 32: 61-87. DOI:10.1615/CritRevTherDrugCarrierSyst.2014011157 |
| [11] |
Jiang LH. Comparision study of clozapine orally disintegrating tablets and clozapine in the treatment of schizophrenia[J]. Guide China Med (中国医药指南), 2013, 11: 478-479. |
| [12] |
Zhi YM, Qin YF, Li WB, et al. Relationship between dosage and serum concentration of clozapine in schizophren and the gender difference[J]. Chin J Clin Pharm (中国临床药学杂志), 1999, 8: 5-8. |
| [13] |
Ma W. Overview of 3D printing technology in pharmaceutical preparations research[J]. Pharm Today (今日药学), 2018, 28: 204-206. |
| [14] |
Wang CY, Zhao JP, Chen YG, et al. The pharmacokinetics of clozapine correlated with a caffeine test[J]. Chin J Psychiat (中华精神科杂志), 2000, 33: 15-18. |
| [15] |
Alomari M, Mohamed FH, Basit AW, et al. Personalised dosing: printing a dose of one's own medicine[J]. Int J Pharm, 2015, 494: 598-577. |
| [16] |
Li XY, Wu YH, Zhang S. Principle and experimental research of three dimensional printing[J]. China Mech Eng (中国机械工程), 2006, 17: 1355-1359. |
| [17] |
Du Y, Zhang YZ, Tan XD. Application of design of experiment in the formulation screening of antibody drug conjugate[J]. Shanghai Med Pharm J (上海医药), 2018, 39: 71-75. |
| [18] |
Chen TT, Li SY, Qin TT, et al. Formulation optimization of alginate mPEG-b-PLGA nanoparticles by Box-Behnken response surface method[J]. Chin Pharm J (中国药学杂志), 2019, 54: 1590-1598. |
 2021, Vol. 56
2021, Vol. 56


