2. 北京市一六一中学, 北京 100020;
3. 贵州中医药大学, 贵州 贵阳 550001
2. Beijing No. 161 High School, Beijing 100020, China;
3. Guizhou University of Traditional Chinese Medicine, Guiyang 550001, China
细菌耐药已经成为公共卫生安全的世界难题, 在后抗生素时代亟需研究和开发新型抗菌药物[1, 2]。2010~2018年, 美国FDA共计批准了8种抗生素新药, 分别为头孢洛林、奥利万星、达巴万星、泰地唑利、头孢洛赞/他唑巴坦、头孢他啶/阿维巴坦、地拉氟星和美罗培南/法硼巴坦复方——这些新药都是由已知抗菌药物衍生得到或者是与上市药物的组合物[3]。在细菌对临床药物耐受加剧和新型抗菌药物研发进展缓慢的双重夹击下, 对现有抗菌药物的结构优化修饰是当下发现新型抗菌药物最有前景的途径之一[4]。当前生物医学领域对抗生素药物作用机制及耐药性机制研究的逐步深入, 为现有抗生素药物的二次开发利用提供了新的机遇。
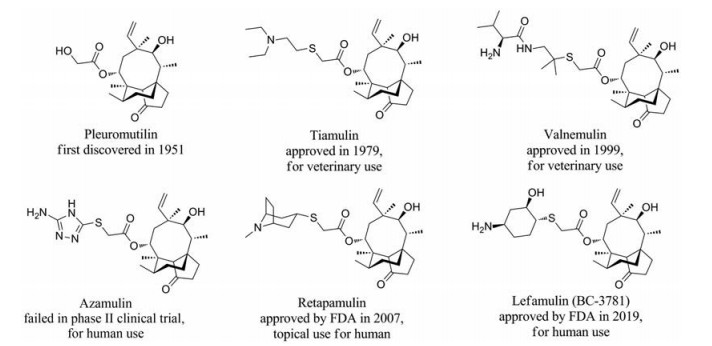
截短侧耳素(pleuromutilin) 是从高等真菌担子菌纲侧耳属Pleurotus mutilis和Pleurotus passeckeranius菌种中分离得到的一种三环二萜类抗生素, 主体骨架由一个五元环、一个六元环和一个八元环拼合而成, 具有三环刚性结构(图 1)[5]。目前, 截短侧耳素类抗生素已经上市近50年, 泰妙菌素(tiamulin, 1979年批准) 是首个兽用截短侧耳素类抗生素, 在大约20年后沃尼妙林(valnemulin) 被欧盟批准。两个兽用抗生素主要用于预防和治疗猪痢疾, 抗菌谱较广, 对多数革兰阳性细菌(MIC小于1.0 μg·mL-1)、肠道螺旋体和支原体(MIC = 0.03~2.0 μg·mL-1) 等具有较好的抗菌活性(图 1)[6]。该类化合物具有体内蓄积性低, 毒性小, 宿主耐受性好, 不易于产生耐药性等优点, 在家禽和畜牧中得到广泛的应用。
|
Figure 1 Clinical application of pleuromutilin derivatives |
阿扎妙林(azamulin) 是Sandoz公司开发的半合成人用抗生素, 虽然具有良好的抗菌活性和安全性, 但是在临床Ⅱ期试验中发现口服生物利用度过低, 且细胞色素P450 (CYP450) 代谢快, 半衰期短而终止了研发(图 1)[7]。瑞塔莫林(retapamulin) 是葛兰素史克公司研发的一种局部使用的1%的软膏剂(商品名为Altabax), 主要用于治疗胞脓病等皮肤感染性疾病。在2007年经美国FDA批准用于治疗胞脓病, 同年获欧洲药物管理局(European Medicines Agency, EMA) 批准用于短期治疗继发性表皮感染, 成为第一个局部人用截短侧耳素类抗生素[4]。Lefamulin (BC-3781) 是由奥地利Nabriva Therapentics公司研发的治疗CABP的半合成抗生素, 在2019年上半年完成了Ⅲ期临床试验(图 1)[8], 是近20年FDA批准的第一个具有新作用机制的抗菌药物, 也是第一个用于治疗人类全身性细菌感染的截短侧耳素类药物。本文针对截短侧耳素类新药Lefamulin的作用机制、抗菌谱、临床前和临床试验数据等四个方面进行综述。
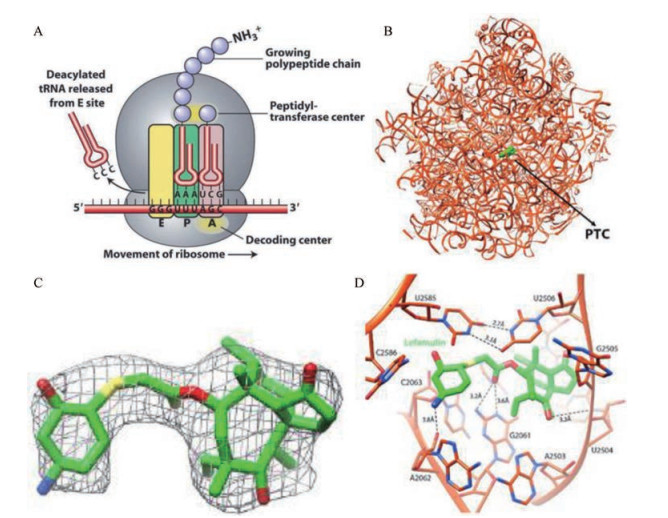
1 Lefamulin的作用机制核糖体是一个复杂的生物机器, 是蛋白质合成的关键场所, 同时也是抗生素作用的重要靶点。细菌的核糖体沉降系数为70S, 由30S和50S亚基组成。肽键形成过程首先需要位于50S亚基内tRNA的3'端与肽基结合位点(A位点) 的正确结合, 通过氨酰-tRNA上的氨基酸与其中一个肽酰-tRNA结合后固定核糖体的P位点, 然后在肽基转移酶的作用下与A位点的氨基酸脱水缩合形成肽键(图 2)。任何一个环节出现问题都会直接影响蛋白质的合成, 目前临床使用的诸多抗生素如氨基糖苷类抗生素、四环素类抗生素、大环内酯类抗生素和噁唑烷酮类抗生素等都是通过抑制和干扰细菌的蛋白质合成而发挥其抗菌作用[9]。在哺乳动物中, 核糖体的体积较大, 沉降系数为80S, 由40S和60S亚基组成。哺乳动物和细菌核糖体的结构差异, 以及近年来冷冻电镜技术在解析大型生物机器精细结构中的成功应用, 为发现选择性作用于细菌核糖体亚基的抗生素提供了可能[10]。
|
Figure 2 The mechanism and the binding site of Lefamulin with the SA50S-lef structure at the PTC[6, 11]. (A) The function of the ribosomal PTC in the protein synthesis. (B) The binding site of Lefamulin (green) within the SA50S-lef subunit at the PTC. (C) The 2Fo-Fc electron density map of the complex S50S-lefamulin contoured at 1.0 σ. (D) The complex structure of Lefamulin (green) and the PTC 23S rRNA nucleotides (orange), hydrogen bonds are presented with dashed lines |
截短侧耳素类化合物的三环骨架母核结构对细菌核糖体具有独特的结合作用, 主要是通过选择性的作用于细菌核糖体50S亚基的23S rRNA而抑制细菌蛋白质合成[11]。金葡菌核糖体50S亚基的晶体结构显示, Lefamulin结合在肽酰基转移酶活性中心(the peptidyl transferase center, PTC) (图 2)。23S rRNA的核苷酸U2585和U2506之间的U: U相互作用稳定了Lefamulin的结合部位, Lefamulin的乙酰羰基与核苷酸G2061的NH以及NH2形成氢键, C11的羟基与G2505的磷酸基团形成氢键, C14侧链延伸的NH2基团与A2062也形成氢键。此外, Lefamulin与rRNA核苷酸C2063、U2506、A2503、U2504、G2505、A2453、C2452、A2425和C2424的其他相互作用均为疏水作用或者范德华力(图 2)[11]。Lefamulin通过诱导契合机制与核糖体50S亚基的A位和P位结合干扰肽基转移酶中心, 阻止了肽键的形成从而抑制细菌蛋白质的合成。这种作用机制与噁唑烷酮相似, 并且可以与氯霉素竞争相同的结合位点, 但与之不同的是Lefamulin产生独特的诱导契合作用, 导致肽基转移酶中的核苷酸发生构象变化, 阻止tRNA正确定位, 从而阻止进一步的肽基转移[12]。这是一种抑制细菌肽链延长的新机制, 使得Lefamulin显示出较低的交叉耐药性。
2 Lefamulin的抗菌活性研究Lefamulin的体外抗菌活性较强, 对需氧革兰阳性细菌和部分厌氧及非典型的病原微生物具有抗菌活性, 另外对少部分需氧革兰阴性细菌也具有较好的抗菌活性, 尤其是引起CABP和急性细菌性皮肤和皮肤结构感染(acute bacterial skin and skin structure infection, ABSSSI) 的病原体[13, 14]。对金葡菌(包括MRSA和CA-MRSA)、溶血性链球菌(包括化脓链球菌和无乳链球菌)、肺炎链球菌、流感嗜血杆菌、卡他菌、放线杆菌、淋病奈瑟氏球菌, 流感嗜血杆菌、非典型呼吸道病原体嗜肺杆菌、肺炎支原体及肺炎衣原体等病原微生物表现良好的抗菌活性, 其最小抑菌浓度(MIC) 为0.006~0.5 μg·mL-1[13, 14]。此外, 交叉耐药性研究显示Lefamulin对以下抗生素(类别) 耐药的临床分离株仍然有效: 大环内酯类、林可酰胺类、链霉素B、噁唑烷酮、四环素类、β-内酰胺类、喹诺酮类、甲氧苄啶/磺胺甲噁唑复方、莫匹罗星和万古霉素。
2.1 体外抗菌活性研究Lefamulin对于革兰阳性细菌(除部分屎肠球菌) 具有较好的抗菌活性, 对美国医院临床分离得到的506株金葡菌进行抗菌活性测试, 结果显示Lefamulin的MIC分布相似, 均不超过0.25 μg·mL-1[13]。Lefamulin对金葡菌表现出很强的抗菌活性, 在浓度不低于0.12 μg·mL-1时可以抑制94.6%的临床分离菌株(n = 5 527), 并且其抗菌活性与对甲氧西林的敏感性无关[13]。在Lefamulin浓度不低于2.0 μg·mL-1时抑制了97.8%的凝固酶阴性链球菌分离菌株(n = 267)[13], 在Lefamulin浓度不低于0.12 μg·mL-1时可抑制99.2%的β-溶血性链球菌分离菌株(n = 763)[13]。Lefamulin对草绿色链球菌[13]中的唾液链球菌、牛链球菌、咽峡炎链球菌、轻型链球菌也具有显著抑制作用, MIC90分别为0.12、2.0、0.25和0.5 μg·mL-1。
多种体外研究表明Lefamulin有广泛的抗肺炎链球菌活性。SENTRY监测数据库显示, Lefamulin浓度不低于1.0 μg·mL-1时, 对所有菌株(临床分离822株肺炎链球菌菌株) 均具有抑制作用, MIC90为0.25 μg·mL-1[13]。2015年公布的Lefamulin针对CABP病原菌的抗菌活性研究结果显示, Lefamulin在浓度不高于0.5 mg·mL-1时可以完全抑制945种临床分离的肺炎链球菌菌株[15]。Lefamulin对医院和社区感染中比较常见的耐药菌株如耐甲氧西林金葡菌(MRSA)、中等耐万古霉素金葡菌(VISA)、异源VISA (hVISA) 和耐万古霉素金葡菌(VRSA)、耐青霉素的肺炎链球菌(PRSP)、耐多药肺炎链球菌和耐万古霉素的屎肠球菌(VRE) 均表现出良好的抑制活性[16] (表 1)。另外, Lefamulin对氟喹诺酮类、大环内酯类和四环素类药物耐药的菌株均具有高效的抗菌活性。
| Table 1 Activities of Lefamulin and comparator antimicrobial agents against Gram-positive bacterial pathogens |
2015年SENTRY公布的数据中评估了Lefamulin对欧洲分离的革兰阴性菌卡他氏菌和流感嗜血杆菌的抗菌活性[16]。结果显示Lefamulin的浓度不高于2.0 μg·mL-1时, 可以完全抑制上述菌株的生长, Lefamulin对卡他氏菌和流感嗜血杆菌的MIC90分别为0.12和1.0 μg·mL-1 (表 2)。对全球30个国家(包括美国和欧洲) 临床分离得到的2 817株菌株(CABP相关病原体) 进行抗菌活性测试[16], 结果显示Lefamulin浓度为0.12 μg·mL-1时可抑制99%的黏膜炎莫拉氏菌, 而Lefamulin浓度为2.0 μg·mL-1时抑制99%的流感嗜血菌。同时, β-内酰胺酶的产生和其他耐药机制对Lefamulin的敏感性没有影响。
| Table 2 Activities of Lefamulin and comparator antimicrobial agents against Gram-negative bacterial pathogens |
2017年, 瑞典国家奈瑟氏病原菌标准实验室评价了Lefamulin对251株淋病奈瑟氏球菌的体外抗菌活性, 结果显示Lefamulin对所有淋病奈瑟氏球菌都具有较好的抑制作用, 其MIC90和MIC50分别为1.0和0.25 μg·mL-1, 对临床分离得到的多药耐药菌株MIC值较低[17]。经观察发现Lefamulin与其他药物不发生交叉耐药, 当病原体中MtrCDE外排泵失活时, Lefamulin的MIC降至原MIC的1/6~1/4, 而外排泵NorM和MacAB的失活对Lefamulin敏感性没有显著影响。这些数据表明, 外排泵MtrCDE可能是影响Lefamulin敏感性的主要机制, 但是需要进一步测试以确定不同的外排泵在Lefamulin耐药性选择中的作用[17, 18]。
在对厌氧和非典型微生物的活性研究中, 发现Lefamulin对引起CABP的非典型微生物有良好的抑制活性, 其中包括衣原体、支原体和军团菌等(表 3)[14]。尽管Lefamulin对一些厌氧菌有活性, 包括产气荚膜梭菌、痤疮杆菌、梭状芽孢杆菌、消化链球菌、普氏菌、卟啉单胞菌, 但它对脆弱拟杆菌活性很弱, 并且对艰难梭菌无活性。
| Table 3 Activities of Lefamulin and comparator antimicrobial agents against atypical organisms bacterial pathogens |
在2018年美国微生物学会Microbe会议上, Nabriva Therapeutics公司公布了2015~2016年Lefamulin对3 195株葡萄球菌和4 489株链球菌的耐药菌株筛选结果[19], 发现Lefamulin对其中28株菌株(0.36%, 7 684菌株) 中的最小抑菌浓度不小于0.5 μg·mL-1, 对25株菌株(0.33%, 7 684菌株) 中的最小抑菌浓度不小于1.0 μg·mL-1。其中11株金葡菌经过基因组检测, 发现主要耐药机制来自于vga (A) 外排蛋白, 而vga (E) 和Isa (E) 出现频率较低。另外, 仅在无乳链球菌和弧菌类链球菌中观察到MIC值升高, 通常伴随着Isa (E) 的出现, 但耐药性的发生率总体较低。目前来看, vga (A) 和Isa (E) 的改变是导致Lefamulin对葡萄球菌及链球菌产生耐药的最主要原因。当前暂未分离得到具有较高MIC值的肺炎链球菌菌株, 提示该菌株不易产生耐药, 但应持续对其耐药性进行监测[19]。
2.2 动物试验结果在多种动物模型上, 分别进行了Lefamulin的药代动力学和药效学试验, 明确了药物的组织分布和代谢途径[20]。动物体内实验重点探索了给药剂量和药物疗效的关系, 为后续体内研究的剂量选择提供了依据[21]。在对金葡菌引起的菌血症的治疗中, 动物试验结果显示Lefamulin与临床常用药物达托霉素和万古霉素的作用效果相当[22]。此外, 由于Lefamulin在泌尿生殖道中的分布特点, 对性传播感染也有潜在的治疗效果[23]。
药代动力学试验结果表明给药后Lefamulin在体内快速分布, 主要通过粪便(约81.6%) 和尿液(约13.5%) 排出[20]。在大鼠中静脉注射10 mg·kg-1的[14C]-Lefamulin, 检测全血、血浆、呼出气体、尿液、粪便以及全身的相对放射性强度, 结果表明药物在皮肤、软组织以及肺部的浓度要远远高于血浆, 为Lefamulin在治疗CABP以及皮肤感染中的应用创造了条件[20]。给药5 min后药物在身体各个器官的分布含量均高于血液, 但是在大脑和脊髓含量较低, 说明该药物能够较快的从血液分布到各个组织中, 但并不能跨过血脑屏障[20]。在药物的消除阶段(给药后24~72 h), 所有器官的放射性迅速下降, 表明该药物在组织中无积累。给药后48 h内Lefamulin及其代谢物清除率为92%, 168 h为96%, 可以认为完全清除[20]。
药效学研究揭示Lefamulin的体外抗菌活性与体内药效表现出很强的相关性。在小鼠的肺部感染模型中接种肺炎链球菌或金葡菌, 接种后2 h皮下注射剂量范围在1.25至320 mg·kg-1的Lefamulin进行治疗, 每天注射两次[21]。通过测量血浆和肺泡上皮细胞表面液(epithelial lining fluid, ELF) 中的药物浓度, 建立Hill模型探究用药后24 h菌落形成单位的变化与Lefamulin的AUC: MIC比值间的关系[21]。Hill模型显示, 血浆和ELF中的AUC: MIC比值与菌落形成单位的减少呈正相关, 在肺炎链球菌的感染模型中血浆和ELF中AUC: MIC的比值分别为1.37和14.0, 在金葡菌的感染模型中该比值分别为2.13和21.7[21], 该研究也为Lefamulin在临床应用的剂量选择提供了依据。
在小鼠菌血症模型上, Lefamulin对金葡菌引起的菌血症有效[22]。通过皮下注射Lefamulin (70 mg·kg-1) 及阳性对照药物(达托霉素-22.5 mg·kg-1, 万古霉素-160 mg·kg-1, 利奈唑胺-80 mg·kg-1, 替加环素-6.5 mg·kg-1), 然后检测血液中细菌浓度的变化评价药效[22]。实验结果显示, 所有的抗菌药物均使血液中细菌浓度显著降低, 在Lefamulin治疗组中小鼠血液中细菌浓度均降低超过4个数量级, 其治疗效果明显优于阳性对照药物利奈唑胺和替加环素, 与达托霉素和万古霉素的活性相当[22]。
Lefamulin在动物泌尿系统的药物分布研究结果显示, [14C]-Lefamulin在雄性大鼠的一些腺体组织(如包皮、尿道球部) 和尿道中的浓度较高。与管腔相比, 囊壁(上皮和黏膜) 的放射性浓度更高。给药后24 h, [14C]-Lefamulin在泌尿生殖道组织中的浓度与同一时刻肺中的浓度相似[23]。在雌性大鼠中, [14C]-Lefamulin在阴蒂腺、子宫和尿道均有分布, 在子宫内膜的浓度高于其他部位。在阴道中, Lefamulin均匀分布于管腔、上皮组织和平滑肌壁。注射后24 h, Lefamulin在阴蒂腺的积累最多, 是同一时刻肺部浓度的3倍[23]。Lefamulin在泌尿生殖道组织分布迅速, 浓度与肺中的浓度相似, 不受性别影响, 并且对引起性传播感染的敏感菌株及耐药菌株都有活性, 可以作为性传播感染的潜在疗法[23]。
3 Lefamulin的临床研究自2010年开始启动首个Ⅰ期研究至今, Lefamulin主要针对两种临床适应症: ABSSSI和CABP。临床数据显示, 该药物早期临床试验中重点研究了药物的安全性、生物利用度及药代动力学性质等内容; 在ABSSSI方面进行了Ⅱ期临床研究; 在CABP患者中先后进行了两次全球多中心的Ⅲ期临床试验, 其主要的临床研究进展情况如表 4所示。
| Table 4 Summary of clinical trial results for Lefamulin in various phases of development. ABSSSI: Acute bacterial skin and skin structure infection; CABP: Community acquired bacterial pneumonia; CE: Clinically evaluable; mITT: Modified intent-to-treat; ELF: Epithelial lining fluid; IV: Intravenous; TOC: Test of cure |
奥地利维也纳医科大学首次报道了Lefamulin的临床Ⅰ期研究(欧盟临床注册号: EudraCT-2010-021938-54)。在12名健康男性受试者中, 在1 h内静脉注射150.0 mg的Lefamulin进行其临床药理学及人体安全性评价[24]。在静脉注射后, 药物在血浆中的浓度呈多相下降过程。单剂量给药的药物终末半衰期为8.6~11.7 h, AUC随着用药剂量增加呈线性增长。在多次给药达到稳态后, AUC增加但是Cmax并未发生显著增加。血浆中游离药物的AUC0-24 h为1 500.8 mg·h·L-1, 血浆中游离药物最大浓度Cmax为330.1 mg·L-1, 血浆蛋白结合率为80%~87%, 具体各项参数请见表 5。通过检测Lefamulin在血浆、骨骼肌组织、皮下脂肪组织和ELF的药物浓度发现, 骨骼肌组织(AUC0-24 h = 1 264.5 mg·h·L-1, Cmax = 138.1 mg·L-1) 和皮下脂肪组织(AUC0-24 h = 1 456.6 mg·h·L-1, Cmax = 145.1 mg·L-1) 中的药物浓度与血浆中游离药物浓度相似, 但ELF (AUC0-8 h = 3 871 ng·h·mL-1, Cmax = 706 ng·mL-1) 的药物浓度是血浆中游离药物的5.7倍。这可能是因为P-糖蛋白的主动转运, 将药物从血浆快速转运至ELF中, 使其在肺组织中大量富集。
| Table 5 Summary of the main pharmacokinetic parameters of 150 mg of Lefamulin administered as 1 h infusion. a Free plasma concentrations were calculated assuming plasma protein binding of 87%. b Derived from the mean concentrations of the three subjects per timepoint. c C12 was calculated by extrapolation and AUC0-12 h was derived; each subject underwent only one BAL, and therefore no range is presented for ELF. d Values calculated from corresponding AUC0-12 h |
Lefamulin在健康受试者上表现出良好耐受性, 未出现与治疗相关的严重不良反应。12名健康受试者中的7名(58%) 报告有轻度或中度不良反应[24]: 头痛(25%)、血清胆红素增加(17%)、不适(8.3%)、腹泻(8.3%)、体温升高(8.3%) 和局部输液部位疼痛(8.3%)。
在2015年英国Quotient Clinical Nottingham进行了Lefamulin的安全性、生物利用度及药代动力学临床研究(美国临床注册号: NCT02557789)[25]。将20个健康受试者随机分成4组, 分别按照以下4种方式给药: ①禁食条件下口服600 mg的Lefamulin片; ②禁食条件下, 口服600 mg的Lefamulin胶囊(200 mg/颗); ③静脉注射150 mg的Lefamulin; ④早餐1 h后, 口服600 mg的Lefamulin片。临床研究结果表明口服Lefamulin的耐受性较好, 单次口服剂量为600 mg与单次注射150 mg Lefamulin的药代动力学参数相似。在禁食状态下口服600 mg的Lefamulin后, 药物被快速吸收。在餐后口服Lefamulin导致患者AUC0-inf和Cmax分别降低了10%和28%。空腹时口服含Lefamulin 600 mg的速释片剂与静脉注射Lefamulin 150 mg生物等效。在禁食状态下口服给药的绝对生物利用度为25.8%, 在饱餐状态下为21.0%。
另外, 2017年在英国进行的一项实验中, 通过同位素[14C]标记的方法研究了Lefamulin在健康受试者中的药代动力学性质(美国临床注册号: NCT03131141), 分别设置了两个试验组, 其中一组在餐后单次静脉注射150 mg的Lefamulin; 另外一组在禁食状态下口服600 mg的Lefamulin[26]。这项临床实验重点研究了Lefamulin在人体的吸收、分布、代谢和排泄的特点, 其临床试验数据尚未公开。
3.2 ABSSSI (Ⅱ期临床试验)引起ABSSSI的病原体主要是革兰阳性菌, 包括金葡菌(甲氧西林敏感和甲氧西林耐药菌株)、β-溶血性链球菌(化脓性链球菌、无乳链球菌、停乳链球菌)、咽峡炎链球菌群(S. anginosus、S. intermedius和S. constellatus) 和粪肠球菌(仅万古霉素敏感株)[27]。Lefamulin的Ⅱ期临床试验(美国临床注册号: NCT01119105) 主要是针对ABSSSI患者。临床试验采用双盲随机对照试验, 比较静脉注射Lefamulin和静脉注射万古霉素对ABSSSI患者的疗效, 实验组随机分为每12 h静脉注射100 mg的Lefamulin组和150 mg的Lefamulin组, 对照组每12 h静脉注射1.0 g万古霉素。临床试验的治疗周期为5~14 d, 其主要终点是治疗后7~14 d的临床治愈率(test of cure, TOC), 包括治愈、改善、失败或者无法评估。另外, 根据临床治愈率的微生物检测结果, 将次要终点分为微生物的根除、假定根除、残留、假定残留、重复感染、缺失和不确定。
共计207位患者至少接受过不少于1次药物治疗[定义为改良意向-治疗分析人群(modified intent-to-treat, mITT)], 其中186位患者完成了整个治疗方案[定义为临床可评估的人群(clinically evaluable, CE)]。本临床试验中主要的皮肤感染类型包括两类: ①蜂窝组织炎(Lefamulin组48%; 万古霉素组56%); ②脓肿性蜂窝组织炎(Lefamulin组33%; 万古霉素组26%)。在各治疗组中, 病原体的分布大致相当, 最常见的革兰阳性病原体是金葡菌(mITT人群中占90.8%, MRSA占69.1%)。在参与临床评价的人群中, 各组之间的TOC相似, 分别为Lefamulin 100 mg (90%)、Lefamulin 150 mg (88.9%) 和万古霉素(92.2%)。在mITT人群中也观察到相似的结果, Lefamulin 100 mg (82%)、Lefamulin 150 mg (82.4%) 和万古霉素(82.2%)。每组的平均治疗时间分别为: Lefamulin 100 mg组为5.9 (SD 3.1) d、Lefamulin 150 mg组为8.1 (SD 21.2) d、万古霉素组为5.6 (SD 3.1) d。在临床试验中, 有6名患者因为发生药物相关不良反应而终止治疗。最常见的不良反应是恶心、腹泻和头痛, 万古霉素治疗组中不良反应的发生率略高, 其中药物相关的不良反应发生率分别为34.3% (100 mg的Lefamulin组)、39.4% (150 mg的Lefamulin组) 和53.0% (万古霉素组)[28]。
美国临床研究机构采用PK模型对Ⅱ期临床试验的数据进行了回顾性研究, 进一步确定了其关键的药代动力学参数。该分析采用了129名患者的1 167个PK血浆样品, PK参数与患者的个体差异之间无强相关性, 患者的个体差异约为22%。静脉注射100 mg和150 mg的Lefamulin主要药代动力学参数分别为(平均偏差): Cmax = 1.57 (0.974) 和1.90 (0.705) µg·mL-1, AUC0-24 h = 10.9 (5.97) 和14.1 (5.76) µg·h·mL-1, t1/2 = 11.0 (5.18) 和13.2 (5.79) h[29]。
3.3 CABP临床研究(Ⅲ期临床试验)截至2020年9月, ClinicalTrials.gov未显示FDA批准的针对ABSSSI的Ⅲ期临床试验。Lefamulin的Ⅲ期临床试验主要针对社区获得性细菌性肺炎, 分别在2015年和2016年开展了两次全球多中心的临床研究。
首个Ⅲ期临床试验(LEAP1, 美国临床注册号: NCT02559310) 是一项全球性非劣效试验, 旨在评价Lefamulin治疗CABP患者的有效性和安全性[30]。在全球18个国家104个临床研究中心共计招募551位CABP患者, 通过“肺炎患者预后研究小组” (pneumonia patient outcomes research team, PORT) 评分系统对551位成人患者的肺炎严重程度进行评估, 结果显示除一位患者为轻症外, 其余患者的肺炎风险分级预后评分指数均大于等于Ⅲ, 72.1%的患者为中度或重度肺炎。采用随机分组的方法将患者分为两组, 其中一组每12 h静脉注射Lefamulin 150 mg, 另一组静脉注射莫西沙星400 mg, 对疑似感染耐甲氧西林金葡菌的患者, 除注射莫西沙星以外, 每12 h再静脉注射利奈唑胺600 mg, 而Lefamulin则辅以安慰剂。治疗周期一般为7 d, 感染耐甲氧西林金葡菌的患者治疗周期延长至10 d。如果符合预先确定的标准, 在3 d或至少6次用药后, 研究人员可以将给药方案改为每12 h口服Lefamulin 600 mg或每日口服莫西沙星400 mg (辅助利奈唑胺每12 h 600 mg)。
美国FDA设定的主要终点是首次给药后96 ± 24 h的早期临床反应(early clinical response, ECR)。在ITT人群的非劣效界值为12.5%, EMA根据mITT人群和CE人群在最后一次用药5~10 d后的临床反应(investigator assessment of clinical response, IACR) 评估了主要终点(非劣效界值, 10%)。ECR被定义为病人存活, 在当前FDA指南中概述的4种主要CABP症状中(如呼吸困难、咳嗽、脓性痰的产生和胸痛), 至少有两种症状有所改善, 4种主要症状中的任何一种都无恶化, 并且在首次服用研究药物后的120 h内没有接受除利奈唑胺以外的抗生素治疗CABP。
在随机分配的276例接受Lefamulin治疗的患者中, 共计273位患者接受过不少于1次药物治疗(mITT), 其中236位患者完成了整个治疗方案, 对9名疑似感染耐甲氧西林金葡菌的患者进行了辅助安慰剂治疗。在275例接受莫西沙星治疗的患者中, 共计273患者至少接受过不少于1次药物治疗(mITT), 其中245位患者完成了整个治疗方案, 14名患者疑似感染耐甲氧西林金葡菌, 辅助利奈唑胺治疗。在早期临床应答率上, Lefamulin组和莫西沙星±利奈唑胺组早期临床应答率分别为87.3%和90.2% (差异为-2.9%, 95%的置信区间为-8.5%~2.8%)。在用药5~10 d后的临床反应率上, Lefamulin组和莫西沙星±利奈唑胺组在mITT人群临床应答率分别为81.7%和84.2% (差异为-2.6%, 95%的置信区间为-8.9%~3.9%); CE人群对应的临床应答率分别为86.9%和89.4% (差异为-2.5%, 95%的置信区间为-8.4%~3.4%)。此外, 两组中均出现了由治疗突发不良反应导致的停药, Lefamulin组的停药率为2.9%, 莫西沙星±利奈唑胺组为4.4%。Lefamulin组和对照组的患者病原微生物分布相似, 最常见的分离微生物是肺炎链球菌(190例)、卡他莫拉氏菌(107例)、非典型微生物(101例)、金葡菌(45例) 和流感嗜血杆菌(15例)。LEAP1首次证明了Lefamulin在主要疗效终点方面不劣于莫西沙星, 总体上安全且耐受性良好[30]。
为了进一步评价口服Lefamulin治疗CABP的疗效和安全性, 在全球19个国家99个临床研究中心进行了Lefamulin的第二个Ⅲ期临床研究[8, 31] (LEAP2, 美国临床注册号: NCT02813694)。该临床研究采用非劣效性随机临床试验, 其入组要求是肺炎严重程度评分等级为Ⅱ、Ⅲ或Ⅳ, 急性, 影像学确诊, 同时出现至少3种CABP症状并伴有两种或者以上生命体征异常。受试者随机分为两组, 共计招募738名成年CABP患者(平均年龄57.5岁; 女性351名; 360名患者的肺炎严重程度评分等级为Ⅲ或Ⅳ类), Lefamulin治疗组的给药方案为连续5 d每12 h口服Lefamulin 600 mg (n = 370), 对照组的给药方案为连续7 d每24 h口服莫西沙星400 mg (n = 368)。依据美国FDA主要终点评价标准, Lefamulin和莫西沙星的早期临床有效率均为90.8% (差异为0.1%, 95%的置信区间为-4.4%~4.5%)。在用药5~10 d后, Lefamulin组和莫西沙星组在mITT人群中的临床应答率分别为87.5%和89.1% (差异为-1.6%, 95%的置信区间为-6.3%~3.1%); 在CE人群中临床应答率分别为89.7%和93.6% (差异为-3.9%, 95%的置信区间为-8.2%~0.5%)。LEAP2的临床数据表明, 口服Lefamulin 600 mg (其口服生物利用度约为0.25) 与LEAP1静脉注射Lefamulin 150 mg对CABP具有非劣效的治疗效果。
在药物安全性和耐受性方面, Lefamulin组和莫西沙星组呈现出较为类似的临床结果(表 6)。在LEAP1临床研究中, Lefamulin组中38.1% (104/273) 的患者至少发生过一次与治疗相关的不良反应, 其中轻度治疗突发性不良反应(treatment-emergent adverse event, TEAE) 和严重TEAE占比分别为15.0%和7.0%。莫西沙星±利奈唑胺组中有37.7% (103/273) 的患者至少发生过一次不良反应, 轻度TEAE和严重TEAE占比分别为14.3%和4.8%。各组之间轻度TEAE和严重TEAE的发病率相似, 药物相关不良反应的发生率也相似, 但是Lefamulin注射后更有可能出现注射部位疼痛的症状。在LEAP2临床研究中, Lefamulin组中32.6% (120/368) 的患者至少发生过一次治疗相关的不良反应, 其中轻度TEAE和严重TEAE占比分别为15.8%和4.6%。莫西沙星±利奈唑胺组中有25.0% (92/368) 的患者至少发生过一次不良反应, 其中轻度TEAE和严重TEAE占比分别为7.9%和4.9%。Lefamulin组和莫西沙星组由于TEAE导致的停药率(3.3% vs 2.4%) 基本类似, 但是胃肠道相关不良反应的发生率差异较为显著, 包括腹泻/大便失禁(12.2% vs 1.1%)、恶心(5.2% vs 1.9%)、呕吐(3.3% vs 0.8%), 值得注意的是这些不良反应并未在LEAP1中转口服Lefamulin 600 mg的患者中出现[31]。
| 表 6 Treatment-related adverse effects > 1% for Lefamulin in LEAP1 and LEAP2 trial. ALT: Alanine aminotransferase; AST: Aspartate aminotransferase |
Lefamulin作为第一个用于治疗人类全身性细菌感染的截短侧耳素类药物, 抗菌谱广、安全性高、适用范围较广, 且具有口服和注射给药方式, 对多种常见和难治性感染都具有潜在疗效, 其未来的临床应用空间很大[32]。在CABP的治疗中, Lefamulin具有较高的肺渗透性和有效性, 保证了药物在病灶部位具有较高的暴露量(有效率)。同时Lefamulin避免了氟喹诺酮类抗生素引起的不良反应, 并对大环内酯类耐药的肺炎支原体和肺炎链球菌仍具有较好的抑制活性, 因此可以作为大环内酯类和氟喹诺酮类抗生素的替代药物, 为CABP患者提供了新的选择。截短侧耳素类药物的广谱抗菌活性使其在耐药菌感染的治疗中具有广阔的应用前景, 可以为多药耐药的细菌感染提供新的解决方案。在截短侧耳素为母核结构的抗菌药物开发路上, Lefamulin是一个里程碑式的成功, 同时也为该类复杂母核天然产物的抗菌临床应用拉开了全新的序幕。
作者贡献: 李雪瑶、李天磊负责组织文章的框架、文章的撰写及修改; 吴松负责了文章的思路指导和审阅; 李吉顺、朱子豪、李陶汀月负责资料的收集和整理; 张文轩和夏杰对稿件进行了完善。
利益冲突: 所有作者声明不存在利益冲突。
| [1] |
Levy SB, Marshall B. Antibacterial resistance worldwide: causes, challenges and responses[J]. Nat Med, 2004, 10: S122-S129. DOI:10.1038/nm1145 |
| [2] |
Zhu YG, Johnson TA, Su JQ, et al. Diverse and abundant antibiotic resistance genes in Chinese swine farms[J]. Proc Natl Acad Sci U S A, 2013, 110: 3435-3440. DOI:10.1073/pnas.1222743110 |
| [3] |
Veve MP, Wagner JL. Lefamulin: review of a promising novel pleuromutilin antibiotic[J]. Pharmacotherapy, 2018, 38: 935-946. DOI:10.1002/phar.2166 |
| [4] |
Daum RS, Kar S, Kirkpatrick P. Retapamulin[J]. Nat Rev Drug Discov, 2007, 6: 865-866. DOI:10.1038/nrd2442 |
| [5] |
Kavanagh F, Hervey A, Robbins WJ. Antibiotic substances from basidiomycetes: Ⅷ. Pleurotus multilus (Fr.) Sacc. and Pleurotus passeckerianus Pilat[J]. Proc Natl Acad Sci U S A, 1951, 37: 570-574. DOI:10.1073/pnas.37.9.570 |
| [6] |
Goethe O, Heuer A, Ma X, et al. Antibacterial properties and clinical potential of pleuromutilins[J]. Nat Prod Rep, 2019, 36: 220-247. DOI:10.1039/C8NP00042E |
| [7] |
Hunt E. Pleuromutilin antibiotics[J]. Drugs Future, 2000, 25: 1163-1168. DOI:10.1358/dof.2000.025.11.858699 |
| [8] |
Lefamulin evaluation against pneumonia (LEAP2Phase) 3 topline Results[EB/OL]. https://investors.nabriva.com/static-files/5c34b447-99cc-4739-b9d6-d4ea4c7d13b9.
|
| [9] |
Poehlsgaard J, Douthwaite S. The bacterial ribosome as a target for antibiotics[J]. Nat Rev Microbiol, 2005, 3: 870-881. DOI:10.1038/nrmicro1265 |
| [10] |
Merk A, Bartesaghi A, Banerjee S, et al. Breaking cryo-EM resolution barriers to facilitate drug discovery[J]. Cell, 2016, 165: 1698-1707. DOI:10.1016/j.cell.2016.05.040 |
| [11] |
Eyal Z, Matzov D, Krupkin M, et al. A novel pleuromutilin antibacterial compound, its binding mode and selectivity mechanism[J]. Sci Rep, 2016, 6: 39004. DOI:10.1038/srep39004 |
| [12] |
Poulsen SM, Karlsson M, Johansson LB, et al. The pleuromutilin drugs tiamulin and valnemulin bind to the RNA at the peptidyl transferase centre on the ribosome[J]. Mol Microbiol, 2001, 41: 1091-1099. |
| [13] |
Paukner S, Sader HS, Ivezic-Schoenfeld Z, et al. Antimicrobial activity of the pleuromutilin antibiotic BC-3781 against bacterial pathogens isolated in the SENTRY antimicrobial surveillance program in 2010[J]. Antimicrob Agents Chemother, 2013, 57: 4489-4495. DOI:10.1128/AAC.00358-13 |
| [14] |
Sader HS, Paukner S, Ivezic-Schoenfeld Z, et al. Antimicrobial activity of the novel pleuromutilin antibiotic BC-3781 against organisms responsible for community-acquired respiratory tract infections (CARTIs)[J]. J Antimicrob Chemother, 2012, 67: 1170-1175. DOI:10.1093/jac/dks001 |
| [15] |
Mendes RE, Farrell DJ, Flamm RK, et al. In vitro activity of lefamulin tested against Streptococcus pneumoniae with defined serotypes, including multidrug-resistant isolates causing lower respiratory tract infections in the United States[J]. Antimicrob Agents Chemother, 2016, 60: 4407-4411. DOI:10.1128/AAC.00627-16 |
| [16] |
Paukner S, Gelone SP, Arends SJR, et al. Antibacterial activity of lefamulin against pathogens most commonly causing community-acquired bacterial pneumonia: SENTRY Antimicrobial Surveillance Program (2015-2016)[J]. Antimicrob Agents Chemother, 2019, 63: e02161-18. |
| [17] |
Knöppel A, Näsvall J, Andersson DI. Evolution of antibiotic resistance without antibiotic exposure[J]. Antimicrob Agents Chemother, 2017, 61: e01495-17. |
| [18] |
Butler MM, Waidyarachchi SL, Connolly KL, et al. Aminomethyl spectinomycins as therapeutics for drug-resistant gonorrhea and chlamydia coinfections[J]. Antimicrob Agents Chemother, 2018, 62: e00325-18. |
| [19] |
Mendes RE, Doyle TB, Paukner S, et al. Molecular characterization of resistance mechanisms associated with pleuromutilins among gram-positive clinical isolates from the worldwide SENTRY surveillance studies for lefamulin[EB/OL]. https://www.nabriva.com/Portals/0/Assets/ASM_Microbe_SENTRY%2020152016%20resistance%20mechanisms_P642.pdf.
|
| [20] |
Wicha WW, Ivezic-Schoenfeld Z, Novak R. Pharmacokinetic, mass balance and tissue distribution of[14C]-BC-3781 in non-pigmented rats[EB/OL]. https://www.nabriva.com/Portals/0/Nabriva/Posters/ECCMID_2010/2010%20ECCMID_Nabriva%20poster%20909_abstract%202415_ADME%20BC-3781.pdf.
|
| [21] |
Wicha WW, Paukner S, Strickmann DB, et al. Pharmacokinetics-pharmacodynamics of lefamulin in a neutropenic murine lung infection model[EB/OL]. https://www.nabriva.com/Portals/_default/Skins/ProfessionalUs/pdfs/2015%20pharmacokinetics-pharmacodynamics-lefamulin-in-lung-infection.pdf.
|
| [22] |
Wicha WW, Kappes CB, Fischer E. Efficacy of lefamulin against Staphylococcus aureus induced bacteremia in a neutropenic and immunocompetent murine model[EB/OL]. https://www.nabriva.com/Portals/_default/Skins/ProfessionalUs/pdfs/Poster_1509_ID%20Week%202017_Vivo%20Bacteremia_Final.pdf.
|
| [23] |
Wicha WW, Henson C, Webbley K. Tissue distribution of[14C]-Lefamulin in the urogenital tract in rats[EB/OL]. https://www.nabriva.com/Portals/0/Nabriva/Posters/ECCMID_2018/ECCMID%202018%20QWBA-STI_Final.pdf.
|
| [24] |
Zeitlinger M, Schwameis R, Burian A, et al. Simultaneous assessment of the pharmacokinetics of a pleuromutilin, lefamulin, in plasma, soft tissues and pulmonary epithelial lining fluid[J]. J Antimicrob Chemother, 2016, 71: 1022-1026. DOI:10.1093/jac/dkv442 |
| [25] |
Wicha WW, Lell C, Seltzer E, et al. Pharmacokinetics and safety of an oral, immediate-release (IR) tablet formulation of lefamulin in fed and fasted healthy subjects[EB/OL]. https://www.nabriva.com/Portals/_default/Skins/ProfessionalUs/pdfs/2017-%20pharmacokinetics-immediate-release-tablet-%20p1336-be-study.pdf.
|
| [26] |
A Study to assess mass balance recovery, metabolite profile and identification of IV and oral 14C-BC-3781[EB/OL]. https://www.clinicaltrials.gov/ct2/show/NCT03131141?term=lefamulin&draw=2&rank=4.
|
| [27] |
Cates JE, Mitrani-Gold FS, Li G, et al. Systematic review and meta-analysis to estimate antibacterial treatment effect in acute bacterial skin and skin structure infection[J]. Antimicrob Agents Chemother, 2015, 59: 4510-4520. DOI:10.1128/AAC.00679-15 |
| [28] |
Prince WT, Ivezic-Schoenfeld Z, Lell C, et al. Phase Ⅱ clinical study of BC-3781, a pleuromutilin antibiotic, in treatment of patients with acute bacterial skin and skin structure infections[J]. Antimicrob Agents Chemother, 2013, 57: 2087-2094. DOI:10.1128/AAC.02106-12 |
| [29] |
Rubino CM, Xue B, Bhavnani SM, et al. Population pharmacokinetic analyses for BC-3781 using phase 2 data from patients with acute bacterial skin and skin structure infections[J]. Antimicrob Agents Chemother, 2015, 59: 282-288. DOI:10.1128/AAC.02033-13 |
| [30] |
File TM, Goldberg L, Das A, et al. Efficacy and safety of intravenous-to-oral lefamulin, a pleuromutilin antibiotic, for the treatment of community-acquired bacterial pneumonia: the phase Ⅲ lefamulin evaluation against pneumonia (LEAP 1) trial[J]. Clin Infect Dis, 2019, 69: 1856-1867. DOI:10.1093/cid/ciz090 |
| [31] |
Alexander E, Goldberg L, Das AF, et al. Oral lefamulin vs moxifloxacin for early clinical response among adults with community-acquired bacterial pneumonia: the LEAP 2 randomized clinical trial[J]. JAMA, 2019, 322: 1661-1671. DOI:10.1001/jama.2019.15468 |
| [32] |
Theuretzbacher U, Bush K, Harbarth S, et al. Critical analysis of antibacterial agents in clinical development[J]. Nat Rev Microbiol, 2020, 18: 286-298. DOI:10.1038/s41579-020-0340-0 |
 2020, Vol. 56
2020, Vol. 56


