2. 西南交通大学生命科学与工程学院, 四川 成都 610031;
3. 中国医学科学院基础医学研究所医学分子生物学国家重点实验室, 北京协和医学院基础学院生物化学系, 北京 100005;
4. 中药资源教育部工程研究中心, 北京 100193
2. School of Life and Science, Southwest Jiaotong University, Chengdu 610031, China;
3. State Key Laboratory of Medical Molecular Biology, Institute of Basic Medical Sciences, Chinese Academy of Medical Sciences, Department of Biochemistry, Peking Union Medical College, Beijing 100005, China;
4. Engineering Research Center of Chinese Medicine Resource, Ministry of Education, Beijing 100193, China
中药饮片质量关乎临床用药安全, 近年来各级药品监管部门持续加大对中药饮片监督检查和抽检力度, 依法查处和曝光违法违规企业和不合格产品, 中药饮片总体质量状况有所好转, 2019年全国中药材及饮片质量分析报告显示, 当年全国平均抽检合格率为91%, 较之前有所提升, 但仍存在掺伪掺杂现象, 如金银花与山银花、金钱草与广金钱草、木通与川木通、五加皮与香加皮等, 此外, 还存在染色剂增重、过度硫熏、虫蛀霉变等现象, 严重影响中药材及饮片质量[1]。国家药品监督管理局定期发布“关于药品不符合规定的通告”, 2020年1~10月共发文5次, 总计通报98批次药品不符合规定, 其中中药材及饮片27批次, 占比27.55%, 主要不符合规定的项目为性状、鉴别、含量测定等, 潜在影响临床用药安全。
“中药材DNA条形码分子鉴定法指导原则”自2014年首次被收载于《中国药典》 (2010年版第三增补本)[2]至今已有6年, 在各省市药品检验机构得到一定程度的推广应用。《中国药典中药材DNA条形码标准序列》一书为《中国药典》 (2015年版一部) 收载的动、植物药材提供了标准DNA条形码序列[3], 是采用DNA条形码技术鉴定中药材基原物种的重要依据。现行版《中国药典》 (2020年版四部) 除“中药材DNA条形码分子鉴定法指导原则”[4]外, 还收载“DNA测序技术指导原则”[5]、“标准核酸序列建立指导原则”[6]等, 显示分子鉴定方法在《中国药典》中所占比重逐渐加大。中药材DNA条形码分子鉴定法在中药材基原物种鉴定方面已有大量实践应用报道, 如羌活[7]、秦艽[8]、蛤蟆油[9]等, 亦有报道采用DNA条形码技术鉴定鹿茸饮片[10]及中药破壁饮片[11, 12], 但对于原料药材加工制成的饮片是否适用, 尚缺乏系统文献报道, 因此本研究拟对市售中药饮片基原物种进行鉴定, 验证该方法对中药饮片基原物种鉴定的适用性和准确性。
材料与方法材料 自药店购买常见中药饮片, 每种饮片1~2份, 按不同入药部位归类, 其中根及根茎73份, 果实种子52份, 全草45份, 花15份, 叶11份, 皮6份, 茎木4份, 其他(包括树脂、藻菌地衣等) 6份, 共计212份, 编号为JCS001~JCS212, 样品信息详见表 1。
| Table 1 Sample list and DNA barcoding identification results. "/" referred to genomic DNA degradation and no PCR product; "MI" referred to morphological identification |
DNA提取 参考《中国药典中药材DNA条形码标准序列》一书[3], 对各饮片样本进行前处理, 如: ①根及根茎类、茎木类饮片需用75%乙醇擦拭药材表面后晾干, 刮去外部栓皮, 取内部的饮片切成约2 mm3的小块; ②部分饮片多糖、多酚含量较高, 需加入样品量10%的PVP-40后再进行研磨; ③部分饮片多糖、色素、脂肪含量较高, 在研磨后需采用核分离液漂洗。依照《中国药典》 (2020年版四部) 收载“中药材DNA条形码分子鉴定法指导原则”[4]规定的不同入药部位DNA提取标准操作流程进行实验, 提取各饮片样本基因组DNA。
DNA条形码序列获得 DNA条形码序列扩增、测序及数据处理均依照“中药材DNA条形码分子鉴定法”标准操作流程(DNA barcoding SOP) 进行。参考《中国药典中药材DNA条形码标准序列》一书, 部分物种ITS2序列难以获取, 故扩增其psbA-trnH序列[3]。ITS2序列、psbA-trnH序列通用引物及反应程序见表 2。
| Table 2 Primers and PCR conditions used in the experiment |
物种判定 参照《中国药典》 (2020年版四部) 收载标准操作流程及前期文献[4, 13]报道, 采用“中药材DNA条形码鉴定系统(http://www.tcmbarcode.cn)”进行结果判定。对于不能获得DNA条形码序列或DNA条形码分子鉴定结果存在多个同属近缘物种的样本, 由中国医学科学院药用植物研究所标本馆林余霖研究员进行性状鉴定, 判定其基原物种。
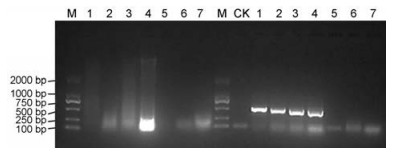
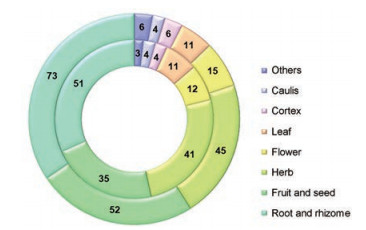
结果 1 市售中药饮片DNA条形码序列获取情况本研究共涉及中药饮片样本212份, 经DNA提取及PCR扩增后, 共有161份样本成功获得PCR扩增产物, 占收集中药饮片样本量的75.9%, 其中147份样本扩增ITS2序列, 12份样本扩增psbA-trnH序列, 2份样本扩增ITS2和psbA-trnH序列; 其余50份样本基因组DNA降解, 无法获得扩增产物; 此外, 1份样本为树脂(乳香), 不含基因组DNA, 故未进行DNA提取实验。以紫草、栀子、薄荷、鸡冠花、红参、苍耳子、莲房等为例展示不同入药部位中药饮片基因组DNA及ITS2序列PCR扩增产物电泳结果(图 1)。PCR扩增产物经纯化后进行双向测序, 测序结果经拼接后, 获得ITS2序列149条, psbA-trnH序列14条, 不同入药部位中药饮片样本获取DNA条形码序列数量见图 2。
|
Figure 1 Genomic DNA and PCR amplification results of ITS2 sequence of the commercial decoction pieces (Left side: Genomic DNA; Right side: PCR products). M: DL2000, CK: Negative control. 1: Zicao, 2: Zhizi, 3: Bohe, 4: Jiguanhua, 5: Hongshen, 6: Cangerzi, 7: Lianfang |
|
Figure 2 Sample size and the DNA barcoding sequence number of different medicinal parts of the decoction pieces. (Outer ring: Sample size; inner ring: DNA barcoding sequence number) |
采用“中药材DNA条形码鉴定系统(http://www.tcmbarcode.cn)”对实验所得161份中药饮片样本的ITS2序列或(和) psbA-trnH序列进行结果判定, 获得与该序列相似度最高的物种, 详细结果见表 1。结果显示, 161份饮片样本中, 138份样本为《中国药典》 (2020年版一部) 收载相应药材的基原物种, 占85.7%; 14份样本分析结果中包含《中国药典》收载相应药材的基原物种以及同属近缘物种, 分别为鸡骨草比对为广州相思子Abrus pulchellus subsp. cantoniensis/毛鸡骨草Abrus mollis, 野菊花比对为野菊Chrysanthemum indicum/毛华菊Chrysanthemum vestitum, 生枳壳、化橘红、佛手均比对为包含各自基原物种在内的同属多个物种, 佩兰比对为佩兰Eupatorium fortunei/轮叶泽兰Eupatorium lindleyanum, 炙甘草比对为甘草Glycyrrhiza uralensis/粗毛甘草Glycyrrhiza aspera/胀果甘草Glycyrrhiza eurycarpa, 川芎比对为川芎Ligusticum chuanxiong/藁本Ligusticum sinense/辽藁本Ligusticum jeholense/尖叶藁本Ligusticum acuminatum, 桑白皮、桑葚、桑叶均比对为桑Morus alba及其同属多个物种, 丹皮比对为牡丹Paeonia suffruticosa/凤丹Paeonia ostii/紫斑牡丹Paeonia rockii subsp. rockii, 车前子比对为车前Plantago asiatica/大车前Plantago major, 菊花比对为菊Chrysanthemum morifolium及其同属多个物种; 7份样本比对结果显示为混伪品, 分别为拳参比对为珠芽蓼Bistorta vivipara、金钱草比对为广金钱草Desmodium styracifolium (图 3)、旋覆花比对为条叶旋覆花Inula linariifolia、茺蔚子比对为细叶益母草Leonurus sibiricus、前胡比对为红前胡Peucedanum rubricaule/多苞藁本Ligusticum involucratum/羽苞藁本Ligusticum daucoides、鹿衔草比对为圆叶鹿蹄草Pyrola rotundifolia/红花鹿蹄草Pyrola incarnata/Pyrola grandiflora, 菊苣比对为苣荬菜Sonchus arvensis/翅果菊Lactuca indica; 2份样本比对结果显示样本中存在掺伪现象, 分别为地锦草和豨莶草, 其中地锦草饮片中检出萹蓄Polygonum aviculare, 豨莶草饮片中检出苍耳Xanthium sibiricum。
|
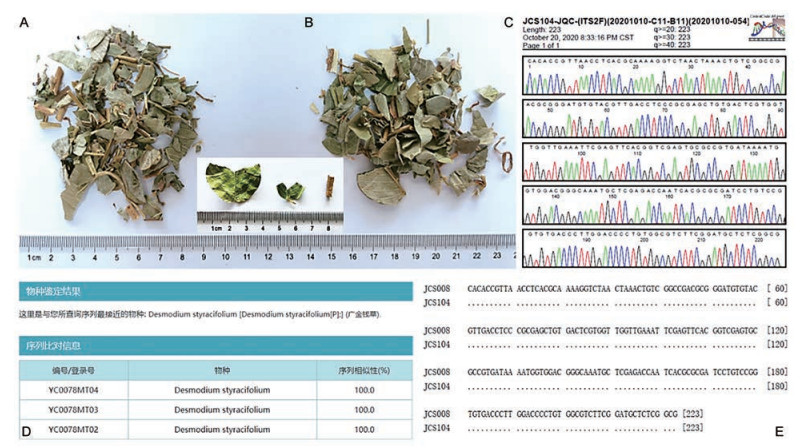
Figure 3 Morphological and DNA barcoding identification of Jinqiancao and Guangjinqiancao. A: Jinqiancao; B: Guangjinqiancao; C: Sequencing result of Guangjinqiancao; D: DNA barcoding identification with "DNA barcoding system for identifying herbal medicine"; E: ITS2 Sequence alignment of Jinqiancao and Guangjinqiancao |
上述结果显示, 本研究共有50份样本基因组DNA降解, 无法获得扩增产物, 1份样本为树脂类药材, 不含有基因组DNA; 14份样本分析结果中包含《中国药典》收载相应药材的基原物种以及同属近缘物种。为进一步确定以上65份饮片样本基原, 对其进行性状鉴定, 结果如下: ① 50份基因组DNA降解的样本, 38份鉴定为《中国药典》收载相应药材的基原物种, 3份样本鉴定为混伪品, 分别为百部鉴定为大百部Stemona tuberosa、首乌鉴定为木藤蓼Fallopia aubertii、金沸草鉴定为伪品(不能确定伪品物种), 9份样本缺少鉴别特征, 不能确定基原, 分别为川乌、桑皮、草乌、明党参、儿茶、橘核、木瓜、青皮、香薷; ② 1份树脂样本(乳香) 缺乏鉴别特征, 不能确定基原; ③ 14份分析结果包含同属近缘物种的样本, 8份样本鉴定为正品, 3份样本中掺有伪品, 分别为丹皮、鸡骨草、佩兰, 3份样本缺少鉴别特征, 不能确定基原, 分别为桑白皮、桑葚、炙甘草。详细结果见表 1。
综合DNA条形码鉴定及性状鉴定结果, 本研究涉及的212份样本中, 共有184份为正品, 占总样本量86.8%; 15份存在混伪/掺伪现象; 13份缺少鉴别特征, 无法确定基原。
讨论中药饮片是指在中医药理论指导下, 可直接用于调配或制剂的中药材及其加工炮制品。中药饮片包括部分经产地加工的中药切片(包括切段、块、瓣), 原形药材饮片以及经过切制(在产地加工的基础上)、炮炙的饮片。中药饮片既能直接配方使用, 如制丸剂、散剂, 又可以继续加工, 如煎制汤剂、熬制膏方, 亦或用于中成药生产, 其真伪优劣直接关乎患者生命健康安全。中药饮片在炮制加工过程中会损失部分性状鉴别特征, 且较之原药材而言更易发生掺伪现象, 使得中药饮片真伪鉴定难度加大。本研究涉及的212份样本均为普通民众在药店中极易获取的中药饮片, DNA条形码分子鉴定结果显示138份样本为《中国药典》 (2020年版一部) 收载相应药材的基原物种, 占获得序列样本数的85.7%; 14份样本分析结果中包含《中国药典》收载相应药材的基原物种以及同属近缘物种, 占获得序列样本数的8.7%; 另有9份样本存在掺伪/混伪现象, 占获得序列样本数的5.6%。以上结果表明, 中药材DNA条形码分子鉴定技术基本适用于市售中药饮片的基原物种鉴定工作, 能够有效检出市售中药饮片的掺伪/混伪现象, 值得在中药饮片加工生产企业及药品监督检验管理机构推广。
另有50份样本(占总样本量23.58%) 因炮制加工程度较高, 如蒸/煮透心、沙烫、炒焦、炒黄、炒炭等, 基因组DNA降解严重, 导致无法获取DNA条形码序列。该结果提示, 中药材DNA条形码分子鉴定法的常规标准操作流程对于炮制后的中药饮片适用性不佳, 为解决此问题, 本研究对上述样本进行性状鉴定, 38份鉴定为正品, 3份样本鉴定为混伪品, 显示性状鉴别方法在中药材及饮片基原鉴定工作中的重要性, 但该方法要求实施者具备扎实的中药鉴定学专业知识及丰富的饮片鉴别实践经验, 非专业人员掌握此方法难度较大。此外, 还可采用高通量测序技术对基因组DNA直接测序后通过生物信息学分析筛选并组装出DNA条形码序列[14], 或有针对性地在ITS2序列或psbA-trnH序列内部设计引物扩增其特异性短序列作为分子身份证[15, 16], 亦或设计TaqMan探针[17]等, 以此实现对基因组DNA降解严重的中药饮片的分子鉴定。
本研究发现, 饮片商品标签名称存在与实际物种不符, 或名称易混淆等现象。如商品标签名称为“地丁”的饮片, 单从名称来看无法确定是“紫花地丁”还是“苦地丁”, 但该份饮片样本中可见扁长椭圆形蒴果, 呈荚果状, 内含扁心形黑色具光泽的种子, 与《中国药典》 (2020年版一部) 收载“苦地丁”饮片的果实及种子性状特征描述一致, 其基原物种为地丁草Corydalis bungeana, 这与DNA条形码鉴定结果一致, 因此其商品标签应标注为“苦地丁”, 以免药店人员抓错药, 类似的情况还有“菖蒲”应明确标注为“石菖蒲”。另有部分饮片名称汉字有误, 如“紫苑”应写作“紫菀”, “山奈”应写作“山柰”, “化桔红”应写作“化橘红”等, 也值得从业人员重视。此外, 按《中国药典》 (2020年版一部) 规定, 中药金钱草基原物种为报春花科聚花过路黄Christina lysimachiae, 广金钱草基原物种为豆科广金钱草Desmodium styracifolium, 二者来源于不同科。但本研究涉及的商品标签名为“金钱草”和“广金钱草”的两种饮片外观性状极为相似、难以区分(图 3), 两个样本实验所得ITS2序列测序结果均质量极佳, 序列无变异位点, 经“中药材DNA条形码分子鉴定系统”分析证实两份饮片基原物种均为广金钱草Desmodium styracifolium。发生该现象的潜在原因有两点: ①因“金钱草”资源量及产量低于“广金钱草”, 且价格高于“广金钱草”, 饮片生产者有意用“广金钱草”替代“金钱草”出售, 从中牟利, 属于人为混伪; ②药店商品标签标识不清, 或从业人员专业知识水平有限, 未能明确区分两种饮片, 抓药时误将两种饮片当做同一种饮片出售给消费者。以上实例提示, 药店在出售饮片时应当依照《中国药典》规范标注饮片名称, 以免造成混淆, 影响临床用药安全。
又如中药“泽泻”, 《中国药典》 (2015年版一部) 收载其为泽泻科植物泽泻Alisma orientale (Sam.) Juzep.的干燥块茎, 然而依据《中国植物志》记载, 中文名“泽泻”对应的物种拉丁名应当为Alisma plantago-aquatica L., 而拉丁名Alisma orientale (Samuel.) Juz.对应的物种中文名应当为“东方泽泻”, 上述两个物种外观性状极为相似、难以区分, 且市场上均有销售, 属于因名称混淆导致的中药材混伪现象。文献报道显示DNA条形码技术能够有效鉴别上述两个物种, 虽然二者ITS2序列仅存在1个SNP位点, 但能够作为市售泽泻药材基原物种的鉴别特征[18], 显示DNA条形码分子鉴定技术的准确性。目前, 现行版《中国药典》 (2020年版一部) 已对中药“泽泻”的基原物种进行修订, 指明该药材来源于泽泻科东方泽泻Alisma orientale (Sam.) Juzep.或泽泻Alisma plantago-aquatica Linn., 而本研究涉及的饮片“泽泻”, 经DNA条形码鉴定为泽泻Alisma plantago-aquatica, 依照现行版《中国药典》, 应视为正品。
对于饮片“地锦草”和“豨莶草”, 在实验过程中发现所购饮片中存在性状明显不同的样本, 因此分别取样并进行DNA条形码分子鉴定, 结果显示, 饮片“地锦草”中检出“萹蓄”, “豨莶草”中检出“苍耳”, 上述药材或饮片因外观性状差异明显, 可直接区分, 故不属于混伪品, 发生此现象的潜在原因可能为: ①药材或饮片生产加工过程中, 因晾晒、切制或储藏位置相近, 工人在操作过程中无意识混入; ②不同药材及饮片混用生产线, 导致残存在机器中的前一种药材的碎片被混入后续加工的其他药材。该案例提示中药材及饮片生产加工企业应规范生产操作流程, 制定有效的监管措施, 避免此类情况发生。在新版《中华人民共和国药品管理法》实施后, 虽然取消了GMP认证, 但也意味着国家对药品监管措施更加严格, 中药全产业链都应当从根本上重视原材料的准确性, DNA条形码分子鉴定技术在中药全产业链各关键环节发挥其重要作用[19, 20], 有助于保证中药产业健康发展, 推动中药走向世界。
中医药作为凝聚中华民族传统哲学智慧的宝库, 为人类健康做出的贡献举世瞩目。自抗疟药青蒿素的发现获得2015年诺贝尔生理学或医学奖以来, 公众对中医药的关注程度日渐加深, 本草基因组学为传统中药和现代生命科学架起沟通的桥梁[21], 大量西医学或生命科学领域的研究人员开始将目光投向中药, 并从不同角度对中药药效的作用机制展开探讨。例如, 研究人员在金银花水煎液中发现一种miRNA——MIR2911, 它能够显著抑制H1N1、H5N1、H7N9病毒复制, 且显著降低感染H5N1病毒小鼠的死亡率, 这是中药中发现的首个直接作用于流感病毒(IAVs) 的活性成分[22]。此外, 最新研究表明, MIR2911能够显著抑制SARS-CoV-2病毒(新型冠状病毒) 复制, 且在临床上能加速患者转阴[23]。蒋澄宇研究员团队发现红景天中的miRNA HJT-sRNA-m7可有效降低肺纤维化标志基因及蛋白表达水平, 创新性提出中药材miRNA可作为口服药物的治疗策略[24]。以上研究均为中药创新药物研发提供新思路。但因非中医药领域的研究人员对中药鉴定学专业知识了解有限, 在选定研究对象后, 去市场上直接购买药材或饮片时, 无法准确判断所购药材或饮片是否为《中国药典》收载的正品基原物种, 存在买到混伪品或掺伪品的可能性。如若开展实验前未对所购样品进行基原鉴定, 可能获得与预期不一致的实验结果, 影响研究进度, 亦会造成科研经费及资源浪费。因此, 建议在实验前务必对实验材料进行基原鉴定。中药材DNA条形码分子鉴定技术操作简便、快捷, 非专业人员也能够在短时间内掌握该技术, 因而值得向其他学科研究人员推广该技术, 辅助其研究工作顺利进行, 同时也有助于促进中药学研究的跨学科交流, 共同挖掘中药作用靶点和药效机制, 推动个性化精准医疗及“精准药物研发”。
作者贡献: 辛天怡负责实验设计、数据分析及文章撰写;娄千、郝利军、李冉郡、许文杰和马婷玉负责饮片DNA条形码鉴定实验工作;林余霖负责饮片性状鉴定工作;林烨暄和董一昕负责市售饮片样本收集工作;蒋澄宇参与实验设计、样本收集等工作;宋经元负责实验设计、总体把关和稿件修改等工作。
利益冲突: 本文的研究内容无任何利益冲突。
| [1] |
Zhang P, Li N, Li M, et al. Report of supervision and quality of Chinese materia medica and decoction pieces in 2019[J]. Mod Chin Med (中国现代中药), 2019, 22: 663-671. |
| [2] |
State Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2010 Ed. Enlarged text Ⅲ. Beijing: China Medical Science Press, 2014: 92-94.
|
| [3] |
Chen SL. Standard DNA Barcodes of Chinese Material Medica in Chinese Pharmacopoeia (中国药典中药材DNA条形码标准序列)[M]. Beijing: Science Press, 2015.
|
| [4] |
State Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2020 Ed. Part IV. Beijing: China Medical Science Press, 2020: 490-492
|
| [5] |
State Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2020 Ed. Part IV. Beijing: China Medical Science Press, 2020: 492-493.
|
| [6] |
State Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2020 Ed. Part IV. Beijing: China Medical Science Press, 2020: 493-494.
|
| [7] |
Xin T, Yao H, Luo K, et al. Stability and accuracy of the identification of Notopterygii Rhizoma et Radix using the ITS/ITS2 barcodes[J]. Acta Pharm Sin (药学学报), 2012, 47: 1098-1105. |
| [8] |
Luo K, Ma P, Yao H, et al. Identification of Gentianae Macrophyllae Radix using the ITS2 barcodes[J]. Acta Pharm Sin (药学学报), 2012, 47: 1710-1717. |
| [9] |
Shi L, Liu J, Tang X, et al. Herbalogical studies of Ranae Oviductus (Hamayou) and its species identification using DNA barcoding method[J]. Sci Sin Vit (中国科学·生命科学), 2019, 49: 1032-1040. DOI:10.1360/N052018-00231 |
| [10] |
Zhang R, Liu C, Huang L, et al. Study on the identification of Comu Cervi Pantotrichum with DNA barcoding[J]. Chin Pharm J (中国药学杂志), 2011, 46: 263-266. |
| [11] |
Xiang L, Tang H, Cheng J, et al. The species traceability of the ultrafine powder and the cell wall-broken powder of herbal medicine based on DNA barcoding[J]. Acta Pharm Sin (药学学报), 2015, 50: 1660-1667. |
| [12] |
Zheng X, Lai Z, Cheng J. Application of DNA barcoding technology in species identification of ultrafine granular powder of herbal medicine[J]. Mod Chin Med (中国现代中药), 2016, 18: 846-850. |
| [13] |
Chen S, Pang X, Song J, et al. A renaissance in herbal medicine identification: from morphology to DNA[J]. Biotechnol Adv, 2014, 32: 1237-1244. DOI:10.1016/j.biotechadv.2014.07.004 |
| [14] |
Xin T, Su C, Lin Y, et al. Precise species detection of traditional Chinese patent medicine by shotgun metagenomic sequencing[J]. Phytomedicine, 2018, 47: 40-47. DOI:10.1016/j.phymed.2018.04.048 |
| [15] |
Gao Z, Liu Y, Wang X, et al. Derivative technology of DNA barcoding (nucleotide signature and SNP double peak methods) detects adulterants and substitution in Chinese patent medicines[J]. Sci Rep, 2017, 7: 5858. DOI:10.1038/s41598-017-05892-y |
| [16] |
Liu Y, Wang X, Wang L, et al. A nucleotide signature for the identification of American ginseng and its products[J]. Front Plant Sci, 2016, 7: 319. |
| [17] |
Yun K, Xiang L, Wang X, et al. Identification of Ophiocordyceps sinensis and its adulterants based on portable and CFX96 real-time fluorescent PCR systems[J]. Acta Pharm Sin (药学学报), 2019, 54: 746-752. |
| [18] |
Ma X, Yao H, Xin T, et al. SNP identification of Alisma orientale, Alisma plantago-aquatica and Alismatis Rhizoma in the market based on DNA Barcoding[J]. Chin Pharm J (中国药学杂志), 2015, 50: 746-752. |
| [19] |
Lou Q, Xin T, Song J. Application of DNA barcoding technology in the whole industrial chain of traditional Chinese medicine[J]. Acta Pharm Sin (药学学报), 2020, 55: 1784-1791. |
| [20] |
Li R, Xin T, Song L, et al. Research progress on the original species identification in the indus-try chain of Rhei Radix et Rhizoma[J]. China J Chin Mater Med (中国中药杂志), 2020. DOI:10.19540/j.cnki.cjcmm.20201207.60 |
| [21] |
Xin T, Zhang Y, Pu X, et al. Trends in herbgenomics[J]. Sci China Life Sci, 2019, 62: 288-308. DOI:10.1007/s11427-018-9352-7 |
| [22] |
Zhou Z, Li X, Liu J, et al. Honeysuckle-encoded atypical microRNA2911 directly targets influenza A viruses[J]. Cell Res, 2015, 25: 39-49. DOI:10.1038/cr.2014.130 |
| [23] |
Zhou L, Zhou Z, Jiang X, et al. Absorbed plant MIR2911 in honeysuckle decoction inhibits SARS-CoV-2 replication and accelerates the negative conversion of infected patients[J]. Cell Discov, 2020, 6: 54. |
| [24] |
Du J, Liang Z, Xu J, et al. Plant-derived phosphocholine facilitates cellular uptake of anti-pulmonary fibrotic HJT-sRNA-m7[J]. Sci China Life Sci, 2019, 62: 309-320. DOI:10.1007/s11427-017-9026-7 |
 2021, Vol. 56
2021, Vol. 56


