2. 南京中医药大学药学院, 江苏 南京 210023
2. School of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China
急性呼吸道感染是由多种微生物包括细菌、病毒、支原体、真菌、寄生虫等引起的感染性疾病[1]。根据部位不同又分为上呼吸道感染和下呼吸道感染, 临床可出现相应症状, 如发热、咳嗽、咳痰、呼吸困难等, 且非常容易形成聚集性流行, 不同年龄段人群均易感染[2]。中医认为, 急性呼吸道感染属于中医学“时行感冒”范畴, 病因以感受风邪为主, 亦有感受时邪疫毒而致者, 具有“肺脏娇弱, 脾常不足, 肝常有余”的生理特点[3]。多年的临床实践表明, 中医药在防治急性呼吸道感染中, 因疗效确切、不良反应较小, 其在临床上的实际治疗特色完善了临床定位, 包括退热、改善临床症状和抑制流感病毒3个方面, 越来越受到重视[4]。中成药蒲地蓝消炎口服液(PDL) 由黄芩(君)、蒲公英(臣)、板蓝根(佐使) 和苦地丁(佐使) 四味药组方而成, 共奏清热解毒、抗炎消肿之效, 临床上常用于急性呼吸道感染的治疗, 效果良好[5]。Yang等[6]报道PDL对脂多糖(lipopolysaccharides, LPS) 所致大鼠急性肺损伤具有保护作用, 可减轻与NF-κB、IL-10表达相关的肺组织炎症反应, 并对组织病理损伤有修复作用。LPS是革兰阴性菌主要细胞表面抗原和激发宿主对细菌感染发生反应的主要生物效应器, 它可以激活单核-巨噬细胞系统(mononuclear phagacytic system, MPS), 释放大量炎症介质(TNF-α、IL-12、IFN-γ等), 导致全身过度炎症反应, 常被用作急性呼吸道感染的造模剂[7]。
作为在整体观指导下中医临床治疗的主要手段, 中医方剂常被视作一个复杂体系, 其通过有协同作用的活性成分与人体生物学网络之间存在的复杂调控网络对人体施加疗效。因此, 在新的层面上采用网络化的整合策略系统开展中医药复杂体系的整体调控作用机制研究有其必要性[8]。作为系统生物学(system biology) 主要技术之一的代谢组学(metabolomics), 是研究某一生物或细胞在一特定生理时期内所有的低分子量代谢产物的一门学科[9]。同系统生物学中的蛋白质组学与基因组学等其他组学相比, 它更能反映细胞、组织、体液或生物体的表型(phenotype), 并能帮助探究物质在体内正在发生或已经发生的代谢[10]。本课题组前期通过建立宽范围代谢组学研究策略并结合网络药理学技术手段研究了“清上补下第一方”二至丸治疗肝肾阴虚证的作用机制, 为基于生物网络的中药复方作用机制研究做出了有益地探索[11]。因此, 本文拟以GC-MS的血清代谢组学为技术手段, 结合多变量数据处理方法筛选LPS诱导小鼠急性呼吸道感染的生物标记物, 并基于网络药理学手段构建相关生物网络探讨PDL抗急性呼吸道感染的作用机制。
材料与方法实验动物 ICR小鼠50只(约25 g左右), 雌雄各半, 动物合格证号SCXK (苏) 2012-0004, 由南京市江宁区青龙山动物繁殖场提供。实验动物所有操作均严格按照南京中医药大学动物伦理委员会标准执行(批准号: 201906A029)。
药品与试剂 蒲地蓝消炎口服液(批号1807012, 济川药业集团有限公司); 拜阿司匹林乙醚(上海马陆化工厂); 甲醇(德国Merck公司); 1, 2-13C-肉豆蔻酸、吡啶、N, O-双三甲基硅基三氟乙酰胺(BSTFA)、甲氧基胺盐酸盐(美国Sigma-Aldrich公司); 正己烷(美国ROE Scientific公司); 氯化钠(江苏太仓化工厂); 娃哈哈纯净水。
仪器 低速台式离心机TDL-80-2B, 上海安亭科学仪器厂; Milli-Q超纯水系统, 美国Millipore公司; New Classic MS型分析天平(d = 0.01 mg), METTLER TOLEDO; KH-500B型超声清洗器, 昆山市超声仪器有限公司; Trace 1310气相系统(美国Thermo); 色谱柱: TG-5MS毛细管色谱柱(0.25 mm×30 m, 0.25 μm); TSQ 8000质谱仪(Thermo公司)。
动物实验与样品收集 50只ICR小鼠按体重随机分为5组, 每组10只即对照组、模型组、PDL低剂量组(1.3 mL·kg-1)、中剂量组(3.9 mL·kg-1)、高剂量组(11.7 mL·kg-1)。PDL各剂量组给予相应剂量药物, 每天1次, 连续5天后, 空白组和模型组灌胃同等剂量的生理盐水。末次给药1 h后, 除空白组外, 其余各组复制呼吸道损伤模型, 将小鼠使用异氟烷麻醉后, 用LPS (2 mg·kg-1) 给予小鼠滴鼻造模, 空白组滴入相同体积生理盐水, 造模12 h后进行取材。各组小鼠摘眼球取血, 分离血清, 置于-80 ℃保存, 进行后续生化指标及代谢组学的检测。
GC-MS样品前处理 取上述血清50 μL, 加入预冷(-80 ℃) 的含13C-肉豆蔻酸(12.5 μg·mL-1) 的甲醇溶液200 μL。涡旋3min, 14 000 r·min-1离心10 min, 吸取上清液100 μL于1.5 mL EP管中, 30 ℃真空离心浓缩仪挥干。在已挥干的EP管中加10 mg·mL-1甲氧胺吡啶30 μL, 涡旋5 min, 30 ℃振荡1.5 h后, 继续加入双(三甲基硅烷基) 三氟乙酰胺溶液[bis (trimethylsilyl) trifluoroacetamide, BSTFA] 30 μL, 涡旋5 min, 37 ℃振荡0.5 h, 最后将样品在4 ℃下, 14 000 r·min-1离心10 min, 取上清进样。
GC-MS分析条件 美国Thermo Fisher Scientific公司Trace 1310气相系统, TG-5MS毛细管色谱柱(0.25 mm×30 m, 0.25 μm), 采用程序升温: 起始温度设为60 ℃, 维持1 min, 再以每分钟20 ℃的速率升温至320 ℃, 维持5 min。载气为氦气, 流量为1.2 mL·min-1, 进样口温度为300 ℃, 采用分流进样, 分流流速为24.0 mL·min-1, 分流比为20:1, 进样量为1 μL。Thermo公司TSQ 8000质谱仪, 采用电子轰击离子化(EI电离源), 电子能量为70 eV, 传输线温度为300 ℃, 离子源温度为300 ℃。质谱采用一级全扫描的采集方式, 起始扫描时间为3.8 min, 扫描范围为m/z 50~500。
多变量数据处理 将GC-MS采集的色谱质谱图谱信息, 使用MS-DIAL软件进行色谱峰提取(最小峰高: 10 000, 质量宽度: 0.5 Da, 质量准确度: 0.5 Da), 并结合NIST鉴定化合物[12]。将提取得到的各物质峰高与内标物峰高比值进行数据归一化, 所得数据矩阵导入多变量数据处理软件SIMCA-P 13.0进行多维统计分析, 采用偏最小二乘法判别分析(PLS-DA) 筛选对分组贡献大的差异变量。采用SPSS软件对筛选到的差异变量的质谱响应在对照组和模型组中按是否满足正态分布进行独立双样本T检验或曼-惠特尼非参数检验, 以同时满足VIP > 1和P < 0.05选取具有显著性的差异变量, 寻找有可能反映LPS诱导小鼠急性呼吸道感染及PDL治疗作用的潜在生物标志物。借助MetaboAnalyst 4.0 (http://www.metaboanalyst.ca/) 对数据进行聚类分析及代谢通路分析。
生物网路的构建与分析 采用MetaboAnalyst通路分析工具, 对鉴别出的潜在生物标志物进行通路富集分析和通路拓扑分析。上述KEGG通路通过Cytoscape的插件Cytokegg搜索导入, 利用软件的Merge功能将所有通路整合到一起, 建立代谢物-通路蛋白网络。通过GeneCards网站输入关键词“respiratory tract (呼吸道)”、“infection (感染)”搜索疾病蛋白, 通过韦恩图求通路蛋白和疾病蛋白的交集。采用Metascape对筛选出的共有蛋白进行GO富集分析和靶点通路富集分析。将韦恩图所得共有蛋白导入STRING (https://string-db.org/) 在线数据库分析, 得到蛋白质-蛋白质相互作用网络(PPI网络), 网络导入Cytoscape软件, 利用其CytoHubba插件对网络中的节点以最大集团中心度(maximal clique centrality, MCC) 进行排名, 获得排名前十的蛋白为潜在治疗靶点。
结果与讨论 1 血清抗炎指标的检测为研究PDL对LPS诱导的急性呼吸道感染小鼠的抗炎作用, 本文检测了血清中的炎症相关细胞因子NF-κB, TNF-α和IL-10, 结果见图 1。模型组促炎细胞因子(NF-κB和TNF-α) 与对照组相比明显增加(P < 0.01, P < 0.0001), 抑制炎症细胞因子(即IL-10) 低于阴性对照组(P < 0.05) LPS处理后。虽然不同浓度的PDL均可显著回调LPS诱导的NF-κB、TNF-α和IL-10水平, 但是高剂量的PDL在三个指标上表现出最好的抗炎作用。上述结果表明LPS能够成功诱导小鼠的急性呼吸道感染模型, PDL高剂量组可以起到显著的预防作用。因此, PDL高剂量组的小鼠血清用于后期的代谢组学研究, 可以获取更多的代谢物信息。

|
Figure 1 The effect of Pudilan Xiaoyan oral liquid (PDL) on the expression of related inflammatory cytokines in mice serum (n = 10, x±s). PDL-H, PDL-M and PDL-L represent the high, middle and low dose of PDL for mice, respectively. #P < 0.05, ##P < 0.01, ####P < 0.000 1 vs control group; *P < 0.05, **P < 0.01, ***P < 0.001, ****P < 0.000 1 vs model group |
为了研究与LPS诱导小鼠呼吸道感染相关的血清内源性代谢标志物以及PDL的可能防治作用, 结合前期的抗炎作用研究结果, 将对照组、模型组和PDL高剂量组的多维数据矩阵导入SIMCA-P 13.0建立PLS-DA模型(R2Y = 0.859, Q2 = 0.798), 一般认为R2Y及Q2值大于0.5的模型良好, 因此该模型拟合较好, 稳定性较高。从图 2A可以看出PDL防治组相对于模型组更加接近于对照组, 说明PDL对于LPS诱导的呼吸道感染具有一定的恢复作用, 这与血清炎性细胞因子的检测结果一致。为了进一步分析LPS诱导小鼠呼吸道感染后的血清代谢物变化, 本文建立对照组和模型组的PLS-DA模型(图 2B, R2Y = 0.953, Q2 = 0.849), 并采用100次的置换检验模型验证(图 2C) 可以看出, 位于左边的R2Y值(模拟) 均低于最右侧的R2Y, Q2Y值(模拟) 均低于右侧的Q2Y值, 且Q2的回归线截距为负(-0.249), 说明该模型预测能力较好, 没有出现过拟合现象, 而该拟合良好的PLS-DA模型变量的VIP值(图 2D) 可以用于寻找对分类比较重要的显著性变量。

|
Figure 2 Multivariate analysis of GC-MS metabolomics data. A: PLS-DA score plot of the control group, model group and PDL high-dose group; B: PLS-DA score plot of the control group and model group; C: PLS-DA model verification of control group and model group; D: VIP value of variable in PLS-DA model of control group and model group |
首先根据对照组和模型组构建的PLS-DA模型的VIP值和T检验或者非参数检验的P值, 以同时满足VIP > 1和P < 0.05选取显著性差异变量共12个。对筛选到的差异变量在给药组中的变化进行独立样本T检验或者曼-惠特尼非参数检验, 选取检验结果P < 0.05变量作为给药组相对于模型组的差异显著性变量, 在上述12个内源性物质中共发现有8个存在显著性变化, 结果见表 1。相比对照组, 模型组中1-单硬脂酸甘油酯(glycerol 1-octadecanoate)、3-磷酸甘油酸(3-phosphoglyceric acid)、左旋多巴(L-dopa)、α-氨基己二酸(aminoadipic acid)、D-核酮糖-5-磷酸(D-ribulose 5-phosphate)、β-甘露糖基甘油酸[2(α-D-mannosyl)-D-glycerate]、尿素(urea) 和1-棕榈酸单甘油酯(monopalmitin-1-glyceride) 的含量均显著下降, D-果糖(D-fructose)、D-麦芽糖(D-maltose)、鸟氨酸(ornithine) 和乙醇胺(ethanolamine) 的含量显著上升, 提示这12种内源性物质可能是LPS诱导的小鼠呼吸道感染血清潜在生物标志物, 而在给药组中这12个内源性代谢物均得到了不同程度的恢复, 其中3-磷酸甘油酸、α-氨基己二酸、D-核酮糖-5-磷酸、β-甘露糖基甘油酸、D-果糖、尿素、D-麦芽糖和鸟氨酸得到显著性回调。
| Table 1 Potential biomarkers of LPS-induced respiratory tract infection in mice serum and the intervention effect of PDL. *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
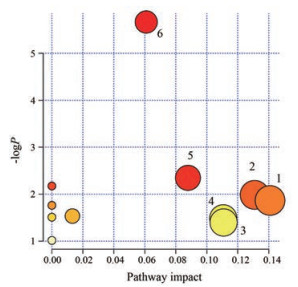
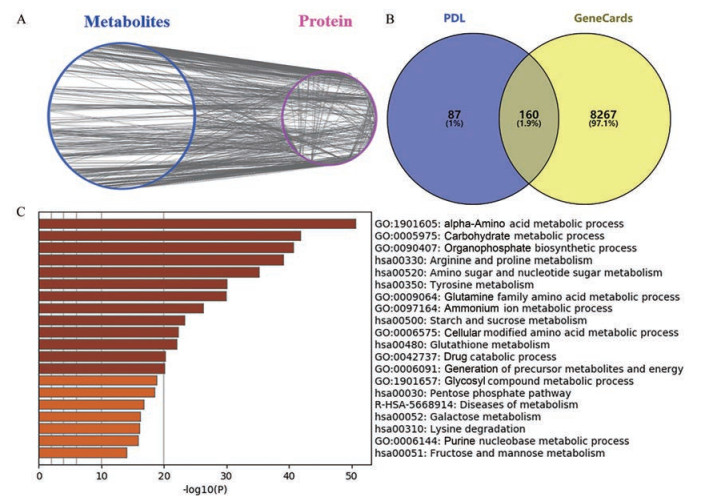
采用MetaboAnalyst通路分析工具, 对经模型组与对照组比较鉴别出的潜在生物标志物进行通路富集分析和通路拓扑分析, 发现影响较大的潜在靶向途径包括赖氨酸降解、磷酸戊糖途径、酪氨酸代谢、精氨酸和脯氨酸代谢、淀粉和蔗糖代谢、精氨酸生物合成等11条通路, 由通路分析的结果可以看出, 这些通路可能与LPS诱导的小鼠急性呼吸道感染最为相关(图 3)。将上述MetaboAnalyst所得到的KEGG通路通过Cytoscape的插件Cytokegg搜索导入软件, 利用软件的Merge功能将所有通路整合到一起, 建立代谢物(598种) 和通路蛋白(247种) 的关联网络, 见图 4A。通过GeneCards网站输入关键词“respiratory tract (呼吸道)”、“infection (感染)”搜索疾病蛋白, 共得到8 427种。通过韦恩图求通路蛋白和疾病蛋白的交集发现两者的共有蛋白靶点为160种(图 4B)。
|
Figure 3 Pathway analysis of significant metabolites in LPS-induced acute respiratory infections of mice. 1: Lysine degradation; 2: Pentose phosphate pathway; 3: Tyrosine metabolism; 4: Arginine and proline metabolism; 5: Starch and sucrose metabolism; 6: Arginine biosynthesis |
|
Figure 4 Metabolite-pathway protein network (A), Venn diagram of disease protein and pathway protein (B), and pathway enrichment and biological process analysis of shared targets (C) |
为了更深一步探究PDL治疗急性呼吸道感染的作用机制, 采用Metascape对筛选出160个共有靶点进行GO富集分析和靶点通路富集分析, 结果见图 4C。通路富集分析图中横坐标代表富集的统计学显著性, 用-lgP表示, 该值越大, 富集越明显。由图 4C可知, 富集分析共得到20条P≤0.05的生物过程, 颜色深浅代表富集程度, 颜色越深富集越显著, 根据颜色深浅排名前10的生物过程依次为α-氨基酸代谢过程(α-amino acid metabolic process)、碳水化合物代谢过程(carbohydrate metabolic process)、有机磷酸酯生物合成过程(organophosphate biosynthetic process)、精氨酸和脯氨酸代谢(arginine and proline metabolism)、氨基酸和核苷酸糖代谢(amino sugar and nucleotide sugar metabolism)、酪氨酸代谢(tyrosine metabolism)、谷氨酰胺家族氨基酸代谢过程(glutamine family amino acid metabolic process)、铵离子代谢过程(ammonium ion metabolic process)、淀粉和蔗糖代谢(starch and sucrose metabolism)、细胞碳水化合物代谢(cellular carbohydrate metabolic process)。通过这些生物过程可知PDL调控急性呼吸道感染主要可能与氨基酸代谢、有机磷酸酯生物合成、能量代谢等方面有关, 由此可推测出PDL可能通过调节以上生物过程来发挥其治疗急性呼吸道感染的作用。
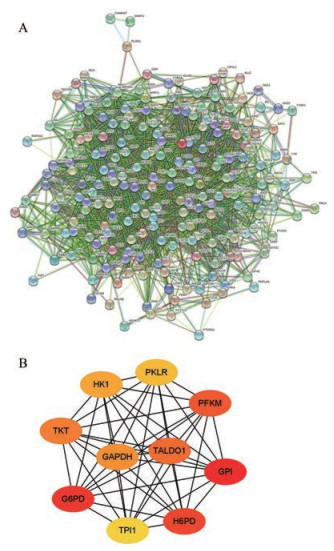
将韦恩图所得160种蛋白导入STRING (https://string-db.org/) 在线数据库分析, 得到蛋白质-蛋白质相互作用网络(PPI网络), 见图 5A, 将此PPI网络导入Cytoscape软件, 利用其CytoHubba插件对网络中的节点进行排名, 以最大集团中心度(maximal clique centrality, MCC) 得分最高的前十个蛋白靶点由黄色至红色表示, 颜色越红代表MCC分数越高, 更倾向于是关键蛋白[13, 14], 获得排名前十的蛋白靶点分别为GPI、G6PD、H6PD、PFKM、TALDO1、TKT、GAPDH、HK1、PKLR和TPI1 (图 5B), 在网络图中起主要作用, 主要分布于糖酵解和磷酸戊糖途径[15]。Michaeloudes等[16]研究发现TGF-β/胎牛血清刺激的慢性阻塞性肺疾病急性机械通气综合征患者表现出脂肪酸氧化能力的恢复, 戊糖磷酸途径产物核糖-5-磷酸和核苷酸生物合成中间体的上调, 以及谷氨酰胺分解代谢物谷氨酸盐水平的增加。糖酵解的抑制和谷氨酰胺的减少减弱了细胞的生长, 糖酵解、谷氨酰胺和脂肪酸代谢的变化可能导致生物合成和氧化还原平衡的增加, 支持慢性阻塞性肺病ASMC生长。因此, 研究结果提示PDL可能通过干预糖酵解和磷酸戊糖途径治疗急性呼吸道感染。
|
Figure 5 Protein-protein interaction network (A), and the network of protein target with the top ten MCC values in the interaction network (B) |
本研究通过整合代谢组学和网络药理学技术, 从生物网络角度系统分析了PDL治疗急性呼吸道感染的可能作用机制。3-磷酸甘油酸、α-氨基己二酸、D-核酮糖-5-磷酸、β-甘露糖基甘油酸、D-果糖、尿素、D-麦芽糖和鸟氨酸等8个内源性代谢物被筛选作为PDL治疗急性呼吸道感染的显著性生物标记物, 进一步的网络研究分析表明主要属于糖酵解和磷酸戊糖途径的GPI、G6PD、H6PD、PFKM、TALDO1、TKT、GAPDH、HK1、PKLR和TPI1等10个蛋白可能为PDL干预急性呼吸道感染的治疗靶点。研究发现, 代谢组学和网络分析相结合的策略有助于解释PDL对急性呼吸道感染的可能作用机制, 并揭示PDL可能通过调节紊乱的代谢途径来治疗急性呼吸道感染的病理过程。
作者贡献: 田刚和胡远卓负责资料调研、实验和写作论文; 李超、翟园园、冯丽和包贝华参与实验; 姚卫峰、张丽和丁安伟提出想法、设计实验、指导并修改论文。
利益冲突: 本文作者声明无利益冲突。
| [1] |
Li H. Study on epidemic characteristics of M. pneumonia in patients with acute respiratory tract infection in Beijing area and its countermeasures[J]. Anti Infect Pharm (抗感染药学), 2019, 16: 2118-2121. |
| [2] |
Liao JY, Zhang T. Distribution characteristics of mycoplasma pneumoniae, chlamydia pneumoniae, and Legionella pneumophila in hospitalized children with acute respiratory tract infection: an analysis of 13198 cases[J]. Chin J Contemp Pediatr (中国当代儿科杂志), 2016, 18: 607-613. |
| [3] |
Wang J, Hu SY, Jin L, et al. Clinical research skill point on acute upper respiratory tract infection in children treated by traditional Chinese medicine and new drugs[J]. China J Tradit Chin Med Pharm (中华中医药杂志), 2014, 29: 1109-1111. |
| [4] |
Zhou B, Lv JK. Interpretation of clinical research guidelines for new drugs of Chinese traditional medicine on influenza treatment[J]. Chin J Clin Pharmacol (中国临床药理学杂志), 2017, 33: 1382-1384. |
| [5] |
Tong XH, Zheng Y, Huang WL, et al. Pharmacological and clinical research progress of Pudilan anti-inflammatory preparation[J]. J Yunnan Univ Tradit Chin Med (云南中医学院学报), 2018, 41: 98-102. |
| [6] |
Yang YF, Zhang GP, Gao YH, et al. Effect of Pudilan Xiaoyan oral liquid on acute lung injury rat induced by lipopolysaccharide[J]. Chin J Exp Tradit Med Form (中国实验方剂学杂志), 2019, 25: 55-59. |
| [7] |
Li L, Dong L, Zhao D, et al. Classical dendritic cells regulate acute lung inflammation and injury in mice with lipopolysaccharide‑induced acute respiratory distress syndrome[J]. Int J Mol Med, 2019, 44: 617-629. |
| [8] |
Li B, Han F, Wang Z, et al. Clinical value evaluation of Chinese herbal formula in context of multi-omics network[J]. China J Chin Mater Med (中国中药杂志), 2017, 42: 848-851. |
| [9] |
Nicholson JK, Lindon JC, Holmes E. 'Metabonomics': understanding the metabolic responses of living systems to pathophy-siological stimuli via multivariate statistical analysis of biological NMR spectroscopic data[J]. Xenobiotica, 1999, 29: 1181-1189. DOI:10.1080/004982599238047 |
| [10] |
Fiehn O. Metabolomics-the link between genotypes and phenotypes[J]. Plant Mol Biol, 2002, 48: 155-171. DOI:10.1023/A:1013713905833 |
| [11] |
Zhai YY, Xu J, Feng L, et al. Broad range metabolomics coupled with network analysis for explaining possible mechanisms of Er-Zhi-Wan in treating liver-kidney Yin deficiency syndrome of traditional Chinese medicine[J]. J Ethnopharmacol, 2019, 234: 57-66. DOI:10.1016/j.jep.2019.01.019 |
| [12] |
Kind T, Wohlgemuth G, Lee DY, et al. FiehnLib: mass spectral and retention index libraries for metabolomics based on quadrupole and time-of-flight gas chromatography/mass spectrometry[J]. Anal Chem, 2009, 81: 10038-10048. DOI:10.1021/ac9019522 |
| [13] |
Chin CH, Chen SH, Wu HH, et al. CytoHubba: identifying hub objects and sub-networks from complex interactome[J]. BMC Syst Biol, 2014, 8: S11. DOI:10.1186/1752-0509-8-S4-S11 |
| [14] |
Chen Y, Luo L, Zhong YJ, et al. Screening and identification of key genes involved in lymphatic metastasis of oral squamous cell carcinoma[J]. J Third Mil Med Univ (第三军医大学学报), 2019, 41: 1149-1155. |
| [15] |
Zhao YH, Chahar HS, Komaravelli N, et al. Human metapneumovirus infection of airway epithelial cells is associated with changes in core metabolic pathways[J]. Virology, 2019, 531: 183-191. DOI:10.1016/j.virol.2019.03.011 |
| [16] |
Michaeloudes C, Kuo CH, Haji G, et al. Metabolic re-patterning in COPD airway smooth muscle cells[J]. Eur Respir J, 2017, 50: 1700202. DOI:10.1183/13993003.00202-2017 |
 2021, Vol. 56
2021, Vol. 56


