2. 北京中医药大学中药学院, 北京 100029;
3. 北京中医药大学中医学院, 北京 100029
2. School of Chinese Medicine, Beijing University of Chinese Medicine, Beijing 100029, China;
3. School of Traditional Chinese Medicine, Beijing University of Chinese Medicine, Beijing 100029, China
2018年世界卫生组织报告显示, 冠心病(coronary heart disease, CHD)引起的慢性心血管疾病已成为全球的头号死因[1]。CHD是由于冠状动脉粥样硬化使管腔狭窄或闭塞, 导致心肌缺血、缺氧或坏死而引发的心脏病, 是临床常见的心血管疾病。冠心病属于中医“胸痹”和“真心痛”范畴, 其中血瘀证作为冠心病的最基本证素贯穿始终[2]。对应治则“活血化瘀”临床疗效确切, 获得中医药界第一个国家科技进步一等奖。与此对应的活血化瘀中药丹参和三七使用频率最高, 由此形成的丹七片组方简单, 临床广泛使用[3], 已被列入2010年国家药典[4]。前期研究提示, 丹七片对冠心病具有心肌保护作用[5], 但是丹七片治疗CHD的作用机制报道较少, 缺乏起效成分与对应靶标的确认。因此, 本研究从网络药理学入手, 对其治疗CHD的起效成分、潜在靶点及其通路进行研究。
网络药理学是基于系统生物学的理论, 对生物系统的网络分析, 选取特定信号节点进行多靶点药物分子设计的新学科[6]。它运用系统生物学、网络生物学、基因冗余度等原理解释疾病发展的过程, 使用网络平衡的整体观来认识药物与机体的相互作用, 其“多基因、多靶点”的特点与中医药治疗复杂疾病的治疗理念相吻合, 具有较高的应用价值。因此, 针对丹七片治疗CHD的作用机制, 本研究采用网络药理学研究方法, 对丹七片的作用物质基础及机制进行研究, 为临床冠心病的治疗提供理论依据, 为中药复方多靶点、多成分作用模式的研究提供新思路。
材料与方法丹七片活性成分及靶标蛋白的筛选 本研究采用中药系统药理学分析平台TCMSP[7] (http://tcmspw.com)检索丹参和三七主要活性成分及作用靶点。以口服生物利用度(oral bioavailability, OB)≥30%和类药性(drug like, DL)≥0.18作为筛选条件。借助Uniprot[8] (https://www.uniprot.org/)数据库, 通过导入筛选得到的蛋白名称并限定物种为人, 使靶点的蛋白和基因信息标准化。
CHD相关靶点的筛选 通过GeneCards (https://www.genecards.org/)数据库进行系统挖掘, 以“coronary heart disease”作为关键词进行检索及筛选, 再与丹七片作用靶点相映射, 得到交集靶点, 即为丹七片活性成分治疗CHD的潜在作用靶点。
蛋白质相互作用(protein-protein interaction network, PPI)网络的构建和关键核心靶点的筛选 将得到的交集靶点蛋白上传到STRING (https://string-db.org/)数据库, 选择研究物种为人类, 进行蛋白与蛋白的相互作用分析, 导出TSV格式文件。将“node1、node2和Combine score”数据导入Cytoscape-3.6.2软件进行可视化处理, 并利用Cytoscape-3.6.2软件中Network Analyzer计算节点度(degree)等拓扑参数来评价靶点度中心性, 确定关键核心靶点。
丹七片治疗CHD潜在靶点作用通路的筛选、注释和分析 将潜在作用靶点导入DAVID (https://david.ncifcrf.gov/)数据库, 对靶点进行通路富集分析。在DAVID数据库的基因列表中复制粘贴基因列表, Select Identifier选择“official gene symbol”, List Type设置为“gene list”, 提交基因列表, 选择对应的物种“Homo sapiens”, 选择GO (gene ontology)生物学过程富集分析和KEGG信号通路富集分析。筛选条件设定阈值P < 0.01, 得到靶点蛋白在基因功能和信号通路中的作用。
“活性成分-潜在靶点-作用通路”网络构建 使用Cytoscape-3.6.2软件构建“中药-活性成分-潜在靶点-作用通路”网络, 该网络由丹参和三七两味药材及其对应的活性成分、交集靶点蛋白和作用通路4个部分组成。通过度中心性分析, 研究丹七片治疗CHD多成分、多靶点和多通路的作用机制。
药物无毒范围筛选 将H9C2心肌细胞以8 000个/孔的密度接种到96孔板中, 放置于37 ℃、5% CO2恒温培养箱中培养, 24 h后从培养箱中取出96孔板。弃去培养液, 加入含有不同浓度的丹参酮IIA (50、75、100和200 μmol·L-1)的培养基以及在正常对照组加入DMEM (Dulbecco's modified Eagle's medium)完全培养液各100 μL, 每组设置6个复孔, 重新放回培养箱中培养。培养25 h后, CCK-8 (cell counting kit-8)法检测细胞活力。
过氧化氢(H2O2)诱导的心肌细胞损伤模型的建立和药物处理 心肌细胞H9C2置于37 ℃、5% CO2恒温培养箱里培养, 经细胞计数后, 按照8 000个/孔, 将心肌细胞接种至96孔板中, 继续放入培养箱中培养, 24 h后从培养箱中取出96孔板, 待细胞生长至80%时, 加入含有不同浓度的丹参酮IIA (50、75、100和200 μmol·L-1)的培养基以及在正常对照组加入DMEM完全培养液各100 μL, 每组设置6个复孔, 重新放回培养箱中培养, 24 h后, 加入50 μmol·L-1 H2O2刺激H9C2心肌细胞1 h, CCK-8法检测细胞活力。
CCK-8法检测细胞活力 上述实验结束后, 弃去培养基, 每孔加入100 μL的DMEM和10 μL的CCK-8试剂, 37 ℃、5% CO2恒温培养箱继续孵育2 h, 结束后取出96孔板, 用酶标仪检测, 450 nm处检测吸光度值(A)。将正常组的细胞活力看作100%, 其他组都与正常组比较, 得到细胞的相对存活率, 确定丹参酮IIA对于心肌细胞的影响。
结果 1 丹七片主要活性化合物的筛选本研究通过TCMSP平台检索到丹七片共有321个化合物, 依据OB≥30%和DL≥0.18共筛选出主要活性化合物73个, 其中丹参有65个, 三七有8个。通过Uniprot数据库对丹七片中活性成分对应靶点蛋白进行标准化处理, 去除重复后, 得到丹参对应靶点蛋白156个, 三七对应靶点蛋白181个。绿色箭头代表中药, 黄色三角代表活性化合物, 圆形代表对应靶点(图 1)。

|
Figure 1 The main active ingredients of Radix Salviae and Panax Notoginseng-target network diagram. The green arrows represent traditional Chinese medicine, yellow triangles represent active compounds, and circles represent corresponding targets. Use Cytoscape-3.6.2 software to visualize the data |
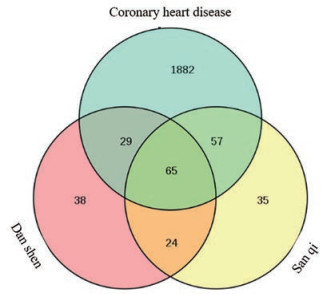
在GeneCards数据库中以“coronary heart disease”为关键词进行检索, 选择物种为“Homo sapiens”, 筛选CHD相关靶点, 删除重复靶点后得到2 033个靶点, 将靶点进行Uniprot ID的标准化。将丹七片和CHD相关靶点上传至在线韦恩图, 筛选出65个交集靶点(图 2)。
|
Figure 2 Danqi tablets and coronary heart disease (CHD) target Wayne diagram. Sixty-five intersection targets were screened. Use online Venn software to visualize data |
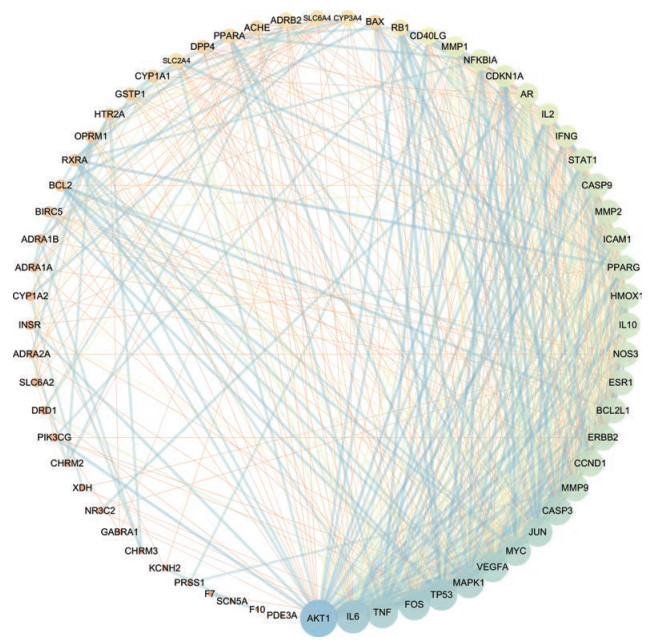
丹七片PPI网络图(图 3)共涉及65个节点和602条边, 其中节点越大度值越大, 边的粗细反映连接评分, 边越粗关系越密切, 颜色由蓝变黄程度与度值呈正相关。在网络中, 1个节点的度值表示网络中和节点相连的节点的数量, 利用节点度值排序确定网络关键节点是目前网络分析的主要策略之一, 一般认为节点的连接度≥所有节点连接度2倍中位数则对整个网络具有重要的贡献意义[9]。本研究根据网络的拓扑学性质度值排序确定关键节点, 网络中度值≥中位数(28)的核心靶点共19个。度值大的靶点在网络中起着关键的作用, 其可能是丹七片治疗CHD的关键核心靶点(表 1)。
|
Figure 3 Network diagram of protein–protein interaction (PPI), according to the protein interaction relationship in the STRING database. The size of the circle in the figure represents the strength of the interaction between the proteins |
| Table 1 Topological attribute parameters of Danqi tablets for the treatment of CHD core targets |
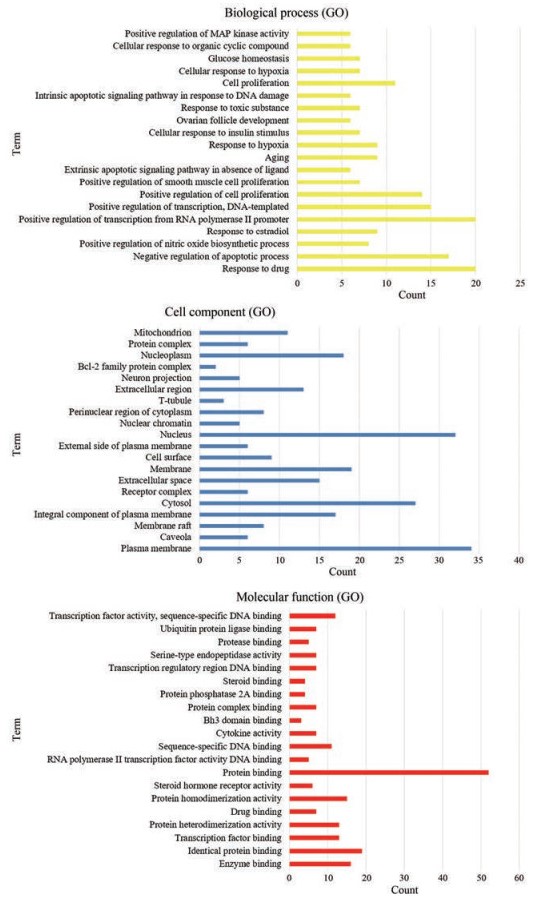
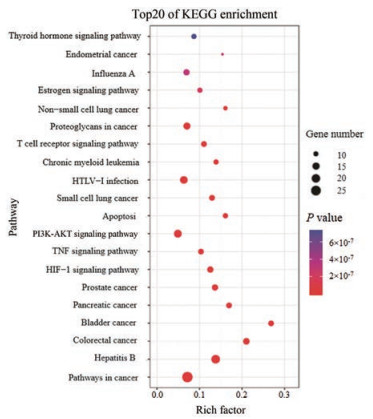
利用DAVID数据库对65个潜在靶点进行GO富集分析, 获得靶点基因的生物学过程(biological process)、细胞组分(cell component)和分子功能(molecular function)共461条信息, 将P < 0.01作为筛选条件。获得生物过程149条、细胞组成20条和分子功能28条。选取前20条目绘制柱状图(图 4)。利用DAVID数据库对筛选出的潜在靶点蛋白进行KEGG通路富集分析, 共获得75条重要通路富集结果, 主要涉及癌症通路、HIF-1 (hypoxia inducible factor-1)、PI3K/AKT (phosphatidylinositol 3 kinase/protein kinase B)、细胞凋亡和TNF (tumor necrosis factor)等信号通路。根据P值从大到小选取前20条通路绘制相应气泡图(图 5)。其中Y轴代表通路名称, X轴代表基因所占百分比, 气泡面积代表通路富集基因数, 气泡颜色代表P值的大小。
|
Figure 4 Analysis of gene ontology (GO) enrichment of potential targets for treatment of CHD with Danqi tablets. The abscissa represents the number of genes enriched in the pathway, and the ordinate represents the name of the pathway |
|
Figure 5 KEGG enrichment analysis of Danqi tablets for treating CHD potential targets. The abscissa represents the proportion of the number of genes in the pathway, the ordinate represents the name of the pathway, the size of the bubble represents the number of genes, and the redder the color, the more significant the difference |
将活性成分、共同靶点和筛选出的排名前20条信号通路导入Cytoscape-3.6.2软件中, 构建“活性成分-共同靶点-作用通路”图(图 6)。如图所示:蓝色菱形代表活性, 黄色圆形代表通路, 红色正方形代表作用靶点。由网络图及节点信息可知: 62个活性成分与排名前20条关键信号通路密切相关, 根据“degree值≥2倍度值中位数”筛选出关键化合物47个, 共涉及到41个靶点。其中排名靠前的有10个成分, 主要作用于炎症因子和细胞凋亡相关通路。丹七片多成分作用于多靶点、多通路, 体现了丹七片多成分、多靶点、多通路相互协调、共同调节的作用特性。
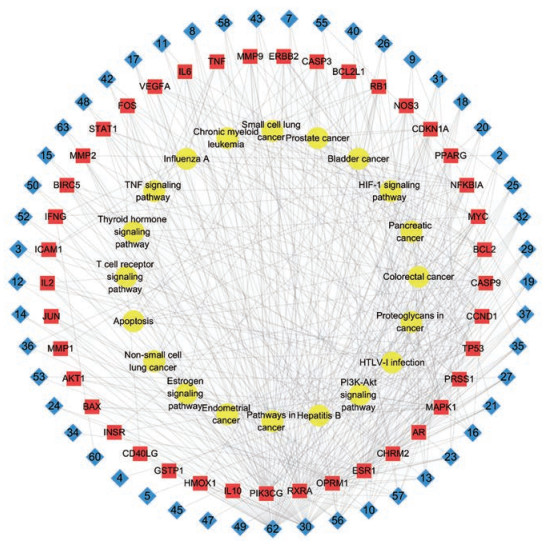
|
Figure 6 Danqi tablets of active ingredients-common target-pathway network. Yellow nodes represent pathways, red nodes represent core targets, and blue nodes represent active compounds. Use Cytoscape-3.6.2 software to visualize the data |
丹参酮IIA在H9C2心肌细胞中无毒范围为50~100 μmol·L-1, 对H9C2心肌细胞进行H2O2处理, 模型组细胞的存活率为60%左右。与模型组相比, 丹参酮IIA对心肌细胞活力有提高作用, 浓度为50、75和100 μmol·L-1时有统计学意义(P < 0.05, 图 7)。

|
Figure 7 Tanshinone IIA protects against H9C2 cardiomyocyte injury induced by H2O2. Ten percent of cell counting kit-8 (CCK8) solution dissolved in DMEM was added to cells for 2 h at 37 ℃, and the optical density was measured at 450 nm via a microplate reader. The left graph shows a non-toxic range of tanshinone IIA on H9C2 cardiomyocytes, and the right graph shows the protective effect of tanshinone IIA on H9C2 cardiomyocyte injury induced by H2O2 at different concentrations, the model group represents H9C2 cardiomyocyte injury induced by H2O2. n = 6, x±s. **P < 0.01, ***P < 0.001 vs model group |
辨证论治是中医治疗的特色, 中药的成分复杂多样, 组方成分更加复杂, 建立能反映中医药整体特色的研究新策略和新方法迫在眉睫。近年来, 网络药理学在中医药研究取得了迅速的发展而引发关注[10]。网络药理学综合了中药活性成分、相关对应靶点和相关疾病3个方面, 并将其作为3种不同类型的节点, 即可构成“成分-靶点-疾病”网络, 再通过网络分析方法, 从而揭示中医药治疗相关疾病的起效成分和作用机制。OB是药物吸收和代谢的重要参数, 其值越高, 代表药物的生物活性和类药性DL越好[11], 因此选择以文献中常用标准OB≥30%且DL≥0.18进行活性成分筛选。本研究采用网络药理学的方法预测了丹七片治疗CHD的主要活性成分及潜在靶点分子作用机制, 共筛选出丹七片中化合物321个, 活性成分47个, 潜在作用靶点248个, 与CHD重合靶点65个, 涉及461条GO生物过程与75条信号通路, 说明丹七片治疗CHD具有多成分、多靶点的特点。
根据“活性成分-共同靶点-通路图”, 按“degree≥2倍度值中位数”筛选出关键化合物47个, 前10名分别为槲皮素、木犀草素、丹参酮IIA、鼠尾草酚酮、β-谷甾醇、4-亚甲丹参新酮、二氢丹参内酯、隐丹参酮、脱氧基新隐丹参酮和异隐丹参酮(编号62、30、56、10、57、13、23、16、21和27)。研究显示, 槲皮素具有降低血压、降血脂、扩张冠状动脉和增加冠脉血流量等药理学作用, 对冠心病及高血压患者有辅助治疗作用[12], 其机制可能是通过直接激活氧化应激下的血管内皮祖细胞(endothelial progenitor cells, EPCs)下游的PI3K/AKT信号通路来影响EPCs的各种生物学行为[13]。木犀草素具有消炎、抗病毒和免疫调节等药理作用, 临床主要用于消炎、降尿酸、治疗心血管疾病和肝炎等[14], 课题组前期研究和文献均报道, 木犀草素通过调节活性氧介导的P38MAPK/NF-κB (mitogen-activated protein kinase/nuclear factor-kappa B)和钙诱导的线粒体凋亡信号通路而保护人脐静脉内皮细胞(human umbilical vein endothelial cells, HUVECs), 减少H2O2诱导的氧化应激损伤[15]。对丹参酮IIA的研究更为广泛, 本课题组前期研究表明, 丹参酮IIA能够通过调节Beclin 1/LAMP 1 (Beclin 1/lysosomal associated membrane protein 1)相关自噬通路减少多柔比星产生的心脏毒性, 保护心肌细胞[16], 同时丹参酮IIA还通过激活AMPK/mTOR (AMP-activated protein kinase/mammalian target of rapamycin)信号通路预防心肌梗死后的心力衰竭[17]。β-谷甾醇有一定的抗炎作用, 且没有激素类药物的不良反应[18]; 隐丹参酮等衍生物具有抗氧化、抗衰老功能, 对治疗冠心病、心绞痛等有一定疗效[19]。综上, 丹七片的前10个关键化合物基本都具有抗炎、降脂、抗氧化应激和保护心血管的作用, 且部分已得到实验验证, 进一步证实了丹七片治疗CHD的起效物质基础。
根据PPI网络拓扑参数节点degree≥2倍度值中位数的筛选的核心靶点共19个, AKT1、IL6 (interleukin-6)、FOS (proto-oncogene c-Fos)、TP53 (cellular tumor antigen p53)、TNF (tumor necrosis factor)、MAPK1 (mitogen-activated protein kinase 1)和VEGFA (vascular endothelial growth factor A)等。它们主要分为以下几类:炎性介质、丝裂原活化蛋白激酶、原癌基因、氧化应激、能量代谢、凋亡和其他。其中炎性介质主要由细胞因子白细胞介素(IL6、IL2和IL10)、肿瘤坏死因子(TNF)和黏附分子1 (intercellular cell adhesion molecule-1, ICAM1)构成。AKT1可以介导体内PI3K依赖的细胞黏附、侵袭和转移等效应, 调控细胞凋亡[20]; 有研究显示, 槲皮素可以通过调节大鼠心肌组织中TNF-α、IL-1β和丙二醛含量发挥明显的抗炎、抗氧化和抗凋亡作用, 并能有效地保护大鼠急性心肌损伤[21]; MAPK1对细胞炎症性反应和肿瘤细胞的增殖、分化、转化和凋亡的调控均有显著影响[22]; IL10是一种抗炎因子, 通过活化的巨噬细胞来抑制炎症因子如TNF、IL6和IL1的表达[23]; BCL2 (B-cell lymphoma-2)是一种抗凋亡因子, 能够抑制多种细胞系统的凋亡[24]; 本课题组前期研究发现, 丹七片通过增加大鼠VEGF-2 (vascular endothelial growth factor 2)和降低血清中NOS (nitric oxide synthase)的含量, 发挥对冠心病促血管生成作用[25], 同时丹七片可以通过调节PPARγ (peroxisome proliferator-activated receptor gamma)介导的能量代谢通路, 改善急性心梗大鼠糖脂代谢紊乱和保护心功能[26]。
GO和KEGG通路富集分析结果表明, 显著富集通路集中在癌症途径、乙型肝炎、PI3K-AKT信号通路、HIF-1信号通路、TNF信号通路、细胞凋亡、T细胞受体信号通路等方面。PI3K/AKT信号通路可调控炎症细胞活化和炎性介质释放等途径, 发挥对慢性炎症调控作用[27]; HIF-1是一种缺氧诱导因子, 可激活编码参与低氧稳态反应蛋白质的基因, 还可以诱导控制葡萄糖代谢、细胞增殖和血管形成的蛋白质表达, 在缺血缺氧心肌中发挥关键作用[28]。以上推断丹七片通过作用于机体系统相关靶点, 调节炎症、凋亡和氧化应激相关通路, 从而达到治疗CHD的效果。
综上所述, 本研究通过对丹七片治疗CHD的主要活性成分及潜在分子作用机制的初步探讨, 得出丹七片中槲皮素、木犀草素、丹参酮IIA等有效成分可能通过PI3K-AKT信号通路、HIF-1信号通路、TNF信号通路、细胞凋亡等多个通路作用于AKT1、IL6、TNF、MAPK1、VEGFA、IL10、IL2、BCL2、PPARγ和ICAM1等多个靶点, 发挥治疗CHD的作用。进一步通过实验证明, 丹七片中主要特征成分丹参酮IIA可以有效保护H2O2导致的心肌细胞凋亡。部分结果已经得到文献的证实[29, 30], 但分子之间的协同用药以及靶点之间的相互作用尚待进一步研究, 最终为“起效成分清楚、作用机制明确”的中药药理学研究提供实验依据。
作者贡献:王勇和李春为本文提供思路设计并为实验提供了资金支持; 马林完成了大部分数据分析和文章撰写工作; 邵明燕完成了体内细胞实验; 孙乾斌完成了部分数据整理。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
World Health Organization. World Health Statistics 2017: Monitoring Health for the SDGs[R]. Geneva: World Health Organization, 2017: 47.
|
| [2] |
Wang J, Chen KJ. On the concept and scope of blood stagnation[J]. Acta Med Sin (中国医药学报), 1989, 4: 7-9. |
| [3] |
Gong DK, Zhang XM. Clinical observation of Danqi pill in the treatment of coronary heart disease[J]. Chin J Ethnomed Ethnopharm (中国民族民间医药), 2009, 18: 125. |
| [4] |
Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. Beijing: China Medical Science Press, 2010: 107-116.
|
| [5] |
Guo SZ, Wang Y, Chuo WJ, et al. Effect of Danqi tablet on myocardial structure and function of chronic myocardial ischemia swines[J]. Chin Arch Tradit Chin Med (中华中医药学刊), 2014, 32: 1889-1891. |
| [6] |
Hopkins AL. Network pharmacology[J]. Nat Biotechnol, 2007, 25: 1110-1111. DOI:10.1038/nbt1007-1110 |
| [7] |
Ru J, Li P, Wang J, et al. TCMSP:a database of systems pharmacology for drug discovery from herbal medicines[J]. J Cheminform, 2014, 6: 13. DOI:10.1186/1758-2946-6-13 |
| [8] |
The UniProt Consortium. UniProt:the universal protein knowledgebase[J]. Nucleic Acids Res, 2018, 46: 2699. DOI:10.1093/nar/gky092 |
| [9] |
Yao YX, He ZX, Liu XF, et al. Potential material basis of Kangbingdu Granules for treatment of coronavirus disease 2019(COVID-19) based on network pharmacology and molecular docking technology[J]. Chin Tradit Herb Drugs (中草药), 2020, 51: 1386-1396. |
| [10] |
Dai JR, Wei WF, Huo JH, et al. Research progress of network pharmacology in traditional Chinese medicine[J]. Heilongjiang J Tradit Chin Med (黑龙江中医药), 2018, 47: 105-107. |
| [11] |
Guo TT, Zhou D, Dang W, et al. Study on anti-Alzheimer's disease mechanism of sesquiterpene coumarins based on network pharmacology[J]. J Shenyang Pharm Univ (沈阳药科大学学报), 2020, 37: 69-76. |
| [12] |
Li C, Hu Q, Zhang YX, et al. Research progress on pharmacological activity of quercetin[J]. Hubei J Tradit Chin Med (湖北中医杂志), 2018, 40: 63-66. |
| [13] |
Sun J, Wen CM, Zhang BC, et al. The protective effect of quercetin on vascular endothelial progenitor cells by regulating PI3K/Akt signaling pathway and its mechanisms[J]. Chin Pharmacol Bull (中国药理学通报), 2019, 35: 85-90. |
| [14] |
Deng DY. Effects of Luteolin on A 549 Cells Infected with Influenza H1N1 Virus and Its Immunoregulatory Mechanism木犀草素对流感病毒H1N1感染A549细胞的作用及免疫调节机制的研究)[D]. Beijing: Beijing University of Chinese Medicine, 2017.
|
| [15] |
Chang H, Li C, Huo K, et al. Luteolin prevents H2O2-induced apoptosis in H9C2 cells through modulating Akt-P53/Mdm2 signaling pathway[J]. Biomed Res Int, 2016, 2016: 5125836. |
| [16] |
Wang X, Li C, Wang Q, et al. Tanshinone ⅡA restores dynamic balance of autophagosome/autolysosome in doxorubicin-induced cardiotoxicity via targeting Beclin1/LAMP1[J]. Cancers (Basel), 2019, 11: 910. DOI:10.3390/cancers11070910 |
| [17] |
Zhang X, Wang Q, Wang X, et al. Tanshinone ⅡA protects against heart failure post-myocardial infarction via AMPKs/mTOR-dependent autophagy pathway[J]. Biomed Pharmacother, 2019, 112: 108599. |
| [18] |
Wang X, Wang F. Advances in the study of plant sterols[J]. Foreign Med Sci (Hyg) (国外医学(卫生学分册)), 2007, 34: 98-101. |
| [19] |
Zen J, Zhang ZR, Miao P, et al. Advances in pharmacological action of cryptotanshinone[J]. Chin Tradit Pat Med (中成药), 2015, 37: 1309-1313. |
| [20] |
Wu WY, Yang Z, Long FX, et al. The regulation of costunolide on colorectal cancer cell proliferation, apoptosis, invasion and migration through PI3K/AKT signaling pathway[J]. J Chin Med Mater (中药材), 2020, 43: 429-435. |
| [21] |
Li B, Yang M, Liu JW, et al. Protective mechanism of quercetin on acute myocardial infarction in rats[J]. Genet Mol Res, 2016, 15: 15017117. |
| [22] |
Zhang JF, Ma YT, Yang YN, et al. Effects of ischemia postconditioning on ischemia-reperfusion injury and reperfusion injury salvage kinase signal transduction pathways in isolated mouse hearts[J]. Chin J Cardiol (中华心血管病杂志), 2008, 36: 161-166. |
| [23] |
Schülke S. Induction of interleukin-10 producing dendritic cells as a tool to suppress allergen-specific T helper 2 responses[J]. Front Immunol, 2018, 9: 455. DOI:10.3389/fimmu.2018.00455 |
| [24] |
Strobl J, Pandey RV, Kausgruber T, et al. Anti-apoptotic molecule BCL2 is a therapeutic target in steroid-refractory graft-versus-host disease[J]. J Invest Dermatol, 2020. DOI:10.1016/j.jid.2020.02.029 |
| [25] |
Jiao S, Tang B, Wang Y, et al. Pro-angiogenic role of Danqi pill through activating fatty Acids oxidation pathway against coronary artery disease[J]. Front Pharmacol, 2018, 9: 1414. DOI:10.3389/fphar.2018.01414 |
| [26] |
Zhang Q, Shao M, Zhang X, et al. The effect of Chinese medicine on lipid and glucose metabolism in acute myocardial infarction through PPARγ pathway[J]. Front Pharmacol, 2018, 9: 1209. DOI:10.3389/fphar.2018.01209 |
| [27] |
Jiang H, Abel PW, Toews ML, et al. Phosphoinositide 3-kinase gamma regulates airway smooth muscle contraction by modulating calcium oscillations[J]. J Pharmacol Exp Ther, 2010, 334: 703-709. DOI:10.1124/jpet.110.168518 |
| [28] |
Ambrose LJ, Abd-Jamil AH, Gomes RS, et al. Investigating mitochondrial metabolism in contracting HL-1 cardiomyocytes following hypoxia and pharmacological HIF activation identifies HIF-dependent and independent mechanisms of regulation[J]. J Cardiovasc Pharmacol Ther, 2014, 19: 574-585. DOI:10.1177/1074248414524480 |
| [29] |
Li Z, Hou J, Deng Y, et al. Exploring the protective effects of Danqi Tongmai tablet on acute myocardial ischemia rats by comprehensive metabolomics profiling[J]. Phytomedicine, 2020, 74: 152918. DOI:10.1016/j.phymed.2019.152918 |
| [30] |
Zheng S, Zhang Y, Qiao Y. Network analysis of primary active compounds in Danqi analogous formulas for treating cardiovascular disease[J]. J Tradit Chin Med Sci, 2016, 3: 116-123. |
 2020, Vol. 55
2020, Vol. 55


