2. 中国人民解放军 93152部队医院, 吉林 通化 134000
2. 93152 Unit Hospital of Chinese People's Liberation Army, Tonghua 134000, China
“质量源于设计” (Quality by Design, QbD)是美国食品药品质量监督管理局提出的一种药品管理理念, 将药品的质量控制从“生产决定质量”转变为“设计控制质量”, 将QbD理念应用于药品研究可以在质量风险管理的基础上, 对产品的处方工艺进行良好的控制, 从工艺设计入手, 识别药品研发阶段潜在的质量问题, 消除不合理因素对药品质量带来的不利影响, 从而保证药品的质量[1]。
对乙酰氨基酚是一种有效的解热镇痛药物, 广泛适用于各个年龄的人群, 尤其是针对儿童, 已经有散剂、口服液等儿童专用剂型, 但服用这些剂型需要多次给药, 且对于不同年龄的儿童来说, 给予相同剂量的药物会带来一些安全性问题[2], 尤其是对肝脏造成损害[3], 使用切割等方式分剂量给药又会造成极大的不便或剂量的不准确。而3D技术则可以很好地解决上述用药问题[4], 该技术的原理是通过计算机软件控制3D打印机, 将材料以逐层堆积的方式打印成立体物品[5], 目前已广泛应用于医药行业[6, 7]。1996年, Wu等[8]验证了3D打印技术制备药物制剂的可能性, 随后, 该技术在制药行业的研究逐渐增多[9-11], 片剂、膜剂[12]和植入剂[13, 14]等多种剂型均被证实可以用3D打印技术制备, 2015年, 3D打印药物左乙拉西坦的上市[15], 标志着3D打印技术在制剂行业的正式应用, 该技术的优势在于其高度的灵活性与精确性[16], 可以利用计算机调节制剂的外观、尺寸及结构, 实现不同规格、不同形状制剂的制备, 并可以通过内部结构的改变调节制剂的释放[17-22], 实现个体化给药[23]。本研究遵循QbD理念, 以共聚维酮为载药基质、泊洛沙姆407为增塑剂, 应用热熔挤出3D打印技术实现对乙酰氨基酚缓释片的制备, 为个体化给药提供了实验和理论依据。
材料与方法仪器与试剂 对乙酰氨基酚(中国湖北鑫明泰公司, 批号: 20181225, 纯度: 98.4%); 共聚维酮(德国巴斯夫公司, 批号: 31842216KO); 泰诺林(上海强生制药有限公司, 批号: 20180725);倍乐信(成都信瑞制药有限公司, 批号: 20190113);泊洛沙姆407 (德国巴斯夫公司, 批号: WPAH516C); 3D打印机(中国上海富奇凡科技有限公司, 型号: MAM-Ⅱ); 料斗混合机(中国浙江迦南科技股份有限公司, 型号: HSD); 硬度脆碎度检测仪(中国上海黄海药检, 型号: CJY-2C); 溶出仪(美国安捷伦科技有限公司, 型号: 708-DS)。
产品目标质量概况(quality target product profile, QTPP) 根据美国药典(USP)中对乙酰氨基酚缓释片的质量特性, 结合热熔挤出3D打印制备药物的技术特点, 定义为QTPP, 见表 1。关键质量属性(critical quality attributes, CQAs)根据本产品的QTPP及热熔挤出3D打印制剂[24]特点确定, 见表 2。
| Table 1 Quality target product profile (QTPP) of acetaminophen sustained-release tablets |
| Table 2 Critical quality attributes (CQAs) of acetaminophen sustained-release tablets. Refer to the United States Pharmacopoeia (USP) standards for assay, in vitro release and degradation products limits |
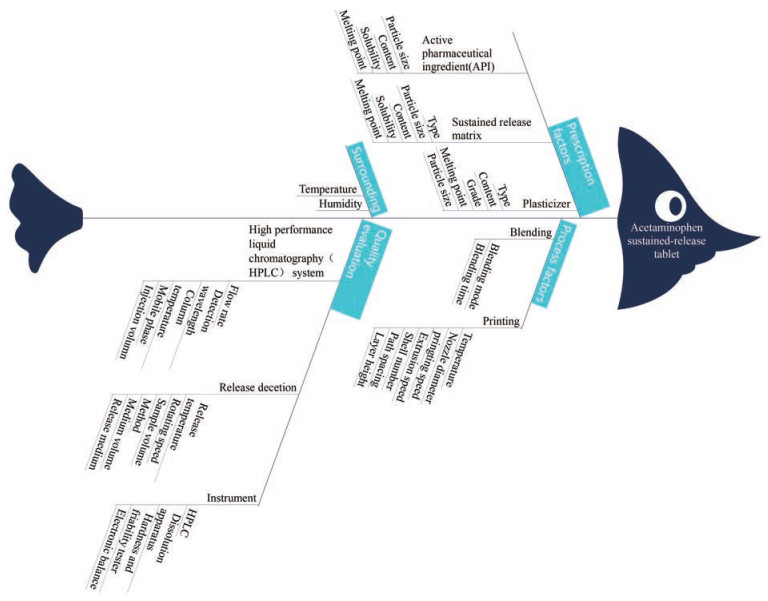
风险评估及单因素考察 根据热熔挤出3D打印制备药物的过程绘制鱼骨图, 筛选影响片剂质量的关键工艺参数(critical process parameters, CPPs), 主要包括处方和工艺因素, 见图 1。应用失效模式和效应分析法(failure mode and effects analysis, FMEA)对各因素进行风险评估[25], 风险评估结果以风险评估系数值表示, 评分原则见表 3, 各因素风险评估系数值为评分原则中影响程度、发生概率和检测难易程度得分之积, 并结合本研究的目的, 规定风险评估系数13~18分之间为高风险因素, 6~12分之间为中风险因素, 低于6分为低风险因素。风险评估系数结果见图 2。
|
Figure 1 Fishbone diagram of factors affecting the quality of tablets |
| Table 3 Principle of risk priority number |

|
Figure 2 Result of risk priority number. The risk priority number between 13 and 18 points is a high risk factor, between 6 and 12 points is a medium risk factor, and less than 6 points is a low risk factor |
风险评估结果显示, 载药基质种类及用量、载药量、增塑剂用量、打印温度、打印速度(喷头移动速度)、挤出速度(活塞挤压材料速度)、层高、路径间距和外壳层数为中风险或高风险因素, 作者分别对上述因素进行单因素考察。
根据单因素考察结果, 载药基质选用共聚维酮可以使载药量达到35%, 打印温度设置为140 ℃, 打印速度范围在16~20 mm·s-1, 挤出速度设定在0.05 mm·s-1, 层高为0.6 mm, 可以较好地完成打印, 且相互之间无明显影响; 而增塑剂用量、路径间距和外壳层数对片剂的影响存在相互作用, 无法通过单因素试验确定最佳参数范围, 所以, 本实验选择增塑剂用量、路径间距与外壳层数作为自变量开展实验设计, 以确定设计空间。
根据对产品CQAs的分析及单因素考察结果, 对实验的响应值进行选择:在单因素试验过程中, 以上拟考察的3个自变量的变化对产品的外观、含量和有关物质影响不大, 但其对产品硬度、脆碎度和释放度的影响较大。硬度和脆碎度虽然不是CQAs, 但对于热熔挤出3D打印技术制备药物制剂来说是较为重要且直观的评价指标, 所以, 选择硬度、脆碎度和释放度作为实验设计的响应值。
全因子实验设计 使用mintab软件进行3中心点23全因子实验设计, 根据单因素考察结果, 确定能保证制剂良好外观的自变量范围, 并参考USP标准确定响应值范围。自变量水平、响应值范围及设计规划见表 4、5。
| Table 4 Factor level and response value of all-factor experiment |
| Table 5 Design planning of all-factors experimental |
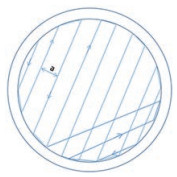
片剂设计及打印 使用计算机辅助软件(computer aided drafting, CAD)设计直径为15 mm、高4 mm的圆柱形模型, 将模型导出为立题光刻文件格式(stereo lithography, STL)并导入至MAM-Ⅱ打印软件中, 片剂内部的打印路径为交叉线型, 外壳打印路径为环形, a代表打印的路径间距, 如图 3所示。
|
Figure 3 The action path of the nozzle during the printing process. a: Path spacing of the print |
使用热熔挤出3D打印机进行片剂打印, 热熔挤出3D打印机主要由加热腔、活塞、热电偶、喷头和打印板组成(图 4)。在打印过程中, 将材料粉末置于加热腔中, 通过热电偶对材料进行加热熔融, 控制活塞将熔融后的材料通过喷头挤出的同时控制喷头在距打印板上方的合适距离沿X-Y-Z轴移动, 将挤出材料按照计算机模型逐层堆积于打印板上。

|
Figure 4 Mechanism of hot melt extrusion 3D printer: 1: Motor; 2: Piston; 3: Cavity; 4: Thermocouple; 5: Heating cavity; 6: Nozzle; 7: Print board |
打印前, 将处方材料按处方比例(对乙酰氨基酚35%、共聚维酮55%~60%和泊洛沙姆407 5%~10%)使用料斗混合机混合30 min, 将混合后的材料加入至3D打印机的加热腔中, 调节活塞向下移动将材料压缩, 升高打印腔温度至140 ℃, 保温40 min后, 调节打印喷头高度使其距打印板0.5 mm, 按照之前导入的片剂模型开始打印, 打印结束30 s后待制剂完全固化将片剂从打印板取下。打印参数为喷头孔径: 0.4 mm; 打印速度: 18 mm·s-1; 挤出速度: 0.05 mm·s-1。
硬度和脆碎度检查 使用硬度脆碎度检测仪对片剂进行硬度检测, 测定结果为各片剂硬度结果的平均值; 使用硬度脆碎度检测仪对片剂进行脆碎度检测, 称取片剂总重m1, 进行脆碎度检测, 每次检测转数100转, 再次称取片剂总重m2, 按公式(m1-m2)/m1×100%计算得出脆碎度。
释放度检查 使用溶出仪测定片剂的释放度, 溶出方法:桨法。溶出介质: pH 1.2盐酸溶液, 介质体积: 900 mL, 溶出温度: 37 ± 0.5 ℃, 转速: 75 r·min-1。检测方法:高效液相法。流动相:甲醇:水= 18:82, 流速: 1.5 mL·min-1, 柱温: 25 ℃, 检测波长: 245 nm, 进样体积: 10 μL。
统计学方法 每组取12片片剂进行检测, 并使用方差分析法对实验结果进行分析, 置信区间为95%。
结果 1 实验设计结果根据实验设计进行不同参数制剂的打印, 并对制剂进行相应的质量检测, 结果见表 6。
| Table 6 Result of the all-factors experimental design. n = 12, x±s |
Pareto图和主效应图(图 5A、6A)表明, 自变量B (路径间距)为影响响应值Y1 (硬度)的显著性因素, P值为0.005, 路径间距的增大, 片剂硬度降低, 各因变量之间交互作用不明显, 回归方程: Y1 = 103.2 + 1.52 A -67.0 B - 6.3 C - 0.84 AB + 0.69 AC + 3.48 BC。

|
Figure 5 Pareto chart of the standardized effects. A: Response is hardness; B: Response is friability, α = 0.05 |

|
Figure 6 Main effect plot for hardness (A) and friability (B) |
Pareto图和主效应图(图 5B、6B)显示, 自变量A (增塑剂用量)为影响响应值Y2 (脆碎度)的显著性因素, P值为0.011, 自变量A (增塑剂用量)与自变量C (外壳层数)具有相互作用(图 7), 在保持路径间距不变的情况下, 增塑剂用量越大, 外壳层数越少, 脆碎度越小, 回归方程: Y2 = 0.048 6 - 0.003 39 A + 0.007 7 B + 0.004 50 C - 0.000 50 AB - 0.000 387 AC - 0.000 29 BC。

|
Figure 7 Contour of plot of friability vs plasticizer content and shell numbers, path spacing = 0.9 mm |
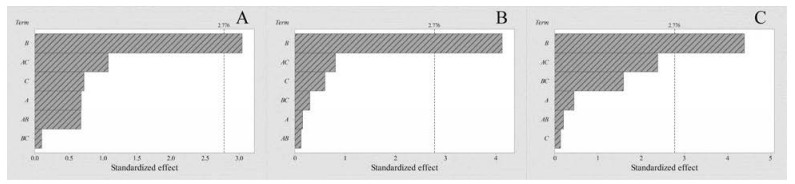
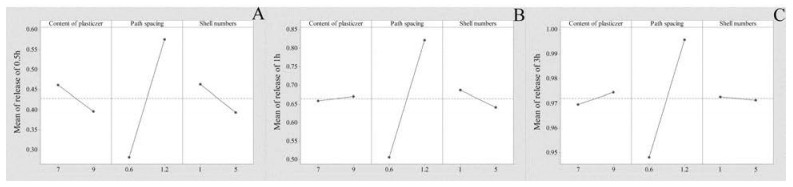
Pareto图(图 8)和主效应图(图 9)结果表明, 对响应值Y3、Y4、Y5 (0.5、1和3 h的释放度), 自变量B的影响是显著的, P值分别为0.005、0.001和0.021, 等值曲线图(图 10)表明, 自变量C与自变量B对释放度的影响具有一定的相互作用, 随着路径间距的增加和外壳层数的减少, 片剂在各时间点的释放度明显增加, 回归方程: Y3 = 0.12 - 0.013 A + 1.38 B - 0.218 C - 0.108 AB + 0.026 0 AC - 0.008 1 BC; Y4 = 0.71 - 0.054 A + 0.34 B - 0.151 C + 0.016 AB + 0.015 3 AC + 0.018 8 BC; Y5 = 0.791 + 0.018 6 A + 0.008 B + 0.038 6 C + 0.003 6 AB - 0.006 49 AC + 0.014 42 BC。
|
Figure 8 Pareto chart of the standardized effects. Response is in vitro release of 0.5 h (A), 1 h (B), 3 h (C), α = 0.05 |
|
Figure 9 Main effect plot for in vitro release of 0.5 h (A), 1 h (B), 3 h (C) |

|
Figure 10 Contour of plot of in vitro release of 0.5 h (A), 1 h (B), 3 h (C) vs path spacing and shell numbers, plasticizer content = 9% |
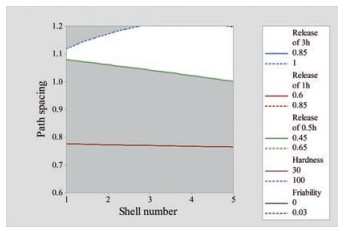
上述结果表明, 增塑剂含量只对脆碎度有显著性影响, 路径间距对硬度、释放度的影响显著, 外壳层数对脆碎度和释放度有一定影响, 为了能更好地确定制剂的设计空间, 作者首先确定处方用量, 由图 6B和图 7表明, 增塑剂含量越大, 片剂的脆碎度越小, 所以选择的增塑剂含量应越大越好。为保证片剂的外观, 增塑剂选择单因素所限定范围的最大用量9%, 在此条件下建立片剂的设计空间, 根据外壳层数和路径间距对硬度、脆碎度、释放度影响的等值曲线叠加图(图 11), 作者得出片剂的设计空间(图中白色区域)。当外壳层数在2~5层内变化时, 均可调整路径间距使片剂满足目标需求, 为使路径间距可以在较大范围内变化并尽量避开使硬度不合格的路径间距范围, 将外壳层数范围选择为3~5层, 路径间距范围为1.05~1.2 mm。
|
Figure 11 Design space of acetaminophen sustained-release tablets |
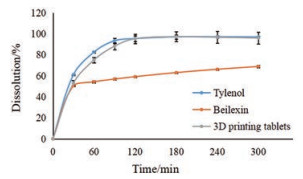
使用确定的处方工艺, 在设计空间内制备一批次对乙酰氨基酚缓释片, 参照USP中对乙酰氨基酚缓释片方法[26]与市售对乙酰氨基酚缓释片进行含量、释放度和有关物质的检测及比较, 选择商品名为泰诺林(Tylenol)和倍乐信(Beilexin)的对乙酰氨基酚缓释片作为对比, 结果见表 7与图 12。结果表明, 泰诺林、倍乐信与3D打印片的含量均在90%~110%, 符合目标要求, 且3种制剂均未检出有关物质。在释放度方面, 3D打印片与泰诺林释放曲线相似, 相似因子为70.68, 且各时间点释放度均能满足目标需求, 而倍乐信的释放度无法满足USP需求, 3D打印片与其释放曲线的相似因子为28.74。质量评价结果证明, 使用3D打印法制备对乙酰氨基酚缓释片的质量满足USP要求, 且与市售制剂泰诺林相似, 进一步证明了3D打印技术制备的对乙酰氨基酚缓释片不仅可以满足释放度标准, 并且可以通过改变内部结构进行释放度的调节。
| Table 7 Quality comparison between 3D printed tablets and commercial preparations |
|
Figure 12 Release curve of 3D printed tablets and commercial acetaminophen sustained release tablets |
遵循QbD理念进行处方工艺的优化可以较为直观地确定CPPs与CQAs之间的关系, 研究结果证明, 对乙酰氨基酚缓释片的硬度受参数中的路径间距影响显著, 随着路径间距的增加, 片剂的硬度会随之减小, 原因是路径间距决定了片剂的内部结构, 路径间距的增大使制剂内部填充度降低, 使内部结构变得疏松, 进而降低了片剂的硬度; 制剂的脆碎度受增塑剂用量以及外壳层数影响显著, 因为增塑剂可以增强熔融材料的成型性与韧性, 所以增塑剂含量的增加可以降低片剂的脆碎度, 外壳层数增加反而使片剂的脆碎度增加, 可能是外壳与制剂内部的连接不够紧密的缘故, 但当增塑剂含量为9%时, 外壳层数对脆碎度的影响很小, 可以不予深入考虑。制剂的释放度受路径间距影响显著, 0.5、1和3 h的释放度结果均表明, 增大路径间距, 片剂的释放速度随之加快, 因为路径间距的增加使片剂的内部填充度降低, 导致片剂内部的通道孔径增大, 使释放介质更加容易进入, 增加了片剂与介质的接触面积, 从而加快了片剂的释放, 这也证明了可以通过改变制剂的内部结构对其进行释放度的调节, 证明了3D打印制备药物制剂的灵活性, 为实现个体化给药提供了实验依据。
本研究遵循QbD理念, 通过FMEA对热熔挤出3D打印技术制备药物制剂的各因素进行风险评估, 使用全因子实验设计进行数据分析, 得出打印的最佳参数范围。证明了使用QbD原则进行3D打印药物制剂的制备能够准确且直观地得出各参数对实验结果的影响并建立合适的控制指标, 对保持制剂的重现性具有重要意义。同时, 利用热熔挤出3D打印技术制备符合目标要求的对乙酰氨基酚缓释片, 进一步证实了3D打印技术制备药物制剂的可行性, 并且证实了可以在不改变制剂处方组成的前提下, 通过改变制剂内部结构的方式对制剂进行释放度的调节, 能够解决普通对乙酰氨基酚缓释片剂量的单一而造成的安全性问题, 为特殊人群提供释放可控的制剂, 为进一步实现个体化给药提供了理论依据。
作者贡献:刘伯石为本实验的主要执行者以及本文的主要撰写者; 王增明为具体实验的指导者, 并对文章进行了修改; 张慧、高静对本文的统计学研究进行了指导; 刘楠、李蒙、高翔共同参与了实验的操作; 郑爱萍为本研究思路以及设备、材料的提供者, 并参与了实验的指导以及文章的修改, 对文章进行最终定稿。
利益冲突:本文与任何组织或个人无任何利益冲突。
| [1] |
Xu XY, Liang Y. Consistency evaluation of generic drugs based on quality by design[J]. Chin Pharm Affairs (中国药事), 2017, 31: 1233-1236. |
| [2] |
Zhao YL, Zheng Y. Comparison of the efficacy of different administration methods of acetaminophen in the treatment of acute fever in children[J]. Chin J Clin Ration Drug Use (临床合理用药), 2018, 34: 100-101. |
| [3] |
Pan JQ, Song DJ, Li PX. Progress in mechanism of acetaminophen-induced hepatotoxicity and its protective strategies[J]. Chin J Pharmacol Toxicol (中国药理学与毒理学杂志), 2014, 28: 618-624. |
| [4] |
Alomari M, Mohamed FH, Basit AW, et al. Personalised dosing:printing a dose of one's own medicine[J]. Int J Pharm, 2015, 494: 568-577. |
| [5] |
Prasad LK, Smyth H. 3D printing technologies for drug delivery:a review[J]. Drug Devel Ind Pharm, 2016, 42: 1-35. |
| [6] |
Brunello G, Sivolella S, Meneghello R, et al. Powder-based 3D printing for bone tissue engineering[J]. Biotechnol Adv, 2016, 34: 740-753. |
| [7] |
Liang K, Carmone S, Brambilla D, et al. 3D printing of a wearable personalized oral delivery device:a first-in-human study[J]. Sci Adv, 2018, 4: 2544-2556. |
| [8] |
Wu BM, Borland SW, Giordano RA, et al. Solid free-form fabrication of drug delivery devices[J]. J Control Release, 1996, 40: 77-87. |
| [9] |
Katstra WE, Palazzolo RD, Rowe CW, et al. Oral dosage forms fabricated bythree dimensional printing[J]. J Control Release, 2000, 66: 1-9. |
| [10] |
He DL, Han FG, Wang Z, et al. A review of 3D printing via fused deposition modeling in pharmaceutics[J]. Acta Pharm Sin (药学学报), 2016, 51: 1659-1665. |
| [11] |
Norman J, Mudarawe RD, Moore CMV, et al. A new chapter in pharmaceutical manufacturing:3D-printed drug products[J]. Adv Drug Deliv Rev, 2017, 108: 39-50. |
| [12] |
Aho J, Johan PB, Genina N, et al. Roadmap to 3D-printed oral pharmaceutical dosage forms:feedstock filament properties and characterization for fused deposition modeling[J]. J Pharm Sci, 2019, 108: 26-35. |
| [13] |
Water JJ, Bohr A, Boetker J, et al. Three-dimensional printing of drug-eluting implants:preparation of an antimicrobial polylactide feedstock material[J]. J Pharm Sci, 2015, 104: 1099-1107. |
| [14] |
Holländer J, Genina N, Jukarainen H, et al. Three-dimensional printed pcl-based implantable prototypes of medical devices for controlled drug delivery[J]. J Pharm Sci, 2016, 105: 2665-2676. |
| [15] |
Zhang Q. From the approving of 3D printing tablet to the innovation of drug delivery systems[J]. Acta Pharm Sin (药学学报), 2016, 51: 1655-1658. |
| [16] |
Zhao J, Jiang ML, Ding Y. Research progress and engineering prospect on the formulation design of 3D printing technology[J]. Acta Pharm Sin (药学学报), 2018, 53: 115-122. |
| [17] |
Shrawani L, Dong HS, Sangkil L, et al. Customized novel design of 3D printed pregabalin tablets for intra-gastric floating and controlled release using fused deposition modeling[J]. Pharmaceutics, 2019, 11: 1-14. |
| [18] |
Khaled SA, Alexander MR, Irvine DJ, et al. Extrusion 3D printing of acetaminophen tablets from a single formulation with tunable release profiles through control of tablet geometry[J]. AAPS PharmSciTech, 2018, 19: 3403-3413. |
| [19] |
Xu XW, Zhao JZ, Wang L, et al. 3D printed polyvinyl alcohol tablets with multiple release profiles[J]. Sci Rep, 2019, 9: 1-8. |
| [20] |
Goyanes A, Robles Martinez P, Buanz A, et al. Effect of geometry on drug release from 3D printed tablets[J]. Int J Pharm, 2015, 494: 657-663. |
| [21] |
Goyanes A, Fina F, Martorana A, et al. Development of modified release 3D printed tablets (printlets) with pharmaceutical excipients using additive manufacturing[J]. Int J Pharm, 2017, 527: 21-30. |
| [22] |
Zhang J, Yang W, Vo AQ, et al. Hydroxypropyl methylcellulose-based controlled release dosage by melt extrusion and 3D printing:structure and drug release correlation[J]. Carbohyd Polym, 2017, 177: 49-57. |
| [23] |
Shaban A, Morgan RA, Ricky D, et al. 3D extrusion printing of high drug loading immediate release acetaminophen tablets[J]. Int J Pharm, 2018, 538: 223-230. |
| [24] |
Chen MW, Chen WR, Chen TK, et al. Application research of hot-melt extrusion in preparation of solid dispersion[J]. Acta Pharm Sin (药学学报), 2012, 47: 33-37. |
| [25] |
Zhang LY, Song JC. Preparation of N-acetylcysteine injection based on quality by design[J]. J Pharm Pract (药学实践杂志), 2019, 37: 552-558. |
| [26] |
The United States Pharmacopieial Convention. United States Pharmacopeia[S]. USP: The United States Pharmacopieial Convention, Vol 42, 2019: 2300-2301.
|
 2020, Vol. 55
2020, Vol. 55


