2. 北京中医药大学, 北京 100029;
3. 解放军总医院医学保障中心, 北京 100048
2. Beijing University of Chinese Medicine, Beijing 100029, China;
3. Medical Supplies Center of the PLA General Hospital, Beijing 100048, China
中药具有数千年的临床应用历史, 在保障我国国民健康方面发挥着重要而独特的作用, 并受到世界范围的重视[1, 2]。中药的原材料主要源自于自然环境下生长的植物、动物或矿物。由于土壤和水源污染[3-8]、自身蓄积或伴生[9-11]、加工方式不当[12]等原因, 部分中药中重金属及有害元素含量偏高, 严重影响了中药的用药安全和公众健康, 引起国内外的广泛关注, 并成为制约中药走向国际市场的瓶颈。与此同时, 越来越多的学者将目光投向有害残留对中药用药健康的影响, 采用暴露限值法、靶标危害系数法、危害指数法等多种方法对中药材中重金属进行风险评估[13-15], 并开始将中药材经煎煮或提取后, 重金属的生物可给性纳入评价体系[16, 17]。
与中药材不同, 中成药不经煎煮, 作为终产品直接为患者使用, 原辅料存在的安全风险可能直接向制剂转移, 外源性污染会通过中成药的服用进入人体, 因此其安全性控制应更加严格。目前中成药中重金属及有害元素健康风险的评估尚未引起足够重视, 相关文献也鲜见报道[18, 19]。本文基于2010~2018年国家药品抽验测定结果, 对295个品种15 054批次中成药中的重金属及有害元素残留特征进行了全面的分析, 首次提出了中成药中重金属及有害元素健康风险评估的通用步骤, 对276个品种14 787批次样品进行了评估。明确了中成药中重金属及有害元素的最大限量理论值计算公式及具体参数, 根据各元素评估结果, 拟定了4个健康风险较高品种的建议限度, 以期为客观了解服用中成药的健康风险以及指导合理用药, 保障药物安全提供技术支撑, 并为中成药中重金属及有害元素健康风险评价和限量制定提供示范和参考。
材料与方法数据概况与分析方法 2010~2018年, 国家药品抽验涉及391个中成药品种(系列), 其中284个测定了重金属和有害元素, 占比73%, 涉及丸剂、片剂、胶囊剂、颗粒剂、糖浆剂、合剂、散剂、酊剂、煎膏剂、注射剂等10种剂型。部分品种(系列)测定值无对应厂家和批号, 不纳入统计。另有含雄黄或/和朱砂的品种(系列), 因其主要安全风险来源于雄黄和朱砂中高含量的As和Hg, 不属于外源性残留, 也不纳入统计。将同一系列中不同品种分开计数, 共对295个品种15 054批次中成药的重金属及有害元素残留值进行分析。所有样品均经微波消解处理, 采用电感耦合等离子体质谱法(ICP-MS)、原子吸收法(AAS)或原子荧光法(AFS)测定元素含量。多数品种考察了Pb、Cd、As、Hg、Cu的残留, 三七胶囊等65个品种还测定了Cr的含量。采用SPSS 16.0和JMP 10软件进行数据统计, 从分布情况、元素和剂型差异、相关性等角度, 分析中成药中重金属及有害元素的残留特征。
因药品服用量是计算暴露量的重要参数之一, 通过质量分析报告无法追溯到准确规格或未规定明确用量的品种和样品暂不进行风险评估, 故对14 787批次样品和276个品种进行健康风险评估, 不同年份抽样的同一品种分开评估。各元素健康风险分开评估, 不计算所有元素的总靶标危害系数。根据每个元素的靶标危害系数确定品种目前具体需要控制何种元素的限度。
中成药中重金属及有害元素健康风险评价 中成药的健康风险评价包括危害识别、危害特征描述、暴露评估和风险特征描述4个基本步骤。危害识别根据重金属及有害元素的理化特性、毒理学试验数据、人群流行病学调查等资料来确定该物质是否会对人体健康造成潜在的危害。中成药的安全风险主要来自中药材原料, 后者中主要的重金属及有害元素为Pb、Cd、As、Hg、Cu[20], 劣质辅料包材或劣质胶类药材也可能引入Cr污染[21, 22]。Pb、Cd、As、Hg是公认的重金属及有害元素, 可导致蓄积性中毒[23]。Cu和三价Cr虽是人体必需的微量元素, 但过量的铜可引起肝、肾、脑的损害[24], 而六价Cr被国际癌症研究机构列为一级致癌物[25]。
危害特征描述, 即剂量-反应关系评估, 根据毒理学或流行病学数据, 定量分析人群摄入或吸收重金属及有害元素的暴露剂量与发生的针对该物质的毒理学改变(毒性反应)之间的关系, 以确定健康指导值。健康指导值(health-based guidance values, HBGV)指人类在一定时期内摄入重金属及有害元素, 而不产生可检测到健康危害的安全限值, 以每千克体重的摄入量表示, 如每日允许摄入量(acceptable daily intake, ADI)、理论最大日摄入量(provisional maximum theoretical daily intake, PMTDI)、暂定每周耐受摄入量(provisional tolerable weekly intake, PTWI)等。在实际操作中, 健康指导值可由未观察到有害作用的剂量水平(no-observed-adverse effect level, NOAEL)或基准剂量下限(lower confidence limit on the benchmark dose, BMDL)推算得到。联合国粮食及农业组织/世界卫生组织食品添加剂联合专家委员会(Joint FAO/WHO Expert Committee on Food Additives, JECFA)不定期制定并发布重金属等有害物质的健康指导值, 一般认为该值具权威性, 应跟踪其最新动态用于危害特征描述。JECFA规定镉的PTMI为每月0.025 mg·kg-1、无机汞的PTWI为每周4 μg·kg-1、铜的PMTDI为每天0.05~0.50 mg·kg-1 (本研究采纳0.50)[26]。JECFA取消了铅和无机砷的PTWI, 本研究分别采纳WHO提出的无机砷导致肺癌发病率比本底值增长0.5%的每日基准剂量下限值(BMDL0.5)每天3.0 μg·kg-1和成年人心血管效应毒性终点收缩压基准剂量下限值(BMDL01)每天1.3 μg·kg-1为砷和铅的健康指导值[26]。JECFA没有规定铬的PTWI, 本研究采纳美国国家环保署(United States Environmental Protection Agency, USEPA)提出的六价铬每天TDI 3 μg·kg-1为健康指导值[27]。为方便后续计算, 各元素健康指导值统一按每千克体重每日允许摄入量(ADI)折算, Pb、Cd、As、Hg、Cu、Cr的ADI分别为1.3、0.8、3、0.6、500和3 μg·kg-1。
暴露评估以重金属及有害元素残留值测定值和临床用量为基础, 根据目标人群的用药特点, 选择能满足风险评估目的最佳统计值。由于重金属及有害元素的半衰期普遍较长, 故应针对整个生命周期内的暴露情况进行长期暴露评估。暴露量(Exp)计算公式如下:
| $ {\rm{Exp}} = \frac{{{\rm{EF}} \times {\rm{ED}} \times M \times C}}{{{\rm{AT}} \times W}} $ | (1) |
式(1)中: Exp为日暴露量, 以每千克体重每日重金属摄入量表示, 单位为μg·kg-1; EF (exposure frequency)为暴露频率, 指每年暴露于中药中重金属的天数, 以中药服用频率表征; ED (exposure duration)为暴露年限, 指暴露于中药中重金属的年限, 以一生服用中药的常规年限表征; 国家食品安全风险评估中心中药消费情况调查结果显示中药年消费频率P95值为90天, 常规使用年限为20年[28-30], 本研究采纳EF为每年90天, ED为20年; M为中成药日最大摄入量, 根据药品使用说明书或药品标准中相关规定计算, 单位为g; C为样品中重金属及有害元素残留值, 单位为mg·kg-1; 当对某中成药品种的整体风险进行评估时, 可采用中位数、平均值或P95值等统计量; AT (average exposure time)为平均寿命天数, 以365×70年计; W为人体平均体重, 以63 kg计。
风险特征描述在危害识别、危害特征描述和暴露评估的基础上, 确定重金属及有害元素对人体健康造成危害的概率及范围。本研究借鉴USEPA创建的靶标危害系数法(target hazard quotient, THQ), 根据暴露量与健康指导值的比值, 即THQ对中成药中重金属及有害元素的风险特征进行描述, 计算公式如下:
| $ {\rm{THQ}} = \frac{{{\rm{Exp}} \times 10}}{{{\rm{ADI}}}} = \frac{{{\rm{EF}} \times {\rm{ED}} \times M \times C \times 10}}{{{\rm{AT}} \times W \times {\rm{ADI}}}} $ | (2) |
式(2)中: THQ为靶标危害系数; HBGV为各元素健康指导值; 其他参数同公式(1); 10为《中国药典》2020年版“9302中药有害残留物限量制定指导原则”规定的安全因子, 表示每日由中药摄取的重金属量不大于日总暴露量(包括食物和饮用水)的10%。当THQ≤1, 认为人体负荷的重金属及有害元素量未对健康造成明显影响, 风险较低; 当THQ > 1, 认为人体所负荷的重金属及有害元素量已危害到人体健康, 风险应予以关注。
口服中成药中重金属及有害元素残留限量制定建议 在制修订中成药标准时, 建议根据样品和品种健康风险评估结果确定需要控制的元素的种类和限量, THQ≤1的元素可不做要求。由于《中国药典》2020年版制剂通则项下已经规定了中药注射剂中重金属及有害元素残留限量, 故本研究仅对口服用中成药中重金属及有害元素最大残留限量理论值做出建议, 在安全的THQ取值情况下(THQ=1)计算限量, 公式如下:
| $ L = \frac{{{\rm{ADI}} \times W}}{{M \times 10}} \times \frac{{{\rm{AT}}}}{{{\rm{EF}} \times {\rm{ED}}}} $ | (3) |
式(3)中: L为最大限量理论值, 单位为mg·kg-1。
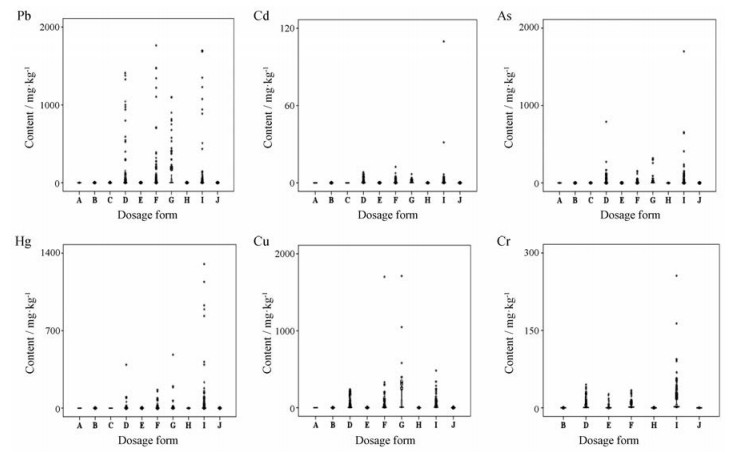
结果与分析 1 中成药中重金属及有害元素残留特征295个品种15 054批次中成药中重金属及有害元素测定值共计73 250个, Pb、Cd、As、Hg、Cu、Cr的残留值均呈趋近于0的偏态分布。单因素方差分析结果表明, 不同元素残留值间存在显著性差异(P < 0.05), 整体残留值最高的是Cu, 最低的是Cd (表 1)。Pb和Cu、Pb和Cr、Cr和Cu残留值之间存在中度相关性, 其他元素残留值间未见相关(表 2)。Pb、Cu、Pb对中药的污染, 或中药对土壤和水中上述元素的吸收是否存在协同等相互作用, 值得进一步深入研究。不同剂型样品各元素残留值存在显著差异(P < 0.05), 片剂、丸剂、胶囊剂、散剂中Pb残留较高, 片剂、胶囊剂、丸剂、散剂中Cd残留较高, 丸剂、胶囊剂、散剂、片剂中As残留较高, 丸剂、片剂、胶囊剂、散剂中Hg残留较高, 散剂、丸剂、片剂、胶囊剂中Cu残留较高, 丸剂、胶囊剂、片剂中Cr残留较高(图 1)。中药原粉制剂指处方中所有药味均未经提取, 以原粉入药的中成药, 其生产工艺相对简单, 主要包括粉碎、过筛、配研、混匀等步骤[31]。相应的, 部分处方药味不经提取直接入药的中成药被称为半原粉制剂。原粉制剂和半原粉制剂主要涉及丸剂、片剂、胶囊剂、糊剂、散剂、膏药等剂型。原粉制剂和半原粉制剂中直接粉碎入药的原料, 不经提取、柱分离净化等处理, 其可能存在的外源性污染会直接向制剂转移, 这也解释了为何丸剂、胶囊剂、片剂、散剂中各元素残留普遍较高。而糖浆剂、合剂、酊剂、煎膏剂、注射剂均使用药材提取溶液制备, 故各元素残留普遍较低。槐角丸、活血止痛胶囊、愈伤灵胶囊、三七伤药片、跌打丸、复方血栓通胶囊、接骨七厘散、清脑降压片、全天麻胶囊、天麻头痛片、接骨续筋片、抗骨增生丸、牛黄清胃丸、乳癖消片胶囊、冠心苏合胶囊、蛤蚧定喘丸、西黄丸、冠心七味片、山楂丸、启脾丸、清火栀麦胶囊、上清丸、补中益气丸、补肾强身胶囊、清眩丸、加味逍遥丸、开胸顺气丸、人参归脾丸、十八味诃子利尿丸、活血止痛散、活血止痛片、藿胆丸、小金丸等33个品种发现重金属及有害元素残留值异常偏高样品, 其中Pb、Cd、As、Hg、Cu、Cr含量高于100 mg·kg-1的样品批次分别为98、1、22、23、158、2, 1个品种(槐角丸) 11批次样品Pb含量高于1 000 mg·kg-1, 1个品种(上清丸) 1批次样品As含量高于1 000 mg·kg-1, 2个品种(活血止痛散、活血止痛片) 3批次样品Cu含量高于1 000 mg·kg-1。对于As、Hg含量异常偏高的情况, 不排除是生产含雄黄、朱砂的中成药后清场不彻底造成污染[32]。
| Table 1 Statistics of content of Pb, Cd, As, Hg, Cu and Cr in 15 054 batches of Chinese patent medicines |
| Table 2 Correlation coefficients of residues of Pb, Cd, As, Hg, Cu and Cr in Chinese patent medicines |
|
Figure 1 Box plots of content of Pb, Cd, As, Hg, Cu and Cr in Chinese patent medicines with different dosage forms. A: Tincture; B: Mixture; C: Concentrated decoctions; D: Capsules; E: Granules; F: Tablets; G: Powders; H: Syrups; I: Pills; J: Injection |
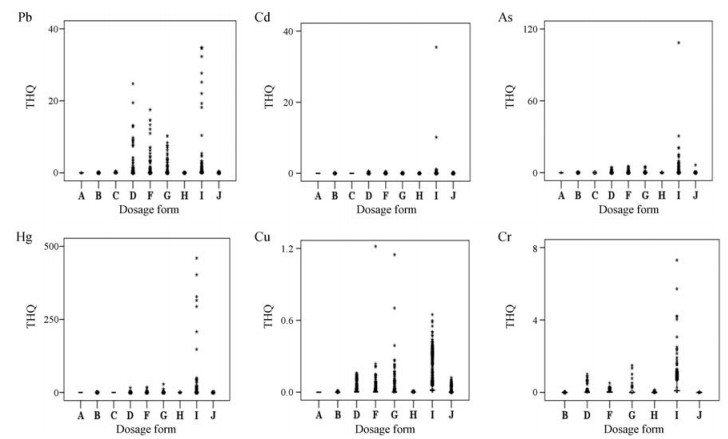
按前文建立的基本步骤, 对有明确规格和用量的276个品种14 787批次中成药中重金属及有害元素进行健康风险评估, 结果显示所有样品Pb、Cd、As、Hg、Cu、Cr的THQ均呈趋近于0的偏态分布。单因素方差分析结果表明, 不同元素THQ间存在显著性差异(P < 0.05), 整体THQ值最高的是Hg, 最低的是Cu (表 3)。Pb和Cr、Cd和Cr、Cu和Cr的THQ之间存在中度相关性, Pb和Cu的THQ之间存在弱相关, 其他元素THQ间未见相关(表 4), 各元素间残留值的相关性和THQ的相关性基本一致。不同剂型样品各元素THQ存在显著差异(P < 0.05), 丸剂、胶囊剂、片剂、散剂中Pb的THQ较高, 丸剂中Cd的THQ较高, 丸剂、片剂、胶囊剂中As的THQ较高, 丸剂、散剂、胶囊剂、片剂中Hg的THQ较高, 丸剂、胶囊剂中Cr的THQ较高(图 2)。糖浆剂、合剂、酊剂、注射剂中各元素的THQ普遍较低。板蓝根片、保胎灵片、补肾强身胶囊、补肾强身片、补中益气丸、沉香化气丸、沉香化滞丸、丹栀逍遥丸、跌打活血散、跌打片、跌打丸、耳聋左慈丸、防风通圣丸、妇科止带片、复方丹参片、复方血栓通片、更年安胶囊、宫炎康颗粒、冠心七味片、冠心苏合胶囊、蛤蚧定喘丸、槐角丸、黄连羊肝丸、活血止痛胶囊、活血止痛片、活血止痛散、藿胆丸、济生肾气丸、加味逍遥丸、接骨七厘散、接骨七厘丸、接骨续筋片、橘红丸、开胸顺气丸、抗骨增生丸、连翘败毒丸、羚羊感冒片、龙胆泻肝丸、麻仁润肠软胶囊、麦味地黄丸、礞石滚痰丸、男宝胶囊、尿塞通片、牛黄清胃丸、牛黄上清丸、启脾丸、清脑降压片、清胃黄连丸、清眩丸、全天麻胶囊、人参归脾丸、三七片、三七伤药片、桑菊感冒片、山楂丸、上清丸、少腹逐瘀丸、天麻丸、五子衍宗丸、西黄丸、香砂平胃丸、小金胶囊、小金丸、血栓心脉宁胶囊、玉屏风颗粒、愈伤灵胶囊、云芝肝泰颗粒等67个品种586批次样品THQ > 1, 分别占品种和样品总数的25%和4%, 其中40个品种为中药原粉制剂。THQ > 1的样品中, 丸剂占大多数, 其次是片剂、胶囊剂、散剂。丸剂多为原粉制剂, 故其THQ普遍高于其他剂型。元素方面, Hg的THQ > 1的样品批次最多, 其次是Pb、As、Cr。因Cd在样品中含量普遍较低, 其THQ也普遍较低, 样品中Cu含量虽高, 但因该元素健康指导值高, 故安全风险低。
| Table 3 Statistics of THQs (target hazard quotients) of Pb, Cd, As, Hg, Cu and Cr in 14 787 batches of Chinese patent medicines |
| Table 4 Correlation coefficients of THQs of Pb, Cd, As, Hg, Cu and Cr |
|
Figure 2 Box plots of THQs of Pb, Cd, As, Hg, Cu and Cr in samples with different dosage forms. A: Tincture; B: Mixture; C: Concentrated decoctions; D: Capsules; E: Granules; F: Tablets; G: Powders; H: Syrups; I: Pills; J: Injection |
按上文建立的基本步骤, 以同一品种所有样品测定值的中位数为C, 对有明确规格和用量的276个中成药进行品种健康风险评估, 结果显示4个中成药品种Pb或Hg的THQ > 1 (表 5), 均为原粉制剂, 涉及散剂、片剂、胶囊剂3种剂型, 应特别关注其健康风险。活血止痛散、愈伤灵胶囊和接骨七厘散中均含矿物药自然铜, 其主要成分为二硫化铁, 并含有多种伴生元素。自然铜在入药前需经煅制, 煅后Pb含量显著降低[33]。如企业使用未煅制或煅制不充分的自然铜投料, 则可能造成含自然铜中成药中Pb含量偏高。五子衍宗丸处方中并不含矿物药, 该品种抽验承担单位在对原药材测定和企业调研后发现, 制剂Hg含量高是由于与含朱砂的丸剂共线生产, 清场不彻底而造成交叉污染[34]。
| Table 5 Chinese patent medicines claiming THQs > 1 |
根据风险评估结果, 首先对品种THQ > 1的中成药的相关元素制定限量, 按公式(3)计算, 4个健康风险较高品种的建议限量见表 5。
讨论本文以国家药品抽验大数据为基础, 对中成药中重金属及有害元素残留情况进行分析和风险评估, 并提出了口服中成药中重金属及有害元素残留限量制定方法。通过识别危害、找出特征、评估可能、确定边界、制定对策, 以期为风险交流和风险管控提供技术支撑, 达到降低或消除安全隐患的目的。
结果显示中成药中重金属及有害元素整体安全状况一般, 口服液、糖浆剂、合剂、酊剂、注射剂风险较低。其他剂型个别品种和样品风险高, 提示应重视丸剂、胶囊剂、片剂、散剂, 尤其是原粉制剂中Hg、Pb、As的残留风险。企业应重视原料药材和饮片的有害残留和生产线交叉污染问题, 加强质量管理, 降低中成药重金属污染的风险。建议对自然铜炮制前后重金属及有害元素的含量、形态、价态进行分析, 讨论其对药品安全性的影响。
国家药品抽验的大部分品种为国家基本药物, 样品批次多、来源广泛、代表性好, 将风险评估引入国家药品抽验, 既可更全面地评价品种质量风险, 以直接服用的中成药为抓手, 向下游延伸, 实现精准高效监管, 也可为药品有害残留物限量制订和修订提供科学的依据。
中药的风险评估应遵循科学规范、平稳高效、服务监管的原则, 追踪品种风险变化和各元素健康指导值更新情况, 研究并建立中药消费模式模型, 获得更加准确、客观的参数, 计算中药重金属及有害元素的理论残留限量值, 对于风险较高的品种, 应进一步进行毒理研究, 确定安全限度值, 适时纳入标准规定。
致谢: 各省药检部门提供了研究资料。
作者贡献:聂黎行负责文章构思和撰写, 钱秀玉、蒋沁悦、李静负责数据收集和整理, 聂黎行、左甜甜、常艳负责数据分析和检查, 李翔、金红宇、戴忠、马双成负责文章审核。
利益冲突:本文研究内容无任何利益冲突。
| [1] |
Cyranoski D. Why Chinese medicine is heading for clinics around the world[J]. Nature, 2018, 561: 448-450. |
| [2] |
Fu ZP, Zhou ZX, Liu XY, et al. Advances in the study of antiviral natural products[J]. Acta Pharm Sin (药学学报), 2020, 55: 703-719. |
| [3] |
Ji C, Hou DW, Li FZ, et al. Assessment and spatial characteristics analysis of human health risk of heavy metals in cultivated soil[J]. Environ Sci (环境科学), 2020, 41: 1440-1448. |
| [4] |
Li YL, Lu YF, Chen WP, et al. Spatial-temporal variation and source change of heavy metals in the cropland soil in the industrial city[J]. Environ Sci (环境科学), 2020, 41: 1432-1439. |
| [5] |
Yu Y, Lü YN, Wang WJ, et al. Spatio-temporal distribution and risk assessment of heavy metals in middle and lower reaches of Le'an River[J]. Environ Sci (环境科学), 2020, 41: 691-701. |
| [6] |
Yang A, Wang YH, Hu J, et al. Evaluation and source of heavy metal pollution in surface soil of Qinghai-Tibet Plateau[J]. Environ Sci (环境科学), 2020, 41: 886-894. |
| [7] |
Mu HY, Zhuang Z, Li YM, et al. Heavy metal contents in animal manure in China and the related soil accumulation risks[J]. Environ Sci (环境科学), 2020, 41: 986-996. |
| [8] |
Wang JZ, Liu Z, Wei H, et al. Spatial characteristics, risk assessment, and source analysis of elements in surface sediments from the Baiyangdian Lake[J]. Environ Sci (环境科学), 2020, 41: 224-231. |
| [9] |
Pandey AK, Gautam A, Dubey RS. Transport and detoxification of metalloids in plants in relation to plant-metalloid tolerance[J]. Plant Gene, 2019, 17: 100171. |
| [10] |
Duttaa M, Kushwahab A, Kalitaa S, et al. Assessment of bioaccumulation and detoxification of cadmium in soil-plant-insect food chain[J]. Bioresour Technol Rep, 2019, 7: 1-6. |
| [11] |
Guo JM, Yang JX, Yang J, et al. Interaction of Cd and Zn affecting the root morphology and accumulation of heavy metals in Sedum aizoon[J]. Environ Sci (环境科学), 2019, 40: 470-479. |
| [12] |
Zhang H, Zhang TP, Zhang Y, et al. Influence of different processing methods on contents and speciation of heavy metals in Cortex Eucommiae[J]. J Int Pharm Res (国际药学研究杂志), 2017, 44: 437-441. |
| [13] |
Li YL, Yue L, Xiao H, et al. Arsenic species in Cordyceps sinensis and its potential health risks[J]. Front Pharmacol, 2019, 10: 1471-1481. |
| [14] |
Kong DD, Li XY, Yan HX, et al. Establishment of health risk assessment model for assessing medicinal and edible plants contaminated by heavy metals-take Astragali Radix, Codonopsis Radix and Laminariae Thallus as examples[J]. China J Chin Mater Med (中国中药杂志), 2019, 44: 5042-5050. |
| [15] |
Zuo TT, Li YL, Jin HY, et al. Determination and risk assessment of heavy metals and harmful elements in ultrafine granular powder of American ginseng[J]. J Shenyang Pharm Univ (沈阳药科大学学报), 2019, 36: 243-248. |
| [16] |
Zuo TT, Li YL, He HZ, et al. Refined assessment of heavy metal-associated health risk due to the consumption of traditional animal medicines in humans[J]. Environ Monit Assess, 2019, 191: 171-182. |
| [17] |
Zhou L, Yang J, Zhan ZL, et al. Determination of heavy metals in Coptidis Rhizoma of different habitats and risk assessment of heavy metals under different ways of administration[J]. Acta Pharm Sin (药学学报), 2018, 53: 432-438. |
| [18] |
Nie LX, Zha YF, Zuo TT, et al. Determination and risk assessment of heavy metals and harmful elements residues in Niuhuang Qingwei Pills[J]. China J Chin Mater Med (中国中药杂志), 2019, 44: 82-87. |
| [19] |
Li XY, Kong DD, Wang R, et al. Safety evaluation of heavy metals contaminated Xiaochaihu Tang using health risk assessment model[J]. China J Chin Mater Med (中国中药杂志), 2019, 44: 5058-5064. |
| [20] |
Wang ZZ, Wang HB, Wang HJ, et al. Heavy metal pollution and potential health risks of commercially available Chinese herbal medicines[J]. Sci Total Environ, 2019, 653: 748-757. |
| [21] |
Chen YX, Wang J, Zhou HQ, et al. Establishment of a new method for determining chromium in gelatin hollow capsule shells by ICP-MS[J]. China Licens Pharm (中国合理用药探索), 2018, 15: 150-152. |
| [22] |
Long XY, Chen Y, Fei YQ, et al. Determination and risk evaluation of 25 metals and harmful elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla[J]. Chin J Pharm Anal (药物分析杂志), 2019, 39: 870-880. |
| [23] |
Li HB, Li MY, Zhao D, et al. Oral bioavailability of As, Pb, and Cd in contaminated soils, dust, and foods based on animal bioassays:a review[J]. Environ Sci Technol, 2019, 53: 10545-10559. |
| [24] |
Miao DR, Li X, Yang WQ. Health risk assessment of Cu, Pb, Zn, Cd, Cr and As in tea leaves from Fengqing County in Yunnan[J]. J Kunming Univ (昆明学院学报), 2019, 41: 56-60. |
| [25] |
Bavaresco J, Fink JR, Rodrigues MLK, et al. Chromium adsorption in different mineralogical fractions from subtropical soils[J]. Pedosphere, 2017, 27: 106-111. |
| [26] |
Zuo TT, Wang Y, Zhang L, et al. Guideline of risk assessment of exogenous harmful residues in traditional Chinese medicines[J]. Chin J Pharm Anal (药物分析杂志), 2019, 39: 1902-1907. |
| [27] |
U.S. Environmental Protection Agency. IRIS Summaries Chromium (Ⅵ) (CASRN 1854002909)[R]. Washington DC: U.S. Environmental Protection Agency, 1998.
|
| [28] |
Mao WF, Wang YBN, Zuo TT, et al. Risk assessment of lead exposure of Chinese medicinal herbs in Chinese population[J]. Drug Stand China (中国药品标准), 2018, 19: 275-281. |
| [29] |
Wang YBN, Jin HY, Zhang L. The situation investigation of traditional Chinese medicine adult consumers in 11 Provinces of China[J]. J Yunnan Univ Tradit Chin Med (云南中医学院学报), 2017, 40: 71-75. |
| [30] |
Wang YBN, Liu AD, Li JW, et al. The survey of traditional Chinese medicine consumption among adult residents in 11 provinces and cities[J]. Chin Pharm Aff (中国药事), 2017, 31: 666-672. |
| [31] |
Nie LX, Zha YF, Li J, et al. Discussion on quality status of TCM raw powder preparation based on national post-market drug surveillance 2018[J]. Chin Pharm J (中国药学杂志), 2019, 54: 1617-1621. |
| [32] |
Ma SC, Wang C, Zhu J, et al. Overall quality status of Chinese patent medicines and analysis of related problems[J]. Chin Pharm J (中国药学杂志), 2019, 54: 1369-1373. |
| [33] |
Jiang YP, Gan YX, Yan X, et al. Progress of study on Pyritum[J]. Pharm Clin Chin Mater Med (中药与临床), 2017, 7: 54-56. |
| [34] |
Zhou JL, Liu W, Tan CM, et al. Quality control study of Wuziyanzong Pills[J]. Chin Pharm J (中国药学杂志), 2015, 54: 125-130. |
 2020, Vol. 55
2020, Vol. 55


