经典名方是至今应用广泛、疗效好、有明显特点与优势的古代中医古典籍所载录的方剂[1]。为了保护和支持经典名方的创新发展, 国家出台了许多相关的政策。2018年4月, 国家中医药管理局会同国家药品监督管理局公布了第一批《古代经典名方目录》, 2018年5月国家药品监督管理局发布的《古代经典名方中药复方制剂简化注册审批管理规定》中指出“经典名方物质基准”, 皆遵照《医疗机构中药煎药室管理规范》制备而成, 物质基准作为保证传统中药与现代剂型一致性的中间过渡对照物, 是衡量制剂与中医临床所使用的药用物质是否一致的标准。2019年3月22日国家药品监督管理局发布了“古代经典名方中药复方制剂及其物质基准的申报资料要求” (征求意见稿), 提供不同批次饮片制备及同批次饮片制备的多批次对应实物的质量研究资料, 明确经典名方物质基准的关键质量属性。经典名方虽然免临床研究, 但从研发和注册审评的角度, 其在质量控制和评价方面要求甚高。因此, 开展经典名方物质基准质量控制的研究, 建立能全面反映经典名方化学质量概貌的质量控制标准, 对于其复方制剂的研究和申报显得尤为重要[2]
清金化痰汤出自《杂病广要》引《医学统旨》, 由明代叶文龄撰写, 该方由黄芩、炒瓜蒌仁、栀子、橘红、甘草等11味药味组成[3]。黄芩泻肺火、化痰热, 主要化学成分为黄酮类, 具有解热抗炎作用[4], 为该方的君药。炒瓜蒌仁清肺化痰、止咳, 主要化学成分为油脂类、有机酸类, 具有镇咳、抗炎作用[5]; 栀子泻火除烦、清热利湿, 主要成分为栀子苷、山栀子苷B, 具有抗炎、平喘作用[6]; 桑白皮泻肺平喘, 主要成分为桑皮苷A, 具有镇咳平喘作用[7]; 川贝母清热化痰, 主要化学成分为西贝母碱, 具有镇咳、祛痰、平喘的作用[8]; 桔梗开宣肺气、祛痰利气, 主要成分为皂苷类成分, 具有祛痰、镇咳作用[9]; 五味药合用宣肺化痰, 作为该方的臣药。橘红下气消痰, 主要成分为橙皮苷, 对呼吸道炎症有较好的治疗作用[10]; 茯苓健脾利湿, 主要成分为茯苓酸, 具有抗炎、抗过敏的活性[11]; 知母清热泻火、生津润燥, 主要成分为甾体皂苷类, 具有抗炎、抗病毒作用[12]; 麦门冬养阴清热、润肺止咳, 主要成分为甾体皂苷类, 具有抗炎、镇咳作用[13]; 四味药合用养阴润燥、生津止渴, 作为该方的佐药。甘草清热补土和中、补脾益气, 主要成分为甘草酸、甘草苷, 具有解毒、抗炎、镇咳作用[14]; 作为该方的使药。以上11味药味相辅相成, 共奏清热化痰, 止咳润肺之功, 该方被收载于2018年国家中医药管理局发布的《古代经典名方目录(第一批)》中。
经典名方清金化痰汤作为中医药传承与发展过程中保留下来的中药方剂杰出代表之一, 在现代临床上有着广泛的应用, 尤其对以咳嗽咳痰为主要症状的呼吸道感染疗效显著。但目前清金化痰汤的质量控制较为简单, 主要采用薄层色谱法对其化合物进行鉴别, 或者采用高效液相色谱法对清金化痰汤主要成分中的单个化合物进行含量检测, 不能全面反映清金化痰汤的质量。因此, 本研究建立了UHPLC同时检测清金化痰汤中多种指标成分的含量测定方法, 实现对经典名方清金化痰汤中多个指标成分的控制, 对今后清金化痰汤的开发和质量控制具有十分重要的意义。
材料与方法仪器 Agilent Technology 1290II超高效液相色谱仪(美国Agilent公司), AB135-S天平(METTLER TOLEDO仪器有限公司), KH200B型超声波清洗器(昆山禾创超声仪器有限公司), SHZ循环水式真空泵(巩义市予华仪器有限责任公司)。
试剂与样品 山栀子苷B (CHB180125)、新芒果苷(CHB170915)、栀子苷(CHB171010)、芒果苷(CHB171027)、黄芩素(CHB170724)、汉黄芩素(CHB171227)、甘草酸(CHB180610 (均购自成都克洛玛生物科技有限公司, 纯度均≥98%), 甲醇(色谱纯, 山东禹王实业有限公司化工分公司), 乙腈(色谱纯, 美国Sigma-Aldrich公司), 实验用水(纯净水, 杭州娃哈哈集团)。黄芩、栀子、炒瓜蒌仁、橘红、知母、桔梗、麦门冬、茯苓、川贝母、桑白皮、甘草各10批均由某企业提供, 经沈阳药科大学中药学院王东教授鉴定为唇形科植物黄芩Scutellaria baicalensis Georgi的干燥根、茜草科植物栀子Ganiema jasminoides Ellis的干燥成熟果实、葫芦科栝楼Trichosanlhes kirilovuii Maxim的干燥成熟种子(炒制)、芸香科植物橘Citrus reticulata Blanco的干燥成熟果皮、百合科知母属植物知母Anemarrhena asphodeloides Bunge的根茎、桔梗科植物桔梗Platycodon grandiflorus (Jacq.) A. DC.的干燥根、百合科植物麦冬Ophiopogon japonicus (L.f) Ker-Gaw的干燥块根、多孔菌科真菌茯苓Poria cocos (Schw.) Wolf的干燥菌核、百合科植物川贝母Fritillaria cirrhosa D.Don的干燥鳞茎、桑科植物桑Morus alba L.的干燥根皮、豆科植物甘草Glycyrrhiza uralensis Fisch.的干燥根和根茎。
UHPLC色谱条件 色谱柱: Waters cortecs T3色谱柱(150 mm×2.1 mm, 1.6 μm); 流动相: 0.04%磷酸水(A)-乙腈(B)梯度洗脱(0~12 min, 5%~9% B; 12~18 min, 9%~10% B; 18~25min, 10%~19% B; 25~35 min, 19%~22% B; 35~42 min, 22%~30% B; 42~47 min, 30%~40% B; 47~50 min, 40%~45% B; 50~52 min, 45%~90% B; 52~54 min, 90%~5% B); 流速: 0.3 mL·min-1; 柱温: 25 ℃; 进样量: 1 μL; 检测波长: 238、280 nm。
混合对照品溶液的配制 取山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸对照品适量, 精密称定, 加甲醇制成每1 mL中含山栀子苷B 249.6 μg、新芒果苷212.3 μg、栀子苷2 120 μg、芒果苷136.3 μg、黄芩素118.0 μg、汉黄芩素32.0 μg、甘草酸202.5 μg的混合溶液, 摇匀, 即得。
供试品溶液的配制 步骤a:根据《医疗机构中药煎药室管理规范》取黄芩5.63 g、栀子5.63 g、甘草1.5 g、知母3.75 g、炒瓜蒌仁3.75 g、茯苓3.75 g、麦门冬4.5 g、桔梗7.5 g、橘红3.75 g、桑白皮3.75 g、川贝母3.75 g共46.51 g, 第一煎加入8倍量水, 加热回流30 min, 120目筛趁热过滤, 第二煎加入6倍量水, 加热回流25 min, 120目筛趁热过滤, 合并两煎液, 65 ℃减压浓缩至85 mL制备成经典名方清金化痰汤物质基准[15]。步骤b:取上述经典名方清金化痰汤物质基准, 摇匀, 精密量取5.0 mL, 置20 mL的瓶中, 加甲醇稀释至刻度, 摇匀, 离心并取上清液, 过0.22 μm微孔滤膜, 取续滤液, 即得。阴性对照溶液的制备:按照经典名方清金化痰汤配方分别称取除黄芩、橘红、栀子、知母、甘草外的其他药材, 依物质基准制备方法制备[15], 按上述供试品溶液制备方法制成阴性对照溶液。
线性与范围 分别精密量取混合对照储备液0.8、1.6、3.2、4.0、6.4、8.0 mL置于10 mL量瓶中, 加入甲醇定容至刻度, 摇匀, 配制成不同质量浓度的混合对照溶液。
精密度 精密量取同一批经典名方清金化痰汤物质基准2.5、5.0、7.5 mL, 按“供试品溶液的制备”项下的方法制备低、中、高3个浓度的供试品溶液, 每一种浓度平行操作3份, 按上述UHPLC色谱条件进样分析, 测定峰面积, 计算各待测物的浓度, 作为重复性实验。精密量取同一批清金化痰汤物质基准5.0 mL, 按“供试品溶液的制备”项下方法制备相同浓度的标准汤剂供试品溶液3份, 按上述UHPLC色谱条件连续3天进样分析, 测定峰面积, 计算各待测物的浓度, 作为日间精密度实验。
准确度 取已知含量的经典名方清金化痰汤物质基准9份, 每份精密量取2.5 mL, 分别按已知含量的50%、100%、150% 3个浓度水平加入对照品, 按“供试品溶液的制备”项下的方法制备低、中、高3个不同浓度的供试品溶液, 每一种浓度平行制备3份。
稳定性 取同一批经典名方清金化痰汤物质基准5.0 mL, 按“供试品溶液的制备”项下方法制备成供试品溶液, 室温放置, 按上述UHPLC色谱条件分别于0、2、4、6、8、10、12、24 h进样分析, 记录峰面积, 计算RSD值。
耐用性 取混合对照品溶液和同一批经典名方清金化痰汤物质基准5.0 mL, 按“供试品溶液的制备”项下方法制备成供试品溶液, 按上述UHPLC色谱条件, 分别考察色谱条件的不同进样体积(0.5、1和1.5 μL), 不同检测波长(236、238和240 nm)、(278、280和282 nm), 不同流速(0.25、0.30和0.35 mL·min-1), 不同柱温(24、25和26 ℃), 不同酸度(0.03%磷酸-水、0.04%磷酸-水和0.05%磷酸-水), 测定待测成分的总含量并计算不同条件的RSD值。
系统适用性实验 分别取混合对照品溶液和供试品溶液, 按上述UHPLC色谱条件进样分析, 色谱峰与其相邻色谱峰之间的分离度均大于1.5, 理论塔板数以栀子苷计不低于2 300, 取混合对照品溶液, 连续进样6次, 计算峰面积的RSD均小于2%, 表明系统适用性良好。
结果 1 方法学考察 1.1 专属性通过对比混合对照品溶液、供试品溶液、阴性对照溶液, 结果显示, 山栀子苷B、栀子苷来自于栀子; 新芒果苷、芒果苷来自于知母; 黄芩素、汉黄芩素来自于黄芩; 甘草酸来自于甘草, 空白及阴性对照溶液在测定成分出峰时间处均无干扰, 典型色谱图见图 1, 表明该方法专属性良好。
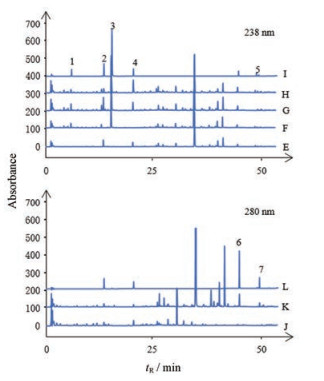
|
Figure 1 UHPLC chromatogram of negative solution. Negative control sample of QingJinHuaTan Decoction without Ganiema jasminoides Ellis (E), or Anemarrhena asphodeloides Bunge (F), or Glycyrrhiza uralensis Fisch (G), and typical chromatogram of test solution (H), mixed standard solution (I) under 238 nm; negative control sample of QingJinHuaTan Decoction without Scutellaria baicalensis Georgi (J), typical chromatogram of test solution (K), mixed standard solution (L) under 280 nm. 1: Gardenoside B; 2: Neomangiferin; 3: Geniposide; 4: Mangiferin; 5: Glycyrrhizin; 6: Baicalein; 7: Wogonin |
以各质量浓度x (μg·mL-1)为横坐标, 峰面积A为纵坐标y, 绘制标准曲线, 计算回归方程。山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸在考察范围内线性关系良好, 相关系数均大于0.999。以对照品溶液逐级稀释法进样检测, 以信噪比为3:1和10:1为基准分别测得各化合物的检测限和定量限, 结果见表 1。
| Table 1 Regressive data of quantification of 7 investigated components |
山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸的RSD分别为1.3%、1.3%、1.6%、2.2%、3.7%、2.7%、1.1%, 结果表明方法重复性良好。山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸的RSD分别为2.0%、2.3%、1.8%、2.1%、1.6%、2.3%、1.6%, 结果表明方法日间精密度良好。
1.4 准确度各成分的回收率均在92.5%~104.7%内, 方法准确度良好。
1.5 稳定性山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸的RSD分别为1.3%、1.2%、1.1%、0.8%、0.8%、1.2%、1.3%, 表明供试品在室温放置24 h内稳定。
1.6 耐用性结果表明, 各条件下山栀子苷B、新芒果苷、栀子苷、芒果苷、黄芩素、汉黄芩素、甘草酸的RSD值均小于2.7%, 说明方法耐用性良好。
2 样品含量测定分别取混合对照品溶液、10批经典名方清金化痰汤物质基准按“供试品溶液的制备”项下方法制备成供试品溶液, 按上述UHPLC色谱条件进样分析, 记录各成分峰面积, 采用外标法将各成分峰面积计算各批次样品中有效成分的含量。含量测定结果见表 2。
| Table 2 Content of 7 components in 10 batches of QingJinHuaTan Decoction |
中药质量是对中药有效性和安全性的反映和表征, 是中医临床用药和中成药有效性控制的重要依据。因此在选择指标成分时, 应选择质量标志物进行质量控制, 依据中药质量标志物的确定原则选择与功效有关的化合物, 以上7种指标成分均具有解热、抗炎、镇咳、平喘的作用。为体现中药制剂在中医理论指导下的组方配伍的原理, 制剂质量标志物的确定应遵循组方配伍, 以君药为主, 臣、佐、使药兼顾的原则[16, 17]。根据古代医籍的描述, 确定了该方剂的君臣佐使, 本文以君药为主, 臣、佐、使药兼顾的原则对上述7种质量标准进行质量控制, 同中国药典各药指标成分相比, 君药黄芩增加了汉黄芩苷、黄芩素、汉黄芩素的测定, 臣药栀子增加了山栀子苷B的测定, 佐药知母增加了新芒果苷的测定, 从而更加全面对该方进行质量控制。
本研究建立了UHPLC同时检测清金化痰汤中多种指标成分的含量测定方法, 实现对经典名方清金化痰汤中多个指标成分的控制。检测方法快速、简便、准确、可靠, 为经典名方清金化痰汤物质基准的全面质量控制提供新的思路和方法。
作者贡献:刘静主要进行了本文的选题与设计、方法建立、实验数据处理、撰写文章及对编辑部修改意见进行核修等。刘然对本文的实验思路、方法建立及文章修改提供了宝贵的意见。李丹丹在制备经典名方清金化痰汤物质基准及配制溶液时提供帮助。许华容在实验过程中对仪器检修、方法建立及文章修改提供了宝贵的意见。李清对本文选题与设计、实验思路、方法建立及文章修改提供了宝贵的意见。毕开顺从选题的设计、实验思路、方法建立及文章修改提供了专业的指导。
利益冲突:无任何利益冲突。
| [1] |
Yang HJ, Huang LQ. The research and development of classical prescription is one of the breakthrough points for the inheritance and development of traditional Chinese medicine[J]. Mod Chin Med (中国现代中药), 2018, 20: 775-779. |
| [2] |
Chen JT, Liu A. Classic famous research and development strategy[J]. China J Tradit Chin Med(中国中药杂志), 2017, 42: 1814-1818. |
| [3] |
Xu B. Qing Jin and stop verging phlegm pills[J]. J Benef Read Drug Inf Med Advices (开卷有益求医问药), 2015, 4: 53-53. |
| [4] |
Wang DF, Wang YL, Wang YW, et al. Effect of Huang qin Tang on serum metabolic profile in rats with ulcerative colitis based on UHPLC-MS[J]. Acta Pharm Sin (药学学报), 2017, 52: 1306-1312. |
| [5] |
Wan LJ. Research progress of chemical composition and pharmacological action of Fructus Trichosanthis[J]. China Pharm (中国药房), 2015, 26: 4440-4443. |
| [6] |
Zhang X, Wang Y, Li SJ, et al. The potential antipyretic mechanism of Gardeniae Fructus and its heat-processed products with plasma metabolomics using rats with yeast induced fever[J]. Front Pharmacol, 2019, 10: 491-497. DOI:10.3389/fphar.2019.00491 |
| [7] |
You S, Kim GH. Protective effect of Mori Cortex radicis extract against high glucose induced oxidative stress in PC12 cells[J]. Biosci Biotechnol Biochem, 2019, 83: 1893-1900. DOI:10.1080/09168451.2019.1621154 |
| [8] |
Li ZH, Gao ZY, Huang W, et al. Effects of Fritillariae Cirrhosae Bulbus onMMP-2, MMP-9 and TIMP-1 in murine asthma model[J]. China J Chin Mater Med (中国中医药杂志), 2017, 42: 4180-4186. DOI:10.19540/j.cnki.cjcmm.20170928.018 |
| [9] |
Wang C, Zhang N, Wang Z, et al. Rapid characterization of chemical constituents of Platycodon graniflorum and its adulterant Adenophora stricta by UPLC-QTOF-MS/MS[J]. J Mass Spectrom, 2017, 52: 643-656. DOI:10.1002/jms.3967 |
| [10] |
da Silva LM, Pezzini BC, Somensi LB, et al. Hesperidin, a citrus flavanone glycoside, accelerates the gastric healing process of acetic acid-induced ulcer in rats[J]. Chem Biol Interact, 2019, 308: 45-50. DOI:10.1016/j.cbi.2019.05.011 |
| [11] |
Zhang N, Li ZX, Li J, et al. Research progress on chemical constituents and biological activities of Poria cocos[J]. Mod Tradit Chin Med Mater Med World Sci Technol (世界科学技术中医药现代化), 2019, 21: 220-233. |
| [12] |
Pan T, Chen H, Liu PW, et al. Effects of total saponins of Anemarrhena asphodeloides on succinic acid/GP R91/IL-1β pathway in adjuvant arthritis model rats[J]. Chin J Basic Med Tradit Chin Med (中国中医基础医学杂志), 2019, 41: 610-613. |
| [13] |
Peng W. Advances in studies on chemical constituents and pharmacological effects of Radix Ophiopogonis[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 477-488. |
| [14] |
Fei WJ, Qian Y. The contents of liquiritin and glycyrrhizin in licorice from different producing areas were determined by UHPLC[J]. J Food Saf Qual Insp (食品安全质量检测学报), 2019, 10: 339-343. |
| [15] |
The State Administration of Traditional Chinese Medicine.TCM (2009) No.3 Standard for Management of TCM Decocting Rooms in Medical Institutions (医疗机构中药煎药室管理规范)[S]. Beijing: The State Administration of Traditional Chinese Medicine, 2009.
|
| [16] |
Liu CX, Chen SL, Xiao XK. The Q-marker of traditional Chinese medicine:new concept of quality control of pharmaceutical products[J]. Chin Tradit Herb Drugs (中草药), 2016, 47: 1443-1457. |
| [17] |
Liu CX, Chen SL, Xiao XK. Quality markers research on Chinese materia medica:quality evaluation and quality standards of Corydalis Rhizoma[J]. Chin Tradit Herb Drugs (中草药), 2016, 47: 1458-1467. |
 2020, Vol. 55
2020, Vol. 55


