骨质疏松(osteoporosis, OP)是以骨矿物质含量降低、骨小梁变细、断裂、数量减少, 皮质骨多孔、变薄为特征, 致使骨脆性增加, 骨折危险性提高的一种全身性骨骼系统疾病[1]。目前医学界根据OP的发病原因将其分为3类, 分别是原发性骨质疏松、继发性骨质疏松和特发性骨质疏松[2]。二至丸是由女贞子和墨旱莲(1:1)配伍形成, 具有补益肝肾之功效, “肾主骨生髓”是二至丸治疗OP的中医药理论依据[3, 4]。Zheng等[5]通过对未成熟小鼠子宫系数、血清雌二醇、雌激素受体ERα和ERβ表达影响的研究发现, 二至丸具有拟雌激素样作用, 并发现该作用可能与上调血中雌二醇含量和靶器官雌激素受体有关。但是目前有关二至丸复方中成分对OP治疗作用的研究较少, 本课题组前期基于网络药理学技术初步探讨了二至丸治疗OP的物质基础及作用机制, 但缺少对二至丸主要成分的抗骨质疏松作用验证[6]。分子对接(molecular docking)是一种将科学计算与物理化学结合在一起, 基于“诱导契合”的原理, 深入地了解蛋白质与配体的相互作用以及与蛋白质活性位点的结合方式的科学方法, 对于虚拟药物筛选方面有着广泛的应用[7]。小鼠胚胎成骨细胞MC3T3-E1属于前成骨细胞, 它具有成骨细胞体外培养的所有特性, 在研究药物对骨作用的影响中, MC3T3-E1细胞是最为常用的骨代谢细胞模型[8, 9]。本研究拟采用分子对接技术筛选二至丸治疗OP的效应成分并通过MC3T3-E1骨细胞的体外药效验证, 以期为进一步的开发利用提供参考。
材料与方法细胞株 小鼠MC3T3-E1前成骨细胞购自上海中乔新舟生物科技有限公司。
药物与试剂 磷酸盐缓冲液(PBS)、α-Mem培养基(Hyclone公司); 0.25%胰蛋白酶(Gibco公司); 胎牛血清(FBS, 杭州四季青公司); Cell Counting Kit-8 (CCK-8, 批号: C00028)、青霉素-链霉素溶液(双抗, 批号: C0222) (碧云天公司); 矿化结节染色液(批号: R30132-2, 南京建成生物工程研究所)。
仪器 倒置显微镜(日本Olympus公司); DMi8倒置荧光显微镜(德国Leica公司); HYQ-3110微量振荡器涡旋混匀器、TDL-80-2B低速台式离心机(上海安亭科学仪器厂); Milli-Q超纯水系统(美国Millipore公司); Tecan Pro200酶标仪(瑞士Tecan公司)。
二至丸成分的收集 利用中药系统药理学数据库与分析平台[10] (TCMSP, http://ibts.hkbu.edu.hk/LSP/tcmsp.php), 并结合中药综合数据库[11] (TCMID, http://www.megabionet.org/tcmid/)及中药潜在靶点数据库[12] (TCM-PTD, http://pharminfo.zju.edu.cn/ptd/)等数据库收集二至丸中女贞子和墨旱莲中的主要化学成分, 并根据TCMSP数据平台提供的药物的吸收、分配、代谢、排泄和毒性(ADME/T)参数, 删除不能同时满足口服生物利用度(OB)≥ 30%和类药性(DL)≥ 0.18且在二至丸中含量不高的化学成分[13, 14]。
*.mol2格式文件的建立 通过文献挖掘并利用CAS数据库、Chemspider (http://www.chemspider.com)和SciFinder (https://scifinder.cas.org/scifinder/view/scifinder/scifinderExplore.jsf)等确定19种化学成分的结构。将在数据库中获得的各自成分结构图以MDL Molfile (*.mol)格式存储, 再导入Chem Bio 3D Ultra12.0软件, 将该成分的二维结构式转换为三维立体结构式, 通过“另存为”将MDL Molfile (*.mol)格式转换为*.mol2格式文件。
靶蛋白对接预处理 通过对OP发病机制进行文献调研, 以及Therapeutic Target Database (TTD, http://bidd.nus.edu.sg/BIDD-Databases/TTD/TTD.asp)、Online Mendelian Inheritance in Man (OMIM, https://omim.org/)和Genetic Association Database (GAD, http://geneticassociationdb.nih.gov/)等疾病数据库搜索, 选择与OP发病机制相关的靶蛋白, 在PDB蛋白质晶体结构数据库(https://www.rcsb.org/)搜索并下载含有原配体的靶蛋白晶体结构。为验证所选取的靶蛋白复合晶体结构是否可靠, 利用Discovery Studio™ 2.5 (简称DS)软件[15], 将原配体抽离出来, 再导入Autodock tools 4.2.5.1重新对接回复合物的活性位点, 对接后配体的构象与原晶体结构中配体构象进行对比, 若得到的均方根偏差值(RMSD)小于2 Å ,证明选取的蛋白晶体结构较可靠[16]。将靶蛋白结构导入Autodock tools, 对靶蛋白进行去水、加氢及分配原子类型等处理, 并根据靶蛋白复合物中配体的坐标确定分子对接的活性位点, 为活性成分和靶蛋白的对接准备。
活性成分与靶蛋白对接及结果选择 利用Autodock tools对二至丸成分及靶蛋白进行对接, 用autogrid计算格点能量, 用autodock进行分子对接, 运算采用拉马克遗传算法。同时, 将靶蛋白与其对应阳性药同法进行对接, 对接完成后, 以二至丸成分与靶蛋白对接的结合能(binding energy)小于阳性药与靶蛋白对接的结合能为参考挑选二至丸活性分子[17]。结合能值越小, 配体与受体结合越稳定[18]。结合能小于0表明配体分子可以与受体分子自发结合, 但是目前对于活性分子的选择标准尚无统一规定。
类药性分析 根据上述挑选出来的二至丸化学成分的靶点预测结果, 以靶蛋白复合物中的原配体对接分数为阈值, 打分高于此阈值的成分则认为可能是作用于该靶点的主要成分。但这些成分不一定具有类药性, 使用里宾斯基(Lipinski)类药性5规则对高于阈值的成分进一步筛选, 最后获得满足5规则的化合物[19]。
化合物溶液的制备 精确称量分子对接挑选得到的化合物粉末, 溶解于1 mL DMSO, 将含药DMSO用α-Mem稀释10倍, 超声溶解, 0.22 μm滤膜过滤除菌后, 制成1×103 μmol·L-1溶液。使用α-Mem将药液稀释成1×102μmol·L-1储存液, 分装密封, -20 ℃保存备用。
细胞培养 将细胞株冻存管从-80 ℃超低温冰箱中取出, 立即放入37 ℃水浴锅, 持续摇晃约1 min, 融化后迅速转移到含5倍体积10% FBS的α-Mem培养基中, 混合均匀, 1 000 r·min-1离心5 min, 弃上清, 将沉淀细胞用含10% FBS的α-Mem培养基2 mL重新悬浮, 转移至培养瓶中, 加入10% FBS的α-Mem培养基5 mL, 置于37 ℃、5% CO2培养箱中培养, 24 h换液, 连续两天, 待细胞长满。
化合物对MC3T3-E1细胞增殖的影响 将处于对数生长期细胞用0.25%胰蛋白酶1 mL消化, 再用含10% FBS的α-Mem培养基悬浮, 用吸管轻轻吹打成单细胞悬液, 调整细胞数为3×104个/mL。每孔100 μL将细胞接种于96孔板中, 每个浓度复制6孔。37 ℃、5% CO2培养24 h后; 吸弃培养基, 设给药组和空白组。空白组:不含药液的空白培养基100 μL; 给药组:加入不同浓度的100 μL药液。在37 ℃、5% CO2培养箱中培养72 h后, 每孔加入Cell Counting Kit (CCK-8)溶液20 μL, 继续培养4 h。待培养结束后, 振摇10 min, 490 nm检测吸光度(A490)值。
化合物对MC3T3-E1细胞矿化的影响 调整细胞数至2×104个/mL, 接种于24孔板, 每孔体积1 mL。细胞贴壁后48 h, 换液加药, 采用不含药液的培养液作为空白对照。每组设6个复孔, 37 ℃、5% CO2培养箱中培养21天, 每3天换液1次。之后, 采用茜素红染色方法进行染色, 每个处理组随机选10个视野在相差显微镜下进行拍摄。
数据处理 采用GraphPad Prism 7软件对独立设计的两组连续变量进行差异显著性分析。若两组数据均呈正态分布, 则对数据进行F检验(方差齐性检验), 若方差齐性, 对数据进行t检验; 若方差不齐性, 对数据进行Welch法近似t检验。若需要比较的两组数据中有任何一组数据不符合正态分布, 则对两组数据进行非参数检验(曼-惠特尼U检验, Mann-Whitney test)。所有实验数据均采用(x±s)表示, 以P < 0.05表示具有统计学意义。
结果 1 二至丸中候选活性成分的选择通过TCMSP、TCMID和TCM-PTD等数据库以及文献挖掘, 共得到化学成分167个。根据TCMSP数据平台计算所得的ADME/T值, 删除不能同时满足OB≥30%和DL≥0.18且在二至丸中含量不高的化学成分, 得到化合物10个。此外, 虽然女贞苷、G13、女贞子苷、特女贞苷、红景天苷、β-谷甾醇、10-羟基女贞苷、齐墩果酸和熊果酸等成分的OB和DL值较低, 但在二至丸中含量较高或是二至丸及其组方药物的特征性成分, 因此, 将这些成分也纳入候选成分中, 共得到候选活性成分19个(表 1) [20]。
| Table 1 Active compounds in Erzhi pill with corresponding pharmacokinetic parameters. OB: Oral bioavailability; DL: Drug-likeness |
OP的病理机制主要与机体的骨重建功能、激素水平、营养因素及免疫能力相关[21, 22]。根据文献调研、PDB (http://www.rcsb.org/)及PubMed (https://www.ncbi.nlm.nih.gov/pubmed/)等数据库搜索[23-26], 选择与OP发病机制相关的靶蛋白共15个(表 2)。
| Table 2 Information of target proteins related to mechanism of osteoporosis (OP) |
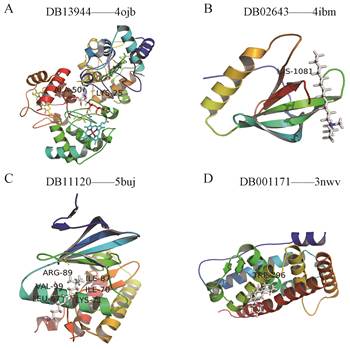
通过DS软件对选取15个靶蛋白结构的可靠性进行验证, 并利用Drugbank (https://www.drugbank.ca/)查找靶蛋白对应的阳性药, 最终选取有阳性药的且结构较稳定的4个靶蛋白, 凋亡蛋白酶激活因子1 (APAF-1)、胰岛素样生长因子I (IGF-1)、丝裂原活化蛋白激酶1 (MAPK1)和雄激素受体(AR), 与19个二至丸活性成分进行分子对接, 结合能见表 3。同时, 将4个靶点的阳性药DB00171 (3nwv)、DB02643 (4ibm)、DB11120 (5buj)和DB13944 (4ojb)与各自靶蛋白APAF-1、IGF-1、MAPK1和AR进行对接, 结合能分别是-7.0、-5.7、-6.8和-6.1 kJ·mol-1, 对接结果图见图 1。将4个靶蛋白与处理好的19个二至丸活性成分对接结果和阳性药与靶蛋白的结合能对比, 并结合类药性分析, 选择出结合能小于阳性药与靶蛋白的结合能且符合Lipinski类药性5规则的分子共14个, 分别是β-谷甾醇(beta-sitosterol)、红景天苷(salidroside)、紫杉叶素(taxifolin)、3'-O-methylguanyanaglycones、槲皮苷(quercetin)、金合欢素(acacetin)、齐墩果酸(oleanic acid)、熊果酸(ursolic acid)、蒙花苷(linarin)、蟛蜞菊内酯(wedelolactone)、漆黄素(fisetin)、去甲蟛蜞菊内酯(demethylwedelolactone)、女贞苷(ligustroflavone)和花旗松素(taxifolin)。为了验证上述14个化合物的抗骨质疏松作用, 本研究选取了二至丸中含量较高或复方及其组方药材的中国药典指标成分红景天苷、槲皮素和蟛蜞菊内酯用于体外验证。因特女贞苷是二至丸及其组方药材女贞子的中国药典质控成分且含量较大, 其在体内易脱糖可能转化为红景天苷, 而酪醇是红景天苷的主要代谢产物[27, 28], 为了更好地比较研究细胞代谢条件下红景天苷可能主要来源的特女贞苷、红景天苷及其代谢产物酪醇的抗骨质疏松作用, 故最终选择红景天苷、槲皮素、蟛蜞菊内酯、特女贞苷和酪醇进行下一步实验。
| Table 3 The binding energy value of the 19 compounds with part of targets (APAF-1, IGF-1, AR, MAPK1). "—"represent the binding energy value > -5 kJ·mol-1 |
|
Figure 1 Molecular docking diagram of DB13944 with 4ojb (A), DB02643 with 4ibm (B), DB11120 with 5buj (C), and DB00171 with 3nwv (D) |
根据前期实验条件的摸索, 临用前用含2.5%α-Mem培养基分别配制10、5、1和1×10-1 µmol·L-1特女贞苷和红景天苷溶液, 60、40、20、10、1 µmol·L-1槲皮素和酪醇溶液, 4、2、1和1×10-1 µmol·L-1蟛蜞菊内酯溶液, 采用不加药液的α-Mem培养基作为对照组, 进行细胞增殖率实验。由图 2A可见, 与对照组相比, 0.1和1 µmol·L-1特女贞苷可显著促进MC3T3-E1细胞增殖(P < 0.01), 5µmol·L-1特女贞苷对细胞增殖不明显(P>0.05), 而10 µmol·L-1特女贞苷对细胞有抑制作用。由图 2B可见, 与对照组相比, 0.1、1和5 µmol·L-1红景天苷可以显著促进MC3T3-E1细胞增殖(P < 0.01, P < 0.05), 10 µmol·L-1红景天苷对细胞增殖不明显(P>0.05)。由图 2C、D可见, 与对照组相比, 各浓度酪醇和蟛蜞菊内酯对细胞增殖均不明显(P>0.05)。由图 2E可见, 与对照组相比, 各浓度槲皮素均可以显著促进MC3T3-E1细胞增殖(P < 0.01)。

|
Figure 2 Effect of ingredients on proliferation of MC3T3-E1 cells. A: Specnuezhenide; B: Salidroside; C: Tyrosol; D: Wedelolactone; E: Quercetin. n = 6, x ± s. *P < 0.05, **P < 0.01 vs control group (0 μmol·L-1) |
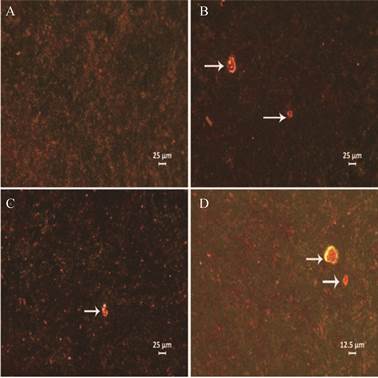
根据细胞增殖率实验结果, 选择考察1µmol·L-1特女贞苷和0.1 µmol·L-1红景天苷对MC3T3-E1细胞矿化结节的影响, 因酪醇是红景天苷的一级代谢产物, 也将酪醇(20 µmol·L-1)作为化合物对MC3T3-E1细胞矿化结节影响的成分之一。茜素红染色结果显示(图 3), 21天时各组均可见不同成骨钙化结节形成, 但钙化面积及颜色深浅程度不同。与对照组比较, 0.1 µmol·L-1红景天苷和20 µmol·L-1酪醇对MC3T3-E1形成面积均有明显增多、颜色加深, 1 µmol·L-1特女贞苷对MC3T3-E1细胞形成矿化结节的影响次之。
|
Figure 3 Effect of ingredients on mineralized nodule of MC3T3-E1 cells. A: Control; B: Salidroside; C: Tyrosol; D: Specnuezhenide |
中医基于“肾主骨藏精”理论, 认为肾精亏虚是骨质疏松症的基本病机。二至丸是传统的补肾中药, 具有促进骨分化的作用, 其有效成分也被证实具有促进骨形成的作用[29]。因此, 本研究首次从分子角度和细胞水平出发, 利用分子对接技术和细胞验证实验筛选二至丸中可能对骨质疏松症有作用的效应成分。
本研究共挑选出二至丸中19个候选活性成分, 其中黄酮类5种、醚萜类5种、香豆草醚类3种、苯酚类2种、苯乙醇类2种、三萜类1种、甾醇类1种, 黄酮类和醚萜类占多数, 这与二至丸的药理作用的主要物质基础是黄酮类和醚萜类相一致[17]。另外, 本研究通过数据库搜索和文献调研, 共收集到与OP相关的蛋白15个, 经过DS软件对蛋白结构稳定性的进行鉴定, 选择4个用于靶点对接。
对接结果表明, 本研究有14个化合物与靶点的结合能小于该靶点与阳性药的结合能, 包括红景天苷、紫杉叶素、槲皮素、蒙花苷、蟛蜞菊内酯等。但将二至丸主要醚萜类成分如女贞苷、G13和女贞子苷进行分子对接, 发现其对接效果较差, 这可能与其分子量大且结构复杂、成分未经过体内代谢转化、不易结合有关。Zhen等[30]通过给大鼠灌胃槲皮素, 发现其能增加OP大鼠的骨密度(BMD), 改善骨的生物学性能; 然后通过体外培养骨髓间充质干细胞(BMSCs), 研究表明槲皮素可以促进细胞的增殖和分化。Léotoing等[31]研究表明漆黄素可通过Runt相关转录因子2 (Runx 2)转录活性促进成骨细胞分化, 进而对OP有良好的疗效。Chen等[32]研究表明红景天苷可以通过调节维生素D代谢、细胞外钙转运蛋白及钙传感受体(CasR)表达, 改善钙稳态, 从而发挥骨保护作用。Zheng等[33]通过研究发现, 红景天苷可以上调骨保护蛋白(OPG)/核因子-Kβ受体活化因子配体(RANKL)的比值, 改善去卵巢后糖尿病大鼠的骨组织病理状态, 起到防治OP的作用。本研究中, 红景天苷与APAF-1和IGF-1的结合能均小于阳性药与该靶点对接的结合能, 表明红景天苷与骨质疏松部分靶点较容易结合, 可能会通过作用于该靶点而达到抗骨质疏松的作用。
根据分子对接结果、成分在二至丸及其组方药材中含量较高、是否为中国药典质控成分及成分的代谢等因素, 本研究选取特女贞苷、红景天苷、蟛蜞菊内酯、槲皮素和酪醇等5个化合物作为细胞验证成分。MC3T3-E1细胞是一种成骨细胞前体, 可在成骨相关信号的诱导刺激下进一步分化为成熟的成骨细胞, 是一种良好的成骨细胞分化研究模型[34]。因此, 通过骨细胞增殖实验和矿化结节实验验证分子对接得到的化合物对MC3T3-E1的影响。骨细胞增殖实验结果发现, 特女贞苷、红景天苷和槲皮素具有显著的促进细胞增殖的作用(P < 0.01, P < 0.05), 而酪醇和蟛蜞菊内酯的作用不明显, 这可能与化合物的结构有关, 已有文献[35, 36]报道醚萜类和黄铜类物质有抗OP作用。本研究为了进一步分析二至丸中抗OP作用成分, 将红景天苷的代谢产物酪醇、红景天苷和特女贞苷作为对细胞矿化结节研究的药效成分。有文献[37]表明, 成骨细胞分化晚期会形成矿化结节, 标志具有成骨功能。本研究中茜素红S法染色发现, 红景天苷对MC3T3-E1成骨细胞矿化能力最为显著, 其次是特女贞苷和酪醇, 这与文献[25, 26]报道一致。
本研究在靶点与抗OP阳性药结合能的参考下, 借助分子对接技术筛选二至丸抗OP化学成分并通过MC3T3-E1细胞增殖实验和矿化实验进行了部分成分的验证, 发现了红景天苷和特女贞苷在体外具有较好的促进成骨细胞增殖和矿化效应, 揭示了二至丸具有多种抗OP活性成分, 为二至丸抗OP作用机制的研究和现代中药的创制提供了参考。
| [1] |
Fuggle NR, Curtis EM, Ward KA, et al. Fracture prediction, imaging and screening in osteoporosis[J]. Nat Rev Endocrinol, 2019, 15: 535-547. DOI:10.1038/s41574-019-0220-8 |
| [2] |
Yang DH, Yang MY. The role of macrophage in the pathogenesis of osteoporosis[J]. Int J Mol Sci, 2019. DOI:10.3390/ijms20092093 |
| [3] |
Zhai Y, Xu J, Feng L, et al. Broad range metabolomics coupled with network analysis for explaining possible mechanisms of Er-zhi-wan in treating liver-kidney Yin deficiency syndrome of traditional Chinese medicine[J]. J Ethnopharmacol, 2019, 234: 57-66. DOI:10.1016/j.jep.2019.01.019 |
| [4] |
Liu FX, Tan F, Tong WW, et al. Effect of Zuogui wan on osteoporosis in ovariectomized rats through RANKL/OPG pathway mediated by β2AR[J]. Biomed Pharmacother, 2018, 103: 1052-1060. DOI:10.1016/j.biopha.2018.04.102 |
| [5] |
Zheng HX, Zhao Y, Xu Y, et al. Estrogenic effect of Erzhi wan on immature mice[J]. Chin J Exp Tradit Med Formul (中国实验方剂学杂志), 2018, 24: 103-107. |
| [6] |
Xu SN, Ding AW, Zhuang L, et al. Material basis and mechanism of Erzhi pill for preventing osteoporosis based on network pharmacology[J]. Chin Pharm J (中国药学杂志), 2018, 53: 1913-1920. |
| [7] |
He JB, Zhao P, Hu ZM, et al. Molecular and structural characterization of a promiscuous C-glycosyltransferase from Trollius chinensis[J]. Angew Chem Int Ed Engl, 2019, 58: 11513-11520. DOI:10.1002/anie.201905505 |
| [8] |
Park YS, Lee JY, Suh JS, et al. Selective osteogenesis by a synthetic mineral inducing peptide for the treatment of osteoporosis[J]. Biomaterials, 2014, 35: 9747-9754. DOI:10.1016/j.biomaterials.2014.08.007 |
| [9] |
Izquierdo-Barba I, Santos-Ruiz L, Becerra J, et al. Synergistic effect of Si-hydroxyapatite coating and VEGF adsorption on Ti6Al4V-ELI scaffolds for bone regeneration in an osteoporotic bone environment[J]. Acta Biomater, 2019, 83: 456-466. DOI:10.1016/j.actbio.2018.11.017 |
| [10] |
Ru JL, Li P, Wang JN, et al. TCMSP:a database of systems pharmacology for drug discovery from herbal medicines[J]. J Cheminform, 2014, 6: 13. DOI:10.1186/1758-2946-6-13 |
| [11] |
Mao X, Xu HY, Li S, et al. Exploring pharmacological mechanisms of Xueshuan-Xinmai-Ning tablets acting on coronary heart disease based on drug target-disease gene interaction network[J]. Phytomedicine, 2019, 54: 159-168. DOI:10.1016/j.phymed.2018.09.018 |
| [12] |
Tao LJ, Chen WT, Jing L, et al. A network pharmacology approach to establish the pharmacological mechanism of JiaWeiXianJi tang on inflammatory bowel disease[J]. Biomed Rep, 2017, 6: 272-278. DOI:10.3892/br.2017.853 |
| [13] |
Zhuang L, Zhai YY, Yao WF, et al. The mechanism study of protecting kidney of Erzhi pill based on network pharmacology[J]. Acta Pharm Sin (药学学报), 2019, 54: 877-885. |
| [14] |
Li H, Yao W, Liu Q, et al. Application of UHPLC-ESI-Q-TOF-MS to identify multiple constituents in processed products of the herbal medicine Ligustri Lucidi Fructus[J]. Molecules, 2017, 22: 689. |
| [15] |
Bhardwaj P, Biswas GP, Bhunia B. Docking-based inverse virtual screening strategy for identification of novel protein targets for triclosan[J]. Chemosphere, 2019, 235: 976-984. DOI:10.1016/j.chemosphere.2019.07.027 |
| [16] |
Holt PA, Chaires JB, Trent JO. Molecular docking of intercalators and groove-binders to nucleic acids using Autodock and Surflex[J]. J Chem Inf Model, 2008, 48: 1602-1615. DOI:10.1021/ci800063v |
| [17] |
Yao W, Zhai Y, Lin L, et al. Study on effective compounds of Qingfei oral liquid for treating new coronavirus pneumonia (COVID-19) through Integrating " compound-target" network and molecular docking[J]. J Nanjing Univ Tradit Chin Med (南京中医药大学学报), 2020, 36: 174-178. |
| [18] |
Namasivayam V, Günther R. Pso@autodock:a fast flexible molecular docking program based on swarm intelligence[J]. Chem Biol Drug Des, 2007, 70: 475-484. DOI:10.1111/j.1747-0285.2007.00588.x |
| [19] |
Pal S, Kumar V, Kundu B, et al. Ligand-based pharmacophore modeling, virtual screening and molecular docking studies for discovery of potential topoisomerase I inhibitors[J]. Comput Struct Biotechnol J, 2019, 17: 291-310. DOI:10.1016/j.csbj.2019.02.006 |
| [20] |
Fu L, Ding H, Han L, et al. Simultaneously targeted and untargeted multicomponent characterization of Erzhi pill by offline two-dimensional liquid chromatography/quadrupole-orbitrap mass spectrometry[J]. J Chromatogr A, 2019, 1584: 87-96. DOI:10.1016/j.chroma.2018.11.024 |
| [21] |
Kenny AM, Prestwood KM. Osteoporosis:pathogenesis, diagnosis, and treatment in older adults[J]. Rheum Dis Clin North Am, 2000, 26: 569-591. DOI:10.1016/S0889-857X(05)70157-5 |
| [22] |
Chen MY, Xie JY. Advances in the pathogenesis of osteoporosis[J]. Psychologies (心理月刊), 2019, 14: 194. |
| [23] |
Ardawi M, Badawoud M, Hassan S, et al. Lycopene treatment against loss of bone mass, microarchitecture and strength in relation to regulatory mechanisms in a postmenopausal osteoporosis model[J]. Bone, 2016, 83: 127-140. DOI:10.1016/j.bone.2015.10.017 |
| [24] |
Cohen A, Kousteni S, Bisikirska B, et al. IGF-1 receptor expression on circulating osteoblast progenitor cells predicts tissue-based bone formation rate and response to teriparatide in premenopausal women with idiopathic osteoporosis[J]. J Bone Miner Res, 2017, 32: 1267-1273. DOI:10.1002/jbmr.3109 |
| [25] |
Mamolini E, Cervellati C, Greco P, et al. VDR, RANKL and OPG polymorphisms as possible predisposing cofactors of postmenopausal osteoporosis:explorative study in Italian population[J]. Gynecol Endocrinol, 2017, 33: 937-941. DOI:10.1080/09513590.2017.1323205 |
| [26] |
Zhang J, Fu Q, Ren Z, et al. Changes of serum cytokines-related Th1/Th2/Th17 concentration in patients with postmenopausal osteoporosis[J]. Gynecol Endocrinol, 2015, 31: 183-190. DOI:10.3109/09513590.2014.975683 |
| [27] |
Fan MX, Tan C, Wang MM, et al. Comprehensive evaluation of quality of Erzhi wan based on five characteristic components[J]. Chin J Exp Tradit Med Formul (中国实验方剂学杂志), 2018, 24: 88-92. |
| [28] |
Cui J, Guo T, Chao J, et al. Potential of the endophytic fungus Phialocephala fortinii Rac56 found in Rhodiola plants to produce salidroside and p-tyrosol[J]. Molecules, 2016, 21: 502. DOI:10.3390/molecules21040502 |
| [29] |
Liang W, Li X, Li G, et al. Sirt1/Foxo axis plays a crucial role in the mechanisms of therapeutic effects of Erzhi pill in ovariectomized rats[J]. Evid Based Complement Alternat Med, 2018, 2018: 9210490. |
| [30] |
Zhen Y, Min J, Zhao YW, et al. Quercetin rescued TNF-alpha-induced impairments in bone marrow-derived mesenchymal stem cell osteogenesis and improved osteoporosis in rats[J]. Am J Transl Res, 2018, 10: 4313-4321. |
| [31] |
Léotoing L, Davicco MJ, Lebecque P, et al. The flavonoid fisetin promotes osteoblasts differentiation through Runx2 transcriptional activity[J]. Mol Nutr Food Res, 2014, 58: 1239-1248. DOI:10.1002/mnfr.201300836 |
| [32] |
Chen XF, Li XL, Yang M, et al. Osteoprotective effects of salidroside in ovariectomized mice and diabetic mice[J]. Eur J Pharmacol, 2018, 819: 281-288. DOI:10.1016/j.ejphar.2017.12.025 |
| [33] |
Zheng HX, Qi SS, Chen C. Salidroside improves bone histomorphology and prevents bone loss in ovariectomized diabetic rats by upregulating the OPG/RANKL ratio[J]. Molecules, 2018, 23: 2398. DOI:10.3390/molecules23092398 |
| [34] |
Paisrisarn P, Tepaamorndech S, Khongkow M, et al. Alterations of mineralized matrix by lead exposure in osteoblast (MC3T3-E1) culture[J]. Toxicol Lett, 2018, 299: 172-181. DOI:10.1016/j.toxlet.2018.10.008 |
| [35] |
Zhao BJ, Wang J, Song J, et al. Beneficial effects of a flavonoid fraction of Herba Epimedii on bone metabolism in ovariectomized rats[J]. Planta Med, 2016, 82: 322-329. DOI:10.1055/s-0035-1558294 |
| [36] |
Ding Y, Ju ZC, Ma C. A validated LC-MS/MS method for the determination of specnuezhenide and salidroside in rat plasma and its application to a pharmacokinetic study[J]. Biomed Chromatogr, 2018, 32: e4353. DOI:10.1002/bmc.4353 |
| [37] |
Li ZY, Li Q, Lu J, et al. Erzhi wan LC-MS determination and pharmacokinetic study of salidroside in rat plasma after oral administration of suspensions of traditional Chinese medicine and Fructus[J]. J Pharm Anal, 2011, 1: 8-12. DOI:10.1016/S2095-1779(11)70002-8 |
 2020, Vol. 55
2020, Vol. 55


